Резюме
Метою роботи було дослідити екскрецію уромодуліну сечі (uUmod), реактивность вегетативної нервової системи і порушення ниркового кровообігу в пацієнтів з додіалізною хронічною хворобою нирок (ХХН), вплив антиоксидантної терапії на ці показники. Матеріали та методи. У дослідженні ROLUNT (UROmoduLin UbiquinoNe GlutaThione) взяли участь пацієнти з ХХН 1–5-ї ст. (n = 91), середній вік яких становив 47,00 ± 12,12 року. Тридцять (32,97 %) чоловіків і 61 (67,03 %) жінка були розподілені на дві групи, які були репрезентативними за віковим і гендерним складом: 1-ша група (n = 46) — пацієнти з ХХН 1–5-ї ст., які мали індекс коморбідності Чарлсона ≤ 2, 2-га група (n = 45) — пацієнти з ХХН 1–5-ї ст., які мали індекс коморбідності Чарлсона ≥ 3. Перша і друга групи поділялись на підгрупи А і Б. Підгрупи А включали пацієнтів з порушенням вегетативного статусу, підгрупи Б — без порушення вегетативного статусу. Підгрупи 1А і 2Б приймали глутатіон по 100 мг 2 рази на добу під час їди протягом 3 місяців; підгрупи 1Б і 2А приймали убіхінон по 100 мг 1 раз на добу під час їди протягом 3 місяців. У пацієнтів з ХХН 1–5-ї ст. визначено uUmod, співвідношення альбуміну і креатиніну (САК), швидкість клубочкової фільтрації (ШКФ). Було проведено 91 ультразвукове дуплексне кольорове сканування нирок і визначено індекс резистентності (IR) у пацієнтів з ХХН 1–5-ї ст. Результати. Результати парного t-тесту показали, що існує значна різниця між показниками на початку і в кінці дослідження, за винятком таких: у підгрупі 1А: гемоглобін (Hb) (T = –1,5863 [–2,0739; 2,0739], 95% довірчий інтервал (ДІ) [–2,4077; 0,3207], p = 0,127); у підгрупі 1Б: Hb (T = –0,382 [–2,0739; 2,0739], 95% ДІ [–1,3977; 0,963], p = 0,706); САК (T = –1,5899 [–2,0739; 2,0739], 95% ДІ [–16,7323; 2,2105], p = 0,126); систолічний артеріальний тиск (САТ) (T = –0,5625 [–2,0739; 2,0739], 95% ДІ [–2,2414; 1,2849], p = 0,579); діастолічний артеріальний тиск (ДАТ) (T = –1,7936 [–2,0739; 2,0739], 95% ДІ [–2,3437; 0,1698], p = 0,087); анкета Чернова (T = 1,5071 [–2,0739; 2,0739], 95% ДІ [–0,6083; 3,8431], p = 0,146); індекс Кердо (T = 0,9392 [–2,0739; 2,0739], 95% ДІ [–1,1083; 2,9431], p = 0,358); у підгрупі 2А: САК (T = –2,0147 [–2,0796; 2,0796], 95% ДІ [–39,1946; 0,6219], p = 0,057); у підгрупі 2Б: САК (T = –1,3328 [–2,0739; 2,0739], 95% ДІ [–17,4695; 3,7999], p = 0,196). Результати кореляції Пірсона показали, що в підгрупі 1А існує значущий середній позитивний зв’язок між показниками uUmod і рШКФ (r(21) = 0,418; p = 0,047); значущий дуже малий негативний зв’язок між показниками uUmod і віком (r(21) = 0,438; p = 0,037); у підгрупі 1Б існує значущий великий позитивний зв’язок між показниками uUmod і Hb (r(21) = 0,513; p = 0,012); значущий великий позитивний зв’язок між показниками uUmod і Morisky Medication Adherence Scale 8 (MMAS-8) (r(21) = 0,515; p = 0,012); значущий дуже малий негативний зв’язок між показниками uUmod і САК (r(21) = 0,441; p = 0,035); у підгрупі 2А існує значущий дуже малий негативний зв’язок між показниками uUmod та індексом Кердо (r(20) = 0,427; p = 0,048); у підгрупі 2Б існує значущий дуже малий негативний зв’язок між показниками uUmod і анкетою Чернова (r(21) = 0,421, p = 0,045); значущий дуже малий негативний зв’язок між показниками uUmod та індексом Чарлсона (r(21) = 0,481; p = 0,020); значущий дуже малий негативний зв’язок між показниками uUmod і віком (r(21) = 0,471; p = 0,023). У підгрупі 1А в кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкети Вейна і Чернова, MMAS-8, індекси Чарлсона і Кердо. У підгрупі 1Б у кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRs, САТ, ДАТ, Hb, анкети Вейна і Чернова, MMAS-8, індекси Чарлсона і Кердо. У підгрупі 2А в кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкета Вейна, MMAS-8, індекс Чарлсона. У підгрупі 2Б у кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкета Вейна, MMAS-8, індекс Кердо. Висновки. Антиоксидантна терапія глутатіоном і убіхіноном суттєво впливає на показники обстеження пацієнтів із ХХН. Враховуючи безпеку й ефективність антиоксидантної терапії, ми пропонуємо включити антиоксидантну терапію в протоколи лікування пацієнтів із ХХН. Для встановлення стандартного протоколу рекомендовано подальші дослідження.
Background. The purpose of this study was to investigate urinary uromodulin (uUmod) excretion, reactivity of the autonomic nervous system and impaired renal blood circulation in patients with predialysis chronic kidney disease (CKD), and the effect of antioxidant therapy on these parameters. Materials and methods. Ninety-one patients with CKD stage 1–5 took part in the ROLUNT (UROmoduLin UbiquinoNe GlutaThione) study, their average age was 47.00 ± 12.12 years. Thirty (32.97 %) men and 61 (67.03 %) women were divided into two groups, which were representative in terms of age and gender composition: the first one (n = 46) — patients with CKD stage1–5 who had Charlson Comorbidity Index ≤ 2, the second one (n = 45) — patients with CKD stage1–5 who had Charlson Comorbidity Index ≥ 3. The first and second groups were divided into subgroups A and B. Subgroup A included patients with impaired vegetative status, subgroup B — without impaired vegetative status. Subgroups 1A and 2B took glutathione 100 mg twice a day with food for 3 months; subgroups 1B and 2A received ubiquinone 100 mg once a day with food for 3 months. In patients with CKD stage1–5, uUmod, albumin to creatinine ratio (ACR), glomerular filtration rate (GFR) were evaluated. Ninety-one ultrasound duplex color scans of the kidneys were performed and the index of resistance (IR) was determined in patients with CKD stage1–5. Results. The results of the paired t-test showed that there is a significant difference between the indicators at the beginning and at the end of the study, with the exception of the following: in subgroup 1A: hemoglobin (Hb) (T = –1.5863 [–2.0739, 2.0739] 95% confidence interval (CI) [–2.4077, 0.3207], p = 0.127); in subgroup 1B: Hb (T = –0.382 [–2.0739, 2.0739], 95% CI [–1.3977, 0.963], p = 0.706); ACR (T = –1.5899 [–2.0739, 2.0739], 95% CI [–16.7323, 2.2105], p = 0.126); systolic blood pressure (SBP) (T = –0.5625 [–2.0739, 2.0739], 95% CI [–2.2414, 1.2849], p = 0.579); diastolic blood pressure (DBP) (T = –1.7936 [–2.0739, 2.0739], 95% CI [–2.3437, 0.1698], p = 0.087); Chernov questionnaire (T = 1.5071 [–2.0739, 2.0739], 95% CI [–0.6083, 3.8431], p = 0.146); Kérdö index (T = 0.9392 [–2.0739, 2.0739], 95% CI [–1.1083, 2.9431], p = 0.358); in subgroup 2A: ACR (T = –2.0147 [–2.0796, 2.0796], 95% CI [–39.1946, 0.6219], p = 0.057); in subgroup 2B: ACR (T = –1.3328 [–2.0739, 2.0739], 95% CI [–17.4695, 3.7999], p = 0.196). The Pearson correlation results showed that in subgroup 1A, there is a significant average positive relationship between uUmod and eGFR (r(21) = 0.418, p = 0.047); a significant very small negative relationship between uUmod indicators and age (r(21) = 0.438, p = 0.037); in subgroup 1B, there is a significant large positive relationship between uUmod and Hb indicators (r(21) = 0.513, p = 0.012); a significant positive relationship between uUmod and Morisky Medication Adherence Scale-8 (MMAS-8) indicators (r(21) = 0.515, p = 0.012); a significant very small negative relationship between uUmod and ACR indicators (r(21) = 0.441, p = 0.035); in subgroup 2A, there is a significant very small negative relationship between uUmod indicators and Kérdö index (r(20) = 0.427, p = 0.048); in subgroup 2B, there is a significant very small negative relationship between the uUmod indicators and Chernov questionnaire score (r(21) = 0.421, p = 0.045); a significant very small negative relationship between uUmod indicators and Charlson Comorbidity Index (r(21) = 0.481, p = 0.020); a significant very small negative relationship between uUmod and age (r(21) = 0.471, p = 0.023). In subgroup 1A at the end of the study, the following independent variables are not significant as predictors for uUmod: IRd, IRs, SBP, DBP, Hb, ACR, age, Vein and Chernov questionnaires score, MMAS-8, Charlson Comorbidity Index and Kérdö index. In subgroup 1B at the end of the study, the following independent variables are not significant as predictors for uUmod: eGFR, IRs, SBP, DBP, Hb, Vein and Chernov questionnaires score, MMAS-8, Charlson Comorbidity Index and Kérdö index. In subgroup 2A at the end of the study, the following independent variables are not significant as predictors for uUmod: eGFR, IRd, IRs, SBP, DBP, Hb, ACR, age, Vein questionnaire score, MMAS-8, Charlson Comorbidity Index. In subgroup 2B at the end of the study, the following independent variables are not significant as predictors for uUmod: eGFR, IRd, IRs, SBP, DBP, Hb, ACR, age, Vein questionnaire score, MMAS-8, Kérdö index. Conclusions. Antioxidant therapy with glutathione and ubiquinone significantly affects the examination parameters of patients with CKD. Considering the safety and effectiveness of antioxidant therapy, we suggest including antioxidant therapy into the treatment protocols for patients with CKD. Further research is recommended to establish a standard protocol.
Вступ
Від хронічної хвороби нирок (ХХН) страждає понад 800 млн осіб у світі (глобальна поширеність понад 9 %), і до 2040 року ХХН може стати п’ятою основною причиною смертності. Щорічно майже 5 % смертей пов’язані з порушенням функції нирок. На сьогодні ХХН є глобальним тягарем для охорони здоров’я, прогресування ХХН до 5-ї стадії пов’язане зі суттєвим збільшенням витрат (у 1,3–4,2 раза), і витрати на одного пацієнта на рік становлять 20 000–100 000 доларів США [1, 2].
ХХН діагностують, якщо розрахункова швидкість клубочкової фільтрації (рШКФ) протягом 3 місяців і більше становить менше за 60 мл/хв на 1,73 м2 і/або співвідношення альбуміну і креатиніну (САК) — понад 30 мг/г [2, 5, 10]. Існує п’ять стадій (1–5) ХХН, які визначають на підставі рШКФ. На першій стадії ХХН функція нирок збережена (підтверджені лабораторно-інструментально зміни в нирках), а на стадії 5 (термінальна стадія хвороби нирок) приєднується тяжка ниркова недостатність. Стадія 3 включає в себе 3a і 3b, що відповідає «легко або помірно зниженій» і «помірно або сильно зниженій» функції нирок [1, 3]. Уромодулін сечі (uUmod) є біомаркером тубулярної маси та функції канальців (функціональний тубулярний маркер) у загальній популяції та в окремих групах (табл. 1) [4, 5].
/27.jpg)
ХХН, як правило, пов’язана з такими супутніми захворюваннями, як сечокам’яна хвороба (СКХ) (з інфекцією сечовивідних шляхів), цукровий діабет, артеріальна гіпертензія, гіперурикемія (подагра), а також із серцево-судинними захворюваннями. Останнім часом з’являється все більше даних про важливу роль оксидантного стресу, яку він відіграє у розвитку, перебігу захворювання і формуванні ускладнень ХХН. Коморбідність негативно впиває на стан здоров’я пацієнтів за рахунок підвищення захворюваності й смертності. Розлади сну і втома теж погано впливають на загальний стан здоров’я, зокрема на психічне здоров’я (виникають різні психічні розлади й симптоми). Усе це негативно впливає на якість життя (ЯЖ) пацієнтів з ХХН [1, 2, 4, 6–8].
Метою роботи було дослідити екскрецію uUmod, реактивність вегетативної нервової системи (ВНС) і порушення ниркового кровообігу в пацієнтів з додіалізною ХХН, вплив антиоксидантної терапії на ці показники.
Матеріали та методи
До рандомізованого відкритого проспективного в паралельних групах із дизайном POEM (Patient-Oriented Evidence that Matters — пошук результатів, які мають значення для пацієнта) дослідження ROLUNT було включено 91 пацієнта європеїдної раси праце–здатного віку з ХХН 1–5-ї ст., які 3 місяці отримували амбулаторне лікування антиоксидантними препаратами (глутатіон, убіхінон) у ТОВ «Вета Плюс», ТОВ «Нефрологічна клініка Професора Дмитра Іванова» і КДЦ Броварської багатопрофільної клінічної лікарні, що є клінічними базами кафедри нефрології та НЗТ Національного університету охорони здоров’я України імені П.Л. Шупика.
Критеріями включення хворих у дослідження ROLUNT були: наявність результатів лабораторно-інструментальних обстежень, вік від 18 до 64 років, згода пацієнта на участь у дослідженні, здатність до адекватної співпраці в процесі дослідження.
Критеріями виключення з дослідження ROLUNT були відмова пацієнта, психічні розлади, декомпенсація хронічних захворювань, гострі невідкладні стани, тяжкі захворювання печінки, онкологія.
Первинна кінцева точка: рівні uUmod на початку дослідження, через 3 і 6 місяців від початку дослідження.
У дослідженні ROLUNT (UROmoduLin UbiquinoNe GlutaThione) взяли участь пацієнти з ХХН 1–5-ї ст. (n = 91), середній вік яких становив 47,00 ± 12,12 року. Тридцять (32,97 %) чоловіків і 61 (67,03 %) жінка були розподілені на дві групи, які були репрезентативними за віковим і гендерним складом: 1-ша група (n = 46) — пацієнти з ХХН 1–5-ї ст., які мали індекс коморбідності Чарлсона ≤ 2, 2-га група (n = 45) — пацієнти з ХХН 1–5-ї ст., які мали індекс коморбідності Чарлсона ≥ 3. Перша і друга групи ділились на підгрупи А і Б. Підгрупи А включали пацієнтів з порушенням вегетативного статусу, підгрупи Б — без порушення вегетативного статусу. Підгрупи 1А і 2Б приймали глутатіон по 100 мг 2 рази на добу під час їди протягом 3 місяців, підгрупи 1Б і 2А приймали убіхінон по 100 мг 1 раз на добу під час їди протягом 3 місяців.
Діагноз ХХН встановлювали згідно з рекомендаціями Національної нефрологічної спілки (NKF-K/DOQI) США, критеріями KDIGO 2012 року і відповідно до наказу МОЗ України № 593 від 02.12.2004 (із змінами, внесеними згідно з наказом МОЗ України № 384 від 24.05.2012).
ЯЖ оцінювали за допомогою опитувальника Medical Outcomes Study-Short Form-36 (MOS SF-36) (український переклад російської версії, рекомендований Міжнаціональним центром дослідження ЯЖ). MOS SF-36 має 36 пунктів, які об’єднані у вісім шкал: фізична активність (physical functioning (PF)), роль фізичних параметрів в обмеженні життєдіяльності (role physical functioning (RP)), біль (bodily pain (BP)), загальне здоров’я (general health (GH)), життєва активність (Vitality (VT)), соціальна активність (Social functioning (SF)), вплив емоцій на життєдіяльность (role-Emotional (RE)) і психічне здоров’я (Mental health (MH)) [2].
Пацієнти протягом 10–15 хвилин обирали відповіді на запитання. За кожну відповідь нараховували бали, які складали та математично обробляли за запропонованими формулами. Усі показники шкал мають значення від 0 до 100, де 100 означає повне здоров’я. Значення всіх шкал об’єднуються у два показника: фізичний і психологічний компоненти здоров’я. Шкали PF, RP, BP, GH утворюють фізичний компонент здоров’я, а шкали VT, SF, RE, MH — психологічний компонент здоров’я. Сума цих показників має бути понад 50 [2].
Прихильність пацієнтів до лікування оцінювали в кінці дослідження за допомогою опитувальника Моріскі — Гріна, MMAS-8. MMAS-8 — це суб’єктивне оцінювання прихильності пацієнта до лікування з обчисленням бала, який відповідає його прихильності до лікування. За кожну негативну відповідь, за винятком питання про прийом усіх ліків за вчорашній день (1 бал за відповідь «так»), нараховується 1 бал. Останній пункт оцінюється за 5-бальною шкалою Лайкерта. Вважають, що пацієнти, які набрали 8 балів, мають високу прихильність до лікування (пацієнтом приймається понад 85 % призначених ліків), 6–7 балів — середню прихильність (пацієнтом приймається 50–84 % призначених ліків), і ті, хто набрав менше за 6 балів, не мають прихильності (пацієнтом приймається менше за 50 % призначених ліків) (табл. 2).
У всіх пацієнтів визначено індекс маси тіла (ІМТ) за формулою Кетле: ІМТ = маса тіла (кг)/(зріст (м2)), індекс коморбідності (Charlson M.E. et al., 2012) (табл. 3). Індекс Чарлсона запропонований для оцінки віддаленого прогнозу коморбідних хворих у 1987 році вченим M.E. Charlson. Даний індекс оцінює в балах (від 0 до 40) наявні супутні захворювання, а також додається один бал на кожні десять років життя при ≥ 40 років (тобто 50 років — 1 бал, 60 років — 2 бали тощо). За індексом Чарлсона можна визначити летальність пацієнтів, яка за відсутності коморбідності становить 12 %, при 1–2 балах — 26 %; при 3–4 балах — 52 %, а при сумі понад 5 балів — 85 % [2, 10].
Усім пацієнтам було проведене ультразвукове дуплексне кольорове сканування нирок (триплексний режим: кольорове дуплексне дослідження, В-режим, спектральний аналіз допплерівського зсуву частот, картування), вимірювали індекс резистентності (IR) (проводили за умови затримки дихання пацієнта під час запису допплерівської кривої) [12–19]. Усі величини розраховувалися за допомогою 3D-системи ультразвукового апарата, автоматично.
У всіх пацієнтів було досліджено вегетативний статус. Вегетативний статус пацієнтів з ХХН визначали за допомогою анкет-опитувальників (тест О.М. Вейна, анкета Ю.М. Чернова) та індексу Кердо ((1–D/P) × 100, де D — ДАТ у міліметрах ртутного стовпа, Р — частота серцевих скорочень за 1 хв (табл. 4).
Для дослідження ВНС використовували опитувальник «Дослідження вегетативного тонусу» Ю.М. Чернова, який налічує 24 пункти, що відповідають за вегетативну реактивність (табл. 5). Підрахунок результатів поданий в балах, за сумою яких визначали: симпатикотонію (переважання тонусу симпатичної ВНС), ваготонію (переважання парасимпатичної ВНС) або змішаний тонус. Якщо переважає симпатичний тонус, то різниця суми балів симпатичних реакцій і суми балів парасимпатичних реакцій буде ≥ 10; якщо < 10, то переважає змішаний тонус ВНС. Якщо переважає парасимпатичний тонус, різниця суми балів парасимпатичних реакцій і суми балів симпатичних реакцій буде ≥ 10. Якщо < 10, то переважає змішаний тонус ВНС [21].
Об’єктивна оцінка вегетативної реактивності була зроблена на підставі результатів дослідження дермографізму, ртутної термометрії, індексу Кердо.
АТ вимірювали на правій руці сидячи або в горизонтальному положенні після 5 хв у спокої за допомогою автоматичного монітора для вимірювання АТ (PANACARE, Німеччина). АТ вимірювався за допомогою манжети відповідного розміру з інтервалом 60–90 с три рази. Артеріальна гіпертензія встановлювалася на підставі раніше діагностованої гіпертензії і/або виявлення середнього САТ ≥ 140 мм рт.ст. і/або середнього ДАТ ≥ 90 мм рт.ст. або при прийомі пацієнтом антигіпертензивних ліків.
Ступені артеріальної гіпертензії відповідно до критеріїв Міжнародної асоціації гіпертензії та ВООЗ (1999):
— І ступінь — САТ 140–159 мм рт.ст., ДАТ 90–99 мм рт.ст.;
— ІІ ступінь — САТ 160–179 мм рт.ст., ДАТ 100–109 мм рт.ст.;
— ІІІ ступінь — САТ > 180 мм рт.ст., ДАТ > 110 мм рт.ст.
рШКФ у нормі становить 95 ± 20 мл/хв/1,73 м2 у жінок і 125 мл/хв/1,73 м2 у чоловіків (до 30 років). Щорічно після 30 років рШКФ знижується на 1 мл/хв/1,73 м2 (Levey et al., 2011). рШКФ оцінювали за допомогою формули конвертації рівня креатиніну плазми Співробітництва епідеміології ХХН (Chronic Kidney Disease Epidemiology Collaboration (CKD-EPI)) (табл. 6).
Наявність анемії визначалась за критеріями EDTA-ERA (1999):
— для жінок у пременопаузі та пацієнтів у препубертаті — Hb < 110 г/л;
— для чоловіків і жінок у постменопаузі — Hb < 120 г/л.
Методика визначення рівня uUmod така. Зразки сечі (середня порція), зібраної вранці, відразу після отримання розподіляли в пробірки (1,5 мл). Усі зразки сечі зберігалися при температурі –20 °C. uUmod вимірювали за допомогою комерційно доступного набору для імуноферментного аналізу (ELISA) (OriGene Technologies GmbH, Герфорд, Німеччина). Надані виробником характеристики ІФА: назва — високочутливий сендвіч-набір ELISA для кількісного визначення Umod людини (Human Uromodulin/umod ELISA Kit); 96 лунок зі стріпами; чутливість < 10 пг/мл;
діапазон виявлення 312–20 000 пг/мл; при 4 °C — зберігання протягом 6 місяців, при –20 °C — протягом 12 місяців. Рівень uUmod вимірювали за допомогою фотометра при довжині хвилі 450 нм і еталонній довжині хвилі 620 нм. Дослідження проводилось на імуноферментному аналізаторі RT-6100 (Rayto Life And Analytical Sciences Co., Ltd., Китайська Народна Республіка).
Калібрована крива відповідає діапазону і нормам виробника даного реактиву та наведеному ним прикладу стандартної кривої, яка входила до реактиву: Human Uromodulin/umod ELISA Kit (EA102492). Приклад стандартної кривої подано на рис. 1. Найвищий О.D. значення може бути вищим або нижчим, ніж у прикладі. Результат експерименту є статистично значущим, якщо найвищий O.D. значення не менше за 1,0. Концентрація 0/312/625/1250/2500/5000/10 000/20 000 (пг/мл), O.D. 0,124/0,166/0,196/0,291/0,436/0,676/1,158/2,017. На підставі цих даних можна стверджувати, що реактив робочий і якість дослідження висока.
Для оцінки розподілу даних використовувався критерій Колмогорова — Смирнова (тест Лілліфорса). Дані з нормальним розподілом були подані як середнє ± стандартне відхилення (M ± SD), з ненормальним — як медіана та інтерквартильний розмах (Mе (IQR)). Викривлені дані перед аналізом були логарифмічно перетворені. Категорійні дані подані у відсотках.
Кореляцію Пірсона використовували для оцінки зв’язку на початковому етапі. Лінійну регресію проводили із залежною змінною і незалежними змінними. Непарний t-критерій Стьюдента використовували при нормальному розподілі кількісних показників, U-критерій Манна — Уїтні — при ненормальному розподілі, для безперервних змінних для порівняння базових характеристик між групами протягом періоду дослідження. Кореляційний аналіз і аналіз множинної регресії проводили за коефіцієнтом кореляції Пірсона (r). Р-значення < 0,05 вважалося статистично значущим.
Математичний аналіз і статистична обробка результатів здійснювались за допомогою Microsoft Excel 2010 на ПК.
Дослідження було схвалено комісією з питань етики Національного університету охорони здоров’я України імені П.Л. Шупика.
При проведенні дослідження ROLUNT дотримувались правил безпеки для збереження життя, здоров’я і прав пацієнтів, морально-етичних норм і канонів людської гідності згідно з Гельсінською декларацією Всесвітньої медичної асоціації (етичні принципи проведення наукових медичних досліджень за участю людини (1964–2008 рр.)), основних положень конвенції Ради Європи про права людини та біомедицину (від 04.04.1997), Етичного кодексу вченого України (2009) і наказу МОЗ України № 690 від 23.09.2009 (зі змінами, внесеними згідно з Наказом МОЗ України № 523 від 12.07.2012).
Результати
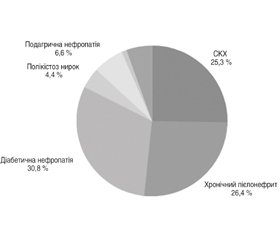
У структурі ХХН переважну більшість становила СКХ — 23 особи (25,3 %), хворих на хронічний пієлонефрит було 24 особи (26,4 %), діабетична нефропатія була у 28 пацієнтів (30,8 %), 4 хворих мали полікістоз нирок (4,4 %), подагрична нефропатія була в 6 (6,6 %), хронічний гломерулонефрит — в 1 (1,1 %), 5 хворих мали гіпертензивну нефропатію (5,4 %). Питома вага хворих залежно від діагнозу ХХН подана на рис. 2.
Соціальна характеристика пацієнтів подана в табл. 7. Вік людей був однорідним, у середньому становив 46–47 років, жінки переважали в обох групах. Тривалість ХХН у першій групі становила 6,18 ± 4,32 (1; 15) року, у другій групі — 5,79 ± 3,88 (1; 16) року, є вірогідна різниця між групами за віком і статтю (U 44,5; р = 3,664e-15).
Для всіх пацієнтів індекс коморбідності Чарлсона становив від 0 до 4. У кінці дослідження 2 пацієнти (2,2 %) мали 8 балів за шкалою Моріскі — Гріна, що означало високу прихильність до терапії, із середньою прихильністю (6–7 балів) було 14 пацієнтів (15,4 %) і без прихильності (< 6 балів) — 75 (82,4 %) (табл. 8).
/33_2.jpg)
Було оцінено такі параметри: рШКФ, САТ, ДАТ, САК, оскільки вони були релевантними маркерами прогресування ХХН. Також визначався рівень uUmod. Виявлено статистично значущу різницю в підгрупах А першої і другої груп на початку дослідження за такими показниками: рШКФ (U = 371,5, [166,7482 : 339,2518]); Hb (U = 391 [166,9391 : 339,0609]); САТ (U = 141 [166,7653 : 339,2347]); у підгрупах Б першої і другої груп на початку дослідження — за такими показниками: ДАТ (U = 157 [175,8266 : 353,1734]); САТ (U = 156 [175,3903 : 353,6097]); рШКФ (U = 437 [175,3518 : 353,6482]); uUmod (U = 360 [175,294 : 353,706]); IRd (U = 168,5 [175,7464 : 353,2536]); у підгрупах А першої і другої груп у кінці дослідження — за такими показниками: рШКФ (U = 352 [166,7738 : 339,2262]); Hb (U = 343 [166,8422 : 339,1578]); ДАТ (U = 87,5 [166,9647 : 339,0353]); у підгрупах Б першої і другої груп у кінці дослідження — за такими показниками: рШКФ (U = 443 [175,3656 : 353,6344]); uUmod (U = 380,5 [175,3078 : 353,6922]); IRd (U = 153 [176,3178 : 352,6822]). За іншими показниками статистично значущої різниці не виявлено.
Результати парного t-тесту показали, що існує значуща велика різниця між показниками на початку і в кінці дослідження, за винятком таких: у підгрупі 1А: Hb (T = –1,5863 [–2,0739; 2,0739], 95% ДІ [–2,4077; 0,3207], p = 0,127); у підгрупі 1Б: Hb (T = –0,382 [–2,0739; 2,0739], 95% ДІ [–1,3977; 0,963], p = 0,706); САК (T = –1,5899 [–2,0739; 2,0739], 95% ДІ [–16,7323; 2,2105], p = 0,126); САТ (T = –0,5625 [–2,0739; 2,0739], 95% ДІ [–2,2414; 1,2849], p = 0,579); ДАТ (T = –1,7936 [–2,0739; 2,0739], 95% ДІ [–2,3437; 0,1698], p = 0,087); у підгрупі 2А: САК (T = –2,0147 [–2,0796; 2,0796], 95% ДІ [–39,1946; 0,6219], p = 0,057); у підгрупі 2Б: САК (T = –1,3328 [–2,0739; 2,0739], 95% ДІ [–17,4695; 3,7999], p = 0,196) (табл. 9).
/34.jpg)
Було оцінено показники опитувальників Вейна і Чернова та індекс Кердо. Виявлено статистично значущу різницю в підгрупах А першої і другої груп на –початку дослідження за такими показниками: індекс Кердо (U = 350 [166,7084 : 339,2916]); у підгрупах Б першої і другої груп — у кінці дослідження за такими показниками: анкета Чернова (U = 136,5 [175,3463 : 353,6537]). За іншими показниками статистично значущої різниці не виявлено.
Результати парного t-тесту показали, що існує значуща велика різниця між показниками на початку і в кінці дослідження, за винятком таких: у підгрупі 1Б — анкети Чернова (T = 1,5071 [–2,0739; 2,0739], 95% ДІ [–0,6083; 3,8431], p = 0,146); індексу Кердо (T = 0,9392 [–2,0739; 2,0739], 95% ДІ [–1,1083; 2,9431], p = 0,358) (табл. 10).
Результати кореляції Пірсона показали, що в підгрупі 1А існує значущий середній позитивний зв’язок між показниками uUmod і рШКФ (r(21) = 0,418; p = 0,047); значущий дуже малий негативний зв’язок між показниками uUmod і віком (r(21) = 0,438; p = 0,037); у підгрупі 1Б існує значущий великий позитивний зв’язок між показниками uUmod і Hb (r(21) = 0,513; p = 0,012); значущий великий позитивний зв’язок між показниками uUmod і MMAS-8 (r(21) = 0,515; p = 0,012); значущий дуже малий негативний зв’язок між показниками uUmod і САК (r(21) = 0,441; p = 0,035); у підгрупі 2А існує значущий дуже малий негативний зв’язок між показниками uUmod та індексом Кердо (r(20) = 0,427; p = 0,048); у підгрупі 2Б існує значущий дуже малий негативний зв’язок між показниками uUmod і анкетою Чернова (r(21) = 0,421; p = 0,045); значущий дуже малий негативний зв’язок між показниками uUmod та індексом Чарлсона (r(21) = 0,481; p = 0,020); значущий дуже малий негативний зв’язок між показниками uUmod і віком (r(21) = 0,471; p = 0,023) (табл. 11).
/35.jpg)
Результати кореляції Пірсона щодо основних показників підгрупи 1А в кінці дослідження показали, що існує значущий середній позитивний зв’язок між uUmod і рШКФ (r(21) = 0,418; p = 0,047) (рис. 3).
Результати кореляції Пірсона щодо основних показників підгрупи 1Б у кінці дослідження показали, що існує значущий великий позитивний зв’язок між Hb і uUmod (r(21) = 0,513; p = 0,012) (рис. 4).
Результати кореляції Пірсона щодо основних показників підгрупи 2А в кінці дослідження показали, що існує незначущий малий позитивний зв’язок між віком та uUmod (r(20) = 0,278; p = 0,211) (рис. 5).
Результати кореляції Пірсона щодо основних показників підгрупи 2Б у кінці дослідження показали, що існує незначущий малий позитивний зв’язок між ДАТ і uUmod (r(21) = 0,235; p = 0,28) (рис. 6).
У підгрупі 1А в кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкети Вейна і Чернова, MMAS-8, індекси Чарлсона і Кердо. У підгрупі 1Б у кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRs, САТ, ДАТ, Hb, анкети Вейна і Чернова, MMAS-8, індекси Чарлсона і Кердо. У підгрупі 2А в кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкета Вейна, MMAS-8, індекс Чарлсона. У підгрупі 2Б в кінці дослідження такі незалежні змінні не є значущими як предиктори для uUmod: рШКФ, IRd, IRs, САТ, ДАТ, Hb, САК, вік, анкета Вейна, MMAS-8, індекс Кердо (табл. 12).
/37.jpg)
Результати множинної лінійної регресії основних показників підгрупи 1А в кінці дослідження показали, що існує помірний сукупний значущий ефект між показниками: вік, індекс Чарлсона, MMAS-8, тест –Вейна, опитувальник Чернова, індекс Кердо, IRd, IRs, рШКФ, САК, Hb, САТ, ДАТ і uUmod (F(1, 21) = 4,45; p = 0,047; R2 = 0,17; R2adj = 0,14) (рис. 7, 8).
Результати множинної лінійної регресії основних показників підгрупи 1Б у кінці дослідження показали, що існує сильний сукупний значущий ефект між показниками: вік, індекс Чарлсона, MMAS-8, тест Вейна, опитувальник Чернова, індекс Кердо, IRd, IRs, рШКФ, САК, Hb, САТ, ДАТ і uUmod (F(3, 19) = 7,08; p = 0,002; R2 = 0,53; R2adj = 0,45). Значущими в моделі були предиктори: вік (t = –3,404; p = 0,003), індекс Чарлсона (t = 2,32; p = 0,032) і –MMAS-8 (t = –2,693; p = 0,014) (рис. 9, 10).
Результати множинної лінійної регресії основних показників підгрупи 2А в кінці дослідження показали, що існує помірний сукупний значущий ефект між показниками: вік, індекс Чарлсона, –MMAS-8, тест Вейна, опитувальник Чернова, індекс Кердо, IRd, IRs, рШКФ, САК, Hb, САТ, ДАТ і uUmod (F(2, 19) = 4,87; p = 0,020; R2 = 0,34; R2adj = 0,27). Значущими в моделі були предиктори: вік (t = –2,121; p = 0,047) та індекс Чарлсона (t = –2,886; p = 0,009) (рис. 11, 12).
Результати множинної лінійної регресії основних показників підгрупи 2Б у кінці дослідження показали, що існує сильний сукупний значущий ефект між такими показниками: вік, індекс Чарлсона, MMAS-8, тест Вейна, опитувальник Чернова, індекс Кердо, IRd, IRs, рШКФ, САК, Hb, САТ, ДАТ і uUmod (F(2, 20) = 6,8; p = 0,006; R2 = 0,4; R2adj = 0,35). Окремі предиктори: вік (t = –2,766; p = 0,012) та індекс Чарлсона (t = –2,415; p = 0,025) були значущими предикторами в моделі (рис. 13, 14).
Висновки
Антиоксидантна терапія глутатіоном і убіхіноном суттєво впливає на показники обстеження пацієнтів із ХХН. Враховуючи безпеку й ефективність антиоксидантної терапії, ми пропонуємо включити антиоксидантну терапію в протоколи лікування пацієнтів із ХХН. Для встановлення стандартного протоколу рекомендовано подальші дослідження.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів і фінансової зацікавленості при написанні статті.
Інформація про фінансування. Роботу виконано за власні кошти аспіранта. Стаття є фрагментом науково-дослідної роботи аспіранта кафедри нефрології та нирково-замісної терапії Національного університету охорони здоров’я України імені П.Л. Шупика за темою «Екскреція uUmod і його клініко-лабораторна оцінка, значення в ранній діагностиці, ренопротекції і оптимізації лікування ХХН на фоні молекулярного стресу», у рамках НДР кафедри за темами: «Розроблення технології збереження функції нирок у пацієнтів з ХХН та гіперурикемією» (2021–2022 рр.), номер державної реєстрації 0121U100446, і «Вивчення впливу гіпоурикемічної терапії у пацієнтів з ХХН та обґрунтування оптимальної терапії» (2019–2023 рр.), № 0119U101718.
Інформація про внесок кожного автора. Денова Л.Д. — збір, обробка, аналіз отриманих даних, написання тексту; Іванов Д.Д. — концепція та дизайн дослідження.
Отримано/Received 09.05.2023
Рецензовано/Revised 24.05.2023
Прийнято до друку/Accepted 28.05.2023
Список литературы
1. Rydén A., Nolan S., Maher J., Meyers O., Kündig A., Bjursell M. Understanding the patient experience of chronic kidney disease stages 2-3b: a qualitative interview study with Kidney Disease Qua–lity of Life (KDQOL-36) debrief. BMC Nephrol. 2022 Jun 1. 23(1). 201. doi: 10.1186/s12882-022-02826-3. PMID: 35641914; PMCID: PMC9155979.
2. Денова Л.Д., Іванов Д.Д. Якість життя хворих з додіалізною хронічною хворобою нирок, її зв’язок з оксидантним стресом і екскрецією уромодуліну. Нирки. 2023. 12(1). doi: https://doi.org/10.22141/2307-1257.12.1.2023.389/.
3. Денова Л.Д. Принципи біоетики в лікуванні та реабілітації пацієнтів з хронічною хворобою нирок. Нирки. 2022. 11(4). doi: 10.22141/2307-1257.11.4.2022.382.
4. Денова Л.Д. Значення протеомних досліджень новітніх маркерів ураження нирок у сечі для оцінки перебігу, прогресування й ускладнень у пацієнтів із ХХН. Нирки. 2022. 11(2). doi: https://doi.org/ 10.22141/2307-1257.11.2.2022.363.
5. Денова Л.Д. Уромодулін як потенційний кандидат-маркер прогнозування перебігу хронічної хвороби нирок. Нирки. 2021. 10(4). doi: 10.22141/2307-1257.10.4.2021.247898.
6. Денова Л.Д., Іванов Д.Д, Андруневич Р.Р., Корж О.М., Красюк Е.К. Нефрологічна допомога в умовах воєнного стану в Україні. Нирки. 2022. 11(3). doi: 10.22141/2307-1257.11.3.2022.372.
7. Denova L.D., Ivanov D.D. Influence of oxidative, carbo–nyl, and nitrosative stresses on the course of chronic kidney disease (analytical review). Kidneys. 2022. 11(1). doi: 10.22141/2307-1257.11.1.2022.360.
8. Lightfoot C.J., Howell M., Smith A.C. How to assess quality of life in persons with chronic kidney disease. Curr. Opin. Nephrol. Hypertens. 2021 Nov 1. 30(6). 547-554. doi: 10.1097/MNH.0000000000000740. PMID: 34433189.
9. De Las Cuevas C., Peñate W. Psychometric properties of the eight-item Morisky Medication Adherence Scale (MMAS-8) in a psychiatric outpatient setting. Int. J. Clin. Health Psychol. 2015 May-Aug. 15(2). 121-129. doi: 10.1016/j.ijchp.2014.11.003. Epub 2014 Dec 25. PMID: 30487829; PMCID: PMC6224788.
10. Несен А.О., Чернишов В.А., Грунченко М.М., Шкапо В.Л., Чирва О.В., Валентинова І.А. Коморбідність при хронічних неінфекційних захворюваннях у пацієнтів стаціонару з високим кардіоваскулярним ризиком. Український терапевтичний журнал. 2015. № 4. С. 47-55.
11. Кропачева Е.С., Землянская О.А., Добровольский А.Б., Панченко Е.П. Прогностическая значимость индекса SAMe-TT2 R2 и индекса коморбидности Charlson в отношении недостижения целевого уровня антикоагуляции и риска развития тромботических событий у больных, получающих терапию варфарином (результаты проспективного 10-летнего наблюдения). Кардиологический вестник. 2019. 1. doi: 10.17116/Cardiobulletin20191401123.
12. Petrucci I., Clementi A., Sessa C., Torrisi I., Meola M. Ultrasound and color Doppler applications in chronic kidney disease. J. Nephrol. 2018 Dec. 31(6). 863-879. doi: 10.1007/s40620-018-0531-1. Epub 2018 Sep 6. PMID: 30191413.
13. Iida N., Seo Y., Sai S., Machino-Ohtsuka T., Yamamoto M., Ishizu T., Kawakami Y., Aonuma K. Clinical Implications of Intrarenal Hemodynamic Evaluation by Doppler Ultrasonography in Heart Failure. JACC Heart Fail. 2016 Aug. 4(8). 674-82. doi: 10.1016/j.jchf.2016.03.016. Epub 2016 May 11. PMID: 27179835.
14. Viazzi F., Leoncini G., Derchi L.E., Pontremoli R. Ultrasound Doppler renal resistive index: a useful tool for the management of the hypertensive patient. J. Hypertens. 2014 Jan. 32(1). 149-53. doi: 10.1097/HJH.0b013e328365b29c. PMID: 24172238; PMCID: PMC3868026.
15. Lotfinejad M., Rashedi A., Amirkhanlou S. The Survey of Relationship Between Resistance Index of Renal Artery and Albuminuria in Diabetic Patients Referring to Shahid Sayyad Shirazi Hospital, 2017 to 2018. Iran J. Kidney Dis. 2020 Sep. 14(5). 358-364. PMID: 32943590.
16. Venables H.K., Wiafe Y.A., Adu-Bredu T.K. Value of Doppler ultrasound in early detection of diabetic kidney disease: A systematic review and meta-analysis. Ultrasound. 2021 Aug. 29(3). 141-149. doi: 10.1177/1742271X20977051. Epub 2020 Dec 8. PMID: 34567226; PMCID: PMC8366222.
17. Delsart P., Vambergue A., Ninni S., Machuron F., Lelievre B., Ledieu G. et al. Prognostic significance of the renal resistive index in the primary prevention of type II diabetes. J. Clin. Hypertens. (Greenwich). 2020 Feb. 22(2). 223-230. doi: 10.1111/jch.13819. Epub 2020 Jan 31. PMID: 32003935; PMCID: PMC8029971.
18. Jinadu Y.O., Raji Y.R., Ajayi S.O., Salako B.L., Arije A., Kadiri S. Resistivity index in the diagnosis and assessment of loss of renal function in diabetic nephropathy. Cardiovasc. J. Afr. 2022 Jan-Feb 23. 33(1). 26-32. doi: 10.5830/CVJA-2021-032. Epub 2021 Jul 26. PMID: 34309616; PMCID: PMC9198679.
19. Lin J., Liu G., Lin Y., Wei C., Liu S., Xu Y. Ultrasono–graphy Combined with Blood Biochemistry on the Early Diagnosis of Diabetic Kidney Disease. Dis. Markers. 2022 Oct 5. 2022. 4231535. doi: 10.1155/2022/4231535. PMID: 36246564; PMCID: PMC9556206.
20. Брюханов А.В. Ефективність феварину (флувоксаміну) в лікуванні вегетативних порушень, коморбідних невротичних станів. Міжнародний неврологічний журнал. 2008. 1(17). С. 27-31.
21. Баусова О.Б., Коляда Т.І., Коляда О.М., Трач О.О. Реактивність вегетативної нервової системи у студентів ХНМУ. Український журнал медицини, біології та спорту. 2017. № 1. С. 66-69.
22. Кушніренко С.В. Чи необхідна дієтотерапія для хворих на хронічну хворобу нирок у додіалізному періоді? Нирки. 2014. № 3(9). С. 15-20.

/27.jpg)
/29.jpg)
/30.jpg)
/31.jpg)
/32.jpg)
/32_2.jpg)
/33.jpg)
/33_2.jpg)
/34.jpg)
/35.jpg)
/36.jpg)
/37.jpg)
/37_2.jpg)
/38.jpg)