Імплантовані порт-системи для в/в введення ліків широко використовуються у світі для онкологічних хворих, які потребують тривалого доступу до центральних вен для тривалої терапії. В англомовній літературі найчастіше можна зустріти абревіатуру Long-term CVAD, або Port-A-Cath. У 1982 році Niederhuber представив нинішній тип порт-систем для клінічного використання, які зазвичай імплантуються підшкірно на грудній стінці. Порт-система складається з катетера, який розташовується у центральній вені, та прикріпленої до порту камери, яку розміщують у підшкірній кишені. Доступ до цього повністю імплантованого резервуара можливий за допомогою спеціальної голки Хубера, яка дозволяє проколювати шкіру та силікон мембрани камери порту. Пункція останньої має проходити у стерильних умовах. Крім того, після проведеної терапії пацієнтам не потрібна зовнішня пов’язка у зоні порту та дозволено займатися звичайною діяльністю, наприклад приймати душ або плавати, після видалення голки. Завдяки цілком підшкірному розташуванню порт-системи непомітні, а тому пацієнти не комплексують з цього приводу [1–3]. Через низький рівень екстравазації та інфекції загальними показаннями для використання постійних венозних порт-систем є введення препаратів із місцево-запальною дією на ендотелій судин, як-от препарати для хіміотерапії та парентерального харчування [4].
Імплантація центральних венозних порт-систем виконується у катетерних лабораторіях інтервенційних відділень або в операційних з рентгеноскопічним контролем C-Arm під місцевою анестезією. Останнім часом імплантація порт-систем дозволена в операційних під безпосереднім ECG-контролем з наступним обов’язковим плановим Rö-контролем у післяопераційному періоді [5]. Після встановлення венозного доступу і провідника місцевий анестетик вводять у шкіру, підшкірну клітковину та кишеню для камери порту. Потім катетер тунелюють від кишені до провідника, який розташовується у центральній вені. Після введення розширювального пристрою катетер встановлюють у проколену вену, а розширювальний пристрій забирають. Надлишкову частину катетера зрізають та приєднують до камери порт-системи. За потреби камеру фіксують до фасції вузловими швами. Шкіра та підшкірна клітковина над камерою порт-системи також ушиваються. Після імплантації обов’язкова верифікація положення кінчика катетера в нижній третині верхньої порожнистої вени. Також для підтвердження необхідно зробити рентгенограму грудної клітки, щоб верифікувати правильне розташування центральної венозної порт-системи та негайно усунути можливі ускладнення [6]. У літературі повідомляється про близько 27 % ускладнень від загальної кількості імплантацій [7]. Незважаючи на те, що процедура здається нескладною в технічному плані, необхідні навички адекватного користування центральною венозною порт-системою, щоб уникнути ускладнень, яких є достатньо.
Загалом протипоказання до імплантації порт-системи зустрічаються рідко. Є повідомлення, що навіть у пацієнтів при тромбоцитопенії така імплантація можлива [8].
Ускладнення встановлення центральних венозних порт-систем поділяються на перипроцедурні ранні (≤ 30 днів після імплантації) і відтерміновані (> 30 днів) [1–3, 9]. Ускладнення можна розділити на незначні та серйозні. Незначні ускладнення — це події, які не вимагають додаткового хірургічного або інтервенційного втручання чи застосування медикаментозної терапії > 24 год, тоді як серйозні ускладнення потребують хірургічного втручання, тривалої медикаментозної терапії, перебування в лікарні > 24 год або навіть можуть призвести до смерті [1–3, 9]. Гемоторакс і пневмоторакс — це, най–імовірніше, серйозні ускладнення, залежно від тяжкості. Повідомляється, що загальний рівень ускладнень становить 7,2–12,5 %, причому інфікування порт-систем є найпоширенішим раннім і пізнім ускладненням [2]. Ускладнення у 5–18 % випадків пов’язані з катетер-асоційованим тромбозом [2, 10], що є відносно поширеним явищем і не обов’язково вимагає експлантації катетера. Це залежить від необхідності центрального доступу, функціонального стану порт-системи, протипоказань до антикоагулянтної терапії і стану хворого. Рішення про антикоагулянтну і можливу тромболітичну терапію приймаються персоналізовано [10]. Перелік ускладнень надано в табл. 1 [1–3, 9].
Наводимо клінічний випадок пацієнтки з онкологічною патологією, у якої встановлення центральної порт-системи для проведення хіміотерапії призвело до ускладнення, що погіршило якість життя.
Клінічний випадок
Хвора, 49 років, госпіталізована 02.08.2021 р. у клінічну лікарню «Феофанія» для другої експертної думки стосовно лікування онкологічної і супутньої патології.
Хворіє з квітня 2021 року, коли виявила утворення в лівій грудній залозі J1M3. Пологів — 0, аборти були. Гормональну контрацепцію заперечує. Спадковий анамнез не обтяжений.
13.04.2021 р. виконана мамографія: у центральному секторі на відстані 4 см від соска візуалізується утворення розміром 16 × 22 мм (пальпується). Діагностична категорія: BI-RADS, ACR: права грудна залоза — 1; с, ліва грудна залоза — 5; с. Візуалізуються пахвові лімфатичні вузли округлої форми до 10 мм.
13.04.2021 р. виконана трепан-біопсія пухлини. ПГЗ + ІГХ № 21SP052258 від 22.04.2021: помірно диференційована (С2) інвазивна карцинома неспецифікованого типу (NST) грудної залози, ER+, PR+, HER-2/neu–, Кі67 — 25 %.
15.04.2021 р. МСКТ ОГК, ОЧП, ОМТ з в/в конт-растом: КТ-ознаки новоутворення лівої грудної залози. КТ-ознак вторинних змін органів грудної, черевної порожнини та малого таза не виявлено. Ангіоліпома (?) лівої нирки.
26.04.2021 р. МР-мамографія: категорія: BI-RADS: права залоза — 1, ліва залоза — 6. Мультицентричний Са лівої грудної залози. Ознак аксилярної лімфаденопатії не виявлено.
08.05.2021 р. УЗД грудних залоз: права грудна залоза — BIRADS 2 (УЗД-знахідка доброякісного характеру). Ліва грудна залоза — BIRADS 6. Відомий гістологічно верифікований Са лівої грудної залози на 6:00 годин, що віддає доріжку інфільтрації до соска та ареоли; додатково виявлено підозрілі зміни на 4:00 години ліворуч, що корелюють з MP-знахідкою від 26.04.2021 року. Праворуч проста кіста на 9:00 годин та інтрамамарний лімфатичний вузол на 8:00 годин. Аксілярні лімфовузли з обох сторін ехографічно не змінені.
11.05.2021 р. остеосцинтиграфія: сцинтиграфічні зміни остеобластичного ураження кісткових структур не визначаються. Тамоксифен 14 днів.
01.06.2021 р. операція: квадрантектомія лівої молочної залози з регіонарною лівобічною аксилярною лімфодисекцією.
Імплантація центральної порт-системи для проведення хіміотерапії в одній із лікарень України.
09.06.2021 р. ПГЗ № 38410-27: інвазивна протокова карцинома молочної залози (G2) NST з ознаками лікувального патоморфозу 1-го ступеня. У лімфатичних вузлах (у 6 з 10) метастази карциноми. 04.06.2021 р. ІГХ № 2018,21: ER+++, PR+++, HER2/neu — негативний, Кі67 — 35 %. ПГЗ № 766/21 (інтраопераційно): краї резекції без пухлинного росту.
16.06.2021 р. НАПХТ в режимі ендоксан + доксорубіцин через центральну порт-систему. З 18.06.2021 р. з’явилися симптоми тетраплегії з вираженим больовим синдромом.
Неврологічний статус: у свідомості, контактна, інструкції виконує. Очні щілини S = D. Зіниці симетричні, фотореакції збережені, слабкість конвергенції. Горизонтальний ністагм переважно при погляді вправо, диплопія відсутня. Тригемінальні та окципітальні точки пальпаторно безболісні. Гіпестезія в латеральній зоні Зельдера справа. Обличчя симетричне. Легка девіація язика вліво. Глотковий рефлекс знижений. М’язова сила у нижніх кінцівках знижена до 3–4 балів. М’язовий тонус підвищений за спастичним типом. Сухожильні та періостальні рефлекси D = S, високі. Симптом Бабінського позитивний двобічний, чіткіший справа. Правобічна гемігіпалгезія. Пальценосову пробу виконує з інтенцією. П’ятково-колінну пробу виконує з інтенцією з двох сторін. Функцію тазових органів контролює. Менінгеальні знаки: немає.
В ургентному порядку проведено МРТ головного мозку, шийного та грудного відділів хребта.
18.06.2021 р. МРТ головного мозку без в/в контра-стування: MP-ознаки церебральної мікроангіопатії (Fazekas І). Потовщення слизової оболонки в лівій камері клиноподібного синуса, у комірках решітчастої кістки.
18.06.2021 р. МРТ шийного відділу хребта: МР-ознаки дегенеративно-дистрофічних змін шийного відділу хребта, ускладнені протрузіями м/х дисків на рівні С4-С5, С5-С6, С6-С7, стенозом хребтового каналу, вказані зміни в спинному мозку можуть відповідати мієлопатії, порушенням статичної функції хребта.
08.07.2021 р. НАПХТ у режимі ендоксан + доксорубіцин 2 к. 08.07.2021 р. після сеансу проведеної хіміотерапії неврологічна симптоматика поглибилася.
22.07.2021 р. введено золадекс.
21.07.2021 р. МРТ головного мозку з в/в контрастуванням: MP-ознаки одиничних патологічних вогнищ паренхіми лівої скроневої частки головного мозку та правої тім’яної кістки. З урахуванням анамнезу більш ймовірно обумовлені вторинним (mts) ураженням. MP-ознаки церебральної мікроангіопатії (Fazekas І).
21.07.2021 р. МРТ шийного та грудного відділів хребта: MP-картина вторинного (mts) ураження хребців шийного відділу хребта; інтрамедулярне пухлинне утворення на рівні С2-С6, з урахуванням анамнезу та вираженої негативної динаміки від 18.06.2021 p., більш імовірно обумовлене вторинним mts-генезом, менш вірогідно secondary primary neoplasm. MP-ознаки дегенеративно-дистрофічних змін шийного та грудного відділів хребта (остеохондроз, спондильоз, спондилоартроз), з наявністю протрузій м/х дисків С4-С5,
С5-С6, С6-С7, Th7-Th8, Th8-Th9, Th9-Th10. Центральний дискогенний стеноз хребтового каналу на рівні С4-С5, С5-С6.
При перегляді дисків МРТ в КЛ «Феофанія»: вогнища в хребцях слід диференціювати між інфарктами та mts. Вогнище в скроневій частці зліва — локалізоване в оболонці — характерне для mts. Вогнище в правій тім’яній частці більш характерне для контрастованої судини. Визначається ділянка мієломаляції спинного мозку на рівні С3-С7 у зоні кровопостачання заблокованої a. vertebralis (рис. 1).
02.08.2021 р. хвора надійшла на обстеження в КЛ «Феофанія».
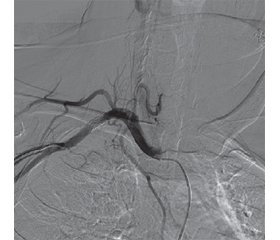
02.08.2021 р. МСКТ-ангіографія грудного відділу аорти і плечоголовних артерій: КТ-ознаки введення порту в праву підключичну артерію. Підозра на тромбоз правої хребцевої артерії (рис. 2, 3).
З огляду на ці обставини пацієнтці було запропоновано оперативне втручання — видалення центральної порт-системи для проведення інфузій з пластикою отвору в артерії.
06.08.2021 р. Черезшкірна транслюмінальна балонна ангіопластика зі стентуванням одиничним стентом і видаленням центральної порт-системи. Це оперативне втручання виконано ендоваскулярно з доступом через праву стегнову артерію і заведенням стент-системи із покриттям 6,0 × 22 мм у ділянці входу катетера порт-системи в підключичну артерію. В асептичних умовах після хірургічного розрізу в правій підключичній ділянці одночасно видалено катетер порт-системи та імплантовано стент-систему (рис. 4–6). Стан пацієнтки після оперативного втручання задовільний.
/99_2.jpg)
Встановлені захворювання (діагноз). Інвазивна протокова карцинома лівої молочної залози неспецифікованого типу ТІ N0M0 (04.2021) G2, ER 95 %(+++), PR 90 % (+++). HER2/neu — негативний, Кі67 — 35 % (люмінальний тип В), ст. І. Стан після операції — квадрантектомії лівої молочної залози з регіонарною аксилярною лівобічною лімфодисекцією від 01.06.2021 р. (урТ1 N2M0) + 2 к. АПХТ (16.06.2021 р. — 08.07.2021 р., ендоксан + доксорубіцин). Prol. morbi: susp. солітарний лептоменінгеальний mts на рівні скроневої частки ліворуч (МРТ від 21.07.2021). Кл. гр. 2.
Супутній: мієлорадикулопатія змішаного (лікарського (хіміотерапія 16.06.2021 р. і 08.07.2021 р.)) та ішемічного (тромбоз правої хребцевої артерії)) генезу з тетрапарезом, порушенням функції тазових органів за центральним типом та атактичними порушеннями зі стійкими, вираженої тяжкості, функціональними порушеннями самообслуговування.
Обговорення
Навіть у досвідчених фахівців встановлення центральних венозних порт-систем (CVAD або Port-A-Cath) можуть викликати труднощі; та й ускладнення можуть виникнути як під час, так й після встановлення доступу. Наразі розглянемо ускладнення, пов’язані з артеріальною пункцією та хибною нерозпізнаною артеріальною канюляцією, що мало місце у наведеному випадку.
Пункція артерій голкою при встановленні порт-систем зустрічається у 3,7–12 %; більш серйозна травма з просуванням дилататора відбувається в 0,1–1,0 % [2]. Порт-системи можна вводити через периферичну вену, внутрішню яремну, пахвові та стегнові вени [3]. Методи, які необхідно використовувати для зменшення ускладнень, — ґрунтовна оцінка пацієнта з попереднім обстеженням судин з використанням УЗД, візуалізація встановлення порт-системи із обов’язковою верифікацією положення кінчика катетера та зображення в режимі реального часу під час встановлення [3].
Для ґрунтовної оцінки судинного доступу з метою запобігання ускладненням рекомендовано використовувати протокол RaCeVa, на якому категорично наполягає і Українська асоціація судинного доступу [18].
Навіть при використанні ультразвуку під час розміщення катетерів може виникнути пошкодження артерії. Під час канюляції вени з використанням ультразвуку візуалізацію кінчика голки можна сплутати з візуалізацією основної частини голки [14].
Це може дати помилкове заспокоєння. Лікар дивиться на УЗД — нібито кінчик голки на екрані, а насправді це ділянка голки, а кінчик голки фактично вже розміщений в артерії. Як варіант, голка може перебувати у вені під контролем УЗД, але потім під час розміщення провідник входить в артерію, оскільки на той момент ультразвук не використовується [14]. Напрацювання практичних навичок може дати досвід відчуття руху голки на цьому етапі. Якщо тримати голку недомінантною рукою і опиратися іншою на пацієнта при виконанні маніпуляції, то можна підвищити стабільність і зменшити ризик переміщення кінчика голки та її міграцію з вени [3].
Положення дистального кінця катетера центральної порт-системи для в/в ін’єкцій має першочергове значення, і його слід перевірити перед початком інфузійної терапії. Слід віддавати перевагу внутрішньопроцедурним методам перевірки розташування кінчика катетера, оскільки вони дозволяють уникнути ризиків, затримок і витрат часу та коштів на зміну положення. На сьогодні використовують 3 методи верифікації положення кінчика катетера: 1) інтраопераційна рентгеноскопія; 2) стандартна трансторакальна чи трансезофагеальна ехокардіографія; 3) внутрішньопередсердна ЕКГ [21]. Кожна з цих методик має свої переваги і недоліки, але будь-яка з них має бути використана при встановленні порт-систем в обов’язковому порядку [3].
Plumhans et al. (2011) порівняли переваги встановлення катетера у внутрішню яремну вену проти пахвових і підключичних на 138 хворих на онкологію та виявили, що сприйняття болю, міграція кінчика катетера, тромбоз, ризик артеріальної пункції були нижчими у пацієнтів, яким проводили катетеризацію через внутрішню яремну вену [19]. У дослідженні, у якому оцінювалося навчання резидентів встановленню порт-систем, було виявлено, що в групах дослідження при виконанні пункцїї підключичної і внутрішньої яремної вени результати були порівнянні, але пункція і катетеризація внутрішньої яремної вени забирала менше часу [20]. Крім того, при розташуванні катетера порт-системи у внутрішній яремній вені виникнення pinch-off синдрому неможливе навіть теоретично [2]. Положення Тренделенбурга значно збільшує розміри внутрішніх яремних вен, що підвищує безпеку процедури [3].
У випадку невпевненості щодо пункції артеріальної судини використовують датчик тиску для оцінки форми венозної/артеріальної хвилі або визначають газовий склад артеріальної чи венозної крові [2].
Якщо під час встановлення порт-системи виявлено факт артеріального доступу, важливим моментом є можливість притиснути місце пункції до щільних тканин (стегнова, плечова кістка). Артеріальний доступ на периферії фіксувати стисненням. Залежно від стану системи коагуляції (наприклад, використання антикоагулянтних препаратів) та розміру і діаметра порт-системи тиск постійно застосовують протягом п’яти і більше хвилин. Наприклад, після встановлення інтродьюсера 6 Fr у загальну стегнову артерію стиснення здійснюють протягом 30 хвилин. Накладання джгута для запобігання утворенню хибних аневризм/гематом може завдати шкоди, викликати ішемію дистальних відділів кінцівки, а також спричинити додаткові кровотечі/гематоми, неврологічні ураження. Усунення пошкоджень артерії при доступі в ділянці шиї або грудної клітки повинно здійснюватися судинним хірургом для безпечної зупинки та профілактики можливої кровотечі [1–3].
У випадку ненавмисного встановлення катетера в артеріальну судину залишення катетера на місці та негайне його видалення з тиском несе певні ризики. Тривала артеріальна катетеризація може призвести до тромбозу, неврологічного дефіциту та гострого інсульту. Негайне видалення аварійного артеріального катетера може призвести до неконтрольованої кровотечі, псевдоаневризми та формування артеріовенозної (AV) фістули, особливо у пацієнтів, які лікуються антикоагулянтами або антиагрегантами [11]. Останні дослідження продемонстрували, що залишення артеріального катетера в місці зі швидким кровотоком несе меншу небезпеку і смертність, ніж видалення катетера з тиском [12, 13]. AV-фістули можна лікувати за допомогою спіралі з контролем Rö-зображення. Псевдоаневризму можна лікувати компресією або застосуванням тромбіну чи спіралі під контролем Rö-зображення. Однак нориці між двома великими судинами (тобто сонною артерією і внутрішньою яремною веною), які не відразу розпізнаються та мають тенденцію зростати з часом, можуть вимагати прямого хірургічного відновлення, як і спроба розміщення спіралі. Ця ендоваскулярна техніка може бути досить складною при високому потоці/високому тиску в системі, що може призвести до катастрофічної спіральної емболізації. На щастя, хірургічне втручання не часто потрібне для відновлення [14]. Оперативне втручання вважається оптимальним для стабільних пацієнтів з невеликим ризиком анестезії; тільки ендоваскулярні втручання вважаються менш ефективними, проте можуть бути більш доцільними при травмі медіальної частини підключичної артерії, наприклад, внаслідок обмеженого хірургічного доступу [1–3].
Якщо ненавмисне введення катетера в артерію не розпізнається, подальші ускладнення можуть виникнути через інфузію в неправильно розташовані катетери. Про рідкісні випадки порушень мозкового кровообігу та неврологічні порушення внаслідок неточно встановлених катетерів і нерозпізнані артеріальні лінії були повідомлення в літературі [15–17]. Що, на жаль, мало місце і в описаному нами клінічному випадку.
Невідкладна медична допомога пацієнтам з онкологією ускладнюється наявністю супутніх захворювань та складністю перебігу хвороби. Лікарі повинні знати, вміти і використовувати найбільш відповідні доступи для внутрішньовенного введення, уникаючи ускладнень та застосовуючи найкращі методики для пацієнтів (Kornbau et al., 2015). Однак повністю усунути ускладнення неможливо, досвід та вміння зменшують їх до мінімуму.
Висновки
1. Встановлення центральних порт-систем для проведення хіміотерапевтичного, парентерального і симптоматичного лікування пацієнтів в онкології є безпечною, малоінвазивною та ефективною процедурою, яка значно покращує якість життя пацієнта і дозволяє уникнути побічних явищ, пов’язаних із інфузією токсичних препаратів. Водночас ця маніпуляція може призводити до негайних і віддалених ускладнень, які вимагають відповідних рішень і можуть погіршувати перебіг захворювання.
2. Для профілактики виникнення ускладнень необхідно суворо дотримуватися правил встановлення порт-систем, щоб максимально їх мінімізувати.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Отримано/Received 08.07.2023
Рецензовано/Revised 17.07.2023
Прийнято до друку/Accepted 26.07.2023
Список литературы
Machat S., Eisenhuber E., Pfarl G., Stübler J., Koelblinger C., Zacherl J., et al. Complications of central venous port systems: a pictorial review. Insights Imaging. 2019 Aug 28. 10. 86. https://doi.org/10.1186/s13244-019-0770-2.
Kornbau C., Lee K.C., Hughes G.D., Firstenberg M.S. Central line complications. Int. J. Crit. Illn. Inj. Sci. 2015 Jul-Sep. 5 (3). 170-178. https://doi.org/10.4103/2229- 5151.164940.
Nancy L. Moureau, editors. Vessel Health and Preservation: The Right Approach for Vascular Access. Springer Open; 2019. 303 p. https://doi.org/10.1007/978-3-030-03149-7.
Simpson K.R, Hovsepian D.M., Picus D. Interventional radiologic placement of chest wall ports: results and complications in 161 consecutive placements. J. Vasc. Interv. Radiol. 2019. 8. 189-195.
Babu S., Bennett J., Binks R., Fee P., Fox B., Johnston A., Association of Anaesthetists of Great Britain and Ireland: safe vascular access 2016. Anaesthesia. 2016. 71(5). 573-85.
Kim D.H., Ryu D.Y., Jung H.J., Lee S.S. Evaluation of complications of totally implantable central venous port system insertion. Exp. Ther. Med. 2019 Jan 18. 17(3). 2013-2018. https://doi.org/10.3892/etm.2019.7185.
Walser E.M. Venous access ports: indications, implantation technique, follow-up, and complications. Cardiovasc. Intervent. Radiol. 2012. 35(4). 751-764. doi: 10.1007/s00270-011-0271-2.
Keulers A.R., Kiesow L., Mahnken A.H. Port implantation in patients with severe thrombocytopenia is safe with interventional radiology. Cardiovasc. Intervent. Radiol. 2018. 41. 80-86. doi: 10.1007/s00270-017-1794-y.
Yong Li, Jianxi Guo, Yanfang Zhang, Jian Kong. Complications from port-a-cath system implantation in adults with malignant tumors: A 10-year single-center retrospective study. Int. Med. 2022. 5. 15-22. https://doi.org/10.1016/j.jimed.2021.12.002.
Wall C., Moore J., Thachil J. Catheter-related thrombosis: a practical approach. J. Intensive Care Soc. 2016. 17. 160-167.
Bowdle A. Vascular complications of central venous catheter placement: Evidence‑based methods for prevention and treatment.
J. Cardiothorac. Vasc. Anesth. 2014. 28. 358‑68.
Guilbert M.C., Elkouri S., Bracco D., Corriveau M.M., Beaudoin N., Dubois M.J. et al. Arterial trauma during central venous catheter insertion: Case series, review and proposed algorithm. J. Vasc. Surg. 2008. 48. 918-25.
Shah P.M., Babu S.C., Goyal A., Mateo R.B., Madden R.E. Arterial misplacement of large‑caliber cannulas during jugular vein catheterization: Case forsurgical management. J. Am. Coll. Surg. 2004. 198. 939-44.
Bhutta S.T., Culp W.C. Evaluation and management of central venous access complications. Tech. Vasc. Interv. Radiol. 2011. 14. 217‑24.
Khouzam R.N., Soufi M.K., Weatherly M. Heparin Infusion through through a central line misplaced in the carotid artery leading to hemorrhagicstroke. J. Emerg. Med. 2013. 45. e87‑9.
Wang R.C., Katz S.E., Lubow M. Visual loss and central venous catheterization: Cortical blindness and hemianopsia after inadvertentsubclavian artery entry. J. Neuroophthalmol. 2000. 20. 32‑4.
Shah P.M., Leong B., Babu S.C., Goyal A.M., Mateo R.B. Cerebrovascular events associated with infusion through arterially malpositioned triple‑lumen catheter: Report of three cases and review of literature. Cardiol. Rev. 2005. 13. 304‑8.
Pittiruti M. RaCeVA: a guide for a rational choice of the most appropriate vein for central venous catheterization. Association for Vascular Access 26th Annual Scientific Meeting. San Antonio; 2012.
Plumhans C., Mahnken A.H., Ocklenburg C., Keil S., Behrendt F.F., Günther R.W. et al. Jugular versus subclavian totally implantable access ports: Catheter position, complications and intrainterventional pain perception. European Journal of Radiology. 2011. 79(3). 338-342. https://doi:10.1016/j.ejrad.2009.12.010.
Matsushima H., Adachi T., Iwata T., Hamada T., Moriuchi H., Yamashita M. et al. Analysis of the Outcomes in Central Venous Access Port Implantation Performed by Residents via the Internal Jugular Vein and Subclavian Vein. Journal of Surgical Education. 2017. 74(3). 443-449. doi: 10.1016/j.jsurg.2016.11.005.
Pittiruti M., La Greca A., Scoppettuolo G. The Electrocardiographic Method for Positioning the Tip of Central Venous Catheters. The Journal of Vascular Access. 2011. 12(4). 280-291. doi: 10.5301/jva.2011.8381.
/98.jpg)
/100.jpg)

/97.jpg)
/99.jpg)
/99_2.jpg)