Журнал «Внутренняя медицина» 5-6(11-12) 2008
Вернуться к номеру
Принципи клінічного застосування та трактування ехокардіографії
Авторы: О.С. Коржелецький, завідувач відділення функціональної та ультразвукової діагностики клінічної лікарні «Феофанія» Державного управління справами, м. Київ
Рубрики: Семейная медицина/Терапия, Терапия
Версия для печати
З усіх, будь-коли створених людиною діагностичних методів досліджень ехокардіографія повною мірою належить до одного з найбільш інформативних методів діагностики серцево-судинної системи (Р.Я. Абдулаєв та ін., 1998). Можливість відтворення і достатня точність методу дозволили широко застосовувати ехокардіографію в практиці досліджень для кількісної оцінки систолічної та діастолічної функції шлуночків, виявлення патології клапанного апарату, визначення розмірів та об’ємів порожнин серця та товщини його стінок (X. Фейгенбаум, 1999).
Новаторські технологічні досягнення в сфері ехокардіографії (трансезофагеальна ЕхоКГ, тривимірна ЕхоКГ, стрес-ЕхоКГ, контрастна ЕхоКГ) розширили уявлення про механізми формування та розвитку патології серця та судин, забезпечили прогрес у вирішенні пріоритетних завдань щодо діагностики ендокардиту, розшарування аорти, а також діагностики та прогнозування перебігу гострого інфаркту міокарда, хронічних форм ішемічної хвороби серця, що значно розширило можливості застосування ехокардіографії в клінічній кардіології (В.Н. Коваленко та ін., 2003; Л.А. Стаднюк та ін., 2004).
I. Фізичні основи ультразвукової візуалізації серця
Ультразвук — це звук із частотою понад 20 000 коливань за 1 секунду (або 20 кГц).
Швидкість поширення ультразвуку в тканинах людини при температурі 37 °С дорівнює 1540 м/с. У гомогенному середовищі хвилі поширюються лінійно. Навіть при незначній різниці щільності між різними середовищами виникає ефект «розподілу фаз» (імпеданс). Ультразвукова хвиля, що доходить до розподілу двох середовищ, може відбитись або пройти через них. При цьому:
1. Кут падіння дорівнює куту віддзеркалення.
2. Через різницю імпедансів середовищ кут заломлення не дорівнює куту падіння.
Співвідношення між кутом падіння (відбивання) та кутом заломлення відображено у формулі:
![]()
де n — акустичний імпеданс, Q — кут між направленням поширення звукової хвилі та перпендикуляром до межі фаз.
Фактори, що впливають на відсоток відбивання ультразвуку:
1. Чим більше різниця акустичного імпедансу середовищ, тим більше відбивання.
2. Кут падіння — чим ближче до 90°, тим більше відбивання.
3. Співвідношення розмірів об’єкту та довжини хвилі — розміри об’єкту повинні бути не менше відсотка довжини хвилі.
Можливість методу для просторового розпізнавання визначає відстань між двома об’єктами, при якому їх ще можна відрізнити. Наприклад, частота 2,0 МГц дає можливість розпізнати об’єкти до 1 мм; однак, чим вища частота, тим менше проникаюча здатність ультразвуку (глибина проникнення), чим легше виникає його затухання. Об’єкти, у яких виникає повне затухання ультразвукових хвиль, або, іншими словами, через які ультразвук не може проникнути, дають після себе акустичну тінь. При дослідженні серця такий ефект справляють кальцифіковані структури та протезовані клапани серця.
Ехокардіографічний датчик — це пристрій, що перетворює електричну енергію на механічну (цифрову) та навпаки. Генерований датчиком сигнал поширюється на деяку відстань, що називається ближньою зоною у вигляді паралельних хвиль, які потім розходяться в так званій дальній зоні. Знаючи швидкість поширення звуку в середовищі та час, за котрий звук пройшов до межі фаз та назад (dt), можна вирахувати відстань між датчиком та цією межею (D):
D = 1540 х dt/2.
II. Принципи оптимальної візуалізації серця
Підсилення, контрастність, яскравість: дотримуватися пропорції між розмірами та яскравістю структур у співвідношенні з їх дійсними розмірами та можливістю віддзеркалювати ультразвук.
Розміри сектора: зменшення розмірів сектора збільшує частоту зміни кадрів.
Фонове підсилення: установлювати достатнє фонове підсилення для візуалізації структур, що слабо відбивають ультразвукові хвилі.
Масштаб: включати в зображення серце та позасерцеві структури; зберігати для загальної оцінки незмінний масштаб: у дорослих з нормальними розмірами серця — глибина 16 см, при кардіомегалії — 20 см.
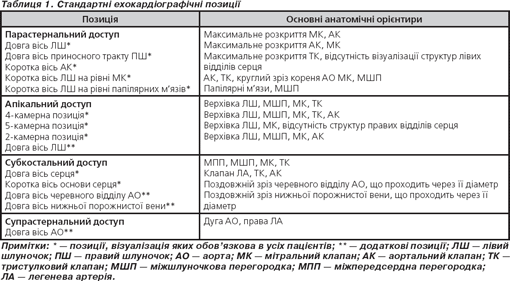
III. Стандартні ехокардіографічні позиції
Стандартні ехокардіографічні позиції — це не стандартні положення ультразвукового датчика, а стандартні відображення структур серця (табл. 1).
Доплерехокардіографія: фізичні принципи та основні виміри
Стосовно кардіології, доплерівський ефект засновується на тому, що при віддзеркаленні ультразвукового сигналу від рухливих об’єктів — еритроцитів, а також стулок клапанів, стінок серця — міняється його частота, тобто виникає зміщення частоти ультразвукового сигналу.
Звуковий сигнал дозволяє точніше направити ультразвуковий промінь, вибрати правильні фільтри. Не можна порівнювати звук, що виникає при доплерівському дослідженні, з аускультативними даними — це явища різного походження.
Імпульсне доплерівське дослідження засноване на використанні ультразвукового сигналу у вигляді окремих серій імпульсів. Датчик посилає серію ультразвукових сигналів та «чекає» їх повернення від еритроцитів у вигляді відбитих сигналів. Місце дослідження кровотоку — пробний (контрольний) об’єм.
Частота повторення імпульсів — це частота, з якою посилаються серії ультразвукових імпульсів (табл. 2). Найбільша швидкість кровотоку, яку можна виміряти методом імпульсної доплер-ехокардіографії, називається межею Нейквіста. При перевищенні цієї межі виникають викривлення спектра. Існування межі Нейквіста — головний недолік імпульсного доплерівського дослідження — неможливість точного виміру високих швидкостей кровотоку.

При дослідженні в постійно-хвильовому доплерівському режимі відбитий ультразвуковий сигнал приймається незалежно від того, коли він був посланий. Отже, досліджується швидкість кровотоку поздовж усього ультразвукового променя. Головна перевага — можливість виміряти будь-які швидкості кровотоку, головний недолік — неможливість точної локалізації місця дослідження кровотоку.
Основні рівняння доплерівської оцінки гемодинаміки (у сучасних сканерах виконується автоматично).
Хвилинний об’єм кровотоку (CO) = 4CC(HR) х ударний об’єм (SV)
Ударний об’єм (SV) = площа перерізу судини х інтеграл швидкості (УТІ)
Інтеграл швидкості (УТІ) = час кровотоку (ЕТ) х середня швидкість (Vmean).
Умови визначення об’єму кровоточу:
1. Площа поперечного зрізу судини визначена там, де і лінійний інтеграл швидкості кровотоку.
2. Доплерівський спектр кровотоку має рівні контури, особливо у фазу прискорення.
3. Кровотік в піддослідній ділянці — ламінарний.
4. Кут між направленням ультразвукового променя та напрямком кровотоку — менше 20°.
5. Площа поперечного зрізу судини не змінюється під час дослідження кровотоку.
Розрахунки градієнту тиску проводяться за допомогою рівняння Бернуллі. Є два способи розрахунків — короткий варіант (швидкості за місцем обструкції до 1,2 м/с) та довгий (швидкості за місцем обструкції перевищують 1,2 м/с).
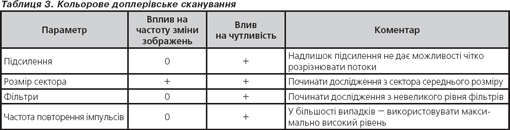
Головна перевага кольорового доплерівського сканування — у швидкому визначенні просторової орієнтації потоків (табл. 3). Кольорове сканування доповнює постійно-хвильове дослідження, тому що дозволяє точніше спрямувати ультразвуковий промінь або внести корективи при неможливості спрямувати промінь паралельно потоку. Головний недолік — відносно низькі розпізнавальні можливості, неможливість вимірювання високих швидкостей.
Найбільше значення кольорове доплерівське сканування має для швидкої оцінки наявності клапанної регургітації та внутрішньосерцевих шунтів (незамінне при діагностуванні уроджених та набутих пороків серця та оцінки роботи протезованих клапанів).
Фактори, що впливають на кольорове відображення потоку:
1. Гемодинамічні: різниця тиску, об’єм кровотоку, ЧСС, переднавантаження та післянавантаження, кінетична енергія потоку.
2. Настройки ехокардіографа.
3. Особливості ехокардіографічних систем: алгоритми розпізнавання тканин, кольорового кодування, усереднення швидкості кровотоку та ін.
Рекомендації із застосування ехокардіографії засновані на кваліфікаційній системі, застосованій у рекомендаціях з ехокардіографії Американського кардіологічного коледжу та Американської асоціації серця (2003).
Класифікація ефективності та доцільності застосування ЕхоКГ:
— клас І — наявність доказів ефективності, доцільності та сприятливої дії ЕхоКГ;
— клас II — спірні докази ефективності, доцільності та сприятливої дії ЕхоКГ;
— клас IIа — чаша терезів схиляється до ефективності та доцільності ЕхоКГ;
— клас IIб — чаша терезів схиляється до неефективності та недоцільності ЕхоКГ;
— клас III — наявність доказів неефективності та недоцільності ЕхоКГ.
Рівні ЕхоКГ-оцінки:
— технічні можливості (адекватність обладнання та особливості проведення дослідження);
— діагностична цінність (чутливість, специфічність та точність у кожному конкретному випадку);
— влив на діагностичні та прогностичні рішення (залежить від рівня підтвердження та важливості підтвердження у кожній конкретній ситуації);
— вплив на лікувальну тактику;
— наслідки, пов’язані зі здоров’ям.
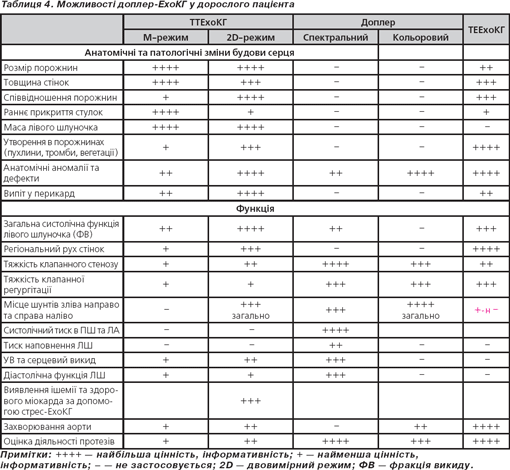
Для аналізу були застосовані такі методики ЕхоКГ: одномірна ЕхоКГ (М-режим); двомірна трансторакальна ЕхоКГ (ТТЕхоКГ), доплер-ЕхоКГ (спектральний та кольоровий режим) (табл. 4) та, за наявності показань, трансезофагеальна ЕхоКГ(ТЕЕхоКГ).
Шуми та клапанні захворювання серця
ЕхоКГ особливо показана у пацієнтів при оцінці серцевих шумів, стенозів та регургітацій, функціонування протезованих клапанів та у хворих з інфекційним ендокардитом. ЕхоКГ надає інформацію щодо діагнозу, морфології клапанів, етіології захворювань клапанів, ідентифікації та кількісної оцінки уражень, визначення супутніх захворювань, параметрів та функції серця, адекватності компенсації шлуночків (J.C.H. Atlenhofer et al., 2000). ЕхоКГ дозволяє виявити структурні порушення, такі як фіброз, кальцифікація, тромби, вегетації; порушення рухливості клапанів, такі як нерухливість, флотація або пролабування стулок, порушення в протезованих клапанах. Повна ЕхоКГ-оцінка повинна забезпечити лікуючого лікаря як діагностичною, так і прогностичною інформацією, дозволяючи стратифікувати ризик, визначити вихідні дані для подальших досліджень і допомогти зорієнтуватись у виборі лікувальних підходів.
Рекомендації з проведення ЕхоКГ при оцінці серцевих шумів
Клас I
1. Пацієнт із шумом та кардіореспіраторною симптоматикою.
2. Пацієнт із шумом без клінічних симптомів, у якого клінічні данні дозволяють запідозрити можливість того, що шум відображає наявність органічного захворювання серця.
Клас IIа
1. Пацієнт без клінічних симптомів, із низькою можливістю серцевого захворювання, але наявність серцевого захворювання не може бути вірогідно виключена за допомогою стандартного клінічного обстеження серцево-судинної системи.
Клас III
1. Дорослий пацієнт без клінічних симптомів, серцевий шум якого досвідчений дослідник оцінює як функціональний або гемодинамічно не значимий.
Цілі ЕхоКГ при оцінці серцевих шумів
1. Виявити первісне вогнище ураження та його причину, визначити його тяжкість, ступінь тяжкості.
2. Визначити параметри гемодинаміки.
3. Виявити супутні відхилення.
4. Виявити ураження, вторинні стосовно первісного ураження.
5. Оцінити параметри та функцію серця.
6. Визначити орієнтири для подальших досліджень.
7. Повторно оцінити параметри пацієнта після лікування.
Рекомендації із застосування ЕхоКГ при клапанних стенозах
Клас І
1. Діагностика; оцінка гемодинамічної тяжкості.
2. Оцінка розмірів, функції та гемодинаміки ЛШ та ПШ.
3. Повторне обстеження пацієнтів із наявним клапанним стенозом при зміні симптоматики або показників.
4. Оцінка змін гемодинамічної тяжкості та шлуночкової компенсації у пацієнтів із наявним клапанним стенозом, під час вагітності.
Клас IIа
1. Оцінка гемодинамічної значимості клапанного стенозу легкої/середньої тяжкості методом стрес-ЕхоКГ.
2. Повторне обстеження пацієнтів.
Стандартні вимоги при проведенні ехокардіографічного дослідження
Загальні вимоги
Під час дослідження з парастернального та апікального доступу пацієнт знаходиться в положенні лежачи на лівому боці; під час субкостального, супрастернального та правого парастернального доступу — лежачи на спині. Реєстрація моніторного відведення електрокардіограми обов’язкова на всіх етапах дослідження. Бажано, щоб глибина сканування під час усього дослідження дорівнювала 16 см для дорослих. Для оптимальної візуалізації передсердь з апікального доступу та для досліджень серця з субкостального або супрастернального доступу необхідна корекція глибини сканування. Швидкість зображення в М-модальному режимі — 50 мм/с, у доплерівському режимі — 100 мм/с. Для реєстрації впливу фаз дихання на внутрішньосерцеві кровотоки швидкість розгортання доплерівського спектра зменшують до 25 мм/с. Бажана реєстрація на зовнішні носії (відеоплівка або CD-, DVD-диски) не менше 15 послідовних серцевих циклів на фоні затримки дихання кожного з етапів дослідження. Для контрастування правих відділів серця та підсилення тристулкової регургітації або наявності дефекту міжпередсердної перегородки (ASD) використовують контрастування за рахунок внутрішньовенного введення фізіологічного розчину з бульбашками повітря.
Алгоритм проведення стандартної ехокардіографії
Двовимірне та М-модальне дослідження
1. Парастернальний доступ, довга вісь лівого шлуночка (дослідження у двовимірному режимі):
— права коронарна та некоронарна стулки аортального клапана повинні бути добре візуалізовані, переріз повинен проходити так, щоб виносний тракт ЛШ мав максимальний розмір;
— для правильної оцінки розмірів міжшлуночкової перегородки в поле зображення не повинні попадати парасептальні структури;
— для кращої візуалізації мітрального клапана — в цей переріз не повинні попадати папілярні м’язи та хорди.
2. Парастернальний доступ, коротка вісь на рівні аортального клапана (дослідження у двовимірному режимі):
— отримання оптимального зображення стулок АК;
— отримання оптимального зображення тристулкового клапана;
— отримання оптимального зображення клапана легеневої артерії та ствола ЛА з її біфуркацією.
Дослідження в М-модальному режимі:
— отримання оптимального зображення аорти, лівого передсердя;
— отримання оптимального зображення кореня АО та стулок АК.
3. Парастернальний доступ — коротка вісь ЛШ на рівні МК (двовимірне та М-модальне дослідження на рівні МК).
4. Парастернальний доступ — коротка вісь ЛШ на рівні папілярних м’язів (двовимірне та М-модальне дослідження):
— якщо дослідження по короткій вісі ЛШ з парастернального доступу технічно ускладнено, його треба замінити дослідженням по короткій вісі з субкостального доступу.
5. Апікальний доступ:
— 4-камерна позиція: оптимальна візуалізація ЛШ;
— 2-камерна позиція: оптимальна візуалізація ЛШ;
— 4-камерна позиція: оптимальна візуалізація лівого передсердя (ЛП);
— 2-камерна позиція: оптимальна візуалізація ЛП;
— 4-камерна позиція: оптимальна візуалізація ПШ;
— 4-камерна позиція: оптимальна візуалізація правого передсердя (ПП);
6. Субкостальний доступ: двовимірне дослідження нижньої порожнистої вени в спокої та під час форсованого дихання.
Доплерехокардіографія
1. Парастернальний доступ, довга вісь лівого шлуночка: Кольорове сканування — переміщення сектора кольорового картування по екрану. При знаходженні патологічних потоків — запис їх на зовнішній носій з використанням імпульсного та постійно-хвильового режиму. Якщо патологічні потоки не виявлені — обмежитися записом кровотоку у виносному тракті з ЛШ.
2. Парастернальний доступ, коротка вісь на рівні аортального клапана:
— кольорове сканування кровотоку через клапан легеневої артерії;
— дослідження кровотоку в ЛА в імпульсному режимі;
— дослідження кровотоку в ЛА в постійно-хвильовому режимі та виміри інтегралу його лінійної швидкості;
— кольорове сканування кровотоку через аортальний клапан для виявлення аортальної регургітації;
— кольорове картування та постійно-хвильове дослідження кровотоку через тристулковий клапан.
3. Парастернальний доступ — коротка вісь правого шлуночка:
— кольорове картування на рівні приносного тракту ПШ;
— при виявленні регургітації на ТК — реєстрація її в постійно-хвильовому режимі.
4. Апікальний доступ, 4-камерна позиція:
— кольорове картування на рівні мітрального клапана;
— імпульсний режим: запис кровотоку через МК у місці, де він найбільший (у більшості випадків — місце змикання стулок МК);
— при виявленні регургітації на МК — реєстрація її в постійно-хвильовому режимі.
5. Апікальний доступ, 5-камерна позиція:
— кольорове картування на рівні виносного тракту ЛШ;
— імпульсний режим: запис кровотоку у виносному тракті ЛШ. Контрольний об’єм у виносному тракті ЛШ має бути розташовано в місці, де візуалізується змикання стулок АК, а не розкриття стулок АК;
— постійно-хвильовий режим — реєстрація кровотоку у виносному тракті ЛШ;
— одночасна реєстрація кровотоку у виносному тракті ЛШ та кровотоку через МК у постійно-хвильовому режимі (для вимірювання часу ізоволюметричного розслаблення ЛШ).
6. Апікальний доступ, 4-камерна позиція:
— кольорове картування на рівні приносного тракту ПШ;
— при виявленні регургітації на ТК — реєстрація її в постійно-хвильовому режимі.
Параметри кількісної оцінки двовимірної ехокардіографії:
— кінцево-діастолічний об’єм лівого шлуночка (КДО ЛШ);
— кінцево-систолічний об’єм лівого шлуночка;
— кінцево-діастолічний індекс лівого шлуночка;
— кінцево-систолічний індекс лівого шлуночка;
— середня товщина міокарда (або товщина задньої стінки ЛШ та товщина міжшлуночкової перегородки ЛШ);
— маса міокарда (можлива маса лівого шлуночка — ММЛШ);
— індекс маси міокарда;
— відношення КДО ЛШ до ММЛШ;
— напруження на стінку ЛШ;
— фракція викиду ЛШ (ФВ ЛШ);
— ударний об’єм;
— хвилинний об’єм;
— серцевий індекс;
— максимальний (кінцево-систолічний) об’єм лівого передсердя.
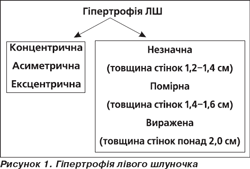
Лівий шлуночок
Нормальні значення кінцево-діастолічного об’єму лівого шлуночка розраховані за трьома алгоритмами (табл. 5).
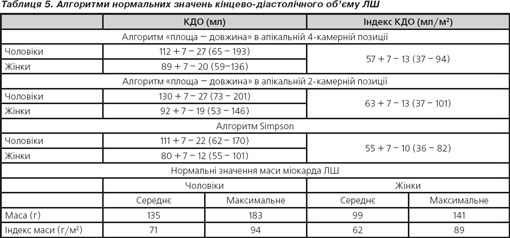
Іноді, хоча товщина стінок дилатованого ЛШ і не перевищує 1,1 см, але збільшення маси міокарда ЛШ дозволяє говорити про гіпертрофію ЛШ. Збільшення відношення КДО до маси ЛШ понад 1,1 мл/г свідчить про те, що гіпертрофія ЛШ не може компенсувати збільшення його об’єму.
Дилатаційна кардіоміопатія
Можна запідозрити застійну (дилатаційну) кардіоміопатію у зв’язку:
— з дифузною гіпокінезією та дилатацією ЛШ;
— дифузною гіпокінезією та дилатацією ЛШ при нормальній товщині його стінок;
— дифузною гіпокінезією та дилатацією ЛШ при нормальній товщині його стінок, збільшенні лівого передсердя;
— дилатацією всіх камер серця, що свідчить про приєднання до патологічного процесу правого шлуночка.
Порушення глобальної скоротливості лівого шлуночка пов’язано:
— з первинним ураженням міокарда;
— ішемічною хворобою серця;
— довготривалим гіпердинамічним станом;
— некомпенсованим пороком серця.
Сферична форма дилатованого ЛШ вказує на давній патологічний процес. При М-модальному дослідженні можна запідозрити ознаки зниження ударного об’єму ЛШ:
— при збільшенні відстані від Е-піку руху передньої стулки мітральпого клапана до міжшлуночкової перегородки (понад 5 мм);
— зменшенні амплітуди руху кореня аорти (менше 7 мм);
— зменшенні розкриття незмінних стулок аортального клапана;
— зменшенні розкриття незмінних стулок мітрального клапана.
Діастолічна дисфункція лівого шлуночка
При доплерівському дослідженні трансмітрального кровотоку виявлено:
1) нормальне співвідношення між раннім діастолічним наповненням лівого шлуночка та передсердною систолою;
2) перевагу наповнення лівого шлуночка під час передсердної систоли над раннім діастолічним наповненням. Цей тип кровотоку свідчить про зниження піддатливості ЛШ та нормальний кінцево-діастолічний тиск в ЛШ;
3) перевагу наповнення лівого шлуночка під час передсердної систоли над раннім діастолічним наповненням (урахування віку пацієнта: похилий вік — варіант норми);
4) значну перевагу раннього діастолічного наповнення, різкий спад швидкості раннього діастолічного наповнення та зменшення часу ізоволюметричного розслаблення ЛШ. Ці зміни свідчать про збільшення діастолічного тиску в ПШ.
Гіпертрофічна кардіоміопатія
Асиметрична гіпертрофія ЛШ. Локалізація ділянки гіпертрофії міокарда:
1. Типова: а) базальні сегменти міжшлуночкової перегородки; б) базальні передньо-перегородкові сегменти.
2. Атипова: а) верхівка; б)задня стінка; в) бокова стінка.
Гіпертрофічна кардіоміопатія може бути:
1) з обструкцією виносного тракту лівого шлуночка в стані спокою;
2) з латентною обструкцією виносного тракту лівого шлуночка:
а) при проведенні проби Вальсальви;
б) інгаляції амілнітрату;
в) фізичному навантаженні.
Рестриктивна кардіоміопатія
Рестриктивну кардіоміопатію можна підозрювати на підставі виявлення нормальних розмірів лівого шлуночка, збільшеного лівого передсердя та нормальної, незначно зниженої, помірно зниженої, різко зниженої — глобальної скоротливості міокарда ЛШ.
Можна запідозрити зв’язок рестриктивної кардіоміопатії та змін, пов’язаних з цукровим діабетом.
Підвищена ехогенність міокарда ЛШ дозволяє запідозрити інфільтративне ураження серця, наприклад — амілоїдоз.
Порушення локальної скоротливості лівого шлуночка
Парадоксальний рух міжшлуночкової перегородки може бути пов’язаний:
— з блокадою лівої ніжки пучка Гіса;
— синдромом передчасного збудження шлуночків;
— констриктивним перикардитом;
— об’ємним перевантаженням правого шлуночка;
— електростимуляцією правого шлуночка.
Етіологія порушень локальної скоротливості ЛШ з урахуванням клініки:
— пов’язані з інфарктом міокарда вказаної локалізації;
— пов’язані з ішемією або інфарктом міокарда вказаної локалізації;
— пов’язані з нестійкою ішемією міокарда вказаної локалізації;
— є проявом гібернованого міокарда (життєздатного міокарда, що перебуває під дією постійної ішемії);
— пов’язані з ураженням міокарда не ішемічного генезу.
Покращення скоротливості вказаних сегментів (після приймання нітрогліцерину; на фоні введення добутаміну; спонтанно, під час дослідження) свідчить, що діагностовано ішемію нестійку (що минає) вказаних сегментів міокарда.
Стоншення стінок та більш яскрава ехоструктура сегментів з порушенням скоротливості свідчать про рубцеві зміни ЛШ.
Наявність регіональної акінезії та дифузної гіпокінезії ЛШ дає підставу запідозрити ішемічну кардіоміопатію.
У більшості випадків порушення локальної скоротливості ЛШ є проявом ішемічної хвороби серця, однак не можна виключити первинне ураження міокарда за типом ідіопатичної дилатаційної кардіоміопатії або міокардиту.
Правий шлуночок
Об’єм:
— збільшення:
1) незначне;
2) помірне;
3) значне: а) займає верхівку серця; б) поділяє верхівку серця з лівим шлуночком.
— зменшення: а) прояви гіповолемії; б) зменшення переднавантаження; в) порушення його кровонаповнення.
Непрямі ознаки інфаркту правого шлуночка:
— збільшення розмірів ПШ;
— розширення нижньої порожнистої вени;
— зменшення амплітуди руху базальних відділів ПШ може свідчити про інфаркт ПШ.
Аритмогенна дисплазія правого шлуночка
Ураховуючи наявність пароксизмальної шлуночкової тахікардії та сімейний анамнез пацієнта, виявлення ізольованої дилатації правого шлуночка, аневризми вільної стінки ПШ, гіперплазії модераторного пучка з великою кількістю прикріплень до вільної стінки ПШ дає підставу запідозрити аритмогенну дисплазію ПШ.
Ехокардіографічний спосіб визначення тиску в легеневій артерії (ТЛА)
Позиції та виміри:
1) потік трикуспідальної регургітації в постійно-хвильовому режимі;
2) оцінка діаметра нижньої порожнистої вени та її реакція на фази дихання;
3) при недостатньо чіткій реєстрації потоку трикуспідальної регургітації — збільшення її внутрішньовенним контрастуванням правих відділів серця.
Розрахунки:
— тиск у правому передсерді прийняти рівним 5 або 15 мм рт.ст. (залежно від реакції нижньої порожнистої вени);
— систолічний ТЛА = систолічний тиск у ПШ = транскуспідальний градієнт + тиск у правому передсерді.
Передсердя
Міжпередсердна перегородка
1. Випуклість МПП у бік лівого передсердя — значне підвищення тиску в правому передсерді.
2. Парадоксальний рух МПП — вирівнювання тиску між передсердями.
3. Відкрите овальне вікно — до 20–25 % здорових людей. Але може бути причиною парадоксальної емболії.
Нижня порожниста вена
1. Нижня порожниста вена не збільшена в розмірах, адекватно реагує на фази дихання, що дає підставу вважати тиск у правому передсерді не більше 5 мм рт.ст.
2. Зменшення діаметра нижньої порожнистої вени — гіповолемія.
3. Нижня порожниста вена розширена, після глибокого вдиху зменшується до 50 % — тиск у ПП приблизно 15 мм рт.ст.

Мітральний клапан
Патологічні зміни МК можуть бути пов’язані з такими факторами:
— пролапс МК;
— ревматичне ураження стулок МК;
— розрив хорд;
— бактеріальний ендокардит;
— кахектичний ендокардит;
— кальциноз мітрального кільця;
— уроджений порок МК;
— карциноїдний синдром;
— міксома;
— механічна травма;
— неспецифічні зміни стулок МК.
Мітральний стеноз
Ступінь тяжкості визначається як:
— незначна (площа отвору МК понад 2,0 см2);
— невелика (площа отвору МК 1,6–2,0 см2);
— помірна (площа отвору МК 1,1–1,5 см2);
— значна (площа отвору МК 0,8–1,0 см2);
— критична (площа отвору МК менше 0,8 см2).
Методи виявлення:
1) якісна оцінка площі мітрального отвору;
2) за результатами планіметричного виміру площі отвору;
3) за результатами доплерівського дослідження трансмітрального кровотоку.
Мітральна недостатність
Ступінь тяжкості визначається як:
— незначна (регургітація в межах стулок МК);
— невелика (регургітація доходить до 1/3 довжини лівого передсердя);
— помірна (регургітація доходить до 2/3 довжини ЛП);
— значна (регургітація до кінця ЛП).
Аортальний клапан
Етіологія аортальної недостатності:
— не встановлена;
— уроджений порок серця — двостулковий АК;
— ревматичне ураження клапана;
— неспецифічні дегенеративні зміни клапана;
— бактеріальний ендокардит;
— кахектичний ендокардит;
— пролапс АК;
— захворювання сполучної тканини;
— патологія корня АО;
— механічне ураження протезованого клапана;
— дисфункція протезованого клапана.

Методи оцінки ступеня тяжкості:
1. Дослідження часу напівспадання тиску при постійно-хвильовому дослідженні аортальної регургітації.
2. Доплерівське дослідження кровотоку в низхідному відділі аорти та черевному відділі аорти.
3. Вимір діаметра потоку регургітації при кольоровому скануванні.
Етіологія аортального стенозу:
— не встановлена;
— уроджений порок серця — двостулковий АК;
— ревматичне ураження клапана;
— неспецифічні дегенеративні зміни клапана.
Аневризма аорти з ознаками розшарування:
— виявлення структури, можливо, ділянки відшарування інтими;
— виявлення структури, можливо, несправжнього каналу, виповненого тромботичними масами;
— форма та локалізація дилатації аорти;
Можливе поширення: висхідний відділ АО, дуга АО, низхідний відділ АО, черевний відділ АО, корінь АО.
Може супроводжуватись: аортальною недостатністю, сепарацією листків перикарду з наявністю випоту в перикард, ознаками гострого інфаркту міокарда.
Тристулковий клапан
Недостатність тристулкового клапана
Ступінь тяжкості визначається як:
— незначна (регургітація в межах стулок ТК);
— невелика (регургітація доходить до 1/3 довжини правого передсердя);
— помірна (регургітація доходить до 2/3 довжини ПП);
— значна (регургітація до кінця ПП).
Може бути пов’язана: з правошлуночковою недостатністю, легеневою гіпертензією, клапанною патологією, з наявністю зонду-електроду в правому шлуночку; також вона має функціональний характер.
Перикард
Випіт у порожнині перикарда та сепарації його листків.
Об’єм:
1) невеликий (до 100 мл);
2) середній (до 500 мл);
3) великий (понад 500 мл).
Виявлений невеликий ехо-негативний простір попереду правого шлуночка може бути ділянкою епікардіальної жирової тканини.
Тампонада серця
Ознаки:
— зменшення розмірів правого шлуночка;
— наявність великої кількості випоту в перикард;
— колабування правого передсердя внаслідок стискання його випотом у перикард, але при нормальних розмірах правого шлуночка та нормальній реакції нижньої порожнистої вени на фази дихання свідчить проти тампонади серця.
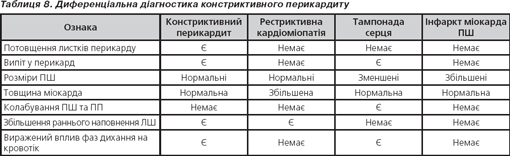
Тампонада серця, констриктивний перикардит
Розширення нижньої порожнистої вени з наявністю:
— випоту в порожнину перикарда — ознаки тампонади серця;
— потовщення листків перикарду — ознаки констриктивного перикардиту.
Колабування правого шлуночка на вдиху з наявністю:
— випоту в порожнину перикарда — ознаки тампонади серця;
— потовщення листків перикарду — ознаки констриктивного перикардиту.
Виражена залежність параметрів внутрішньосерцевого кровотоку від фаз дихання з наявністю:
— випоту в порожнину перикарда — ознаки тампонади серця;
— потовщення листків перикарду — ознаки констриктивного перикардиту.
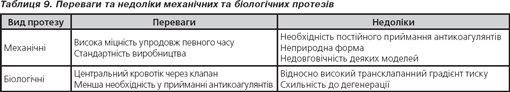
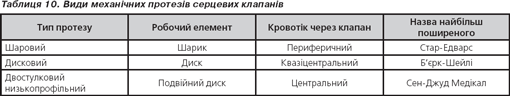
Протезовані клапани серця
Діагностичні можливості окремих видів ехокардіографії при дослідженні протезованих клапанів серця
М-модальна:
— амплітуда розкриття клапана;
— часові інтервали розкриття/закриття клапана.
Двовимірна:
— рух та структура клапана;
— великі тромби та вегетації;
— обструкція виносного тракту лівого шлуночка;
— ураження стінок серця протезованим клапаном.
Імпульсне та постійно-хвильове доплерівське дослідження:
— виявлення клапанної регургітації;
— швидкість кровотоку через клапан та трансклапанний градієнт тиску;
— розрахунок ефективної площі отвору клапана.
Кольорове картування:
— вивчення кровотоку через клапан;
— напівкількісна оцінка тяжкості клапанної регургітації;
— диференційна діагностика клапанної та біляклапанної регургітації.
Черезстравохідна ехокардіографія:
— перевага у візуалізації структури та руху клапана;
— виявлення тромбів та вегетацій невеликих розмірів;
— якісна та напівкількісна характеристика клапанної регургітації.
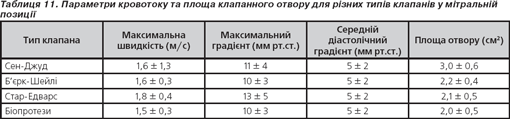
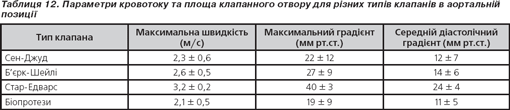
При проведенні обстеження пацієнтів з протезованими клапанами:
1. Структура протеза незмінна; при доплерівському дослідженні швидкості кровотоку через клапан відповідають нормативним вимогам для цього типу протезу; гемодинамічно позначеної регургітації не виявлено — нормально функціонуючий протез.
2. Трансклапанний градієнт тиску перевищує норму для даного типу та розміру протезу. Це може бути обумовлено такими факторами:
а) високий серцевий викид;
б) неадекватний розмір протезу;
в) дисфункція протезу.
3. Виявлена патологія протезу:
а) обструкція клапанного отвору;
б) зміщення опорного кільця;
в) поява біляклапанної регургітації;
г) гемодинамічно позначена трансклапанна регургітація;
д) бактеріальний ендокардит;
е) потовщення стулок біопротезу;
ж) розрив стулки біопротезу.
4. Виявлені ознаки бактеріального ендокардиту з ураженням протезу у вигляді:
а) вегетацій на клапані;
б) біляклапанної регургітації;
в) зміщення опорного кільця;
г) абсцес клапанного кільця.
Серцеві структури, що помилково можуть бути прийняті за патологічні утворення (тромби, пухлини, вегетації)
Ліве передсердя:
— тканини, що відокремлюють легеневі вени від вушка ЛП;
— трабекуляції в ЛП;
— ліва коронарна артерія;
— аневризма міжпередсердної перегородки;
— рудиментарна заслінка овального вікна.
Праве передсердя:
— сітка Хіарі, євстахіїв клапан (клапан нижньої порожнистої вени);
— рудиментарна заслінка типу sinus venosus;
— вушко ПП;
— тканини, що відокремлюють коронарний синус та верхню порожнисту вену;
— накопичення жирових тканин у міжпередсердній перегородці (ліпоматоз);
Лівий шлуночок:
— папілярні м’язи;
— несправжні хорди;
— трабекуляції.
Аортальний клапан:
— вузлики в місці змикання стулок клапана (вузлики Арентіуса).
Мітральний клапан:
— нормальні або подовжені хорди
— нерівні краї (зубці) стулок клапана.
Протезовані клапани:
— шовний матеріал клапанного кільця.
Уроджені пороки серця у дорослих
Пороки, що частіше зустрічаються; вірогідність дожити до дорослого віку велика:
Пороки без ціанозу, без шунта:
— двостулковий аортальний клапан;
— коарктація аорти;
— стеноз клапана легеневої артерії.
Пороки без ціанозу, з шунтом зліва направо:
— дефект міжпередсердної перегородки типу ostium secundum;
— відкритий артеріальний (боталлов) протік;
— рестриктивний дефект міжшлуночкової перегородки (з високим градієнтом тиску між шлуночками).
Пороки, що частіше зустрічаються, вірогідність дожити до дорослого віку низька:
— нерестриктивний дефект міжшлуночкової перегородки (без високого градієнту тиску між шлуночками);
— тетрада Фалло.
Пороки, що рідко зустрічаються, вірогідність дожити до дорослого віку велика:
Пороки без ціанозу, без шунта з ураженням лівих відділів серця:
— уроджена мітральна регургітація;
— уроджений субаортальний стеноз;
— чотиристулковий аортальний клапан.
Пороки без ціанозу, без шунта з ураженням правих відділів серця:
— аномалія Ебштейна;
— аномалія Ула (аплазія або гіпоплазія міокарда ПШ);
— ідіопатічна дилатація стовбура легеневої артерії;
— недостатність ЛА;
— підклапанний стеноз ЛА;
— надклапанний стеноз ЛА.
Пороки без ціанозу, з шунтом зліва направо:
— дефект міжпередсердної перегородки типу ostium primum;
— дефект міжпередсердної перегородки типу sinus venosus;
— часткове аномальне впадання легеневих вен у праве передсердя або порожнисту вену;
— аневризма синусу Вальсальви;
— коронарна артеріовенозна фістула.
Ціанотичні пороки з внутрішньолегеневим шунтом:
— уроджена легенева артеріовенозна фістула.
Інші:
— sinus inversus або situs solitus з декстрокардією;
— уроджена повна атріовентрикулярна блокада;
— уроджена коригована транспозиція магістральних артерій;
— аномальне впадання порожнистої вени в ліве передсердя.
Вибір місця дослідження кровотоку для визначення об’єму внутрішньосерцевого шунтування крові:
— дефект міжпередсердної перегородки — тристулковий клапан, легенева артерія, мітральний клапан, аорта;
— дефект міжшлуночкової перегородки — мітральний клапан, легенева артерія, тристулковий клапан, аорта;
— відкритий артеріальний протік — мітральний клапан, аорта, тристулковий клапан, легенева артерія.
Оперовані уроджені пороки серця (залишкові явища):
— двостулковий аортальний клапан (коарктація аорти);
— розщеплений мітральний клапан;
— залишкова обструкція виносного тракту лівого або правого шлуночка;
— недостатність атріовентрикулярних клапанів (операція Фонтена з приводу атрезії тристулкового клапана або єдиного шлуночка);
— артеріальна гіпертензія (коарктація аорти) та легенева гіпертензія (шунтування крові зліва направо);
— неспроможність правого (транспозиція магістральних артерій) або загального шлуночка виконувати функцію лівого шлуночка, довготривале перевантаження шлуночка тиском або об’ємом, довготривала дія гіпоксемії або еритроцитоза.
Оперовані уроджені пороки серця (наслідки операцій):
— механічні ураження шлуночків (вентрикулотомія);
— порушення ритму та проведення серця: передсердні аритмії, слабкість синусового вузла (закриття ASD або операція Мастарда), блокада правої або передньої гілки лівої ніжки пучка Гіса (закриття VSD), шлуночкові порушення ритму та порушення внутрішньошлуночкового проведення після вентрикулотомії;
— клапанна патологія: клапанна недостатність (вальвіотомія), мітральна недостатність або стеноз (реконструктивні операції на розщепленому МК);
— ушкодження протезних матеріалів: дефекти заплат, загин, перекручування, обструкція шунтів, дисфункція протезованих клапанів.
1. Acquatella H., Rodriguez-Salas L.A., Comez-Mangebo J.R. Doppler echocardiographi in dilated and restrictive cardiomyopathies // Cardiol. Clin. — 1990. — 8. — 349.
2. Appleton C.P., Hatle L.K., Popp R.L. Relation of transmitral flow velocity patterns to left ventricular diastolic function: new insights from a combined hemodynamic and Doppler echocardiographic study // J. Am. Coll. Cardiol. — 1998. — 12. — 426.
3. Bacal F., Stolf N.A., Viega V.S. et al. // Arg. Bras. Cardiol. — 2001. — 76(1). — 29-42.
4. Derumeaux G., Redonnet M., Souer R. et al. // J. Am. Heart Lung. Transplant. — 1998. — 17(3). — 259-67.
5. Hauser M., Gibson B.S., Wilson N. // Eur. J. Pediatr. — 2001. — 160(10). — 607-10.
6. Himmelman R.B., Chung W.S., Chernoff D.M., Hollander H. Cardiac manifestation of human immunodeficiency virus infection: a two — dimensional ehocardiografic studu // J. Am. Coll. Cardiol. — 1990. — 13. — 1030.
7. Sasson Z., Rakowski H., Wigie E.D., Popp R. Echocardiographic and Doppler studies inhypertrophic cardiomyopathy // Cardiol. Clin. — 1990. — 8. — 217.
8. Schiller N.B., Shan P.M., Cawford M. et al. Recommendation for quantitation of the left ventricle by two — dimensional echocfrdiography. American Society of Echocardiography Committee on Standards, Subcommittee on Quantitation of Two — Dimensional Echocardiograms // J. Am. Soc. Echo. — 1989. — 2. — 358.
9. Simonson J.S., Schiller N.B. Descent of the base of the left ventricle: an echographic — index of left ventricular function // J. Am. Soc. Echo. — 1989. — 2. — 25.
10. Smart S.C., Knickelbine T., Malic F., Sagar K.B. // Circulation. — 2000. — 101(3). — 258-63.
11. Mondillo S., Agricola E., Ammaturo T. et al. // Can. J. Cardiol. — 2001. — 17(5). — 571-7.
12. Marwick T.H., Case C., Sawada S. et al. // Hypertension. — 2002. — 39(6). — 1113-8.
13. Contigiani L., Colletta C., Bigi R. et al. // Am. J. Сardiol. — 2003 Apr 15. — 91(8). — 941-5.
14. Geleijnse M.L., Vigna C., Kasprzak J.D. et al. // Eur. Heart J. — 2000. — 21(20). — 1666-73.
15. Yanic A., Yetcin E., Senen K. et al. // Coron. Artery Dis. — 2004. — 11(7). — 545-8.
