Резюме
Актуальність. Поширеність анкілозуючого спондиліту (АС), що значно частіше розвивається у віці 20–30 років, серед населення сягає 0,3 %. Виділяють дві форми АС — дитячу і дорослу, залежно від віку дебюту захворювання. Діагностика ювенільного АС (ЮАС) належить до найбільш актуальних проблем у педіатричній ревматології, при цьому еволюція даного захворювання в дорослому віці залишається невивченою. Існує віковий диморфізм уражень центральної (ЦНС) і периферичної нервової системи (ПНС), але у хворих з ЮАС та в решти випадків він нез’ясований. Мета дослідження: вивчити у хворих на АС частоту й характер окремих клінічних ознак уражень ЦНС та ПНС, оцінити їх особливості при захворюванні, що почалося в дитячому й дорослому віці. Матеріали та методи. Обстежено 217 хворих на АС (193 чоловіки і 24 жінки), середній вік яких — 38 років. Швидкопрогресуючий перебіг констатований у 21 % спостережень, помірний і високий ступінь активності — в 79 %, ІІ–ІІІ стадія — у 82 %, поліартрит — в 65 %. ЮАС відзначено в 16 % випадків (усі хлопчики), у яких ІІІ стадія спостерігалась удвічі частіше, аніж в інших пацієнтів. Результати. Зміни ПНС спостерігаються в 4,9 раза частіше у хворих на ЮАС, а ЦНС — у 2 рази рідше, ніж у випадках дебюту захворювання в дорослому віці, при цьому в пацієнтів 1-ї групи тяжкість ураження ЦНС пов’язана із залученням до процесу шийного відділу хребта і поширеністю спондилопатії, ПНС — з наявністю тендовагінітів, артриту кореневих суглобів (плечових, кульшових) і змін грудного відділу хребта, тоді як у 2-й групі — з параметрами інтегрального індексу активності артриту та рентгенологічної стадії хвороби, з ураженням кореневих й крижово-клубових зчленувань, причому вік початку захворювання впливає на розвиток астеновегетативного і кортиконуклеарного синдромів, виникнення радикулопатії, цервікокраніалгії та синдрому метакарпального каналу, а в патогенетичних побудовах патології ЦНС більшою мірою відіграє роль рівень у крові імуноглобуліну A, ПНС — вміст сироваткового інтерлейкіну-1b, що, крім того, при ЮАС визначають появу цервікокраніалгії, а в інших спостереженнях АС — метатарзалгії Мортона. Висновки. АС із різним віковим дебютом захворювання є чинником ризику розвитку окремих ознак ураження ЦНС та ПНС, які в цих групах мають свої патогенетичні особливості.
Актуальность. Распространенность анкилозирующего спондилита (АС), который значительно чаще развивается в возрасте 20–30 лет, среди населения достигает 0,3 %. Выделяют две формы АС — детскую и взрослую, в зависимости от возраста дебюта заболевания. Диагностика ювенильного АС (ЮАС) относится к наиболее актуальным проблемам в педиатрической ревматологии, при этом эволюция данного заболевания во взрослом возрасте остается неизученной. Существует возрастной диморфизм поражений центральной (ЦНС) и периферической нервной системы (ПНС), но у больных с ЮАС и в остальных случаях он невыясненный. Цель исследования: изучить у больных АС частоту и характер отдельных клинических признаков поражений ЦНС и ПНС, оценить их особенности при заболевании, начавшемся в детском и взрослом возрасте. Материалы и методы. Обследованы 217 больных АС (193 мужчины и 24 женщины), средний возраст которых — 38 лет. Быстропрогрессирующее течение констатировано в 21 % наблюдений, умеренная и высокая степень активности — в 79 %, ІІ–ІІІ стадия — в 82 %, полиартрит — в 65 %. ЮАС отмечен в 16 % случаев (все мальчики), в которых ІІІ стадия наблюдалась вдвое чаще, чем у остальных пациентов. Результаты. Изменения ПНС наблюдаются в 4,9 раза чаще у больных ЮАС, а ЦНС — в 2 раза реже, чем в случаях дебюта заболевания во взрослом возрасте, при этом у пациентов 1-й группы тяжесть поражения ЦНС связана с вовлечением в процесс шейного отдела позвоночника и распространенностью спондилопатии, ПНС — с наличием тендовагинитов, артрита корневых суставов (плечевых, тазобедренных) и изменений грудного отдела позвоночника, тогда как во 2-й группе — с параметрами интегрального индекса активности артрита и рентгенологической стадии болезни, с поражением корневых и крестцово-подвздошных сочленений, причем возраст начала заболевания влияет на развитие астеновегетативного и кортиконуклеарного синдромов, возникновение радикулопатии, цервикокраниалгии и синдрома метакарпального канала, а в патогенетических построениях патологии ЦНС в большей степени играет роль уровень в крови иммуноглобулина A, ПНС — содержание сывороточного интерлейкина-1β, которые, кроме того, при ЮАС определяют появление цервикокраниалгии, а в остальных наблюдениях АС — метатарзалгии Мортона. Выводы. АС с разным возрастным дебютом заболевания является фактором риска развития отдельных признаков поражения ЦНС и ПНС, которые в этих группах имеют свои патогенетические особенности.
Background. The prevalence of ankylosing spondylitis (AS) among the population reaches 0.3 %, it is much more likely to develop at the age of 20–30 years. There are two forms of AS: juvenile (JAS) and adult, depending on the age of the disease onset. The diagnosis of JAS is one of the most urgent problems in pediatric rheumatology, while the evolution of this disease in adulthood remains unexplored. There is an age-related dimorphism of the central nervous system (CNS) and peripheral nervous system (PNS) disturbances, but among patients with JAS and in other cases, it has not been investigated. The purpose of the research was to examine patients with AS in terms of the incidence and nature of the course of CNS and PNS disturbances and to evaluate their characteristics in juvenile- and adult-onset of this disease. Materials and methods. Two hundred seventeen patients with AS (193 men and 24 women), with an average age of 38 years, were exami-ned. The rapidly progressing course was detected in 21 % of cases, moderate and high degree of activity — in 79 %, stage ІІ–ІІІ — in 82 %, and polyarthritis — in 65 %. JAS was diagnosed in 16 % of patients (all boys), among them, stage III occurred twice as often as among other patients. Results. Changes in PNS are observed 4.9 times more often in patients with JAS, and in CNS — 2 times less often than in cases of adult-onset. Moreover, among patients of group 1, the severity of CNS disturbances is associated with involvement of the cervical spine and the prevalence of spondylopathy, and of PNS — with presence of tendovaginitis, arthritis of the shoulder and hip joints, and changes in the thoracic spine, while in the group 2 it is associated with the parameters of the integral index of arthritis activity and the X-ray stage of the disease, with disorders of shoulder, hip and sacroiliac joints, wherein the age of the disease onset affects the development of asthenovegetative and corticonuclear syndrome, the emergence of radiculopathy, cervicocranialgia and carpal tunnel syndrome, and in the pathogenetic architectonics of CNS pathology, the level of immunoglobulin-A plays a greater role, of PNS — the serum interleukin 1-b contents, which, in addition, determine the occurrence of cervicocranialgia in cases of JAC, and in the remaining observations of AS — the Morton’s metatarsalgia. Conclusions. AS with different age of the disease onset is a risk factor for the development of certain symptoms of CNS and PNS disturbances, which in these groups have their pathogenetic features.
Работа является фрагментом комплексных тем Министерства здравоохранения Украины «Оптимизация патогенетической терапии поражений опорно-двигательного аппарата и внутренних органов при ревматических заболеваниях (клинико-экспериментальные исследования)» (№ госрегистрации 0105U008727) и «Обосновать, разработать и внедрить медицинскую технологию ранней диагностики и эффективных методов лечения болезней ревматологического профиля с учетом гендерных и возрастных особенностей в разных экологических регионах» (№ госрегистрации 0116U004057).
Введение
Распространенность анкилозирующего спондилита (АС) среди населения достигает 0,3 % [10, 13], а одним из наиболее частых проявлений заболевания является поражение центральной (ЦНС) и периферической нервной системы (ПНС) [9, 11], что в первую очередь обусловлено патологией позвоночника [8]. К главным причинам тяжелой нейропатии у больных АС относятся подвывихи и микропереломы позвонков [6, 7, 16], а также демиелинизирующая патология [4]. Необходимо отметить, что для таких пациентов свойственны нарушения вегетативного звена нервной системы [14], которые прежде всего затрагивают ее парасимпатическую составляющую [12]. Практически всегда АС сопровождается психосоматическими расстройствами [15, 17], что в конце концов еще больше усугубляет низкое качество жизни больных [2, 5].
Выделяют две формы АС — ювенильную (ЮАС) и взрослую (ВАС), в зависимости от возраста больных в дебюте заболевания [3]. R. Conway, F.D. O’Shea [1] считают, что эти варианты болезни отличаются друг от друга, как яблоки от апельсинов.
Целью данного исследования были изучение у больных АС частоты и характера отдельных клинических признаков поражений ЦНС и ПНС, оценка их особенностей при заболевании, начавшемся в детском и взрослом возрасте.
Материалы и методы
Под наблюдением находились 217 больных АС в возрасте от 16 до 57 лет (в среднем — 37,70 ± 0,64 года), среди которых доля мужчин составила 88,9 %, женщин — 11,1 %. Длительность заболевания составила в среднем 10,50 ± 0,39 года. I степень активности АС установлена в 21,2 % случаев, II — в 56,7 % и III — в 22,1 %, I стадия отмечена у 18,4 % от числа обследованных, II — у 50,7 % и III — у 30,9 %. Медленно прогрессирующее течение заболевания наблюдалось в 79,3 % случаев, быстро прогрессирующее — в 20,7 %. Так называемая центральная форма АС диагностирована в 33,6 % наблюдений, ризомелическая — в 2,8 %, периферическая — в 5,1 %, недифференцированная — в 58,5 %. Офтальмопатия (увеит) и висцеральные изменения диагностированы у 3/4 от числа больных. Периферический артрит установлен у 66,4 % от числа больных, сакроилеит — у 97,2 %, манифестная спондилопатия — у 94,9 %. Параметры распространенности суставного синдрома составили 5,40 ± 0,25 а.е., его активности (DAS) — 4,0 ± 0,1 o.e., индекса Лансбури — 117,10 ± 3,89 балла, индекса прогрессирования артрита — 1,30 ± 0,15 o.e. Метакарпальный индекс Барнетта — Нордина был равен 0,430 ± 0,004 о.е., индекс минеральной плотности кости — 1,490 ± 0,055 SD. У 38,7 % от числа обследованных отмечены энтезопатии, у 28,6 % — тендовагиниты.
Все больные были разделены на две группы: 1-ю (основную) составили 35 (16,1 %) пациентов c ЮАС (все мужского пола с началом болезни в возрасте до 18 лет), а остальные 182 (83,9 %) с ВАС были включены во 2-ю (контрольную) группу. Возраст в дебюте болезни у представителей основной группы составил 14,30 ± 0,52 года, а на момент обследования — 24,90 ± 0,83 года, тогда как в контрольной — соответственно 29,60 ± 0,45 и 40,20 ± 0,58 года. Продолжительность заболевания в 1-й и во 2-й группах была одинакова. Обе группы оказались примерно равны по степеням активности заболевания, но быстро прогрессирующее течение болезни при ВАС наблюдалось в 2,7 раза чаще.
Пациентам выполняли рентгеновское (Multix-Compact-Siеmens, Германия) и ультразвуковое (Envisor-Philips, Нидерланды и ATL3500-Siemens, Германия) исследование периферического артрита, спондилопатии и сакроилеита, проводили двухэнергетическую рентгеновскую остеоденситометрию проксимального отдела бедренной кости (QDR-4500-Delphi-Hologic, США), эхокардиографию (Acuson-Aspen-Siemens, Германия, Еnvisor-C-Philips, Нидерланды) и ультразвуковую допплерографию сосудов (ангиограф Aplia-XG-Toshiba, Япония). У части больных выполнены электронейромиография («Нейро-МВП-4», Россия) с оценкой скорости импульса и амплитуды потенциала, компьютерная (Somazom-Emotion-6-Siemens, Германия) и магнитно-резонансная (Gygoscan-Intera-Philips, Нидерланды) томография крестцово-подвздошных сочленений, позвоночника и головного мозга. С помощью иммуноферментного анализа (ридер PR2100 Sanofi diagnostic pasteur, Франция) изучали уровни в сыворотке крови антител к циклическому цитруллиновому пептиду (аССР), концентрации интерлейкина 1b (IL-1b) и туморнекротического фактора a (TNF-a), а используя иммунобиохимический анализатор Olympus-AU-640 (Япония), в сыворотке крови определяли концентрации С-реактивного протеина (CRP), фибриногена (FG), циркулирующих иммунных комплексов (CIC), иммуноглобулинов (Ig) А, G и M. Показатели aCCР в сыворотке крови обследованных больных АС составили 22,20 ± 8,41 ± 0,57 Е/мл, CRP — 12,00 ± 5,89 ± ± 0,40 мг/л, FG — 7,40 ± 2,99 ± 0,20 г/л, IgA — 2,30 ± 0,58 ± 0,04 ммоль/л, IgG — 15,70 ± 3,23 ± 0,22 ммоль/л, IgM — 2,00 ± 0,62 ± 0,04 ммоль/л, CIC — 104,50 ± 61,08 ± 4,15 усл.ед., IL-1b — 88,50 ± ± 100,17 ± 6,80 пг/мл, TNF-a — 153,50 ± 220,12 ± 14,94 пг/мл.
Статистическая обработка полученных результатов исследований проведена с помощью вариационного, непараметрического, корреляционного, регрессионного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы Microsoft Excel и Statistica-StatSoft, США). Оценивали средние значения (M), их стандартные ошибки и отклонения (SD), коэффициенты параметрической корреляции Пирсона и непараметрической — Кендалла, критерии множественной регрессии, дисперсии Брауна — Форсайта и Уилкоксона — Рао, различий Стьюдента и Макнемара — Фишера, достоверность статистических показателей.
Исследования одобрены этическим комитетом Донецкого национального медицинского университета (г. Лиман).
Результаты
Поражение ЦНС диагностировано у 74,7 % от числа больных АС, ПНС — у 33,2 %, соответственно, у больных ВАС — вдвое чаще, а изменения ПНС — в 5 раз реже. Необходимо отметить, что при этом патология ПНС наблюдалась у всех больных ЮАС. Среди обследованных пациентов с АС дисциркуляторная энцефалопатия установлена в 54,4 % случаев, астеновегетативный синдром — в 39,2 %, кортиконуклеарный — в 22,6 %, корковая атаксия — в 19,4 %, периферическая полинейропатия и пирамидный синдром — по 18,0 %, мозжечковая атаксия — в 17,5 %, радикулопатия — в 16,6 %, псевдобульбарный синдром — в 14,3 %, цервикокраниалгия — в 13,8 %, метатарзалгия Мортона — в 12,9 %, периферическая мононейропатия — в 10,6 %, синдром метакарпального канала — в 9,2 %, преходящие нарушения мозгового кровообращения — в 8,3 %, эпилептиформный синдром — в 7,8 %, невралгия тройничного нерва — в 4,6 %, неврит лицевого нерва — в 3,7 %.
Патология ЦНС проявляется в 72,8 % случаев дисциркуляторной энцефалопатией, в 52,5 % — астеновегетативным синдромом, в 30,3 % — кортиконуклеарным синдромом, в 25,9 % — корковой атаксией, в 24,1 % — пирамидным синдромом, в 23,5 % — мозжечковой атаксией, в 19,1 % — псевдобульбарным синдромом, в 11,1 % — преходящими нарушениями мозгового кровообращения, в 10,5 % — эпилептиформным синдромом, а ПНС — в 54,2 % наблюдений периферической полинейропатией, в 50,0 % — радикулопатией, в 41,7 % — цервикокраниалгией, в 38,9 % — метатарзалгией Мортона, в 32,0 % — периферической мононейропатией, в 27,8 % — синдромом метакарпального канала, в 13,9 % — невралгией тройничного нерва, в 11,1 % — невритом лицевого нерва.
Такие признаки поражения нервной системы, как периферическая мононейропатия, кортиконуклеарный синдром, корковая атаксия, псевдобульбарный синдром и преходящие нарушения мозгового кровообращения при ЮАС, не отмечались, а дисциркулярная энцефалопатия наблюдалась достоверно реже на 70 %, а астеновегетативный синдром — на 85 %, при этом для заболевания, начавшегося в детском возрасте, были характерны периферическая полинейропатия, радикулопатия, цервикокраниалгия, метатарзалгия Мортона, синдром метакарпального канала, невралгия тройничного нерва, неврит лицевого нерва и эпилептиформный синдром, которые наблюдались чаще, чем при ВАС, соответственно в 15,1, 3,3, 2,2, 2,9, 90,5, 7,8, 5,2 и 3,6 раза, что продемонстрировал анализ Макнемара — Фишера и что отображено на рис. 1 и 2.
Обсуждение
По данным многофакторного дисперсионного анализа Уилкоксона — Рао, на интегральные признаки изменений ЦНС оказывает влияние возраст пациентов в дебюте болезни. Мы отобрали те показатели течения АС, которые одновременно имели дисперсионные связи Брауна — Форсайта и корреляционные — Кендалла с тяжестью поражения нервной системы. Оказалось, что при ЮАС существует прямая связь с выраженностью поражения шейного отдела позвоночника и распространенностью спондилопатии, а в случаях ВАС — с параметром DAS и вовлечением в процесс корневых (плечевых, тазобедренных) суставов.
Как свидетельствует анализ Уилкоксона — Рао, возраст больных АС в начале заболевания воздействует также на интегральные клинические признаки поражения ПНС. В основной группе существует прямая связь тяжести изменений ПНС с тендовагинитами, наличием омагрита и вовлечением в процесс грудного отдела позвоночника, а в контрольной группе — со стадией АС, наличием коксита и выраженностью сакроилеита.
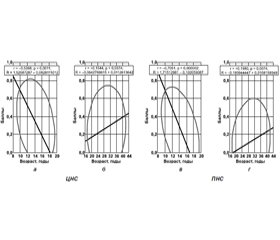
Возраст дебюта болезни в основной группе обратно коррелирует с тяжестью дисциркуляторной энцефалопатии, астеновегетативного и эпилептиформного синдрома, а в контрольной — прямо соотносится с кортиконуклеарным синдромом и имеет негативные корреляционные связи с эпилептиформным синдромом и мозжечковой атаксией, что демонстрируют корреляционные анализы Кендалла и Пирсона (рис. 3).
И в первой, и во второй группе больных АС наблюдаются прямые корреляции с возрастом пациентов тяжести радикулопатии, а обратные — с цервикокраниалгией. Кроме того, существуют разнонаправленные достоверные соотношения у больных ЮАС с невритом лицевого нерва (прямая зависимость) и синдромом метакарпального канала (обратная связь). На основании полученных данных обследования сделаны заключения, имеющие определенную практическую направленность: дебют болезни в возрасте моложе 11 лет (< M – SD пациентов основной группы) является фактором риска развития астеновегетативного синдрома, цервикокраниалгии и синдрома метакарпального канала, а начало заболевания в возрасте старше 35 лет (> M + SD контрольной группы) — прогнознегативным признаком в отношении возникновения кортиконуклеарного синдрома и радикулопатии.
/57.jpg)
Как свидетельствует дисперсионный анализ Брауна — Форсайта, при ЮАС на возникновение астеновегетативного синдрома оказывают влияние параметры DAS, пирамидного синдрома — распространенность спондилопатии, мозжечковой атаксии — стадия патологического процесса, периферической полинейропатии — наличие у больных тендовагинитов, цервикокраниалгии — поражение шейного отдела позвоночника, синдрома метакарпального канала — степень активности заболевания. В случаях ВАС развитие дисциркуляторной энцефалопатии тесно связано с энтезитами, псевдобульбарного синдрома — с поражением корневых суставов, пирамидного синдрома — с изменениями шейного отдела позвоночника, корковой атаксии и синдрома метакарпального канала — с показателем DAS, радикулопатии — со стадией АС.
Независимо от варианта АС и характера поражения нервной системы наблюдается дисперсионная связь тяжести патологии ЦНС и ПНС с уровнями в крови IgA и CIC. Кроме того, выраженность изменений со стороны ЦНС у представителей основной и контрольной групп тесно связана с содержанием в сыворотке аССР, а при ВАС — также и с показателем фибриногенемии. Тяжесть поражения ЦНС у больных ЮАС прямо коррелирует с показателями в крови IgA и TNF-a, а ПНС — с IL-1b. В случае ВАС наблюдаются обратные корреляционные связи тяжести изменений ЦНС с параметрами иммуноглобулинемии, CIC и IL-1b, а прямое соотношение отмечается со значениями TNF-a. Следует подчеркнуть, что выраженность изменений ПНС у больных ВАС обратно коррелирует с концентрацией в крови CIC и прямо — с IL-1b.
С учетом выполненных результатов статистических данных обследования у больных ЮАС прогнозпозитивным признаком в отношении тяжести поражения ЦНС является уровень в крови IgA < 2 ммоль/л (< M – SD основной группы), а при ВАС — сывороточное содержание IgA > 3 ммоль/л (> M + SD контрольной группы).
Следующим этапом нашей работы стала оценка роли иммунных нарушений в патогенетических построениях изменений ЦНС и ПНС у больных ЮАС и ВАС. С этой целью были отобраны показатели, которые одновременно имели достоверные дисперсионные связи Брауна — Форсайта и корреляционные — Кендалла. Оказалось, что при ЮАС от уровня CIC прямо зависит развитие дисциркуляторной энцефалопатии, от CRP — пирамидального синдрома, от IL-1b — периферической полинейропатии, от IgA — цервикокраниалгии, от TNF-a — синдрома метакарпального канала, от FG — метатарзалгии Мортона. У больных ВАС подобные зависимости отсутствовали, а отмечались совершенно иные. Так, с уровнем СІС было связано развитие кортиконуклеарного синдрома, моно- и полинейропатии, с IgM — псевдобульбарного синдрома, с IL-1b — метатарзалгии Мортона, CRP — тяжесть радикулопатии. Эти данные еще раз указывают на совершенно неоднозначные проявления АС с дебютом болезни в детском и взрослом возрасте.
Выводы
Изменения ПНС наблюдаются в 4,9 раза чаще у больных ЮАС, а ЦНС — в 2 раза реже, чем в случаях дебюта заболевания во взрослом возрасте, при этом у пациентов с ЮАС тяжесть поражения ЦНС связана с вовлечением в процесс шейного отдела позвоночника и с распространенностью спондилопатии, ПНС – с наличием тендовагинитов, артрита корневых суставов (плечевых, тазобедренных) и изменений грудного отдела позвоночника, тогда как при ВАС – с параметрами DAS и рентгенологической стадии болезни, с поражением крестцово-подвздошных сочленений, причем возраст начала заболевания влияет на развитие астено-вегетативного и кортиконуклеарного синдромов, возникновение радикулопатии, цервикокраниалгии и синдрома метакарпального канала, а в патогенетических построениях патологии ЦНС в большей степени участвует уровень в организме IgA, ПНС – содержание в крови IL-1b, которые, кроме того, при ЮАС определяют появление цервикокраниалгии, а в остальных наблюдениях АС – мортоновской метатарзалгии.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов, при этом авторы не получали от отдельных лиц и организаций финансовой поддержки исследования, гонораров и других форм вознаграждения.
Работа соответствует принципам Хельсинкской декларации, принятой Генеральной Ассамблеей Всемирной медицинской ассоциации (в 1997–2000 г.), Конвенции Совета Европы по правам человека и биомедицине (в 1997 г.), соответствующим положениям Всемирной организации здравоохранения, Международного совета медицинских научных обществ, Международного кодекса медицинской этики (в 1983 г.), Закону Украины № 3447-1V, полностью исключает ограничение интересов больного и нанесение вреда его здоровью, соответствует всем этическим требованиям.
Информация о вкладе каждого автора: О.Е. Чернышева — обследование больных на предыдущих этапах, анализ полученных данных, подготовка иллюстраций; О.В. Синяченко — концепция и дизайн исследования, написание текста; Т.Р. Полесова — обзор литературы по проблеме, сбор материалов на предыдущих этапах и статистическая обработка материалов; М.В. Ермолаева — сбор материалов, анализ полученных данных.
Список литературы
1. Conway R. Juvenile versus adult-onset ankylosing spondylitis: are we comparing apples and oranges? / R. Conway, F.D. O’Shea // Rheumatol. — 2012. — Vol. 39, № 5. — P. 887-889.
2. Dougados M. Evaluation of whether extremely high enthesitis or Bath Ankylosing Spondylitis Disease Activity Index (BASDAI) scores suggest fibromyalgia and confound the anti-TNF response in early non-radiographic axial spondyloarthritis / M. Dougados, I. Logeart, A. Szumski [et al.] // Clin. Exp. Rheumatol. — 2017. — Vol. 23, № 2. — P. 172-179.
3. Jadon D.R. Juvenile versus adult-onset ankylosing spondylitis — clinical, radiographic, and social outcomes. a systematic review / D.R. Jadon, A.V. Ramanan, R. Sengupta // J. Rheumatol. — 2013. — Vol. 40, № 11. — P. 1797-1805.
4. Kaltsonoudis E. Neurological adverse events in patients recei-ving anti-TNF therapy: a prospective imaging and electrophysiological study / E. Kaltsonoudis, A.K. Zikou, P.V. Voulgari [et al.] // Arthritis Res. Ther. — 2014. — Vol. 16, № 3. — P. 125-135.
5. Kotsis K. Health-related quality of life in patients with ankylo-sing spondylitis: a comprehensive review / K. Kotsis, P. V. Voulgari, A.A. Drosos [et al.] // Expert. Rev. Pharmacoecon. Outcomes Res. — 2014. — Vol. 14, № 6. — P. 857-872.
6. Maarouf A. Iatrogenic spinal cord injury in a trauma patient with ankylosing spondylitis / A. Maarouf, C.M. McQuown, J.A. Frey [et al.] // Prehosp. Emerg. Care. — 2017. — Vol. 19, № 1. — P. 1-5.
7. Mercieca C. Pulmonary, renal and neurological comorbidities in patients with ankylosing spondylitis; implications for clinical practice / C. Mercieca, I.E. van der Horst-Bruinsma, A.A. Borg // Curr. Rheumatol. Rep. — 2014. — Vol. 16, № 8. — P. 434-444.
8. Nugent M. Clinical outcomes following spinal fracture in patients with ankylosing spondylitis / M. Nugent, M.J. Berney, S. Morris // Ir. J. Med. Sci. — 2017. — Vol. 1, № 2. — P. 103-108.
9. Rodrigues C.E. Low prevalence of renal, cardiac, pulmonary, and neurological extra-articular clinical manifestations in spondyloarthritis: analysis of the brazilian registry of spondyloarthritis / C.E. Rodrigues, W.P. Vieira, A.B. Bortoluzzo [et al.] // Rev. Bras. Reumatol. — 2012. — Vol. 52, № 3. — P. 375-383.
10. Rohekar S. 2014 Update of the Canadian Rheumatology Association/spondyloarthritis research consortium of Canada treatment recommendations for the management of spondyloarthritis. Part I: principles of the management of spondyloarthritis in Canada / S. Rohekar, J. Chan, S.M. Tse [et al.] // J. Rheumatol. — 2015. — Vol. 42, № 4. — P. 654-664.
11. Soroush M. Investigation of cardiac complications and their incidence in patients with ankylosing spondylitis / M. Soroush, M. Mominzadeh, Y. Ghelich [et al.] // Med. Arch. — 2016. — Vol. 70, № 1. — P. 35-38.
12. Syngle A. Disease-modifying anti-rheumatic drugs improve autonomic neuropathy in arthritis: DIANA study / A. Syngle, I. Verma, P. Krishan [et al.] // Clin. Rheumatol. — 2015. — Vol. 34, № 7. — P. 1233-1241.
13. Usenbo A. Prevalence of arthritis in Africa: A systematic review and meta-analysis / A. Usenbo, V. Kramer, T. Young, A. Musekiwa // PLoS One. — 2015. — Vol. 10, № 8. — E. 0133858.
14. Wei C.Y. Cardiac autonomic function in patients with ankylosing spondylitis: a case-control study / C.Y. Wei, W.M. Kung, Y.S. Chou [et al.] // Medicine. — 2016. — Vol. 95, № 21. — E. 3749.
15. Xu X. Anxiety and depression correlate with disease and qua-lity-of-life parameters in Chinese patients with ankylosing spondylitis / X. Xu, B. Shen, A. Zhang [et al.] // Patient Prefer. Adherence. — 2016. — Vol. 20, № 10. — P. 879-885.
16. Yang B. Single-session combined anterior-posterior approach for treatment of ankylosing spondylitis with obvious displaced lower cervical spine fractures and dislocations / B. Yang, T. Lu, H. Li // Biomed. Res. Int. — 2017. — Vol. 20, № 17. — E. 9205834.
17. Zou Q. Correlation of axial spondyloarthritis with anxiety and depression / Q. Zou, Y. Jiang, F. Mu [et al.] // Med. Sci. Monit. — 2016. — Vol. 9, № 22. — P. 3202-3208.

/56.jpg)
/56_2.jpg)
/57.jpg)