Журнал «Здоровье ребенка» 1 (22) 2010
Вернуться к номеру
Подходы к профилактике респираторных заболеваний у детей с перинатальными поражениями ЦНС
Авторы: Кривущев Б.И., Юлиш Е.И., Ярошенко С.Я., Донецкий национальный медицинский университет им. М. Горького
Рубрики: Педиатрия/Неонатология
Версия для печати
Через 12 месяцев после начала использования на фоне традиционной терапии иммуномодулятора Бронхомунал П у часто болеющих детей раннего возраста, перенесших пре- и перинатальное поражение головного мозга, индекс респираторной заболеваемости снизился в 2,8 раза, длительность неосложненных форм острых респираторных инфекций — в 1,75 раза, частота осложнений — в 2,6 раза. Данная позитивная динамика получена на фоне нормализации количественных и качественных показателей Т- и В-звеньев иммунной системы, выраженного снижения степени аутоаллергии к структурам головного мозга.
Бронхомунал, часто болеющие дети, перинатальное поражение головного мозга.
Проблема часто и длительно болеющих детей (ЧДБ), составляющих 30–40 % детской популяции, является одной из важнейших в современной педиатрии [1, 2]. Несмотря на большое количество исследований [1, 3–5], число детей, переносящих в раннем возрасте респираторные инфекции более шести раз в год, постоянно растет [1]. Значимыми факторами для развития вторичной иммунологической недостаточности у детей этой категории являются неблагоприятное течение беременности у матери ребенка и родов, перинатальные поражения центральной нервной системы (ЦНС), нарушения гемоликвородинамики, наличие асфиксии ребенка во время родов [6]. Установлено, что у 65 % детей с пре- и перинатальными поражениями ЦНС отмечаются частые респираторные заболевания [7].
В последнее время в педиатрической практике большое распространение получили препараты, содержащие бактериальные лизаты системного действия, используемые с целью уменьшения респираторной заболеваемости [8]. Многочисленными исследованиями показано, что применение Бронхомунала у часто болеющих детей ведет к снижению частоты респираторных заболеваний, снижает вероятность бактериальных осложнений. Применение Бронхомунала для профилактики рецидивов хронического бронхита снижает частоту и тяжесть рецидивов, уменьшает случаи госпитализации в 1,43 раза и ее продолжительность в 1,8 раза. У детей с хроническим риносинуситом отмечено снижение частоты рецидивов и тяжести симптомов [9]. У ЧДБ детей при назначении Бронхомунала в 2–3 раза снижается частота ОРЗ, фарингитов, бронхитов [10].
Иммунологические исследования свидетельствуют, что очевидным противоинфекционным эффектом Бронхомунала является, помимо увеличения уровня специфических антител, нарастание уровней IgA как в сыворотке крови, так и в секрете дыхательных путей. IgA фиксируется на слизистых, поддерживает их барьерную функцию, взаимодействует со специфическими антигенами бактерий.
Бронхомунал также вызывает активацию СD16+-клеток, повышение функциональной активности макрофагов и выработку ряда цитокинов и медиаторов (ИЛ-6, ИЛ-8, ИЛ-2, g -ИФН). Одновременно увеличивается продукция a -интерферона, а также снижаются уровни IL-4, ФНО- a . Повышение уровня IgG усиливает межклеточные взаимодействия макрофагов, натуральных киллеров. Результатом является элиминация микробных факторов, нормализация функций иммунной системы [11]. Эти сдвиги можно интерпретировать как переключение иммунного ответа Th2-типа на Th1-тип. Как показали клинические наблюдения, дети с аллергией при влючении Бронхомунала в комплексную терапию не только реже болеют ОРВИ, но и в меньшей степени подвержены приступам бронхообструкции [12].
Способность очищенных бактериальных лизатов повышать не только специфический иммунный ответ, но и активизировать неспецифическую защиту позволяет их успешно применять в группе ЧДБ детей, у которых нередко вирусно-бактериальный синергизм приводит к затяжному рецидивирующему течению с чередованием инфекций верхних и нижних дыхательных путей и среднего уха. Ранняя иммунизация против основных патогенов снижает процент внутричерепных осложнений со стороны околоносовых пазух и уха у детей раннего возраста.
Использование бактериальных лизатов наиболее оправданно с целью увеличения продукции специфических антител, а также стимуляции неспецифических факторов защиты (секреторных IgA, цитокинов, NK-клеток, клеток макрофагально-фагоцитарной системы и др.).
Бронхомунал представляет собой бактериальный лизат системного действия, влияющий на неспецифические и специфические звенья иммунного ответа, как системного, так и местного, в верхних и нижних дыхательных путях.
Анализируя действие препаратов микробного происхождения, содержащих липополисахариды грамотрицательных бактерий и мембранные фракции, следует отметить, что основной механизм их действия связан с активирующим влиянием на функциональный статус макрофагов. Данные препараты стимулируют фагоцитоз и через него могут воздействовать на иммунокомпетентные клетки.
Бактериальные лизаты (Бронхомунал) инициируют специфический иммунный ответ на бактериальные антигены, присутствующие в препарате.
Использование бактериальных лизатов или бактериальных рибосом обусловливает контакт антигенов с макрофагами MALT-системы респираторного и желудочно-кишечного тракта с последующей их презентацией лимфоцитам. В результате этого появляются коммитированные клоны В-лимфоцитов, продуцирующие специфические антитела к возбудителям, антигены которых содержатся в препарате. Миграция коммитированных В-лимфоцитов в другие лимфоидные образования MALT-системы и последующая их дифференциация в плазмоциты приводят к продукции специфического секреторного IgA и развитию эффективной местной иммунной защиты против основных возбудителей острых респираторных заболеваний [13].
Теснейшее взаимодействие иммунных образований лимфоглоточного кольца дыхательных путей с подобными структурами ЖКТ (пейеровы бляшки, аппендикс и т.д.) дает возможность выбирать различные варианты вакцинотерапии — системную (Бронхомунал) или топическую.
Таким образом, прием бактериальных иммунотропных препаратов имеет вакциноподобное действие, сопровождаясь индукцией специфического иммунного ответа как местного, так и системного иммунитета [13].
Цель исследования — оценить эффективность иммуномодулятора Бронхомунал у часто болеющих детей, перенесших пре- и перинатальное поражение головного мозга.
Материалы и методы исследования
Под нашим наблюдением находился 51 ребенок в возрасте от 10 месяцев до 3 лет. Все дети перенесли пре- и перинатальное гипоксически-ишемическое поражение головного мозга. Эпизоды острых респираторных инфекций (ОРИ) отмечены у всех детей в течение одного года шесть и более раз.
В I группу (основную) вошли 26 детей, получавших дополнительно к основной терапии в качестве иммуномодулятора препарат Бронхомунал П по стандартной схеме — 3,5 мг/сутки однократно утром натощак. Курс лечения состоял из 3 проводимых ежемесячно циклов, продолжительность каждого — 10 дней.
Во II группу (сравнения) вошли 25 детей, получавшие только традиционное лечение (нейротрофические препараты — аминалон, циннаризин, витамины группы В, А, Е, гимнастику, массаж, физиотерапию) без дополнительных иммуномодуляторов.
Все дети I и II групп перенесли респираторные заболевания, в том числе пневмонии, бронхиты, отиты, синуситы от 6 до 12 раз в году.
Контрольную группу составили 26 здоровых сверстников, наблюдавшихся в поликлинике.
Для оценки нервно-психического развития (НПР) детей использовалась методика, разработанная
Р.В. Тонковой-Ямпольской. Изучение состояния количества Т-клеток проводилось с помощью моноклональных антител серии ИПО. Функциональную способность Т-звена иммунитета исследовали методом розеткообразования по Jondal et al. (1972) и Б.В. Пинегину и соавт. (1987). Состояние В-системы изучалось количественно при помощи моноклональных антител, рецепторный аппарат — в реакции М-розеткообразования. Содержание иммуноглобулинов A, M, G в сыворотке крови определяли с помощью реакции радиальной иммунодиффузии по Manchini. Циркулирующие иммунные комплексы (ЦИК) изучались по методу Digione et al. (1976). Для определения степени выраженности аутоиммунного процесса к структурам ЦНС были использованы приготовленные по методике В.А. Фрадкина [14] мозговые антигены из различных структур головного мозга плода (кора, гипоталамус, мозжечок, общий мозг). Статистическая обработка данных проводилась с использованием диалоговой статистической системы STADIA.
Результаты и обсуждение
Перед проведением курса реабилитации в сопоставимых группах ЧДБ детей выявлены: повышение содержания общих Т-лимфоцитов и Т-хелперов; снижение количества В-лимфоцитов и Т-супрессоров, а также функциональной активности Т- и В-клеток; гипоиммуноглобулинемия; выраженное повышение уровня ЦИК; активизация аутоаллергических реакций к структурам головного мозга, прежде всего к гипоталамусу.
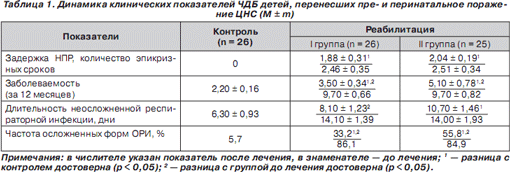
Через 12 месяцев после начала курса реабилитации с использованием Бронхомунала П у ЧДБ детей I группы выявлено значительное улучшение показателей респираторной заболеваемости: индекс респираторной заболеваемости снизился в 2,8 раза, длительность неосложненных форм ОРИ — в 1,75 раза, частота осложнений — в 2,6 раза.
У детей II группы, получавших только традиционный курс реабилитации, положительная клиническая динамика была менее выражена. Индекс респираторной заболеваемости снизился за год наблюдения до 5,10 ± 0,78, частота осложнений уменьшилась соответственно в 1,5 раза, а длительность неосложненных форм ОРИ — в 1,3 раза (табл. 1).
Через 12 месяцев после курса реабилитации у ЧДБ детей I группы количество В-лимфоцитов и их функциональная активность увеличились практически до нормы. Уровень иммуноглобулинов сыворотки крови классов A, M, G также увеличился до показателей здоровых сверстников (табл. 2).
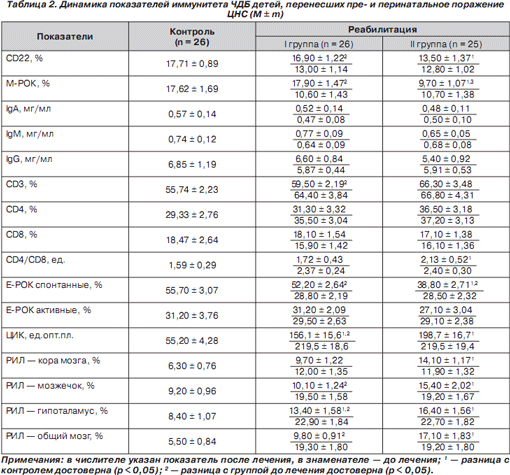
У ЧБД II группы через 12 месяцев после традиционного курса реабилитации остались сниженными по сравнению со здоровыми детьми количество В-лимфоцитов (в 1,3 раза) и их функциональная активность (в 1,8–2 раза), содержание иммуноглобулинов сыворотки крови. Данные показатели мало изменились по сравнению со значениями до проведенного курса реабилитации, что свидетельствует о сохранившемся вторичном иммунодефицитном состоянии гуморального звена иммунитета на фоне довольно высокой антигенной (инфекционной) нагрузки.
Показатели клеточного иммунитета у детей I группы также значительно улучшились. Во II группе детей, получавших только традиционную терапию, сохранилось повышенным (на уровне исходных значений) общее количество Т-лимфоцитов на фоне сниженной функциональной активности, которая была в 1,4 раза меньше, чем у здоровых сверстников. Величина иммунорегуляторного индекса снизилась совсем незначительно, предопределяя склонность к инфекционным заболеваниям. Полученные данные свидетельствуют об устойчивой недостаточности клеточного звена иммунитета у данных детей, перенесших пре- и перинатальное поражение ЦНС.
У ЧДБ детей I группы через 12 месяцев после курса иммунореабилитации отмечено снижение уровня ЦИК до 156,1 ± 15,6 ед.опт.пл., фоновый (нормальный) уровень аутоиммунных реакций к тканям коры головного мозга и общего мозга и слабая (клинически незначимая) степень аутоиммунных реакций к мозжечку и гипоталамусу.
У детей II группы, получавших только традиционную терапию, уровень ЦИК отличался от исходных значений незначительно и недостоверно, степень аутоаллергии к структурам головного мозга расценивалась как слабая (14,1–17,1 %).
Таким образом, через 12 месяцев после курса реабилитации ЧДБ детей, перенесших пре- и перинатальное поражение головного мозга, отмечено значимое и достоверное снижение показателей респираторной заболеваемости на фоне приема иммуномодулятора Бронхомунал П.
Использование только традиционной схемы реабилитации ЧДБ детей, перенесших пре- и перинатальное поражение ЦНС, не позволило добиться стойкого улучшения показателей иммунной системы, хотя индекс респираторной заболеваемости снизился почти в 2 раза.
Полученные нами данные позволяют рекомендовать использование иммуномодулятора Бронхомунал П в реабилитации часто и длительно болеющих детей, перенесших пре- и перинатальное поражение ЦНС.
1. Андрущук А.О., Тяжка О.В., Помиткіна Л.Р. До питання про етіологічні та патогенетичні фактори розвитку і перебігу повторних респіраторних захворювань у дітей // Педіатрія, акушерство та гінекологія. — 1999. — № 4. — С. 69.
2. Ноников В.Е. Применение бактериальных иммуномодуляторов для профилактики обострений хронического бронхита // Український медичний часопис. — 1998. — № 6(8). — С. 3-6.
3. Мозалевський А.Ф. Проблема часто хворіючих дітей за матеріалами X з’їзду педіатрів України «Проблеми педіатрії на сучасному етапі» // Педiатрiя, акушерство та гiнекологiя. — 2000. — № 5. — С. 69-72.
4. Ващенко Л.В., Степаненко Т.І., Вакуленко Л.І. Моніторінг стану здоров’я часто хворіючих дітей, особливості їх лікування та реабілітації // Педiатрiя, акушерство та гiнекологiя. — 2000. — № 5. — С. 61.
5. Фокіна С.Є., Нечитайло Д.Ю. Ступінь біологічної зрілості часто хворіючих дітей раннього віку // Педiатрiя, акушерство та гiнекологiя. — 2000. — № 5. — С. 53-54.
6. Акмаев И.Г. Взаимодействие нервных, эндокринных и иммунных механизмов мозга // Журнал неврологии и психиатрии. — 1998. — № 3. — С. 54-56.
7. Шкоробанець І.Д., Казимірик О.І., Мельничук Л.В. Проблема перинатального ураження центральної нервової системи у часто хворіючих дітей // Педiатрiя, акушерство та гiнекологiя. — 2000. — № 5. — С. 55.
8. Романцов М.Г., Ершов Ф.И. Часто болеющие дети: современная фармакотерапия — М.: ГЭОТАР-МЕД, 2006. — С. 192.
9. Маркова Т.П. Иммунотропные препараты в клинической практике // Практическое руководство по клинической иммунологии и аллергологии / Под ред. Р.М. Хаитова. — М., 2003 — С. 31-45.
10. Гаращенко Т.И., Богомильский М.Р., Маркова Т.П. Бактериальные иммунокорректоры в профилактике заболеваний верхних дыхательных путей и уха у часто болеющих детей // Consilium medicum. Педиатрия (приложение). — 2002. — Т. 4. — № 3. — С. 7-14.
11. Маркова Т.П., Чувиров Д.Г., Гаращенко Т.И. Механизм действия ИРС-19 в группе длительно и часто болеющих детей // Иммунология. — 2000. — № 5. — С. 56-59.
12. Маркова Т.П., Чувиров Д.Г. Длительно и часто болеющие дети // РМЖ. — 2002. — Т. 10, № 3.
13. Бережной В.В. Иммунокоррекция в педиатрии // Здоровье Украины. — 2004. — № 108.
14. Фрадкин В.А. Аллергодиагностика. — М.: Медицина, 1975. — 326 с.
