Журнал «Здоровье ребенка» 2 (23) 2010
Вернуться к номеру
Диагностика и коррекция дисбиозов кишечника у детей
Авторы: Дука Е.Д., Днепропетровская медицинская академия, зав. кафедрой пропедевтики детских болезней
Рубрики: Педиатрия/Неонатология
Версия для печати
Значение микробиоценоза кишечника, особенно у детей раннего возраста, трудно переоценить. Наиболее сложным биотопом микробиоценоза является кишечная кооперация, представленная различными популяциями микроорганизмов. Это система, выполняющая и регулирующая многочисленные функции по поддержанию гомеостаза [4, 5]. Функции нормальной микрофлоры кишечника заключаются в обеспечении колонизационной резистентности, формировании иммунного ответа, переваривании пищи, регуляции моторной функции кишечника и процессов детоксикации. Обеспечение колонизационной резистентности предотвращает заселение организма различными микробами. При снижении колонизационной резистентности происходит увеличение числа и спектра патогенных бактерий, возникает возможность развития инфекционного процесса [8, 11, 12].
Особый интерес представляет состояние колонизационной резистентности по отношению к лактобактериям — это строгая специфичность в отношении конкретного индивидуума. Аутомикроорганизмы обеспечивают очень быстрое восстановление нормального состояния микрофлоры кишечника [6, 14, 17].
Микрофлора человека — это дополнительный орган, вес которого составляет 2,5–3 кг. Нормальная микрофлора желудочно-кишечного тракта (500 видов) является важнейшим барьером для болезнетворных бактерий. В толстой кишке человека содержится около 1,5 кг микроорганизмов. В 1 грамме кишечного содержимого — 250 млрд различных представителей микрофлоры. За сутки человек выделяет свыше 17 триллионов микробов.
В физиологических условиях слизистая кишечника покрыта биопленкой (гликокаликс). Толщина этой пленки составляет всего от долей до десятков микрон. Количество микроколоний нормальной флоры в ней может достигать нескольких сотен и даже тысяч [9, 13]. В микрофлоре желудочно-кишечного тракта различают пристеночную и просветную флору. Состав их различен. Пристеночная флора более стабильна и представлена главным образом бифидобактериями и лактобактериями, которые обусловливают защиту кишки от колонизации патогенными бактериями, образуя слой так называемого бактериального дерна. Просветная флора наряду с бифидо- и лактобактериями включает и других постоянных обитателей кишечника.
Функцию микробной экологической системы желудочно-кишечного тракта можно уподобить работе крупной биохимической лаборатории, осуществляющей сотни биохимических процессов [15].
Основными функциями нормальной кишечной микрофлоры являются:
1) сдерживание роста и размножения в организме патогенных микробов;
2) участие в синтетической, пищеварительной и детоксицирующей функциях кишечника;
3) стимуляция синтеза биологически активных веществ, влияющих на функцию ЖКТ, печени, сердечно-сосудистой системы, кроветворения и др.;
4) поддержание высоких уровней лизоцима, иммуноглобулинов, интерферона и других компонентов иммунной системы.
Микрофлора пищевода и желудка у здоровых детей не бывает стабильной и постоянной, поскольку тесным образом связана с характером принимаемой пищи. Пищевод вообще не имеет постоянной микрофлоры, а присутствующие бактерии представляют микробный мир полости рта. Микробный спектр желудка беден. Высокобактерицидный желудочный сок остается практически стерильным, так как микрофлора, попадающая в желудок в составе пищевого комка, погибает в течение 30 мин. По мере продвижения содержимого внутри кишечной трубки снижается парциальное давление кислорода и повышается значение рН среды.
Биотопом с высокой степенью микробной обсемененности является толстая кишка. В основном это бифидобактерии и бактероиды, на долю которых приходится 90 % всех микроорганизмов. Остальные 10 % составляют: кишечная палочка, лактобактерии, энтеробактерии, стрептококки и спороносные анаэробы [12].
Плотность бактерий в различных отделах ЖКТ составляет:
— желудок — менее 1000 в мл;
— тощая кишка — менее 10 000 в мл;
— подвздошная кишка — менее 100 000 в мл;
— ободочная кишка — менее 1 триллиона в мл.
В состав микрофлоры толстой кишки входят:
1. Облигатная (главная):
— бифидобактерии;
— лактобактерии;
— пропионовокислые бактерии;
— бактероиды.
2. Факультативная (условно-патогенная и сапрофитная):
— E.coli (клоны мутуалистов, комменсалов, истинных патогенов, случайных симбионтов);
— Streptococcus faecium .
3. Транзиторная (случайные м/о):
— Staphylococcus, Clostridium, Citrobacter, Enterobacter, Proteus, Klebsiella, Pseudomonas, Candida и др .
К настоящему времени из биотопа толстой кишки выделено более 400 микроорганизмов — представителей 17 семейств, 45 родов [15].
Функции нормальной микрофлоры кишечника многообразны, они представлены в табл. 1.

Главной функцией нормальной микрофлоры кишечника является формирование колонизационной резистентности.
Поскольку состав микрофлоры кишечника меняется в течение жизни человека, не случайно, что в момент появления на свет новорожденный автоматически обсеменяется естественной микрофлорой материнского организма [9]. При физиологических родах источником первичной контаминации плода становятся микроорганизмы, родственные в антигенном отношении организму ребенка.
Поэтому они обладают максимальной способностью к приживлению (микроорганизмы из микрофлоры влагалища, а также кишечника и кожи), т.е. микробное заселение ребенка в процессе родов является первым этапом формирования его микробиоценоза [13, 15]. Излишняя забота о «стерильности» условий для новорожденного при родах может быть первым шагом на пути к дисбиозам. Эра антибиотиков в условиях их неконтролируемого использования также внесла свой существенный вклад в рост дисбиотических состояний.
Развивая далее идеи микробиологической эндоэкологии, можно предположить, что рождение ребенка путем кесарева сечения также дает определенное количество дисбиозов. Вообще, с этой точки зрения плацентацию и длительное эмбриональное развитие в утробе матери можно рассматривать как ценный эволюционно приобретенный механизм длительной адаптации плода и его иммунологического аппарата к микрофлоре матери и семьи, с которой он встретится после рождения [7, 13]. Факторами, формирующими микрофлору новорожденного ребенка, могут быть факторы экзогенной и эндогенной природы. Во-первых, это состояние микрофлоры кишечника и влагалища матери, сроки первого прикладывания к груди и вид вскармливания, условия окружающей среды (степень обсемененности персонала, предметов ухода).
Дисбактериоз — проблема, которая вызывает немало дискуссий. Признавая возможность существования такого патологического состояния, следует помнить, что такой нозологической единицы не существует. Это стабильное нарушение видового спектра, количественного соотношения и качественных характеристик микроорганизмов облигатной и факультативной микрофлоры с существенным уменьшением защитной роли индигенной микрофлоры [1, 4, 11, 17].
Дисбактериоз и дисбиоз — разные понятия. Дисбактериоз — это микробиологическая оценка изменения состава и количественного соотношения в микробиоценозе ЖКТ. Дисбиоз — более общее понятие: это микробиологический дисбаланс в организме, который со временем проявляет себя местными симптомами, а затем и общими нарушениями, отягощающими течение различных заболеваний. Дисбиоз не может употребляться в качестве основного диагноза, он всегда вторичен и не имеет специфических клинических эквивалентов. Именно поэтому мы должны говорить не о лечении, а о коррекции этого состояния.
Причины дисбактериоза у детей представлены в табл. 2.
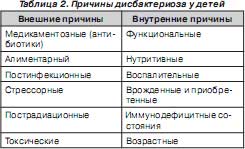
Кроме того, у детей можно выделить 2 критических периода, оказывающих влияние на бактериальную колонизацию кишечника:
— при рождении ребенка (первичная колонизация стерильного кишечника);
— когда ребенка отлучают от груди (изменение характера питания).
Клиническое значение дисбактериоза кишечника заключается не только в понятии микробиологического плана, но и как сопутствующего состояния, имеющего латентное течение или выраженные клинические проявления [8].
Факторами риска в развитии дисбактериоза у новорожденных детей являются: осложненное течение беременности и родов, бактериальный вагиноз и мастит у матери, низкая оценка по шкале Апгар и наличие реанимационных мероприятий у новорожденного, позднее прикладывание к груди, длительное пребывание в родильном доме. Возможности заселения кишечника агрессивными штаммами микроорганизмов окружающей среды способствует физиологическая незрелость моторной функции кишечника, наличие малых гнойных инфекций у новорожденного.
Факторами риска в развитии дисбактериоза у детей раннего возраста чаще всего могут быть: неблагоприятный преморбидный фон, раннее искусственное вскармливание, диспептические нарушения, частые ОРВИ и ОРВИ на 1-м году жизни, явления диатеза, рахита, анемии, гипотрофии, изменения в психоневрологическом статусе ребенка, инфекционная или соматическая патология.
В развитии дисбактериоза у детей дошкольного и школьного возраста следует учитывать: нерациональное питание, пребывание в закрытых коллективах, наличие хронических заболеваний и их нерациональное лечение, частые ОРВИ с применением антибиотиков, аллергические реакции, вегетососудистая дисфункция, гормональная перестройка организма и эндокринопатии.
Вне зависимости от возрастной группы дисбиотические нарушения развиваются после перенесенных кишечных инфекций, лечения антибактериальными препаратами, длительной гормонотерапии или лечения нестероидными противовоспалительными препаратами, оперативных вмешательств, стрессорных воздействий.
Клиническими проявлениями дисбактериоза у детей следует считать: снижение колонизационной резистентности слизистой кишечника; синдром желудочно-кишечной диспепсии; аноректальный синдром; синдром гиповитаминоза В-группы и др., расстройства системы пищеварения и трофики; снижение детоксицирующей функции кишечной микрофлоры; нарушение иммунного статуса.
На сегодня остается проблемой модифицированная классификация дисбактериозов, предложенная А.Ф. Билибиным (1970). Она представлена в табл. 3.
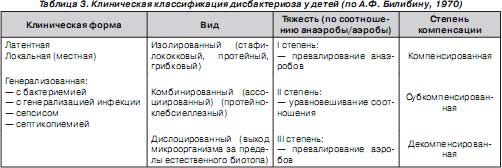
Заболевания, при которых наиболее часто наблюдаются изменения состава кишечной микрофлоры, могут быть различными и многообразными. Однако чаще всего это 4 группы заболеваний.
I группа. Заболевания органов пищеварения: диарея, запоры, синдром мальабсорбции, метеоризм, гастрокардиальный синдром (синдром Ремхельда), гастриты, дуодениты, язвенная болезнь желудка и двенадцатиперстной кишки, энтериты, колиты, псевдомембранозный энтероколит, неспецифический язвенный колит и болезнь Крона, синдром раздраженного кишечника, злокачественные опухоли желудка, толстой кишки, острая мезентериальная ишемия, холецистит, холангит, желчнокаменная болезнь, панкреатит.
II группа. Гнойно-воспалительные заболевания (эндо- и суперинфекции): локальные формы гнойной хирургической инфекции (фурункулы, абсцессы, флегмона, мастит, остеомиелит, гнойные деструктивные пневмонии, некротический колит новорожденных и др.), раневая инфекция, генерализованные воспалительные реакции, пиелонефрит и инфекция мочевыводящих путей, мочекаменная болезнь, бактериальный вагиноз, хронические инфекции, вызванные возбудителями, передающимися половым
путем.
III группа. Иммунопатологические и аллергические заболевания: вторичные дисфункции иммунной системы (частые простудные заболевания и др.), атопический дерматит и другие аллергодерматозы (крапивница и др.), гастроинтестинальная и пищевая аллергия, аллергический ринит, бронхиальная астма, ревматоидный артрит, спондилоартриты, другие болезни суставов и соединительной ткани.
IV группа. Болезни, связанные с нарушением метаболизма: патология периода беременности, хроническая внутриутробная гипоксия плода, церебральная ишемия новорожденных, преморбидные факторы (анемия, рахит, гипотрофия и дефицит питания, гиповитаминозы), гепатиты, печеночная (портальная) энцефалопатия, острая и хроническая почечная недостаточность.
Факторами, определяющими формирование клинических симптомов дисбиоза кишечника, следует считать: избыточную продукцию органических кислот в результате микробного гидролиза пищевых компонентов, повышение осмолярности кишечного содержимого, снижение уровня внутрикишечного рН с инактивацией пищеварительных ферментов, нарушением процессов пищеварения и всасывания. Происходящая преждевременная бактериальная деконъюгация и избыточный пассаж желчных кислот, а также гидроксилирование жирных кислот в толстую кишку сопровождаются: стимуляцией интестинальной секреции слизи и воды с потерей жидкости и электролитов, структурными нарушениями слизистой оболочки кишки, нарушением гидролиза и всасывания пищевого жира.
Моторные расстройства различных отделов кишечника наиболее часто возникают при дуоденальной гипертензии, характеризуются наличием горечи во рту, воздушными отрыжками, чувством быстрого насыщения, тяжести и болей в эпигастрии, тошнотой и эпизодической рвотой, приносящей облегчение. Гипермоторная дискинезия тонкой и/или толстой кишки сопровождается безболевыми поносами и
спастической дискинезией толстой кишки с наличием запоров, бобовидного кала и болей в животе.
Коррекция дисбактериозов у детей включает: соблюдение диеты с учетом основного заболевания и типа диспептических проявлений, проведение энтеросорбции, включение пробиотиков или пребиотиков, ферментных препаратов. В зависимости от степени компенсации дисбактериоза, а именно при субкомпенсированной форме, целесообразным следует считать включение специфических бактериофагов. При декомпенсированном дисбиозе рекомендуется лечение в условиях стационара [1, 3, 13, 16, 18].
В существующей на сегодня классификации пре/пробиотиков выделяют следующие группы:
І — монокультуры нормальной микрофлоры кишечника: коли-, бифидум-, лактобактерин (в 70-е годы назывались эубиотиками);
ІІ — продукты микробного метаболизма: хилак форте (молочная кислота), дуфалак (дисахарид);
ІІІ — самоэлиминирующиеся антагонисты: бактисубтил, энтерол, биоспорин;
IV — комбинированные: облигатная + факультативная или иная микрофлора: бификол — с 6 мес. (бифидобактерии + E.coli ), линекс (лакто-, бифидобактерии + стрептококки);
V — синбиотики: микроорганизмы + компоненты для усиления терапевтического эффекта: бифиформ (бифидофлора + энтерок. + глюкоза + лактулоза + экстр. дрожжей);
VI — монокультуры нормальной микрофлоры кишечника + витамины: Лактовит форте ( L.аcid b acillus +
витамин B 12 + фолиевая кислота).
Примечание: в группу мультипробиотиков включен симбитер [17].
Особое внимание не только педиатров, но и акушеров-гинекологов, неонатологов привлекает значение лактофлоры в коррекции дисбиотических процессов [2, 10, 11, 18].
Как известно, лактобактерии продуцируют молочную кислоту, перекись водорода, лизоцим, лактоцидин, плантарицин, реутерин, лактолин. Кроме того, лактобактерии стимулируют фагоцитоз, синтез Ig, ИЛ-1, ИФН, ФНО, колонизацию облигатной флоры. Лактобактерии участвуют в коррекции биохимических процессов в кишечнике с участием протеолитических активных микроорганизмов, рециркуляции желчных кислот и холестерина, сохранении баланса состава микробных популяций после приема антибиотиков. Они подавляют рост следующих бактерий: Klebsiella pneumoniae, Proteus vulgaris, Pseudomonas aeruginosa, P. f lourescens, Salmonella typhosa, S. s chottmuelleri, Sarcina lutea, Shigella dysenteriae, S. p aradysenteriae, Serratia marcescens, Staphylococcus aureus, Streptococcus faecalis, S.lactis, Vibrio comma.
К оценке клинической картины и лабораторных исследований при дисбактериозах следует подходить дифференцированно. Отличию так называемых дисбиотических реакций от истинного дисбактериоза способствует выполнение 2–3-кратных исследований с интервалом не менее 14 дней. Так, в первом случае сдвиги в составе микрофлоры кишечника непродолжительны и исчезают через 5–7 дней без какого-либо лечения.
Современные подходы к коррекции и поддержанию нормального состава кишечной микрофлоры заключаются в выявлении основного заболевания, лежащего в основе нарушений кишечной микрофлоры, и проведении этиологической и патогенетической коррекции с целью нормализации процессов пищеварения, всасывания и моторики пищеварительного тракта. Важным в этом периоде следует считать соблюдение диеты, соответствующей основному заболеванию, а также типу диспепсии. При бродильных процессах на 5–7 дней ограничивается употребление углеводов, растительной клетчатки, при гнилостных — жиров и белков. Исключаются бобовые, пресное молоко и продукты, богатые эфирными маслами (репа, редька, зеленый лук, чеснок и др.). Обязательно назначение пробиотиков — биологических препаратов, содержащих нормальную микрофлору кишечника, и пребиотиков — препаратов, способствующих ее росту и функционированию. При этом назначение антибактериальных средств для деконтаминации кишечника проводят по строгим показаниям.
Наиболее приемлемым препаратом, удовлетворяющим требованиям патогенетических механизмов развития дисбиозов у детей, на сегодня является Лактовит форте. Он устойчив к воздействию высокой температуры, антибиотиков и кислой среды желудка. Препятствует росту патогенных бактерий в кишечнике и способствует стимуляции роста естественной лактофлоры после прекращения приема. Обладает репаративными и иммуномодулирующими свойствами — повышает общий уровень секреторного IgA и титры специфических секреторных
антител, усиливает фагоцитоз. Медленно выводится из организма (10–12 дней). Содержит витамин В 12 и фолиевую кислоту, которые обладают синергичным действием и восстанавливают слизистую оболочку кишечника.
Показан детям с первых месяцев жизни, беременным и кормящим женщинам.
Показаниями к применению Лактовита форте являются: острые диареи ротавирусной этиологии (профилактическая антидиарейная эффективность), хронические и неспецифические язвенные колиты различной этиологии, дисбактериозы, возникшие в результате применения антибактериальных или сульфаниламидных препаратов и др., антибиотик-ассоциированные диареи, острые кишечные инфекции или как поддерживающая терапия при крапивнице, экземе, диатезе, атопическом дерматите.
Препарат удобен в применении. Назначается 2 раза в день за 40 мин до еды. Детям до 1 года — по 1/2 капсулы, детям от 1 до 6 лет — по 1 капсуле, старше 6 лет и взрослым — по 1–2 капсулы. Для сохранения жизнеспособности компонентов препарата не рекомендуется запивать его горячими напитками. Детям до 1 года препарат дают непосредственно перед кормлением, растворив содержимое капсулы в молоке.
Таким образом, пробиотики на основе спор лактобацилл (Лактовит форте) вполне обоснованно рассматриваются как эффективный метод восстановления состава и функций физиологического микробиоценоза человека. Появление новой информации относительно лактобацилл, бифидобактерий, и в частности пропионовокислых бактерий, создает огромные перспективы для пополнения арсенала современных пробиотиков новыми генерациями этих препаратов с уникальными биологическими свойствами.
1. Ардатская М.Д., Дубинин А.В., Минушкин О.Н. Дисбактериоз кишечника: современные аспекты изучения проблемы, принципы диагностики и лечения // Терап. арх. — 2001. — № 2. — С. 67-72.
2. Баранов А.А., Щербакова Э.Г., Дорофейчук В.Г. и др. Лизоцимсодержащие биосистемы для профилактики и лечения социально значимых болезней детского возраста // Российский педиатрический журнал. — 2000. — № 4. — С. 9-14.
3. Бекетова Т. Нові підходи до лікування порушень мікробіоценозу травної системи у дітей // Ліки України. — 2002. — № 2. — С. 55-56.
4. Бережной В.В., Янковский Д.С., Крамарев С.А., Шунько Е.Е., Дымент Г.С. Нарушения микробной экологии человека, их причины, последствия и способы восстановления физиологической нормы // Здоровье женщины. — 2004. — № 2 (18). — С. 170-178.
5. Билибин А.Ф. Дисбактериоз, аутоинфекция и их значение в патологии // Клиническая медицина. — 1970. — Т. 48, № 2. — С. 7-12.
6. Бондаренко В.М., Рубакова Э.И., Лаврова В.А. Иммуностимулирующее действие лактобактерий, используемых в качестве основы препаратов — пробиотиков // Микробиология, эпидемиология, иммунология. — 1998. — № 5. — С. 107-112.
7. Венцковский Б.М., Товстановская В.А., Янковский Д.С., Дымент Г.С. Микроэкологические аспекты репродуктивного здоровья женщины и современные подходы к его поддержанию // Здоровье женщины. — 2002. — № 3(11). — С. 86-91.
8. Грачева Н.М. Клинические особенности различных форм дисбактериоза // Лечащий врач. — 1999. — № 2–3. — С. 17-21.
9. Дещекина М.Ф., Коршунов В.М., Демин В.Ф. и др. Изучение формирования микрофлоры кишечника у новорожденных детей при совместном и раздельном пребывании с матерью // Педиатрия. — 190. — № 1. — С. 13-17.
10. Копанев Ю.А., Кузьменко Л.Г. Особенности применения препаратов для микробиологической коррекции дисбактериоза у детей // Лечащий врач. — 2000. — № 5–6. — С. 50-51.
11. Копанев Ю.А., Алешкин В.А. Дисбактериоз кишечника и дисбиотические реакции у детей // Педиатрия. — 2002. — № 6. — С. 100-103.
12. Парфенов А.И. Микробная флора кишечника и дисбактериоз // Русский медицинский журнал. — 1998. — Т. 6, № 18. — С. 1170-1173.
13. Тутченко Л.І., Отт В.Д., Марушко Т.Л., Марушко Р.В. та ін. Особливості формування системи мікробіоценозу у новонароджених немовлят та шляхи його оптимізації // Журнал практикуючого лікаря. — 2001. — № 5. — С. 24-30.
14. Тюрин М.В., Шендеров Б.А., Рахимова Н.Г. и др. К механизму антагонистической активности лактобацилл //
Микробиология, эпидемиология, иммунология. — 1989. — № 2. — С. 3-8.
15. Урсова Н.И., Щеплягина Л.А., Краснова Е.Н. Микробиоценоз открытых биологических систем организма в процессе адаптации к окружающей среде // Российский педиатрический журнал. — 2002. — № 5. — С. 21-24.
16. Янковский Д.С., Бережной В.В., Шунько Е.Е., Крамарев С.А., Дымент Г.С. Настоящее и будущее пробиотиков как биокорректоров микроэкологических нарушений // Современная педиатрия. — 2004. — № 1(2). — С. 111-118.
17. Янковский Д.С. Микробная экология человека: современные возможности ее поддержания и восстановления. — Киев, Эксперт ЛТД. — 2005. — 388 с.
18. Gill H.S., Rutherfurd J., Prasad J., Gopal P.K. Enhancement of natural and acquired immunity by Lactobacillus rhamonosus (HN001), Lactobacillus acidophilus (HN017) and Bifidobacterium (HN019) // Brit. J. Nutr. — 2000. — V. 83 (2). — P. 167-176.
19. Marteau P., Pambaud J.C. Potencial for using lactic Acid bacteria for therapy and immunomodulation in nean // FEMS Microbiol. Rev. — 1993. — V. 12. — P. 207-220.
