Журнал «Здоровье ребенка» 3 (24) 2010
Вернуться к номеру
Стан міокарда в дітей із природженими вадами серця у віддалений період після хірургічної корекції
Авторы: Гончарь М.О., Національний медичний університет, кафедра педіатрії № 1 і неонатології, м. Харків
Рубрики: Педиатрия/Неонатология
Версия для печати
У статті подані власні спостереження 110 дітей із природженими вадами серця у віддаленому післяопераційному періоді, на підставі яких проаналізовані дані клініко-інструментального обстеження і плазмова концентрація тропоніну І. Обгрунтована доцільність дослідження рівня тропоніну І з метою діагностики пошкодження міокарда у прооперованих пацієнтів.
Природжені вади серця, тропонін I, міокардіальна дисфункція, діагностика.
Тривалі гемодинамічні порушення в пацієнтів із природженими вадами серця (ПВС) можуть призводити до вторинних змін у міокарді [1], що навіть після адекватної хірургічної корекції несприятливо впливає на перебіг найближчого післяопераційного періоду й на функціональний стан серцево-судинної системи у віддалені строки спостереження [2]. Доведена висока специфічність тропоніну І (ТnІ) щодо ушкодження міокарда [2, 3]. Дані про інформативність тропонінів у дітей та їх використання в клінічному спостереженні й лікуванні пацієнтів із ПВС нечисленні [4–6]. У той же час використання біомаркерів, що дають змогу визначити пошкодження міокарда, може бути корисним для суттєвого доповнення можливостей інструментальної діагностики міокардіальної дисфункції і профілактики серцевої недостатності у прооперованих пацієнтів [5–7].
Метою дослідження стало вдосконалення діагностики пошкодження міокарда в дітей із природженими вадами серця у віддаленому післяопераційному катамнезі шляхом комплексного клініко-інструментального обстеження й визначення плазмової концентрації тропоніну І.
Матеріали і методи
Обстежені 110 пацієнтів у віддаленому катамнезі після хірургічної корекції природжених вад серця, серед яких були 54 (49,1 %) хлопчики і 56 (50,9 %) дівчаток. Проведене клініко-анамнестичне й інструментальне дослідження, що включало ЕКГ, ДЕхоКГ із дослідженням систолічної функції лівого шлуночка (ЛШ) і притокового відділу правого шлуночка (ПШ) методом Simpson, діастолічної функції шлуночків на основі аналізу трансмітрального і транстрикуспідального потоків; визначення середнього тиску в легеневій артерії (ЛА) за методом Кіtabatake. Усім пацієнтам досліджена плазмова концентрація тропоніну І (DAI, США). Для статистичної обробки отриманих результатів використовувався пакет програм обробки даних загального призначення Statistica for Windows версії 6.0, а також пакет аналізу Microsoft Office Excel. Були отримані дані описової статистики для показників кількісної шкали: медіана (Me) як міра положення; квартилі (нижній — LQ та верхній — UQ), інтерквартильний розмах (тобто діапазон, до якого належить 50 % варіації) як міра розсіювання. Для опису якісної варіації використовували частоту зустрічальності ознаки. Для визначення розбіжностей між групами й оцінки міри залежності між змінними використовували непараметричні методи статистики — коефіцієнт рангової кореляції Спірмена й медіанний тест.
Результати і їх обговорення
67 (60,9 %) пацієнтів були прооперовані з приводу вади із гіперволемією малого кола кровообігу (МКК), 33 (30 %) — із приводу вад зі збідненим кровотоком у МКК і 10 (9,1 %) — із приводу вад із незміненим кровотоком у судинах малого кола.
Усі досліджені були розподілені на групи за показником нормального (група І) або підвищеного (група ІІ) рівня тропоніну І. До аномальних показників відносили плазмову концентрацію ТnІ, вищу за 0,5 нг/мл [3]. Нормальний рівень TnІ встановлений у 91 (83 %), Ме І = 0,12 (0,08–0,19) нг/мл; підвищений — у 19 (17 %) досліджених, Ме II = 1,0 (0,96–1,76) нг/мл (p < 0,001). Результати порівняльної характеристики пацієнтів за показниками віку, ваги і зросту у віддаленому післяопераційному катамнезі в межах груп із підвищеним і нормальним рівнями тропоніну І наведені в табл. 1.
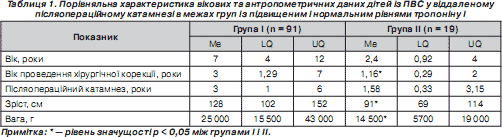
Таким чином, вік радикальної корекції вади становив відповідно 3,0 (1,29–7,0) року в дітей із нормальним значенням тропоніну І і 1,16 (0,29–2,0) року у прооперованих дітей із підвищенням його плазмової концентрації. Проведення кардіохірургічного лікування вірогідно раніше в пацієнтів ІІ групи було обумовлене більшою вираженістю в них гемодинамічних порушень у доопераційному періоді, більшою складністю й тяжкістю природженої вади, що потребувало проведення невідкладної корекції. Термін післяопераційного катамнезу в дітей І і ІІ груп вірогідно не відрізнявся (табл. 1).
У структурі діагнозів обстежених із нормальним рівнем TnІ комбіновані вади становили 30,4 % на відміну від прооперованих із підвищеним рівнем тропоніну, серед яких пацієнти з комбінованими ПВС становили переважну більшість (78,9 %). Клінічні прояви серцевої недостатності виявлені у 24 % пацієнтів із нормальним рівнем тропоніну І і в 68,4 % прооперованих із гіпертропонінемією. Решунтування септальних дефектів також значно частіше діагностувалось у пацієнтів із підвищенням плазмової концентрації TnI, становлячи 17,7 і 47,3 % в І і ІІ групах відповідно. Прояви ремоделювання серця, наявність помірної або значної регургітації на мітральному або трикуспідальному клапанах, клапані легеневої артерії за даними ультразвукового дослідження також значно частіше виявлялись у прооперованих ІІ групи (78,9 на відміну від 32,9 % у дітей із нормальним рівнем TnI).
Дані ДЕхоКГ-дослідження в пацієнтів І і ІІ груп наведені в табл. 2.
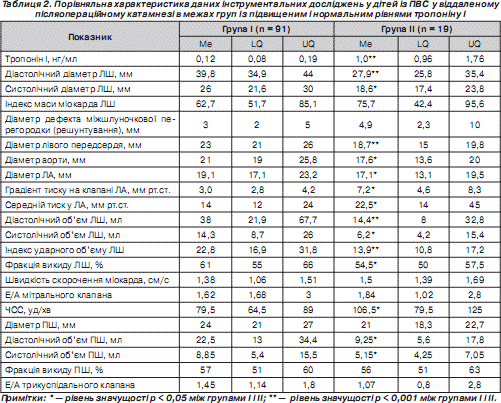
Виявлені розбіжності між показниками діастолічного й систолічного розмірів ЛШ, діастолічного й систолічного об''ємів лівого і притокового відділу правого шлуночків, діаметра лівого передсердя, діаметрами магістральних судин у межах груп із нормальним і підвищеним тропоніном І у першу чергу були обумовлені вірогідною різницею показників фізичного розвитку, тобто віковими відзнаками пацієнтів І і ІІ груп. У той же час аналіз індексованих показників гемодинаміки свідчив про вірогідне зниження індексу ударного об''єму ЛШ і фракції викиду ЛШ у дітей ІІ групи. Індекс маси міокарда ЛШ був вірогідно вищим у дітей із гіпертропонінемією, тобто частіше ушкоджувався гіпертрофований міокард (табл. 2).
Привертала увагу тенденція до дилатації легеневої артерії у дітей ІІ групи (17,1 (13,1–19,5) мм у пацієнтів віком 2,4 (0,92–4,0) року) на відміну від нормальних за віком значень цього показника в дітей І групи. Вищевикладене пояснювалося вірогідно вищим показником середнього тиску в легеневій артерії в пацієнтів із гіпертропонінемією і свідчило про наявність у них резидуальної легеневої гіпертензії (табл. 2). Резидуальна легенева гіпертензія була діагностована в 11,4 % дітей І групи й у 31,5 % ІІ групи. Установлені вірогідні відмінності середніх значень рівня тропоніну в пацієнтів із нормальним тиском у стовбурі легеневої артерії і з високою легеневою гіпертензією до операції на рівні значущості р = 0,002.
З метою аналізу міри залежності між плазмовою концентрацією тропоніну І і показниками клінічного й інструментального обстеження були проаналізовані відповідні коефіцієнти рангової кореляції. Виявлені кореляційні зв''язки між рівнем тропоніну І і наявністю парадоксального руху міжшлуночкової перегородки (r = 0,74, р = 0,01), рівнем тропоніну І і наявністю аритмії (r = 0,41, р = 0,04), рівнем тропоніну І і градієнтом тиску на клапані легеневої артерії (r = 0,38, р = 0,05), рівнем тропоніну І і середнім тиском у легеневій артерії (r = 0,31, р = 0,001).
Заслуговує на увагу високої сили кореляційний зв''язок між TnІ і порушеннями процесів реполяризації міокарда (r = 0,68, р = 0,01). Проявів гострих коронарних подій за даними ЕКГ в обстежених виявлено не було.
Тенденція до зниження фракції викиду ЛШ як показника скоротливої здатності міокарда при зростанні плазмової концентрації тропоніну підтверджувалася також при аналізі даних пацієнтів із різними ступенями тяжкості серцевої недостатності (СН). Так, у пацієнтів із СН І рівень тропоніну І становив Ме = 0 (0–0,2) нг/мл; у групі з СН ІІА Ме = 1,0 (0,1–1,7) нг/мл; у групі з СН ІІБ Ме = 1,7 (0,1–4,2) нг/мл; вірогідність відмін встановлена на рівні значущості p = 0,03. Наведені дані ілюструють тенденцію до підвищення рівня ТnІ у дітей із проявами хронічної серцевої недостатності по мірі зростання ступеня тяжкості останньої.
Висновки
Підвищений рівень плазмової концентрації тропоніну І виявлено у 19 (17,2 %) пацієнтів із природженими вадами серця у віддаленому періоді спостереження після хірургічного лікування.
Пошкодження міокарда частіше розвивається у прооперованих із приводу комбінованих вад із резидуальною легеневою гіпертензією, при наявності гіпертрофії міокарда, решунтування септальних дефектів, сполучується з більш тяжким ступенем серцевої недостатності й аритміями серцевої діяльності.
Перспектива подальших розробок. Вважаемо обгрунтованою й доцільною розробку лікувальної тактики прооперованих із підвищеним рівнем тропоніну І у віддаленому катамнезі після операції.
1. Волосовец А.П., Кривопустов С.П. Инсульт головного мозга и инфаркт миокарда у детей: современный взгляд на проблему // Здоровье ребенка. — 2008. — № 3. — С. 63-69.
2. Сенаторова Г.С., Гончарь М.О., Страшок О.І. Міокардіальна дисфункція у дітей з природженими вадами серця: використання патофізіологічних біомаркерів // Таврический медико-биологический вестник. — 2009. — № 2(46). — С. 41-45.
3. Егорова М.О. Биохимическое обследование в клинической практике. Практическая медицина. — М., 2008. — С. 120-122.
4. Katus H.A., Giannitsis E., Jaffe A.S., Thygesen K. Higher sensitivity troponin assays: Quo vadis? // Eur. Heart J. — 2009. — 30. — 127-128.
5. Lipshultz S.E., Wong J.C., Lipsitz S.R. Frequency of clinicalli unsuspected myocardial injuri at a children’s hospital // Am. Heart J. — 2006. — 151(4). — 916-922.
6. Sabatine M.S., Morrow D.A., de Lemos J.A., Jarolim P., Braunwald E. Detection of acute changes in circulating troponin in the setting of transient stress test-induced myocardial ischaemia using the ultrasensitive assay: results from TIMI 35 // Eur. Heart J. — 2009. — 30. — 162-169.
7. Гончарь М.О., Сенаторова Г.С., Страшок О.І. Спосіб оцінки ефективності терапії серцевої недостатності у дітей з природженими вадами серця. Патент № 40574, Заявл. 19.01.2009; Опубл. 10.04.2009. Бюл. № 7. — 4 с.
