Журнал «Травма» Том 12, №1, 2011
Вернуться к номеру
Проблемы оказания неотложной помощи пациентам с травматическим шоком и основные направления организации интенсивной терапии
Авторы: Колесников А.Н., Серединская А.И., Симаков М.М., Бутко А.С., Стасюк В.Н., Высочин В.Н., Лозовский Р.С., Андреева Т.В., Мендзяк Р.М. Донецкий национальный медицинский университет им. М. Горького Коммунальное медицинское учреждение «Клиническая Рудничная больница», г. Макеевка
Рубрики: Травматология и ортопедия
Версия для печати
В данной статье на основании анализа работы службы неотложной помощи городской клинической больницы крупного промышленного региона сделана попытка выявить основные диагностические, терапевтические и организационные ошибки, которые могут приводить к необоснованной летальности в группе пациентов с травматическим шоком. Разработан алгоритм диагностических и лечебных мероприятий, начиная с этапа приемного отделения. Произведен сравнительный анализ применения препарата гиперХАЕС и комбинации «гидроксиэтилкрахмал — кристаллоиды» при травматическом шоке.
Травматический шок, организация помощи, гиперХАЕС.
Невзирая на то что проблема шока не нова, травматизм и травматический шок (ТШ) — одна из актуальных проблем современной медицины, поскольку среди пострадавших с политравмой отмечается высокая летальность и высокая степень инвалидизации. Травматический шок встречается в 3 % случаев повреждений мирного времени, а при сочетанных и множественных травмах частота его увеличивается до 8–15 %. Шок — одно из самых тяжелых осложнений, он заканчивается смертью у 25–85 % пострадавших.
С необходимостью оказания помощи при травмах человек столкнулся очень давно. О возможности оказания помощи при переломах свидетельствуют археологические раскопки и находки. Вот несколько исторических дат и событий, которые считаются важными в становлении науки о повреждении человеческого тела:
Гиппократ (IV век до н.э.) — труды «О переломах», «О суставах», «Ранения головы». Лечение переломов и вывихов;
Корнелий Цельс (I век до н.э.) — «О медицине», операции на костях (выскабливание, прижигание, трепанация);
Гален (130–200 гг. н.э.) — учение о деформациях скелета;
Амбруаз Паре (XVI век) — лечение ран, открытых переломов;
Г. Дюпюитрен (XIX век) — описание и лечение переломов конечностей; Рентген (1895) — открытие Х-лучей; в России — основатели научных школ XIX века проф. Х.Х. Саломон, Е.О. Мухин, Н.И. Пирогов (военно-полевая хирургия, эфирный наркоз, гипсовая повязка, ампутации конечностей, топографо-анатомический подход).
Существует множество описаний/формулировок шока. Изменения, характерные для шока, описал Амбруаз Паре в 1575 г.: «...при падении с высоты на что-нибудь жесткое или при ударах, вызывающих ушибы...» Термин «шок» (удар) впервые появился при переводе сочинения французского хирурга Ле Драна на английский язык в 1743 г.: «Ядро, выброшенное пороховой пушкой, приобретает такую силу, что повергает всю животную машину в шок и возбуждение...» Весьма интересна клиническая картина шока, нарисованная русским врачом штаб-лекарем Акимом Чаруковским (1836): «Постоянный спутник ушиба есть бесчувствие (stupor); при нем ушибленные части до того теряют свою чувствительность, что их можно совсем отрезать, а раненый того и не заметит, будучи совершенно равнодушен к самому себе, к друзьям и родным своим. Уменьшение теплоты есть второй признак бесчувствия; к ним присоединяется бездействие жизненных отправлений, от раненого места простирающееся на все тело: взгляд раненого страшен, глаза неподвижны, черты лица осунувшиеся, рот полуоткрыт, язык сухой, дыхание медленное, пульс малый, слабый, неправильный и часто перемежный, больной кажется чуждым ко всему вокруг его происходящему, тело его мягкое, слабое». Термин «шок» появился и внедрился в медицинскую терминологию в 1743 году в английском переводе Кларка. Это слово означает удар, толчок. Самое краткое определение понятия «шок»: «Шок — это острое нарушение питающего кровотока», т.е. капиллярного кровообращения, где осуществляется обмен веществ. Травматический шок — синдром гипоциркуляции в ответ на тяжелое механическое повреждение с преимущественным влиянием кровопотери.
Современные же данные статистики выглядят далеко не утешающими: по данным ВОЗ, в год от травмы погибает до 2 млн человек. Наибольший удельный вес в этой статистике занимает не изолированная, а сочетанная травма, составляющая 60–70 % всех травм. Травматизм является основной причиной смерти наиболее трудоспособного контингента людей Украины в возрасте до 40 лет, а смертность по регионам колеблется от 12,4 и более случаев на 10 тыс. населения в Закарпатье до 23,5 на 10 тыс. населения в крупных промышленных центрах. В Украине ежегодно травмы различной тяжести получают более 4,5 млн человек. Летальность вследствие травм в Украине в последние годы имеет стойкую тенденцию к росту. Если в 1993 году погибло 27 494 травмированных, то в 1995 — 30 965, 1998 году — 33 538, в 2001 — 37 431 человек, 2003 году — до 40 000 человек.
В 2008 г. в Донецкой области зарегистрировано 241 383 случая травм (2007 г. — 254 272), кроме того, различных последствий травм — 23 142 (2007 г. — 22 745). От различных несчастных случаев установлена смерть в 7610 случаях (2007 г. — 7777), на 100 тыс. населения — 168,1 (2007 г. — 168,7). От механических травм погибло 2956 (2007 г. — 3313) человек, в т.ч. от автотравм — 667 (2007 г. — 826), мототравм — 155 (2007 г. — 147), велосипедных травм — 17, ж/д травм — 90 (2007 г. — 119). От поражения электротоком погибло 69 (2007 г. — 80) человек, от высоких и низких температур — 833 (2007 г. — 691). Смерть от высоких температур наступила у 159 человек, как и в 2007 году. В 2008 году уровень первичной инвалидности при травмах на 10 тыс. взрослого населения составил 8,8 (2007 г. — 9,1), а на 10 тыс. трудоспособного населения — 11,2 (2007 г. — 11,3), в том числе уровень инвалидности при производственных травмах на 10 тыс. трудоспособного населения составил 3,1 (2007 г. — 3,2).
Цель работы: в данной статье на основании анализа работы службы неотложной помощи (приемное отделение, диагностическое отделение, отделение интенсивной терапии (ИТ), хирургические отделения) городской клинической больницы крупного промышленного региона мы сделали попытку выявить основные диагностические, терапевтические и организационные ошибки, которые могут приводить к необоснованной летальности в группе пациентов с травматическим шоком. Разработать алгоритм оказания неотложной помощи и диагностических/лечебных мероприятий, начиная с этапа приемного отделения. Разработать и применить алгоритм малообъемной реанимации с использованием гипертонических растворов гидроксиэтилкрахмалов (гипер-ХАЕС).
Материал и методы
Анализ за 5 лет (2005–2009 гг.) историй болезни пациентов с тяжелой сочетанной и черепно-мозговой травмой (ЧМТ), находившихся на лечении в отделениях интенсивной терапии, травматологии, нейрохирургии КМУ «КРБ» г. Макеевки. Анализ тактики оказания неотложной помощи больным с сочетанной и комбинированной травмой на этапах госпитализации с разработкой протоколов обследования и алгоритма помощи больным во время пребывания их в приемном отделении и транспортировки в профильные отделения.
На этапах госпитализации умерло 14 больных (6 %).
Результаты и обсуждение
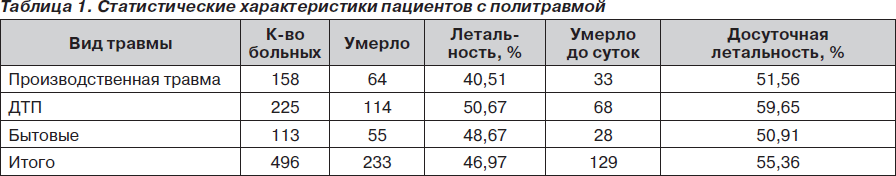
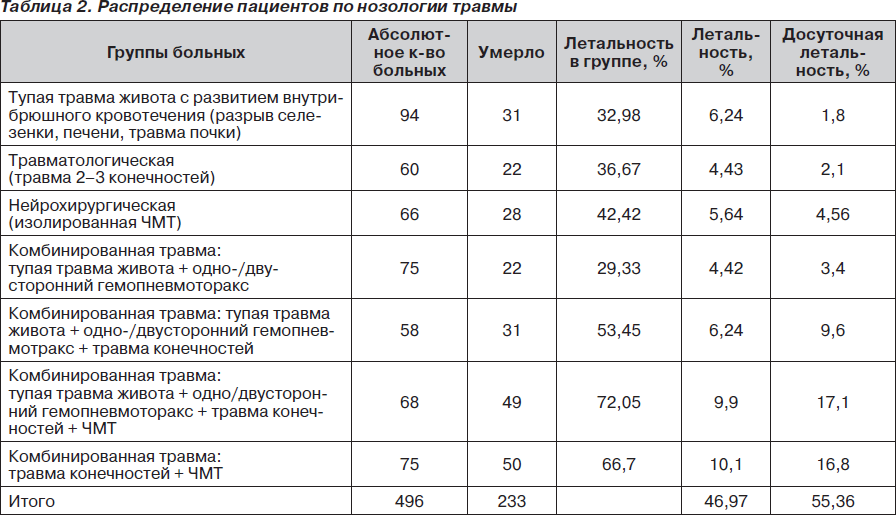
Как видно из табл. 1, 2, летальность среди пациентов с политравмой увеличивается пропорционально областям повреждения и степени важности поврежденных органов. Так, наиболее высокая внутригрупповая летальность отмечается в группе с комбинированной травмой: тупая травма живота + одно-/двусторонний гемопневмотракс + травма конечностей + ЧМТ. В этой же группе отмечается и высокая досуточная летальность. Как показал более детальный анализ историй болезни, среди пациентов с досуточной летальностью более 30 % летальных случаев было отмечено на этапах приемного отделения или транспортировки в операционную/отделение интенсивной терапии. В данной статье умышленно не обсуждаются проблемы догоспитального этапа, хотя влияние именно этого этапа во многих случаях может оказаться решающим.
Шок — заболевание полиэтиологическое. В зависимости от причины возникновения различают следующие виды ТШ: а) в результате механической травмы (раны, переломы костей, сдавление тканей и др.); б) ожоговой травмы (термические и химические ожоги); в) воздействия низкой температуры (холодовый шок); г) электротравмы (электрический шок).
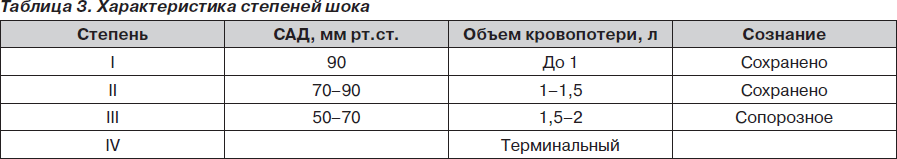
Клиническая классификация подразделяет шок по тяжести на четыре степени (табл. 3).
Шок I степени: сознание сохранено, больной контактен, слегка заторможен. Систолическое артериальное давление (САД) превышает 90 мм рт.ст., пульс учащен.
Шок II степени: сознание сохранено, больной заторможен, САД 90–70 мм рт.ст., пульс 100–120 ударов в минуту, слабого наполнения, дыхание поверхностное.
Шок III степени: больной адинамичен, заторможен, на боль не реагирует, на вопросы отвечает односложно. Кожные покровы бледные, холодные, с синюшным оттенком. Дыхание поверхностное, частое. САД ниже 70 мм рт.ст., пульс более 120 ударов в минуту, нитевидный, центральное венозное давление (ЦВД) равно нулю или отрицательное. Наблюдается анурия (отсутствие мочи).
Шок IV степени: проявляется клинически как одно из терминальных состояний.
Токсическая теория. Согласно токсической теории Е. Кекю, тяжелые изменения в организме при травматическом шоке объясняются отравлением продуктами распада поврежденных тканей, прежде всего мышц. Интоксикация приводит к расширению капилляров и увеличению их проницаемости. Это вызывает снижение объема циркулирующей крови (ОЦК) и определяет картину шока.
Сосудодвигательная теория. В соответствии с этой теорией, разработанной Г. Крайлем, травма вызывает рефлекторный паралич периферических сосудов, что способствует прогрессирующему снижению артериального давления и скоплению крови в венозной системе. Снижается кровоснабжение жизненно важных органов, нарушается их функция вплоть до гибели больного.
Эндокринная теория. Эта теория разрабатывалась отечественными учеными Н.А. Миславским и Л.А. Орбели, а затем была существенно дополнена канадским ученым Г. Селье. Травматический шок Г. Селье рассматривал как III стадию общего синдрома адаптации, возникающую в результате истощения передней доли гипофиза и коры надпочечников.
Теория акапнии. Теория принадлежит Дж. Гендерсону, который объяснял развитие шока уменьшением содержания углекислоты в крови в результате гипервентиляции легких при болях. Акапния приводит к нарушению микроциркуляции и расстройству обмена веществ, запуская весь механизм изменений в организме. Все указанные теории не лишены рациональных зерен, но ни одна из них не может полностью объяснить развитие травматического шока. Травматический шок является по своей природе полиэтиологичным. Среди основных факторов, имеющих значение в развитии шока при травме, следует выделить болевую импульсацию, кровопотерю, токсемию, а также переохлаждение. В каждом конкретном случае может быть преобладание одного или нескольких из перечисленных факторов.
Патофизиология ТШ. В настоящее время нейрогенная теория шока утратила свое значение. Боль и избыточная афферентная импульсация, если нет гиповолемии, не может привести к шоку. Сейчас не различают две фазы ТШ — эректильную и торпидную, отражающие якобы сначала перевозбуждение центральной нервной системы, а затем ее торможение. Психоэмоциональное и двигательное возбуждение после тяжелого механического повреждения бывает крайне редко. В динамике шока наблюдается напряженная борьба двух противоположных начал — реакций повреждения и реакции защиты, исход которой обычно без медицинской помощи складывается в пользу реакций повреждения. Острая кровопотеря — главный пусковой механизм ТШ. Потеря не эритроцитов, а жидкой части крови определяет выживаемость. Даже глубокая анемия (50–70 г/л гемоглобина) относительно удовлетворительно компенсируется больными, если они не совершают значительных физических усилий. Потеря до 50 % нормального объема эритроцитов при условиях устранения ее основных волемических, реологических и метаболических последствий не является показанием для трансфузии крови. Граница безопасного разбавления крови лежит на уровне 1/3 от должного ее объема.
Нейроэндокринные сдвиги при ТШ:
1. Мобилизация симпатоадреналовой системы; централизация кровообращения; перемещение крови в миокард и мозг вследствие спазма сосудов всех остальных органов; тахикардия; гликогенолиз в печени.
2. Активация системы «гипоталамус — гипофиз — кора» с усиленным выбросом гидрокортизона: стабилизация сердечно-сосудистой системы, улучшение электролитного обмена миокарда и сосудистой стенки; гликонеогенез в печени в результате катаболизма белков и жиров; противоаллергическое и противовоспалительное действие.
3. Усиление секреции альдостерона и антидиурез в канальцах, приводящее к увеличению осмотического давления и содержания воды в крови.
Гуморальные сдвиги при ТШ:
1. Высвобождение гистамина и активизация ККС: депонирование крови в капиллярах вследствие паралича прекапиллярных сфинктеров; нарастание гиповолемии из-за увеличения проницаемости сосудов.
2. Образование ферритина (вазодепрессора) в гипоксической печени: гипотензия вследствие расширения кровеносных сосудов.
3. Образование фактора депрессии миокарда в ишемизированной поджелудочной железе: отрицательное инотропное действие на сердце; нарушение моторики кишечника.
4. Повышение продукции в легких сосудорасширяющих простагландинов.
5. Поступление в кровь эндогенных опиатов — энкефалинов и эндорфинов: при любом виде стресса увеличивается содержание эндогенных опиатов, которые, кроме блокады опиатных рецепторов, нарушают регуляцию кровообращения и способствуют развитию неуправляемой гипотензии, угнетению дыхания.
Циркуляторные сдвиги при ТШ:
1. Изменения макроциркуляции: сужение емкостных сосудов (вен); констрикция резистивных сосудов (артериол). Это ведет к фильтрации в сосудистое русло внесосудистой жидкости; централизация кровообращения.
2. Централизация кровообращения: I фаза (легко обратимая) ишемической гипоксии: лактат-ацидоз, ухудшение реологических свойств крови; II фаза (трудно обратимая): фаза застойной гипоксии. Секвестрация крови в капиллярном русле, агрегация форменных элементов крови, развитие «сладжа», транссудация жидкой части крови из капиллярного русла, возникновение ДВС; III фаза (необратимая): фаза паралича сосудов. Полная несостоятельность кровообращения.
Нарушения обмена веществ при шоке
Развивается «энергетический кризис» вследствие высокой активности симпатоадреналовой системы, гиперкатехоламинемии, повышенной концентрации в крови глюкокортикоидов, тироксина и т.д.
Нарушение углеводного обмена: гликогенолиз, приводящий к гипергликемии (действие адреналина; анаэробный гликолиз вследствие гипоксии тканей, в результате развивается лактат-ацидоз; уменьшение активности инсулина вследствие появления контринсулярных гормонов (адреналин, кортизол, глюкагон), развивается диабетогенное состояние организма.
Нарушение жирового обмена: усиленный липолиз, вызванный адреналином и кортизолом, в условиях неполноценности углеводного обмена; липемия способствует агрегации тромбоцитов, развитию жировой эмболии; развитие кетоацидоза из-за увеличения продукции в печени кетоновых тел.
Нарушение белкового обмена: катаболизм белков под влиянием глюкокортикоидов приводит к гипопротеинемии, потере массы тела.
Нарушение электролитного обмена: переход натрия и воды в клетку, выход калия из нее.
Нарушения кислотно-основного состояния: ацидоз вследствие повышения продукции молочной кислоты и кетокислот; в последующем может развиться метаболический алкалоз из-за передозировки гидрокарбоната натрия, перегрузка цитратом при массивной гемотрансфузии, потеря водородных ионов при аспирации желудочного содержимого через зонд. Алкалоз опаснее ацидоза, т.к. увеличивает сродство гемоглобина к кислороду.
Нарушения газообмена при шоке красноречиво описаны А.П. Зильбером: «При травматическом шоке легкие не могут передать кислород в кровь, кровь не может донести его до тканей, а ткани не в состоянии его усвоить». Для предварительной оценки возможности развития травматического шока на этапах медицинской сортировки созданы специальные таблицы, позволяющие прогнозировать развитие шока и его тяжесть. Вот наиболее характерные примеры: наивысшую шокогенность имеет травма живота с повреждением 2 паренхиматозных органов — 10, открытый оскольчатый перелом бедра — 6, ушиб головного мозга, перелом основания черепа — 5, закрытый перелом бедра — 2, множественные переломы ребер без повреждения легкого — 1. Показатель уровня АД не всегда является достаточно информативным для установления тяжести шока. Более информативным является индекс Алговера — отношение частоты пульса к систолическому артериальному давлению.

Показатели 0,8–1,0 соответствуют I степени, 1,1–1,5 — II степени, 1,6 и более — III степени.
Травма любой локализации практически всегда сопровождается кровопотерей. Объем кровопотери условно можно оценить по табличным данным: перелом плеча — 200–500 мл, перелом голени — 350–650 мл, перелом бедра — 800–1200 мл, перелом таза — 1200–2000 мл. Оценка эффективности циркуляции кроме АД и пульса — хорошо оценивает показатель ЦВД — характеризует перфузионную способность сердца и позволяет контролировать проводимую инфузионную терапию (норма — 5–10 см вод.ст.). Критический уровень ЦВД — 15–20 см вод.ст. характеризует сердечную недостаточность, низкие значения — продолжающееся кровотечение, невосполненную кровопотерю. Измерение ЦВД проводится при канюлировании центральной вены. Диурез — почасовой, минутный диурез характеризует выделительную функцию почек. Ниже 40 мл/час — критический уровень, менее 25 мл/час — олигоанурия, ниже 50 мм рт.ст. происходит прекращение фильтрационной способности почек. Контроль осуществляется с помощью постоянного мочевого катетера.
В случаях острой кровопотери начальный (должный) ОЦК рассчитывается путем умножения идеальной массы на 85 мл/кг (если обследуется мужчина) или на 63 мл/кг (если обследуется женщина). Идеальная масса — должный вес данного человека — рассчитывается по формуле Лоренцо [2]:
где Р — рост человека, М — идеальная масса. Этот расчет позволяет избежать ошибки у тучных людей, при пересчете на их вес ОЦК получится завышенным, т.к. подкожно-жировая клетчатка содержит незначительное количество крови. Для определения объема должного ОЦК можно использовать другой, менее точный способ. Сначала определяется идеальная масса тела, а затем вычисляется ОЦК, исходя из того, что он равен 8–12 % от массы тела (у мужчин больше, чем у женщин). Чтобы вычислить процент потери ОЦК и тем самым определить тяжесть кровопотери, необходимо установить объем кровопотери. В ряде случаев (кровотечения в полости тела) это удается сделать сравнительно просто. Полости пунктируются или вскрываются, кровь эвакуируется электроотсосом и измеряется.
Факторами, которые способствуют развитию шока, являются: 1) множественные, сочетанные и комбинированные повреждения, кровопотеря, болевой фактор; 2) нервно-психическое напряжение, утомление, охлаждение; 3) запоздалая и неполноценная первая медицинская помощь.
Нами произведен анализ тактики ведения больных с момента их поступления до момента госпитализации в профильное отделение. Оценивались время поступления больных в приемное отделение, время осмотра их профильными специалистами, время, затраченное на проведение лечебно-диагностических мероприятий (лапаро- и торакоцентез, остановка кровотечения и т.д.), степень тяжести больных при поступлении, время госпитализации больных в профильные отделения, время начала проведения экстренных оперативных вмешательств, объем и качество оказанной неотложной помощи на этапе пребывания в приемном отделении. При анализе тактики ведения больных выявлены недостатки в организации помощи.
В связи с вышеизложенным необходимо выработать единый алгоритм оказания неотложной помощи больным в условиях приемного отделения, обязательный для выполнения всеми специалистами. Исходя из вышеизложенных патофизиологических и клинических особенностей, может создаться впечатление, что терапия травматического шока должна включать в себя огромное количество назначений. Однако, как показывает практика, именно это заблуждение и приводит к смерти пациента в машине скорой помощи или приемном отделении. Полипрагмазия, которая является бичом современной медицины неотложных состояний, уводит врача от примитивных, но действенных средств помощи. Современный врач может с легкостью рассуждать о патобиохимических механизмах критических состояний, не выполняя при этом элементарных приемов азбуки Сафара. Кстати, знание и владение этими приемами обязательно для всех врачей, составляет основу лицензионного экзамена «КРОК 3» и не является прерогативой врача-анестезиолога. Для немедленной интенсивной терапии травматического шока перечень этот крайне небольшой:
— обеспечение проходимости дыхательных путей (воздуховод, ларингеальная маска, при необходимости интубация трахеи);
— подача увлажненного кислорода;
— согревание больного;
— катетеризация периферических вен;
— переливание теплых растворов;
— избежание гиперволемии (использование гидроксиэтилкрахмалов (волювен, ХАЕС-стерил, гекодез), гипертонических растворов NaCl или гипертонических растворов гидроксиэтилкрахмалов (гиперХАЕС));
— иммобилизация шейного отдела позвоночника;
— транспортная иммобилизация пораженной конечности;
— обязательное обезболивание с использованием наркотических анальгетиков;
— первичная хирургическая обработка открытых ран;
— коррекция недостаточности сердечно-сосудистой системы (гидрокортизон, адреналин, норадреналин (норадреналин агетан), мезатон);
— при подозрении на пневмоторакс — пункция во II межреберье.
При поступлении с тяжелой травмой больной без промедления должен быть осмотрен врачом приемного отделения. Необходимо получить от врача скорой помощи возможно полную информацию о состоянии больного и характере травмы: обстоятельства получения травмы, уровень сознания, артериальное давление, частота пульса, объем оказанной помощи. При осмотре больного врач приемного отделения определяет степень тяжести, при диагностировании травматического шока определяется его степень, фиксируется уровень сознания, АД, ЧСС, аускультативная картина в легких, признаки внешнего кровотечения. При отсутствии венозного доступа медсестрой приемного отделения обеспечивается катетеризация периферической вены, начинается инфузия теплого физиологического раствора, обеспечивается согревание больного.
Незамедлительно вызываются профильные специалисты (хирург, травматолог, нейрохирург, реаниматолог, уролог и др.). При вызове уточняется ориентировочный характер повреждений, при подозрении на перелом ребер или внутрибрюшное кровотечение необходимо, чтобы хирург и травматолог приходили в отделение с наборами для торако- и лапароцентеза и в сопровождении операционной сестры. При наличии кровотечения производится его временная остановка. Реаниматолог обеспечивает мониторинг жизненно важных функций, при нарушении сознания оцениваются проходимость верхних дыхательных путей, уровень сознания, адекватность внешнего дыхания. При необходимости — интубация трахеи, искусственная вентиляция легких (ИВЛ), коррекция инфузионной терапии, катетеризация второй периферической вены. Параллельно проводится регистрация ЭКГ, дежурным лаборантом берется клинический анализ крови, определяется гематокрит, сахар крови.
При диагностировании травматического шока I степени при изолированном поражении производится внутримышечное обезболивание больного наркотическим анальгетиком, физическое согревание больного, венозный доступ посредством катетеризации периферической вены медсестрой приемного отделения, при неудаче на этом этапе — медсестрой или врачом травматологического, хирургического или анестезиологического отделения; внутривенно струйно вводится 500 мл теплого физиологического раствора, 500 мл р-ра гидроксиэтилкрахмала (волювен), 4 мл дицинона, 10 мл хлористого кальция, 250 мг гидрокортизона, больному производится временная остановка кровотечения, рентгенологическое исследование пораженных сегментов тела в условиях приемного отделения, при необходимости — лапаро- и торакоцентез; транспортная иммобилизация пораженной конечности; больной переводится в травматологическое или хирургическое отделение для дальнейшего лечения. Параллельно проводится регистрация ЭКГ, дежурным лаборантом берется клинический анализ крови, определяется гематокрит, сахар крови.
При сочетанном поражении больной переводится для дальнейшего наблюдения и лечения в реанимационное отделение.
При травматическом шоке II–III степени осуществляется внутримышечное обезболивание больного наркотическим анальгетиком, физическое согревание больного, венозный доступ посредством катетеризации периферической вены медсестрой приемного отделения, при неудаче на этом этапе — медсестрой или врачом анестезиологического отделения, часто необходима катетеризация центральной вены, обеспечивается внутривенное струйное введение теплого раствора гиперХАЕС 250 мл или волювена (ХАЕС-стерила, гекодеза) 500 мл, 4 мл дицинона, 10 мл хлористого кальция, 500 мг гидрокортизона; производится временная остановка кровотечения, транспортная иммобилизация пораженных конечностей. Параллельно проводится регистрация ЭКГ, дежурным лаборантом берется клинический анализ крови, определяется гематокрит, сахар крови. По показаниям дежурным реаниматологом производится обеспечение проходимости верхних дыхательных путей, оротрахеальная интубация, ИВЛ. Обязательным моментом следует считать пункцию плевральных полостей на этапе приемного отделения (при необходимости). При осуществлении КТ головы данное исследование производится при стабилизации состояния больного на уровне САД не менее 90 мм рт.ст., адекватного самостоятельного или протезированного дыхания. Больной переводится для дальнейших лечебно-диагностических мероприятий в реанимационное отделение. Выполняется рентгенологическое исследование пораженных конечностей, таза, грудной клетки, костей черепа, лапароцентез. По показаниям выполняется экстренное оперативное вмешательство в условиях операционной реанимационного отделения на фоне проведения полного комплекса интенсивной терапии.
При диагностировании терминального состояния в результате получения сочетанной травмы, декомпенсированного травматического шока, крайне тяжелого поражения головного мозга больного целесообразно транспортировать в отделение интенсивной терапии, необходимо соблюдать принцип «консультант к пациенту», производится внутривенное обезболивание больного наркотическим анальгетиком, физическое согревание больного, центральный венозный доступ и, по возможности, дополнительно посредством катетеризации одной или двух периферических вен обеспечивается внутривенное струйное введение теплого раствора гиперХАЕС 250 мл или волювена (ХАЕС-стерила, гекодеза) 500 мл, 4 мл дицинона, 10 мл хлористого кальция, 1000 мг гидрокортизона, временная остановка кровотечения, иммобилизация пораженных конечностей. По показаниям дежурным реаниматологом проводится обеспечение проходимости верхних дыхательных путей, оротрахеальная интубация, ИВЛ, реанимационные мероприятия. Выполняется рентгенологическое исследование пораженных конечностей, таза, грудной клетки, костей черепа, лапаро- и торакоцентез. По показаниям выполняется экстренное оперативное вмешательство в условиях операционной реанимационного отделения на фоне проведения полного комплекса интенсивной терапии.
Необходимо отметить, что с конца 2009 года была начата реформа оказания неотложной помощи в КМУ «КРБ». Выполнение, казалось бы, простых и во многом примитивных действий привело к тому, что за 4 месяца не было зафиксировано ни одного летального случая в приемном отделении у пациентов с политравмой. В 6 случаях благодаря своевременному переводу в отделение ИТ (без излишних дообследований и консультаций, после иммобилизации, согревания и обезболивания) и проведению хирургического вмешательства на фоне продолжающихся реанимационных мероприятий в условиях операционной отделения ИТ удалось избежать летального исхода у пациентов с политравмой (с поражением более 3 анатомических областей). Был зафиксирован только один случай досуточной летальности у пациента после ДТП (травма, несовместимая с жизнью) — смерть в операционной.
Для выполнения полного комплекса вышеперечисленных мероприятий необходимо проведение мероприятий организационного характера, усовершенствование материально-технической базы приемного, диагностического, реанимационного отделений, в частности:
а) обеспечение возможности проведения рентгенографии органов грудной клетки, таза, головы, конечностей в условиях приемного отделения;
б) организация в условиях приемного отделения операционной-противошоковой, с полным оснащением;
в) необходимо создание отдельного приемного отделения с организацией операционной-противошоковой на базе отделений травматологии/нейрохирургии для избежания излишней транспортировки пациентов по территории;
г) организация единой информационной базы с подстанциями скорой помощи для коррекции терапии на догоспитальном этапе и заблаговременного решения о конечной точке транспортировки пациента. В условиях КМУ «КРБ»: общее приемное отделение (превалирует общехирургическая патология и необходимо проведение КТ); приемное отделение травматологического корпуса (превалирует поражение конечностей, нейротравма) или отделение интенсивной терапии (комбинированная травма 2 и более областей поражения, терминальная фаза шока);
д) обеспечение постоянной возможности физического согревания больного, наличия теплых инфузионных растворов (физиологический раствор, волювен, ХАЕС-стерил, гекодез, гиперХАЕС) в условиях приемного отделения;
е) доукомплектование приемного отделения необходимым ассортиментом лекарственных веществ (гиперХАЕС, гипертонические солевые растворы (2%, 5%, 7,5% р-р NaCl), растворы гидроксиэтилкрахмала (волювен, ХАЕС-стерил, гекодез), гемостатики, адреналин, норадреналин (норадреналин агетан), мезатон, атропин, глюкокортикоиды, гидрокарбонат натрия, лидокаин, кордарон); расходными материалами (венозные катетеры G-16, -18, -20, шины Крамера, бинт, вата, спирт, пластырь, жгуты Эсмарха, катетеры Фолея № 16, 18, 20, наборы для лапаро- и торакоцентеза, катетеризации центральных вен); оборудованием (отсасыватель хирургический, дефибриллятор, пульсоксиметр, электрокардиограф, каталки для транспортировки больных);
ж) обеспечение безопасной транспортировки больных в состоянии травматического шока к отделениям для дальнейшего лечения (бесперебойное освещение);
з) дооснащение операционной реанимационного отделения (коагулятор, наборы хирургического инструментария) согласно предполагаемой операции (во избежание пролонгации начала операции в связи с подготовкой операционной и т.д.).
Кроме вышеперечисленных организационных мероприятий нами была проведена реорганизация проводимой инфузионной терапии. Основные изменения при шокогенных травматических повреждениях отмечаются в системе кровообращения. Они связаны не только с истинной кровопотерей (наружное или внутреннее кровотечение), но и с гиповолемией, обусловленной депонированием крови в емкостных сосудах системы гемоциркуляции. Кроме того, происходит миграция жидкой части крови в интерстициальное пространство из-за повышенной проницаемости в зоне микрогемоперфузии, которая приводит к скрытой кровопотере [1, 2]. Большая группа гуморальных факторов, следствием воздействия которых является скрытая кровопотеря, объединены под общим названием «вазотоксины». Среди последних значительную роль играют цитокины [3]. Общеизвестно, что фактор некроза опухолей и провоспалительные цитокины, в частности интерлейкин-1, синтезируются в результате реперфузии органов и тканей [4, 5]. Активация цитокинового каскада способствует микротромбообразованию, нарушает проницаемость сосудистой стенки, приводит к интерстициальному отеку, вазодилатации периферических сосудов и неконтролируемой артериальной гипотензии [5, 6]. Методика малообъемной реанимации (Small volume resuscitation), предназначенная для лечения гиповолемии и шока с гипотензией при острых кровопотерях, травмах, ранениях, хирургических вмешательствах, ожогах, инфекционных заболеваниях, является признанной во всем мире. Препараты малообъемной реанимации определены в качестве стратегических средств для помощи на поле боя в армиях США и НАТО [7, 8].
Нами проведено обследование и лечение 25 пострадавших с травматическим шоком II–III степени в возрасте от 30 до 62 лет. Мужчины составили 75 % от всех пострадавших. В исследование включались пострадавшие с САД менее 90 мм рт.ст. и более 50 мм рт.ст. (шок II–III степени). В зависимости от проводимой терапии пациенты были разделены на две группы. Основную группу составили 5 пострадавших, которым проводилась внутривенная, однократная, быстрая инфузия 250 мл препарата гиперХАЕС.
В контрольную группу входили 20 пострадавших, которым проводилась стандартная противошоковая терапия солевыми (физиологический раствор, трисоль) и коллоидными растворами (рефортан) в соотношении 2 : 1.
Различие в возрасте, степени тяжести состояния, объеме кровопотери в обеих группах было статистически недостоверным.
Определялись частота пульса, показатели систолического и диастолического АД, рассчитывалось среднединамическое артериальное давление (СрАД). Регистрировался общий объем использованных препаратов, контролировалось время от начала инфузионной терапии до стабилизации гемодинамики.
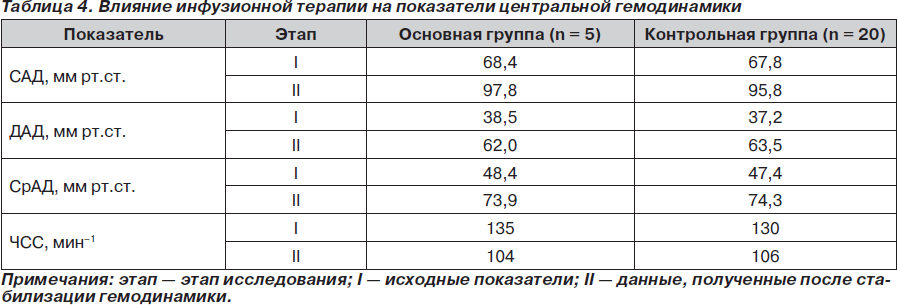
Влияние инфузионной терапии на гемодинамику в основной и контрольной группе представлено в табл. 4. Как видно из представленных данных, показатели центральной гемодинамики повышались после проведенной инфузионной терапии в основной и контрольной группе и не имели значимых отличий между собой.
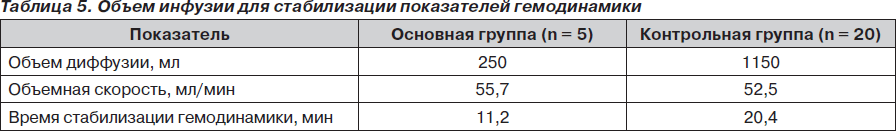
Однако объем инфузионной терапии (табл. 5) в контрольной группе был в 4,6 раза больше, чем в основной группе. Кроме того, при практически одинаковой объемной скорости инфузии в обеих группах время, затраченное на инфузионную программу, в контрольной группе было в 1,8 раза выше.
Таким образом, включение препарата малообъемной реанимации гиперХАЕС в программу инфузионной терапии способствует уменьшению времени нахождения больного в состоянии критической артериальной гипотензии.
Представленные данные являются первым опытом применения препарата гиперХАЭС в протоколе инфузионной терапии в КМУ «КРБ», необходимо продолжать исследования для выяснения воздействия данного препарата на показатели гемостаза, коронарного кровообращения, биохимические показатели. Однако пилотные данные показывают эффективность гиперХАЭС на этапе приемного отделения и вводной анестезии у пациентов с травматическим шоком III степени или терминальным. Также, возможно, применение данного препарата может оказаться незаменимым на догоспитальном этапе.
Выводы
Таким образом, вышеперечисленные мероприятия позволят обеспечить своевременное оказание адекватной комплексной медицинской помощи больным с сочетанной травмой на этапах диагностики в приемном отделении и госпитализации в профильное отделение, что сведет к минимуму гибель больных на этапах госпитализации и обследования, а также улучшит прогноз для жизни и восстановления трудоспособности, полноценной реабилитации функций внутренних органов, уменьшит время пребывания больных в лечебном учреждении, а в конечном итоге будет способствовать снижению инвалидизации и возвращению в строй полноценных кадров. Перспективным является использование растворов гиперХАЭС на догоспитальном этапе, этапе приемного отделения и этапе проведения реанимационных мероприятий при травматическом шоке IV степени.
Скорая медицинская помощь пострадавшим в дорожно-транспортных происшествиях. — СПб.: ИПК «КОСТА», 2007. — 400 с.
Багненко С.Ф., Лапшин В.Н., Шах Б.Н. Депрессия гемодинамики у пострадавших с сочетанной травмой в остром периоде травматической болезни — основа последующих гипоксических изменений и реперфузионных повреждений // Эфферентная терапия. — 2004. — Т. 1, № 5. — С. 23-34.
Решетникова С.Ю., Руднов В.А., Гусева Е.Ю. Цитокиновый ответ и маркеры системной альтерации как критерии раннего прогноза при тяжелой механической травме // Сборник материалов Всероссийского конгресса анестезиологов и реаниматологов и XI съезда Федерации анестезиологов и реаниматологов / Под ред. Ю.С. Полушина. — СПб., 2008. — С. 212-213.
Пивоварова Л.П. Нарушения функции иммунной системы при механической шокогенной травме и методы их коррекции: Дис… д-ра мед. наук. — Л., 1999. — 223 с.
Granger D.N., Kvietys P.R., Perry M.A. Leukocyte-endothelial Cell Adhesion Induced by Ischemia and Reperfusion // Canadian J. of Physiology and Pharmacology. — 1993. — Vol. 71, № 1. — P. 67-75.
Nickerson M. Factors of vasoconstriction and dilatation in shor // J. Michigan St. Med. Society. — 1955. — Vol. 54, № 1. — P. 45-53.
Howard R. Combat fluid resuscitation: introduction and overview of conferences // J. Trauma. — 2002. — Vol. 54. — P. 7-12.
Mawritz W., Schimetta W., Oberreither S. et al. Are hypertonic hyperoncotic solutions safe for prehospital small-volume resuscitation? // Eur. J. Emergency Med. — 2002. — № 9. — P. 315-319.
Багненко С.Ф., Стожаров В.В., Мирошниченко А.Г. и др. Дорожно-транспортный травматизм: Алгоритмы и стандарты оказания скорой медицинской помощи пострадавшим в ДТП (догоспитальный этап). — СПб.: ИПК «КОСТА», 2007. — 380 с.
Буланов А.Ю., Городецкий В.М., Шулутко Е.М. и др. Влияние различных типов коллоидных объемозамещающих растворов на измененную систему гемостаза // Анестезиол. и реаниматол. — 2004. — № 2. — С. 25-29.