Журнал «Здоровье ребенка» 1 (28) 2011
Вернуться к номеру
Дисбактериоз кишечника как фактор риска развития хронических заболеваний кишечника у детей
Авторы: Белоусова О.Ю. Харьковская медицинская академия последипломного образования
Рубрики: Педиатрия/Неонатология
Версия для печати
Изучаются вопросы состояния кишечного биоценоза при воспалительных (хронический неспецифический неязвенный колит) и функциональных (синдром раздраженного кишечника) заболеваниях кишечника у детей. Высказывается мнение, что нарушения кишечной микрофлоры являются одним из важнейших факторов риска возникновения или обострения хронических заболеваний кишечника у детей.
В последние годы в литературе, посвященной заболеваниям пищеварительной системы у детей, широко обсуждается проблема дисбиоза кишечника и его роли в возникновении и/или прогрессировании болезни. Особенно активно эта проблема обсуждается в литературе, посвященной заболеваниям толстой кишки, являющейся резервуаром микробной флоры, анализ которой и позволяет в большинстве случаев судить о наличии дисбиоза и степени его выраженности.
О возможной роли микробного фактора в развитии хронических заболеваний кишечника у детей свидетельствуют, с одной стороны, частое наличие у больных в анамнезе кишечных инфекций, причем особое значение придается агрессивности возбудителя и проведению своевременной адекватной терапии; с другой стороны — изменения состава нормальной кишечной микрофлоры (дисбиоз), который, по данным многих авторов, выявляют при хронических заболеваниях кишечника. Так, значение нарушений кишечного биоценоза в развитии воспалительных заболеваний кишечника подтверждается многочисленными работами [4, 9–11]; не меньшее число исследований посвящено проблеме дисбиоза при функциональных заболеваниях кишечника [2, 5–7, 12]. При этом подчеркивается, что хроническому неспецифическому неязвенному колиту (ХННК) и синдрому раздраженного кишечника (СРК) свойственны однотипные клинические проявления, обусловленные последующими нарушениями моторики кишки (запор, понос, метеоризм).
Нарушение качественного и количественного соотношения микрофлоры кишечника возникает от разнообразных причин: характера питания ребенка, возраста, времени года, проведения антибактериальной терапии, наличия хронических заболеваний ЖКТ, состояния окружающей среды и т.д. Изменения микробиоценоза кишечника развиваются задолго до клинических проявлений и служат предвестниками более глубоких отклонений на уровне целостного организма ребенка. Со временем дисбиоз кишечника проявляет себя клиническими симптомами, а затем общими нарушениями, которые отягощают течение основного заболевания и затрудняют его лечение [3, 4].
Изменение количественного и качественного состава микробной флоры приводит к нарушению различных видов метаболизма, возникновению дефицита микронутриентов — витаминов, микроэлементов, минералов, снижению иммунологического статуса. Анаэробы, продуцирующие в толстой кишке короткоцепочные жирные кислоты, непосредственно обеспечивают нормальное функционирование эпителия кишечника. Функциональные нарушения деятельности толстой кишки обусловлены изменениями именно этой группы бактерий [1, 4]. Нарушения количества и соотношения отдельных короткоцепочных жирных кислот из-за нарушения баланса между анаэробами и аэробами приводят к стрессовому воздействию на кишечный эпителий с переключением метаболизма колоноцитов с цикла Кребса на анаэробный вариант гликолиза, что приводит к изменению порога чувствительности рецепторов и нарушениям моторики. Этот механизм свидетельствует о возможном влиянии дисбиоза как пускового механизма хронических заболеваний кишечника у детей.
В то же время дисбиоз при заболеваниях кишечника может развиться и вторично в связи с нарушениями механического, химического и иммунологического факторов защиты слизистой оболочки кишечника [4]. Нарушением механической защиты является дискинезия кишечника, которая может быть следствием изменения центральной регуляции кишечной перистальтики в связи со стрессовыми факторами, нерациональным питанием, повторными заболеваниями, злоупотреблением жирной пищей. Дискинезия кишечника приводит к нарушениям микробного гомеостаза и развитию дисбактериоза, нарушениям микроциркуляции и трофики тканей кишечной стенки, снижению антиокислительной активности тканей, нарушению мукопротеинового слоя, т.е. к изменениям механической и химической защиты. Это активирует свободнорадикальное окисление, в результате чего нарушается функция биомолекул: возникают разрывы нуклеиновых кислот, полимеризация углеводов, деградация молекул соединительной ткани. Нарушается транспорт ионов, снижается активность дыхательных ферментов и коферментов, в частности коэнзима А, содержащих сульфгидрильные группы, активируется перекисное окисление липидов. Таким образом, дисбиоз может быть и следствием хронических заболеваний кишечника: подобный механизм может считаться ведущим при развитии заболевания у эмоционально лабильных детей, при нарушениях вегетативной иннервации кишечника, при дисфункции желез внутренней секреции, аллергической настроенности организма.
Наблюдения показывают, что в условиях выраженного нарушения состава кишечной микрофлоры происходит истощение механизмов компенсаторной защиты слизистой оболочки: нарушение слизеобразования, изменение градиента пролиферации, дифференциации клеток, массивная антигенная стимуляция при резко выраженной проницаемости эпителиального пласта приводят к существенным изменениям местного иммунитета, развитию транзиторного иммунодефицита, что, в свою очередь, способствует становлению и поддержанию воспалительного процесса — колита — в сигмовидной и прямой кишках [9]. Фактором риска развития бактериального проктосигмоидита является обильный рост условно-патогенных бактерий на фоне дефицита физиологической флоры со снижением местной защиты слизистой оболочки кишечника — угнетение системы местного иммунитета с активацией процессов перекисного окисления липидов.
Таким образом, теоретические предпосылки свидетельствуют о влиянии нарушений кишечного биоценоза на состояние эпителия кишечной стенки, а следовательно, его возможной роли в этиологии и патогенезе хронических воспалительных (хронический неспецифический неязвенный колит) и функциональных (синдром раздраженного кишечника) заболеваний кишечника у детей.
Нами изучено состояние кишечного биоценоза у 134 больных с ХННК. Диагноз заболевания устанавливался на основании ректороманоскопического исследования, выявившего у всех детей явления катарального или катарально-фолликулярного проктосигмоидита. У значительной части больных (86 %) диагноз ХННК подтверждался также результатами морфологического исследования. Бактериологические исследования проводились в баклаборатории института им. Мечникова (проф. Е.М. Савинова). Параллельно исследовался биоценоз 47 детей с диагнозом СРК [3].
Исследования микробного пейзажа кишечника показали, что у всех 134 детей с ХННК имеют место те или иные нарушения кишечного биоценоза (для сравнения, при СРК — у 75 %), которые носили преимущественно однонаправленный характер. Характер изменений кишечной микрофлоры при ХННК у детей представлен в табл. 1.
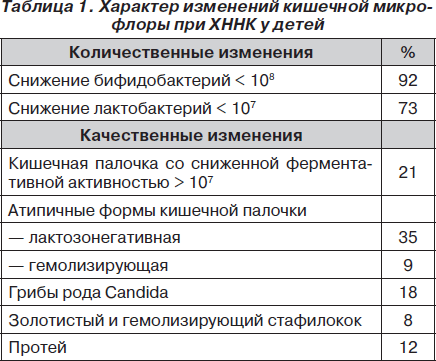
При анализе характера выявленных изменений прежде всего обращают на себя внимание количественные нарушения, характеризующиеся умеренным снижением количества бифидобактерий и лактобактерий. Несмотря на относительно незначительное уменьшение облигатной микрофлоры, значение этого показателя нельзя недооценивать, т.к. снижение ферментативной активности бифидобактерий и лактобактерий, а также сдвиг рН кишечника в щелочную сторону обусловливают торможение процессов утилизации организмом ребенка биологически активных веществ, усиление бродильных и гнилостных процессов. Нарушение колонизационной резистентности вызывает адгезию и колонизацию на слизистой оболочке кишечника патогенных и условно-патогенных бактерий и обусловливает поступление токсинов в кровь.
Кроме количественных, выявляются нарушения качественного состава микрофлоры. Прежде всего это касается изменения качественных свойств кишечной палочки: появление форм со сниженной ферментативной активностью и атипичных форм — лактозонегативной, гемолизирующей. Если принять во внимание, что штаммы E.сoli содержат достаточно широкий набор факторов патогенности — эндо-, экзо- и цитотоксинов, факторы адгезии и тому подобные, то недооценивать ее роль в развитии патологического процесса невозможно.
Качественные изменения микрофлоры при ХННК у детей заключались также в появлении условно-патогенной микрофлоры (золотистый и гемолизирующий стафилококк, грибы рода Candida, протей), что свидетельствует об ослаблении защитных возможностей индигенной анаэробной микрофлоры.
Таким образом, выявленные изменения биоценоза кишечника свидетельствуют о значительных дисбиотических сдвигах у всех больных ХННК, причем нарушения носят не столько количественный, сколько качественный характер. Количественные изменения состоят в незначительном снижении индигенной микрофлоры, качественные — в снижении ее защитных свойств, росте кишечной палочки с измененными свойствами и условно-патогенной микрофлоры. Полученные данные дают основание полагать, что дисбиотические нарушения являются одним из важнейших звеньев формирования патологического процесса при ХННК у детей, наряду с нарушениями нервной регуляции пищеварения и иммунологическими расстройствами, причем в ряде случаев именно дисбиоз кишечника может послужить пусковым механизмом патологического процесса, который можно представить следующим образом: дисбиоз ® нарушение слизеобразования ® изменение градиента пролиферации и дифференциации клеток ® изменение местного иммунитета ® развитие транзиторного иммунодефицита ® развитие воспалительного процесса, факторами риска которого являются: длительное течение заболевания; обильный рост условно-патогенных бактерий на фоне дефицита физиологической флоры; снижение местной защиты слизистой оболочки кишечника; угнетение системы местного иммунитета с активацией процесса перекисного окисления липидов.
Вышеизложенное не только пополняет представления о механизмах формирования ХННК у детей, но и определяет необходимость комплексной терапии дисбиоза с учетом его особенностей в каждом конкретном случае заболевания.
Сходные качественные и количественные изменения кишечной микрофлоры выявлены нами также у 47 больных с синдромом раздраженного кишечника (СРК), однако частота этих нарушений уступала ХННК: при СРК нарушения кишечного биоценоза выявлены у 75 % детей.
Таким образом, проведенные нами исследования подтверждают концепцию, согласно которой в основе развития дисбиоза при хронических заболеваниях кишечника у детей в большинстве случаев лежат нарушения центральной регуляции моторной и секреторной функций кишечника, следствием чего является развитие дискинезии толстой кишки, протекающей по гипокинетическому или гиперкинетическому варианту. Из-за ускоренного пассажа пищевого содержимого по кишечнику часть углеводов, особенно легкоусвояемых, полностью не расщепляется, не всасывается и подвергается в толстой кишке микробному сбраживанию, что создает благоприятные условия для появления и последующего размножения нехарактерной для ребенка микрофлоры, т.е. развития дисбиоза. В свою очередь, дисбиоз, усиливая процессы брожения, приводит к повышенной концентрации в просвете кишки осмотически активных веществ, что способствует раздражению кишки, избыточному газообразованию, увеличению объема кишечного содержимого и в итоге — растяжению и возбуждению перистальтики толстой кишки. В результате развивается диарея, чередующаяся иногда с запорами.
Следовательно, дисбиоз кишечника следует рассматривать не только как клинико-микробиологический синдром, но и как один из важнейших факторов риска развития функциональных и воспалительных заболеваний кишечника у детей, играющих не только этиологическую, но и патогенетическую роль в возникновении и обострении патологического процесса. Необходимость коррекции дисбиотических изменений толстой кишки на всех этапах наблюдения за больным очевидна.
1. Ардатская М.Д., Дубинин А.В., Минушкин О.Н. Дисбактериоз кишечника: современные аспекты изучения проблемы, принципы диагностики и лечения // Терапевт. архив. — 2001. — № 2. — С. 67-72.
2. Бєлоусова О.Ю. Синдром подразненого кишечника у дітей: теорія та практика діагнозу // Перинатологія та педіатрія. — 2002. — № 2. — С. 43-44.
3. Белоусова О.Ю. Кишечный дисбиоз при синдроме раздраженного кишечника у детей: причина или следствие // Здоровье женщины. — 2003. — № 4. — С. 142-143.
4. Григорьев П.Я., Яковенко Э.П. Диагностика и лечение болезней органов пищеварения. — М.: Медицина, 1997. — 516 с.
5. Гриднева С.В., Звягинцева Т.Д., Шаргород И.И. Новые подходы к лечению синдрома раздраженного кишечника с запорами // Сучасні досягнення в гастроентерології: Матеріали Укр. науково-практ. конф. — Х., 2006. — 97-99.
6. Запруднов А.М., Харитонова Л.А., Богомаз Л.В. Синдром раздраженной кишки у детей с холелитиазом: Материалы 7-го Междунар. славяно-балт. форума «Санкт-Петербург-Гастро-2005» // Гастроэнтерология Санкт-Петербурга. — 2005. — № 1/2. — С. 51.
7. Малышева Е.Б., Калинникова Л.А., Кизова Е.А., Рябчевский В.А. Синдром раздраженного кишечника: новые возможности патогенетической терапии // Рос. журнал гастроэнтерологии, гепатологии, колопроктологии. — 2003. — Т. 13, № 5, прил. № 21. — С. 63.
8. Копанев Ю.А., Соколов А.Л. Дисбактериоз кишечника: микробиологические, иммунологические и клинические аспекты микробиологических нарушений у детей. — М., 2002. — 147 с.
9. Костенко М.Б. Локальный бактериальный колит как форма синдрома раздраженного кишечника // Рос. журн. гастроэнтерологии, гепатологии, колопроктологии. — 2001. — Т. 11, № 5, прил. № 15. — С. 53.
10. Коррекция дисбиотических нарушений микрофлоры кишечника у детей / С.В. Орлова, Д.И. Тарасова, Л.В. Озерова, Е.М. Исакова // Акт. проблемы абдоминальной патологии у детей: Материалы ХIV конгр. дет. гастроэнтерологов России. — М., 2007. — С. 283-285.
11. Ott S.J., Vusfeld. M., Wenderoth D.F. et al. Reduction in diversity of the colonic mucosa associated bacterial microflora in patients with active inflammatory bowel diseas // Gut. — 2004. — № 53. — P. 685-693.
12. Si J.M., Yu Y.C., Fan V.J., Chen S.J. Intestinal microecology and quality of life in irritable bowel syndrome patients // World J. Gastroenterology. — 2004. — № 10. — P. 1802-1805.
