Журнал «» 3(17) 2011
Вернуться к номеру
Нейрогуморальные факторы в формировании нарушений углеводного обмена у подростков с артериальной гипертензией
Авторы: Коренев Н.М., Богмат Л.Ф., Носова Е.М., Яковлева И.М., Сулима Т.Н., ГУ «Институт охраны здоровья детей и подростков НАМН Украины», г. Харьков
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
Целью настоящего исследования явилось установление нейрогуморальных механизмов формирования нарушений углеводного обмена у подростков с артериальной гипертензией. У 93 юношей с первичной артериальной гипертензией в возрасте 13–18 лет и 56 их сверстников с артериальной гипертензией, которая сопровождалась избыточной массой тела, изучено состояние углеводного обмена по уровню гликемии натощак в венозной крови, результатам орального глюкозотолерантного теста, уровню базального иммунореактивного инсулина, индексу тощаковой инсулинорезистентности. Активность симпатоадреналовой системы (САС) изучали по содержанию в суточной моче (отдельно дневной и ночной фракции) норадреналина и адреналина, определяли уровень суточной экскреции мелатонина, а также исследовали состояние ренин-ангиотензин-альдостероновой системы (РААС) по уровню активности ренина плазмы, содержанию ангиотензина II и альдостерона в периферической венозной крови. С помощью множественного регрессионного анализа выявлены особенности влияния биогенных аминов и системы РААС на отдельные показатели углеводного обмена. Полученные данные свидетельствуют о том, что у подростков с артериальной гипертензией активация САС и РААС при отсутствии адекватного повышения мелатонина может быть одним из элементов патогенеза нарушений углеводного обмена, который проявляется развитием инсулинорезистентности, гиперинсулинемии и гипергликемии.
Подростки, метаболический синдром, артериальная гипертензия, углеводы.
Проведенные ранее исследования показали, что у подростков под влиянием нейрогуморальных изменений пубертатного периода и неблагоприятных экзогенных и эндогенных факторов транзиторные подъемы артериального давления (АД), нарушения в липидном спектре крови и в углеводном обмене могут трансформироваться в хронические стабильные формы артериальной гипертензии (АГ) и нарушения метаболизма углеводов и липидов [1–4].
Доказано, что АГ и метаболические нарушения в виде дислипопротеидемий, нарушений инсулинорезистентности (ИР) являются взаимопотенцирующими составляющими, которые дополняют друг друга и утяжеляют течение каждого из них [5–8]. Комплекс взаимозависимых нарушений углеводного и жирового обмена, механизмов регуляции АД и функции эндотелия, которые формируются на фоне дисфункции нейроэндокринных систем в условиях сниженной чувствительности тканей к инсулину — ИР и ожирения, объединен в так называемый метаболический синдром (МС).
Изначально МС, включающий в себя абдоминальное ожирение, дислипопротеидемию, нарушение толерантности к глюкозе и АГ, описывался как исключительно «взрослый» феномен. Однако сегодня проявления МС широко распространены в детской и подростковой популяции и имеют отчетливую тенденцию к увеличению [9, 10].
Патогенетической основой метаболического синдрома является ИР, которая чаще всего генетически детерминирована (мутации генов рецепторного и пострецепторного инсулинового аппарата), но проявлению ее способствуют экзогенные факторы: гиподинамия, избыточное потребление пищи, богатой жирами и углеводами, стресс, курение [12].
Важную роль в формировании ИР играют абдоминальное ожирение и сопутствующие ему сдвиги в нейрогормональной регуляции. Висцеральный жир имеет ряд патофизиологических особенностей, в частности высокую чувствительность к липолитическому воздействию катехоламинов и низкую — к антилиполитическому действию инсулина, что стимулирует липолиз. В результате свободные жирные кислоты тормозят действие инсулина, еще более усугубляя ИР и гипергликемию. Помимо этого, висцеральный жир также является и эндокринным органом, синтезирующим множество биологически активных веществ (лептин, адипонектин, провоспалительные цитокины и др.), действие которых в рамках метаболического синдрома также приводит как к ИР, так и к другим метаболическим нарушениям [13–15].
Таким образом, в диагностике МС имеет значение не столько сам факт избыточной массы тела, сколько прежде всего абдоминальный тип ожирения. Было показано, что среди детей с одинаковым индексом массы тела чувствительность к инсулину ниже в группе детей с увеличением висцерального жира [16]. Подобные нарушения могут способствовать прогрессированию АГ и формированию уже в молодом возрасте тяжелых сердечно-сосудистых осложнений.
В связи с этим целью настоящего исследования явилось установление механизмов формирования нарушений углеводного обмена у подростков с артериальной гипертензией.
Объем и методы
Под наблюдением находилось 93 юноши с первичной артериальной гипертензией (ПАГ) в возрасте 13–18 лет и 56 их сверстников с АГ, которая сопровождалась избыточной массой тела (индекс массы тела которых превышал 85 ‰ процентильного распределения). Контрольную группу составили 19 практически здоровых подростков с нормальными росто-весовыми показателями и АД.
Показатели индекса массы тела (ИМТ) между 85 ‰ и 95 ‰ расценивались как избыточная масса тела, а выше 95 ‰ — как ожирение. Критерием абдоминального ожирения считали объем талии, равный 94 см и более для юношей старше 16 лет и более 90 ‰ процентильного распределения для детей до 15 лет (IDF, 2007). Для выявления абдоминального типа ожирения у подростков старше 16 лет используется, так же как и у взрослых, индекс отношения объема талии к объему бедер (ОТ/ОБ).
Для оценки состояния углеводного обмена определяли уровень гликемии натощак в венозной крови, оценивали результаты орального глюкозотолерантного теста, уровень базального иммунореактивного инсулина (ИРИ), коэффициент (индекс) тощаковой инсулинорезистентности (НОМА-IR).
Уровень гликемии в венозной крови определяли методом GOD-PAP с помощью набора Glucose liquicolor (производство Human, Германия) на фотометре «Микролаб-200».
Оральный глюкозотолерантный тест проводили по стандартной методике с определением уровня глюкозы натощак, через 1 и 2 часа после нагрузки глюкозой (75 мг/кг массы тела, но не более 75 г). Повышение уровня глюкозы натощак определялось при уровне глюкозы, равном 5,6 ммоль/л (126 мг/л) и более. Нарушение толерантности к глюкозе диагностировалось, если уровень глюкозы через 2 часа составлял 7,8 ммоль/л (140 мг/дл) и выше, но меньше 11,1 ммоль/л (200 мг/дл), а диагноз сахарного диабета — при уровне глюкозы натощак 6,1 ммоль/л или выше, а через 2 часа после нагрузки глюкозой — 11,1 ммоль/л и выше.
Для количественного определения уровня базального ИРИ в сыворотке крови использовали метод твердофазного энзимосвязанного иммуносорбентного анализа (ELISA) с использованием набора DRG инсулин ELISA (производство Германии). Гиперинсулинемия диагностировалась при повышении уровня инсулина выше референтного значения 25 мкЕД/мл. Пограничными значениями считали уровень инсулина 20–24,9 мкЕД/мл.
Инсулинорезистентность оценивалась по непрямым показателям: уровню базальной инсулинемии и гомеостатической модели ИР с определением параметров НОМА-IR, которые рассчитываются по формуле (D.R. Matthews et al., 1985 г.):
НОМА-IR = Уровень гликемии натощак (ммоль/л) ґґ уровень инсулина натощак (мкЕД/мл) / 22,5.
Критерием высокой ИР является уровень НОМА-IR более 3,6 [17, 18]. Средней (пограничной) степенью ИР считается уровень НОМА-IR от 2,77 до 3,59. Сохраненная чувствительность к инсулину диагностируется при уровне НОМА-IR менее 2,77.
Оценку состояния симпатоадреналовой системы (САС) проводили по определению содержания в суточной моче (отдельно дневной и ночной фракции) свободных катехоламинов — норадреналина (НА) и адреналина (А) — флюорометрическим методом по Е.Ш. Матлиной и соавт. (1976). Уровень экскреции мелатонина в суточной моче определяли по методу Друекса в модификации Г.В. Зубкова (1974).
Ренин-ангиотензин-альдостероновую систему (РААС) оценивали по уровню активности ренина плазмы (АРП), содержанию ангиотензина II (АII) и альдостерона (Альд) в периферической венозной крови с помощью радиоиммунологического анализа на гамма-счетчике «Наркотест». Использовали наборы «Ангиотензин-1-ренин», «Ангиотензин II» и «Альдостерон» фирмы Immunotech (Чехия).
Все исследования проводились через 2–3 дня после поступления пациента в стационар, в условиях свободного режима, до назначения лечения.
Статистический анализ проводился с помощью пакета прикладных программ Statgraphics Plus for Windows 3.0 (Manugistic Inc., USA). Анализ ассоциации отдельных показателей углеводного обмена с набором гормонов САС, РААС и мелатонином проводился методом множественного регрессионного анализа. Результаты приведены в виде таблиц набора зависимых (Yj) и независимых (Хі) переменных (детерминант), а также коэффициента детерминации (R2).
Результаты и их обсуждение
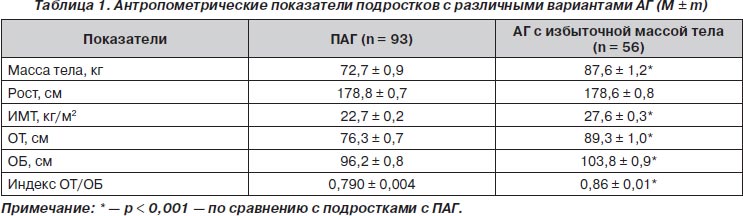
Средние значения антропометрических показателей исследуемых подростков представлены в табл. 1 и свидетельствуют о достоверном превышении массы тела, ИМТ, ОТ, ОБ и индекса ОТ/ОБ у пациентов с АГ и избыточной массой тела, по сравнению с подростками с первичной артериальной гипертензией (табл. 1).
Следует отметить, что ИМТ у 15 % юношей с ПАГ находился также в пределах от 24,8 до 28,1 кг/м2, но был обусловлен хорошо развитой скелетной мускулатурой. Ожирение 1-й степени (ИМТ превышал 95 ‰ и находился в пределах от 30,0 до 33,3 кг/м2) регистрировалось лишь у юношей второй группы и составило 17,9 %.
Установлены также достоверные различия средних показателей индекса ОТ/ОБ у подростков исследуемых групп (0,790 ± 0,004 с ПАГ против 0,86 ± 0,01 у подростков с АГ и избыточной массой тела; р < 0,001) (табл. 1). Повышение массы тела с распределением жира по висцеральному типу не было выявлено ни у одного подростка с ПАГ, в то время как среди юношей второй группы этот тип ожирения выявлен у 19 (33,9 %) подростков, а показатель ОТ у них колебался от 92 до 105 см.
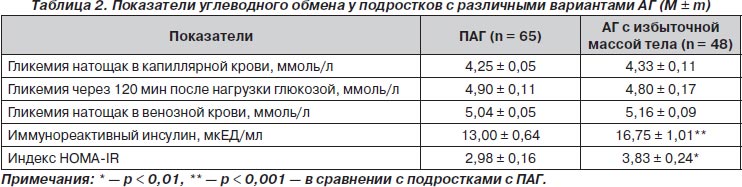
При изучении основных показателей, характеризующих углеводный обмен у подростков с различными вариантами АГ, не установлено достоверных различий по уровню гликемии натощак в капиллярной крови, гликемии через 120 мин после нагрузки раствором глюкозы и гликемии натощак в венозной крови, но при этом выявлено достоверное повышение средних значений уровня иммунореактивного инсулина у подростков с АГ и избыточной массой тела по сравнению с подростками с ПАГ (16,75 ± 1,01 против 13,0 ± 0,64 мкЕД/мл; р< 0,001) (табл. 2).
Исследование особенностей углеводного обмена у юношей с АГ и различной массой тела выявило вариабельность основных его показателей в исследуемых группах. Так, в группе подростков с ПАГ показатели уровня глюкозы натощак колебались в пределах от 2,9 до 5,5 ммоль/л, ИРИ — от 5,2 до 27,72 мкЕД/мл, а НОМА-IR — от 1,18 до 6,4 усл.ед. У подростков с АГ и избыточной массой тела эти показатели находились в следующих пределах: уровень глюкозы натощак варьировал от 2,9 до 7,5 ммоль/л, ИРИ — от 6,8 до 41,7 мкДЕ/мл, а НОМА-IR — от 1,74 до 8,56 усл.ед.
Частота гиперинсулинемии (ИРИ выше 25 мкЕД/мл) была достоверно выше у подростков с АГ и избыточной массой тела (12,50 ± 4,77 против 3,08 ± 2,14 %; р < 0,05), но пограничные значения ИРИ регистрировались примерно с одинаковой частотой в обеих группах (у 10,77 ± 3,84 % — с ПАГ и у 12,50 ± 4,77 % — с АГ и избыточной массой тела).
Инсулинорезистентность различной степени выраженности выявлялась у 74,50 ± 6,36 % больных с АГ и избыточной массой тела и лишь у 40,00 ± 6,32 % подростков с ПАГ (р < 0,001).
Установлены также различия между группами и в степени выраженности ИР. Так, высокая степень ИР (HOMA-IR больше 3,59) выявлялась у 40,50 ± 6,36 % подростков с избыточной массой тела и лишь у 21,70 ± 5,32 % пациентов с ПАГ (р < 0,02), средняя степень (HOMA-IR — 2,77–3,59) достоверно преобладала также среди подростков с избыточной массой тела (34,04 ± 6,91 против 18,33 ± 4,99 %; р < 0,05).
Эти данные свидетельствуют о том, что в обеих исследуемых группах подростков с АГ встречались лица с пониженной чувствительностью к инсулин-опосредованному усвоению глюкозы.
Известно, что мощным фактором, который способствует формированию изменений со стороны сердечно-сосудистой системы, центрального и периферического ее звеньев, а также региональных отделов (церебрального, почечного, коронарного), является активация нейрогуморальных систем, обладающих прессорными свойствами. К ним относят прежде всего симпатико-адреналовую и ренин-ангиотензин II-альдостероновую.
Доказано, что норадреналин и адреналин являются гормонами, одновременно вовлеченными в регуляцию метаболических и соматических функций организма, а мелатонин осуществляет координацию циркадной активности многих гормонов, в том числе и ренин-ангиотензин-альдостероновой системы.
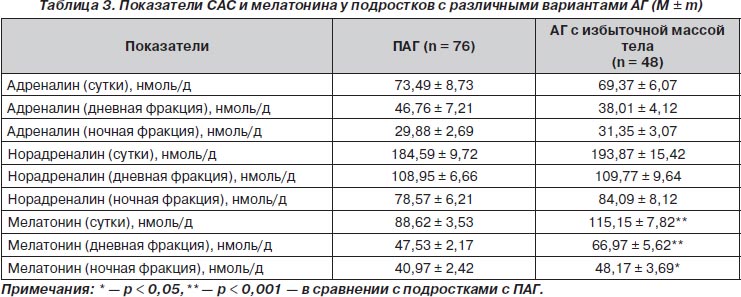
При изучении их активности у подростков исследуемых групп было установлено, что наиболее значимые различия имелись лишь в отношении уровня экскреции мелатонина с мочой (табл. 3). Так, у подростков с АГ и избыточной массой тела достоверно выше были показатели экскреции мелатонина, особенно дневной его фракции, по сравнению с подростками с ПАГ.
В связи с этим с помощью множественного регрессионного анализа изучены особенности влияния биогенных аминов (А, НА, мелатонина) на отдельные показатели углеводного обмена.
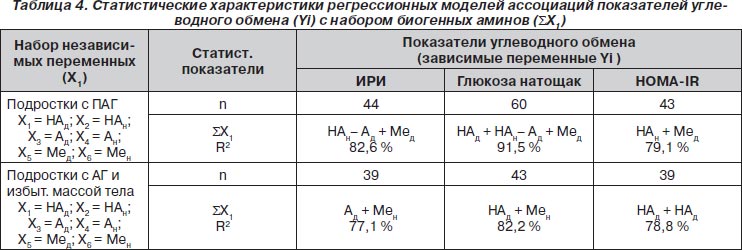
При предварительном анализе ни один из отдельно взятых биогенных аминов не оказывал статистически значимого влияния на показатели углеводного обмена. Однако совместное взаимодействие их может быть рассмотрено в качестве комплекса детерминант, содержащих более полную информацию о соотношении катаболических и анаболических аспектов метаболизма углеводов. Это нашло свое подтверждение в полученных в результате системного анализа достаточно высоких значениях коэффициента детерминации R2, который варьировал для отдельных показателей углеводного обмена от 77 до 92 % (табл. 4).
Как следует из табл. 4, у подростков с ПАГ наблюдался избирательный вклад катехоламинов в уровень ИРИ, глюкозы натощак и, соответственно, показателей НОМА-IR.
Так, повышенный уровень ИРИ ассоциировал с высокими показателями ночной экскреции НА и низким уровнем дневной экскреции А. Базальный уровень глюкозы был выше у подростков с более высокими значениями экскреции НА и низким уровнем экскреции А в дневное время.
Наряду с вышеуказанными закономерностями свой статистически значимый вклад в каждый из показателей углеводного обмена давал повышенный уровень мелатонина в дневное время суток. При этом у подростков с ПАГ уровень экскреции мелатонина в дневной и ночной период времени практически не отличался (Мен/Мед = 0,97 ± 0,06), что является также отклонением от нормы и может оказывать негативное влияние как на взаимодействие регуляторных систем, так и на метаболические их эффекты. Не исключено, что описанные закономерности сочетанного влияния катехоламинов и мелатонина на метаболизм глюкозы могут приводить к обратимым изменениям чувствительности к инсулину в рамках индивидуального циркадного ритма.
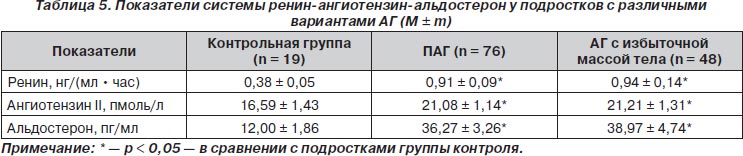
У подростков с АГ и избыточной массой тела на показатели ИРИ, глюкозы натощак и, соответственно, индекс НОМА-IR существенное влияние оказывали активность катехоламинов в дневное время и уровень мелатонина в ночной период суток (табл. 5). Учитывая то, что в этой группе подростков средний уровень ночной фракции мелатонина был достоверно ниже, чем дневной (48,17 ± 3,69 против 66,97 ± 5,62 нмоль/д; р < 0,001), это можно рассматривать у них как недостаточную функцию мелатонина в ночное время, что может способствовать возникновению резистентности к инсулину гепатоцитов и усилению эндогенной продукции глюкозы на исходе ночи.
Рядом исследователей сообщалось также о способности мелатонина активировать секреторную функцию b-клеток поджелудочной железы [15, 19]. Поэтому, с одной стороны, пониженный уровень ночного мелатонина вносит вклад в резистентность рецепторов к инсулину, а с другой — способствует снижению уровня секреции инсулина, что существенно влияет на поддержание гомеостаза глюкозы.
В связи с этим при оценке патогенетической роли мелатонина в развитии метаболических нарушений необходимо учитывать как его эффекты на мишени (секреторное или рецепторное звено регуляции углеводного обмена), так и базальный уровень для данного времени суток.
При изучении показателей ренин-ангиотензин-альдостероновой системы у подростков с АГ было установлено достоверное повышение всех ее составляющих по сравнению с контрольной группой независимо от показателей ИМТ (табл. 5).
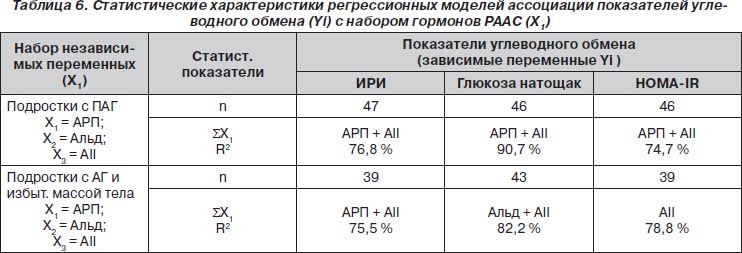
По результатам множественного регрессионного анализа изучены особенности влияния гормонов РААС на отдельные показатели углеводного обмена у подростков с АГ в зависимости от ИМТ (табл. 6).
Как следует из табл. 6, у подростков с ПАГ выявлена статистически значимая (р < 0,001) положительная ассоциация показателей углеводного обмена с АРП и уровнем АII, которая отличалась достаточно высокой степенью детерминации зависимых переменных — от самой низкой (R2 = 74,7 %) для НОМА-IR до самой высокой (R2 = 90,7 %) для глюкозы.
Необходимо отметить, что в пределах указанных выше значений показателей углеводного обмена система ренин-ангиотензин II вносит статистически значимый вклад в уровень инсулина, глюкозы и индекс НОМА-IR .
Полученные данные могут служить доказательством возможности снижения чувствительности к инсулину у лиц с ПАГ при повышении АРП и уровня ангиотензина II. Эти выводы совпадают с результатами как экспериментальных работ по блокированию активности РААС для предупреждения развития и прогрессирования ИР, так и клинических исследований, подтверждающих эффективность применения ингибиторов РААС для предупреждения формирования и прогрессирования ИР у больных с АГ [13–15].
У подростков с АГ и избыточной массой тела выявлен несколько иной, более селективный характер взаимосвязи гормонов РААС с показателями углеводного обмена (табл. 6). Так, уровень ИРИ статистически значимо (р < 0,001) ассоциирован с АРП и содержанием ангиотензина II (R2 = 75,5 %), тогда как показатели глюкозы натощак — с уровнем альдостерона и ангиотензина II (R2 = 86,8 %), а индекс НОМА-IR — только с уровнем ангиотензина II (R2 = 73,4 %).
Следовательно, у подростков с АГ и избыточной массой тела наблюдается более сложный характер влияния компонентов РААС на углеводный обмен. Так, на уровень ИРИ оказывает влияние преимущественно сосудистая составляющая гуморальной регуляции (ренин-ангиотензин), в то время как на базальный уровень глюкозы — еще и минеральный компонент функции коры надпочечников (альдостерон).
У подростков этой группы чувствительность рецепторов к инсулину находится под многокомпонентным влиянием, которое реализуется прежде всего через суммарный уровень ангиотензина II. В результате у этих подростков формируются более часто и более серьезные нарушения углеводного обмена с развитием не только гиперинсулинемии, но и гипергликемии, что является отражением устойчивого снижения чувствительности рецепторов тканей-мишеней к инсулину.
Полученные данные позволяют сделать заключение о том, что у подростков с артериальной гипертензией активация САС и РААС, при отсутствии адекватного повышения мелатонина, может быть одним из элементов патогенеза нарушений углеводного обмена, который проявляется развитием инсулинорезистентности, гиперинсулинемии и гипергликемии.
1. Кисляк О.А. Артериальная гипертензия в подростковом возрасте [Текст] / О.А. Кисляк. — Москва, 2007. — С. 138-141.
2. Громнацкий Н.И. Липидный спектр крови у детей и подростков с артериальной гипертонией [Текст] / Н.И. Громнацкий, Н.Н. Громнацкая // Росс. кардиол. журн. — 2006. — № 4. — С. 24-26.
3. Lipid screening and cardiovascular health in childhood [Text] / S.R. Daniel, F.R. Greer // Pediatrics. — 2008. — № 122(1). — Р. 198-208.
4. Гурьева Е.Н. Характер гуморально-метаболических нарушений в подростковом возрасте в зависимости от варианта первичной АГ и основных компонентов метаболического синдрома [Текст] / Е.Н. Гурьева, С.В. Иванова, И.Г. Морено // Детская кардиология 2010: тезисы 6-го Всероссийского конгресса. — М., 2010. — С. 158-159.
5. Структура факторов риска поражения органов-мишеней и метаболических изменений у больных артериальной гипертензией в различных возрастных группах [Текст] / С.А. Бойцов [и др.] // Кардиология. — 2009. — № 4. — С. 19-24.
6. Нефедова Ж.В. Метаболические и нейрофизиологические аспекты артериальной гипертензии у детей и подростков [Текст]: Автореф. дис. д-ра мед. наук: 14.00.09 «Педиатрия» / Ж.В. Нефедова; Новосибирский государственный медицинский университет Росздрава. — Новосибирск, 2007. — 35 с.
7. Reaven G.M. Insulin resistance, cardiovascular disease, and the metabolic syndrome [Text] / G.M. Reaven // Diabetes Care. — 2004. — Vol. 27. — P. 1011-1012.
8. Taittonen L. Insulin and blood pressure among healthy children [Text] / L. Taittonen, M. Uhari, M. Nautinen // Amer. J. Hypertens. — 1996. — Vol. 9. — P. 193-199.
9. Плотникова И.В. Маркеры метаболического синдрома у подростков с артериальной гипертензией [Текст] / И.В. Плотникова, Т.Е. Суслова, Н.М. Желтоногова // Педиатрия. — 2007. — Т. 86, № 3. — С. 39-43.
10. Метаболический синдром у детей и подростков: Консенсус Международной диабетической федерации [Текст] // Междунар. эндокрин. журн. — 2008. — № 2(14). — С. 100-103.
11. Бутрова С.А. Метаболический синдром: патогенез, клиника, диагностика, подходы к лечению [Электронный ресурс] / C.А Бутрова. Режим доступа: MR httр // med. ru / doc / 141504. htm.
12. Клинико-генетические аспекты нарушений углеводного обмена и эффективность их коррекции моксонидином и метформином у больных артериальной гипертонией / Ж.Д. Кобалова, В.В. Толкачева, И.В. Игнатьев и др. // Тер. архив. — 2005. — № 1. — С. 46-51.
13. Henriksen E.J. Improvement of insulin sensitivity by antagonism of the renin-angiotensin system // AJP — Regul. Physiol. — 2007. — Vol. 293, № 3. — P. R947-R980.
14. Lastra G., Habibi J., Whaley-Connell A.T. et al. Renin inhibition improves systemic insulin resistance and skeletal muscle glucose transport in a transgenic rodent model of tissue renin overexpression // Endocrinology. — 2009. — Vol. 150, № 6. — P. 2561-2568.
15. Kwang Kon Koh, Sakuma I., Quon M.J. Role of renin-angiotensin system blockades in reciprocal relationship between insulin resistence end endothelial dysfunction // Hypertension. — 2010. — Vol. 56. — P. e169.
16. Болотова Н.В., Лазебникова С.В., Аверьянов А.П. Особенности формирования метаболического синдрома у детей и подростков // Педиатрия. — 2007. — № 3. — Т. 86. — С. 35-39.
17. Homeostasis model assessment: insulin resistance and — cell function from fasting plasma and insulin concentrations in man [Text] / D.R. Mathews, J.P. Hosker, A.S. Rudenski et al. // Diabetologia. — 1985. — Vol. 28. — P. 412-419.
18. Ghosh A. Factor analysis of risk variables associated with metabolic syndrome in Asian Indian adolescents / A. Ghosh // Am. J. Hum. Biol. — 2007. — Vol. 19, № 1. — P. 34-40.
19. Nogueira T.C., Lellis-Santos C., Jesus D.S. et all. Absence of melatonin induces night-time hepatic insulin resistance and increased gluconeogenesis due to stimulation of nocturnal unfolded protein response // Endocrinology. — 2011. — Vol. 152, №. 4. — P. 1253-1263.