Журнал «Боль. Суставы. Позвоночник» 2 (02) 2011
Вернуться к номеру
Системный остеопороз и заболевания крови
В клинической практике дифференциальная диагностика остеопороза представляет собой не всегда легкую задачу. При установлении диагноза системного остеопороза, основываясь только на низких показателях минеральной плотности костной ткани или установленных с помощью рентгенографии переломов тел позвонков, данные изменения следует дифференцировать как от множества других патологий, являющихся причиной вторичного остеопороза, так и самостоятельных заболеваний, таких как остеомаляция, миеломная болезнь и др. Ниже представлен клинический пример, анализ которого побуждает уделить особое внимание дифференциальной диагностике остеопороза.
Пациентка З., 59 лет, направлена в Украинский научно-медицинский центр проблем остеопороза из Института нейрохирургии для проведения дополнительного обследования в связи с планируемым оперативным вмешательством (вертебропластика).
Предъявляет жалобы на резкие боли в грудном и поясничном отделе позвоночника, не купирующиеся неопиоидными анальгетиками и являющиеся причиной обращения в Институт нейрохирургии. Боли в нижнегрудном и поясничном отделе позвоночника усиливаются в вертикальном положении и иррадиируют по ходу ребер и в область живота. Также беспокоит выраженное ограничение подвижности в позвоночнике, быстрая утомляемость и потеря работоспособности. В связи с выраженным болевым синдромом была госпитализирована в отделение возрастных изменений опорно-двигательного аппарата ГУ «Институт геронтологии АМН Украины» с диагнозом «системный остеопороз, тяжелая форма» (февраль 2011 г.).
Анамнез жизни и заболевания. Из анамнеза заболевания известно, что боли в позвоночнике беспокоят в течение полугода (с лета 2010 г.). Тогда же во время лечения в одном из неврологических отделений г. Киева установлены деформационные изменения тел позвонков (согласно рентгенологическому заключению — по типу «рыбьих»). Выписана с улучшением после курса противовоспалительной и анальгетической терапии.
В декабре 2010 года после поднятия тяжести состояние пациентки резко ухудшилось, в связи с чем была повторно госпитализирована в нейрохирургическое отделение. Выписана без существенного эффекта и направлена на оперативное лечение.
Менструальная функция: менархе — 14, менопауза — 56 лет. В 1958 году резекция правого яичника в связи с его кистой. Болеет гипертонической болезнью (около 5 лет), находится на гипотензивной терапии; а также хроническим холециститом.
Заключение МРТ от 14.01.2011 (исследование позвоночника проведено на уровне Th9-S5 за 1 мес. до обращения!): МР-признаки правостороннего сколиоза І ст., дегенеративно-дистрофических изменений поясничного отдела позвоночника, протрузии дисков на уровне L3-S1.
Данные объективного обследования. Рост 156 см, масса тела 88,0 кг, индекс массы тела 36,2 усл.ед. Кожные покровы и видимые слизистые оболочки бледные, периферических отеков нет; дыхание везикулярное, хрипов нет; тоны сердца несколько приглушены, ритмичны, гемодинамика стабильна; живот — без особенностей; симптом Пастернацкого отрицательный с двух сторон. Осанка сутулая, походка замедленная, передвигается с палочкой. Усилен грудной кифоз в нижнегрудном и верхнепоясничном отделах позвоночника, уплощен поясничный лордоз. При пальпации области позвоночника отмечаются выраженные боли в проекции остистых отростков и паравертебральных точек на уровне Th6-Th11 и L1-L5. Движения в нижнегрудном и поясничном отделе позвоночника резко ограничены и болезненны. Чувствительных и двигательных нарушений не обнаружено. Изменений со стороны крупных и мелких суставов не обнаружено.
Учитывая характер жалоб, возраст пациентки и особенности течения заболевания было проведено лабораторно-инструментальное обследование.
Основные результаты лабораторного и инструментального исследований
Общий анализ крови: Hb — 93 г/л (N: 110–165); Ht — 0,29 (N: 0,35–0,50); эр. — 3,44 • 109/л (N: 3,8–5,8); лейк. — 7,4 • 106/л (N: 4–10); тромбоциты — 211 (150–400); СОЭ — 42 (N: 2–18 мм/ч), формула крови — без особенностей, за исключением количества палочкоядерных гранулоцитов — 14 (N: 1–4).
Общий анализ мочи: удельный вес — 1,020; реакция кислая, следы белка, плоский эпителий — небольшое количество, лейкоциты — 2–3 в поле зрения, слизь — небольшое кол-во.
Биохимический анализ крови: общий белок — 86,7 г/л (N: 35–50); альбумин — 28,85 г/л (N: 35–50); кальций — 2,27 ммоль/л (N: 2,15–2,58); магний — 0,62 мкмоль/л (N: 0,70–0,98); фосфор — 1,3 мммоль/л (0,81–1,45). Другие биохимические показатели в пределах нормы.
Иммуноферментный анализ маркеров костного ремоделирования — tP1ND — 82,12 нг/мл (N: 20,0–100,0); остеокальцин — 19,91 нг/мл (N: 11,0–43,0); βCTx — 1,24 нг/мл (для женщин в постменопаузе N: < 1,008); паратгормон — 9,37 пг/мл (N: 15,0–65,0), витамин D — 32,66 нмоль/л (N: 50,0–100,0).
Заключение ультразвукового исследования органов брюшной полости: признаки хронического холецистита, полип желчного пузыря, диффузные изменения в поджелудочной железе.
Данные электрокардиографического исследования — без особенностей.
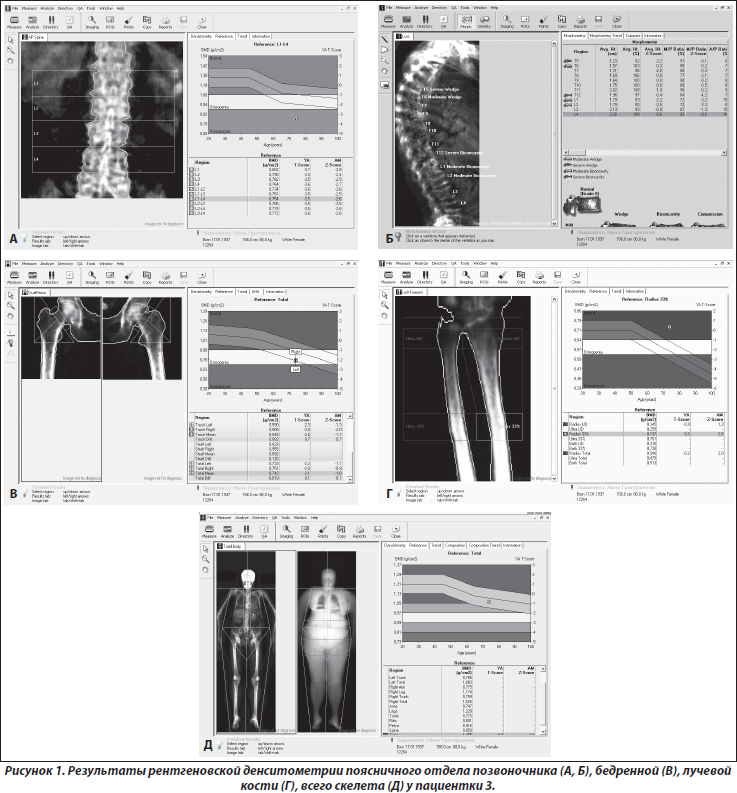
По данным двухфотонной рентгеновской абсорбциометрии (рис. 1) Т-критерий составил на уровне позвоночника –3,5 SD; бедренной кости — –2,1; лучевой кости — 0,3; всего скелета — –0,9 SD. По данным рентгенморфометрического исследования позвоночника — деформации тел Th5, Th6, Th12, L1 и L2 позвонков.
Таким образом, по данным рентгеновской денситометрии установлен системный остеопороз с множественными переломами тел позвонков, однако изменения в биохимическом анализе крови вызывают необходимость дополнительных исследований (рентгенографического исследования, консультации других специалистов и др. для исключения диагноза вторичного остеопороза).
На следующий после поступления день пациентка пожаловалась на резкие боли за грудиной, усиливающиеся при дыхании на вдохе после утренней гимнастики. Консультирована терапевтом, подтвердившим диагноз гипертонической болезни и не выявившим признаков нарушений коронарного кровообращения. Направлена на рентгенологическое исследование.
По результатам рентгенографии грудной клетки определяется вздутие грудины и ее перестройка с патологическим переломом в области мечевидного отростка. Структура ребер изменена с наличием мелких очагов перестройки и переломами справа — ІІ, ІІІ, VІ ребер и слева — V и VI ребер по подмышечным линиям с реакцией костальной плевры на этих уровнях.
В связи с выявленными изменениями проведено рентгенологическое исследование костей черепа в 2 проекциях: во всех костях свода и лицевого черепа определяются округлые мелкие дефекты ткани в диаметре от 0,1 до 0,5 см с достаточно четкими контурами.
На основании полученных результатов установлен диагноз «миеломная болезнь, множественная очаговая (классическая) форма».
Миеломная болезнь (множественная миелома, генерализованная плазмоцитома, болезнь Рустицкого — Каллера) — парапротеинемический гемобластоз, характеризующийся злокачественной опухолевой пролиферацией В-лимфоцитов плазматических клеток одного клона с гиперпродукцией парапротеинов (моноклонального иммуноглобулина или свободных моноклональных легких цепей иммуноглобулинов). Частота заболевания составляет 2–4 случая на 100 000 человек в год и одинакова для мужчин и женщин. Большинство больных имеет возраст старше 40 лет.
В клинике консультирована гематологом, подтвердившим данный диагноз, в том числе и на основании данных миелограммы.
Результаты миелограммы, выполненной при стернальной пункции: миелоциты — 4,0, юные — 2,0, палочкоядерные — 8,0, сегментоядерные — 8,0, эозинофилы — 3,5, базофилы — 0,5, моноциты — 2,5, лимфоциты — 7,0, плазматические клетки — 34,5.
С учетом жалоб больной, анамнеза заболевания и жизни, данных объективного статуса и дополнительных методов исследования был верифицирован клинический диагноз «миеломная болезнь, множественная очаговая (классическая) форма».
В связи с основным заболеванием пациентке рекомендован перевод в гематологическое отделение для решения вопроса о выборе терапии.
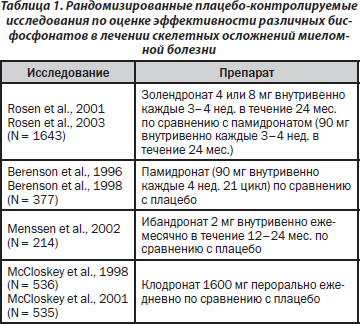
В настоящее время для лечения костных осложнений миеломной болезни широко применяются бисфосфонаты (табл. 1). Накоплены большой опыт и доказательная база относительно эффективности этих агентов в рандомизированных исследованиях, однако контроль за эффективностью лечения должен проводить специалист онколог-гематолог.
В феврале 2011 года пациентка выписана из клиники с соответствующими рекомендациями, однако в течение последующих 4 мес. за специализированной медицинской помощью не обратилась. В мае 2011 года больная умерла от осложнений основного заболевания.
Механизмы костной деструкции при миеломной болезни состоят в нарушении процессов остеобласто- и остеокластогенеза, индукции ангиогенеза и снижении иммунного контроля.
Клетки миеломы секретируют в повышенном количестве DKK1, нарушающего процессы остеобласто- и остеокластогенеза в сторону преобладания остеолитических процессов, поддерживающих рост миеломы. Первичный эффект DKK1 заключается в препятствии дифференцирования стромальных клеток в остеобласты. Угнетение Wnt-сигнального пути с помощью увеличенной секреции DKK1 при дифференцировке остеобластов способствует усиленной продукции RANKL и IL-6 и уменьшенному образованию остеопротегерина (OPG). Нарушение соотношения RANKL/OPG и усиление продукции IL-6 способствуют усиленному остеокластогенезу. Синдекан-1 (CD138), секретирующийся клетками миеломы, может связывать растворимый OPG, таким образом предотвращая угнетающее действие на функцию RANKL. Кроме того, клетки миеломы секретируют различные растворимые факторы, способствующие остеолизису (MIP-1a, sFRP-2, IL-3, sFRP-3, FRZB). Изменения в микроокружении костной миеломы индуцируют ангиогенез, увеличивают уровень сосудистого эндотелиального фактора роста, снижают иммунный контроль.
Угнетение остеобластогенеза, усиление остеокластогенеза и выраженные остеолитические процессы приводят к возникновению гиперкальциемии и нарушению нормального функционирования костного мозга, замыкая порочный круг.
Представленный клинический случай заставляет задуматься врача о своевременности и точности установления данного диагноза на этапах медицинского обследования. В настоящее время миеломная болезнь все чаще приобретает атипичное течение, однако настороженность врача в дифференциальной диагностике потери костной ткани и вертебрального болевого синдрома позволяет вовремя установить диагноз и назначить адекватное лечение.
Подготовила Н.В. Григорьева, д. м. н., главный научный сотрудник отдела клинической физиологии и патологии опорно-двигательного аппарата ГУ «Институт геронтологии НАМН Украины»