Журнал «Травма» Том 9, №1, 2008
Вернуться к номеру
Трансплантация тканей и органопротективное обезболивание
Авторы: Л.М. Смирнова - Институт хирургии и трансплантологии АМН Украины им. А.А.Шалимова, Киев, Украина
Рубрики: Травматология и ортопедия, Анестезиология-реаниматология
Разделы: Справочник специалиста
Версия для печати
В условиях регионарной анестезии осуществляли хирургическую коррекцию отдаленных последствий травматичнеских повреждений тканей с использованием микрохирургической техники. В качестве критериев адекватности анестезии использова-ли органопротективную доставку (ОПДК) и органо-протективное использование (ОПИК) кислорода.
В умовах регіонарної анестезії проводили хірургічну корекцію віддалених наслідків травматичних ушкоджень тканин з використанням мікрохірургічної техніки. Як критерії адекватності анестезії використовували органо-протективне постачання (ОППК) та органопротективне використання (ОПВК) кисню.
Regional anesthesia was applied while performing surgical correction of consequences of traumatic damages of tissues using microsurgical technique. The targeted value organoprotection delivery (OPDO) and organoprotection consump-tion (POCO) of oxygen were used as criterion of the anesthesia adequacy.
регионарная анестезия, органопротективная доставки, органопротективное потребление кислорода
регіонарна анестезія, органопротективне постачання та органопротективне використання кисню
regional anesthesia, organoprotection delivery, organoprotection consumption of oxygen
Свободная аутодермопластика имеет успешную полувековую историю. Методика микрохирургической аутотрансплантации свободных реваскуляризованных тканей в конце ХХ века совершила революцию в пластической хирурги в целом и в частности в таких ее разделах, как реконструкция и восстановление [12].
Хирургические вмешательства с использованием микрохирургической техники требуют специфического подхода к выбору способа анестезии. В литературе значительное внимание уделяется методам регионарного обезболивания, которые считаются самыми оптимальными при выполнении оперативных вмешательств с использованием микрохирургической техники [1].
Успех регионарной анестезии (РА) определяется в первую очередь теоретическими знаниями и практическим опытом специалиста проводящего анестезию, во вторую – местным анестетиком, в третью – технической оснащенностью [9, 10].
Как ни досадно, но снижение интереса к регионарным методам обезболивания прежде всего связано с недостаточными знаниями анестезиологов патофизиологических аспектов регионарных блокад, боли и операционного стресса – с одной стороны, с другой – нежеланием пациентов присутствовать на своей операции, страх перед техническим выполнением РБ. Безусловно важным моментом негативного отношения к РБ есть и то, что пациенты, которым предыдущее оперативное лечение проводили в условиях РА без нейроаналгоседации, долго, на протяжении нескольких часов находились в фиксированном положении и это «принуждение» вызывало психоэмоциональный дискомфорт [6].
Первый ряд причин легко устраняется благодаря обучению молодых специалистов методам РБ. Развитие технического прогресса и внедрение в клиническую практику новых технологий, таких как управляемая ультразвуковая РА, позволяющая идентифицировать расположение нервных стволов, сосудов, эпидурального пространства [13, 15]. Это является важным моментом автоматизации серьезных манипуляций, нивелирующим возможные осложнения [15]. Повышение уровня безопастности особенно значемо у молодых специалистов.
Достижение психоэмоционального комфорта всецело зависит от квалификации анестезиолога и наличия фармакологических средств. Решение этой проблемы кроется в разумной многофакторной комбинации фармакологических препаратов, которые имеют разные свойства и утонченные технологии их введения. Обязательным условием угнетения сознания должен быть естественный сон.
Непосредственное влияние на структуры ЦНС происходит через ГАМК-эргическую систему и опосредованое – через NMDA-рецепторы. Следовательно, наиболее перспективным препаратом из всех гипнотиков является оксибутират натрия, фармакологическое действие которого связано с естественной ГАМК-эргической системой. В литературе есть сообщения о том, что оксибетират натрия более безопасен, чем пропофол, но имеет недостаток – его длительный фармакологический эффект [11]. Однако всегда надо помнить о том, что продолжительность фармакологического эффекта натрия оксибутирата дозозависима и использование низких доз 20-30 мг/(кг×час) обеспечивает физиологический сон без угнетения функции внешнего дыхания.
Основной задачей анестезиологии является защита организма больного от хирургической агрессии различной степени выраженности. Достижение позитивного результата в реконструктивно-пластической хирургии (РПХ) невозможно без специальных мер по обеспечению жизнеспособности реваскуляризированных аутотканевых комплексов. В основе такого подхода лежит предупреждение периферического вазоспазма и поддержание проходимости микрососудистых анастомозов, что побуждает к поиску методов эффективного контроля. Кроме оценки адекватности анестезиологического пособия необходимо иметь постоянную информацию о состоянии перфузии тканей в микрососудистом русле. Современные методики, отражающие состояние микрососудистого русла, такие как тетраполярная реоплетизмография, транскутанное мониторирование в тканях РткО2 и РткСО2, дорогостоящи и не являются общедоступными [7]. В этом плане актуально, целесообразно и перспективно определять, какое количество кислорода в данный момент потребляют ткани организма для того, чтобы доставка кислорода отвечала потребностям организма. Несоответствие в соотношении доставка/потребление ведет к оксидантному стрессу или гипоксии. Оксигенация тканей организма – генетически детерминированый процесс, и любые нарушения кислородоресурсообеспечения вначале ведут к напряженной работе систем жизнеобеспечения, а затем наступает состояние декомпенсации. Одним из ответов клетки на действие повреждающих факторов является активация суицидальной программы, получившей название программируемой гибели клеток [2].
Цель исследования: определить органопротективность РА с психоэмоциональным торможением у больных во время хирургической коррекции отдаленных последствий травматического повреждения тканей с использованием микрохирургической техники на основании показателей ОПДК и ОПИК и сравнить их с общепринятыми показателями транспорта и потребления кислорода.
Материал и методы
Проведено обследование и лечение 20 больных в молодом возрасте, у которых в отдаленном периоде после травматического повреждения возникли гнойно-некротические дефекты мягких тканей. У пациентов установлен 2-й функциональный класс физического статуса, что соответствует 4 баллам по шкале оценки операционно-анестезиологического риска Г.А.Шифрина [8].
Для анестезиологического обеспечения операций свободной трансплантации комплекса тканей использовали РА с нейроаналгоседацией.
Для нейроаналгоседации использовали натрия оксибутират, болюсная доза которого 20 мг/кг, и кетамин 0,5 мг/кг. Поддерживающая доза натрия оксибутирата 20 мг/(кг×час) и кетамин 0,3 мг/(кг×час) вводились постоянно.
Для замещения дефектов покровных тканей использовали многослойный комплекс тканей, состоящий из мышц, подкожной основы, кожи, питающих сосудов. После предварительной подготовки реципиентного места, иссечения рубцово-измененных или нежизнеспособных тканей на него переносили выделенный свободный комплекс тканей. Накладывали микрососудистые артериальные и венозные анастомозы. Восстанавливали анатомические структуры и осуществляли окончательную послойную фиксацию комплекса тканей к окружающим тканям.
Возобновление кровотока в пересаженных тканях является наиболее важным моментом операции, определяющим жизнеспособность и приживление трансплантата. В этот период недопустима венозная гипоксемия и венозный стаз.
Во время операции, наркоза и ближайшего послеоперационного периода изучали показатели центральной гемодинамики, кислородного режима и метаболизма. Измеренные с помощью микроанализатора газов крови (RapidLab – 248 фирмы Bayer) основные показатели кислотно-основного состояния корригировали с помощью прикладной компьютерной программы O.Siggard-Andersen [14]. Полученные значения показателей Cx, Qx из глубокой картины кислородного статуса [14] использовали для вычисления ОПДК и ОПИК.
Проблема гипоксии является одной из ведущих в анестезиологии: несомненно, оценка транспорта кислорода и его потребление тканями составляет наиболее важную и ответственную часть ежедневной работы врача-анестезиолога.
Обеспечение соответствия между доставкой и потреблением кислорода у всех пациентов является важнейшей задачей современных лечебных мероприятий, определяет конечный результат лечения [3]. Исход заболевания зависит от полноты устранения нарушений кислородного режима и тканевой гипоксии.
Выраженность ОПИК (ВОПИК) во время анестезиологического обеспечения операции определяли по формуле [4]:
ВОПИК=100 (Сx × СИ - VO2) : (Сx × СИ), %,
где: 100 - коэффициент пересчета для выражения величины в процентах; СИ - сердечный индекс, л/(мин×м2); VO2 - потребление кислорода, мл/л (по общеизвестной формуле); Сx - артерио-венозная разница содержания кислорода, удовлетворяющая энергетические потребности организма. Недостаток или избыток кислорода определяется в процентах.
Выраженность ОПДК (ВОПДК) тканями организма определяется по формуле [5]:
ВОПДК = (ПтДК-СТК) : ПтДК×100%,
где: ПтДК – потребность в доставке кислорода, мл/(мин×м2); СТК - системный транспорт кислорода, мл/(мин×м2); 100 - коэффициент пересчета в проценты. ПтДК = Qx × CaO2 × СИ, мл/(мин×м2), где Qx – фактор компенсации кислорода артериальной крови; CaO2 – содержание кислорода в артериальной крови (по общепринятой формуле), мл/л.
Изменение параметра Qx и определение в соответствии с его значением ПтДК обеспечивает повышение точности определения ВОПДК, поскольку основано на точном измерении количества кислорода, необходимого тканям для окисления энергопродуктов в данное время.
Результаты вычислений, отклонение показателя от уровня 100 % позволяют определить степень нарушения составляющих органопротективности и определить возможности их устранения.
Статистическая обработка результатов исследования проведена с помощью персонального компьютера с использованием пакета Statistica for Windows. В тексте приведены достоверные изменения изучаемых показателей.
Результаты и обсуждение
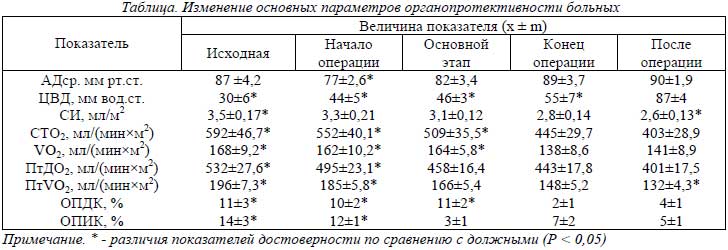
Полученные данные представлены в табл. АДср. в условиях применения изучаемого метода анестезии удерживалось на уровне должных значений в течение интраоперационного и периоперационного периода. Только в момент начала операции его величина регистрировалось в среднем на 10 % ниже.
Показатель ЦВД на всех изучаемых этапах был ниже должного значения, что свидетельствует о относительной гиповолемии. В результате интраоперационного восполнения с использованием инфузионных сред и создания напряженного объема жидкости уровень ЦВД повысился в среднем на 65 % от исходного к концу операции. Это свидетельствует о том, что в течение операции и наркоза удавалось создавать напряженный объем жидкости и удерживать его на уровне нормоволемии.
Производительность сердечно-сосудистой системы на всех этапах исследования была гипердинамической с переходом в нормодинамическую к концу оперативного лечения, о чем свидетельствует показатель СТО2, который превышал в среднем на 23 % должный уровень в начале исследования. В конце операции и в ближайший послеоперационный период достоверных отличий от должной величины этот показатель не имел.
В исходном состоянии и в течение первого часа оперативного лечения потребление кислорода тканями было высоким и показатель VO2 превышал должный уровень в среднем на 19 %. Нормализация процессов кислородоресурсообеспечения под влиянием фармакологических препаратов способствовала снижению уровня метаболизма, и в конце операции показатель VO2 достоверно не отличался от своего должного значения.
Волнение пациента перед предстоящим оперативным лечением и недостаточный эффект премедикации приводили к повышению интенсивности метаболических процессов в организме в среднем на 14 %, о чем свидетельствует показатель ОПИК. Отсутствие патологических изменений сердечно-сосудистой системы и гипердинамический тип кровообращения обеспечивали транспорт кислорода тканям на уровне, не лимитирующем процессы потребления. В конце операции потребность в доставке кислорода и потребность в потреблении кислорода соответствовали должному значению. Стабилизация показателей ПтДК и ПтИК на базальном уровне свидетельствует об органопротективности используемого анестезиологического пособия. Эта стабильность подтверждается показателями ОПДК и ОПИК, которые достоверно не отличаются от должных величин (100 %) , а незначительное отклонение показателя существенного значения не имеет, так как допустимым является отклонение от референтного значения в пределах 10 %.
Выводы
- РА с нейроаналгоседацией по предложенной схеме у пациентов с отдаленными последствиями травматического повреждения тканей является органопротективной.
- Показатели ОПДК и ОПИК информативны, их легко рассчитать, используя показатели общепринятого обследования пациента; они могут быть применены в любом отделении анестезиологии и интенсивной терапии для определения адекватности анестезии и эффективнности лечения.
- Галич С.П., Петах А.В., Дабижа А.Ю. и др. Пересадка мышечных перфорантных лоскутов для замещения дефектов тканей конечностей // Клінічна хірургія. -2005. -№ 9. -С. 47-51.
- Голубев А.М, Москалева Е.Ю., Северин С.Е., Веснянко Т.П., Кузовлев А.Н., Алкадарский А.С., Порошенко Г.Г. Апоптоз при критических состояниях. Общая реаниматология. -2006. -Т. 2. - № 5-6. –С. 184-190.
- Гнатів В.В. Порушення кисневого забезпечення тканин у хворих при різних фазах перітоніту виразкового генезу // Інфекц. Хвороби. -2002. -№ 4. –С.51-54.
- Деклараційний патент 9276 А Україна. МПК 7 А61В17/00, А61М15/00. Спосіб визначення вираженості органопротективного компонента використання кисню під час анестезіологічного забезпечення / Л.М. Смирнова, Г.А. Шифрин (Україна). – Заявл.09.03.05; Опубл. 15.09.05. Бюл. № 9.
- Деклараційний патент 11050 А Україна. МПК 7 А 61 М 19//00, а 61 В5/145, Спосіб визначення вираженості органопротективного компонента постачання кисню тканинам організму / Л.М. Смирнова, Г.А. Шифрин (Україна) – Заявл.11.05.05; Опубл.15.12.05//Бюл. 12.
- Зайцев А.Ю., Светлов В.А., Марков Г.А. и др. Новый метод мониторинга психоэмоционального состояния во время сбалансированной анестезии на основе регионарных блокад // Анестезиол.и реаниматол. – 2004 .-№ 5.-С. 64-68.
- Назырова Л.А., Садыкова М.А. Периоперационный контроль температурного градиента при реконструктивно-пластических вмешательствах на нижних конечностях // Анестезиол. и реаниматол.-2006. -№ 4. –С. 39-42.
- Организация и стандартизация интенсивной терапии и обезболивания: Практическое руководство / Шифрин Г.А.- Запорожье: ВПК “Запоріжжя”, 2001. - 80 с.
- Орлов Г.С., Кудимов С.А., Кострикова Э.В,.Хмызов А.А. Возможности и перспективы регионарной анестезии в ортопедии и травматологии // Международный медицинский журнал.-2002. -Т. 8, № 1/2. -С.139-143.
- Семенюта И.П., Щеголев А.А., Ларин А.А., Титков В.Е. Современная регионарная анестезия при операциях на конечностях //Рос. мед. Журнал.-2002. -№ 5.-С.46-48.
- Светлов В.А., Зайцев А.Ю., Козлов С.П. Сбалансированная анестезія на основе регіонарних блокад: стратегія и тактика //Анестезиол. и реаниматол. – 2006. -.№ 4.-С.4-12.
- Эюбов Ю.Ш. Свободная аутодермопластика в восстановительной микрохирургии // Вестник хирургии.-2003.-№6.-С.43-46.
- Gray A.T. Ultrasound –guided Regional Anesthesia. //Anesthesiology.-2006. -V.104 (2). –P.368-73.
- Siggard-Andersen O. The oxygen status algorhythm: a computer program for calculation, and displaing pH and blood gas data // Scand. J.Clin.Lab.Invest. – 1990.-Vol.50,suppl.203.-P.29.
- Vincent W. S. Chan, Hugo Nova, Sherif Abbas, Colin J. L. McCartney, Anahi Perlas, Da Quan Xu. Ultrasound Examination and Localization of the Sciatic Nerve.Anesthesiology, 2006 .V 104, No 2, 309-341.