Журнал «» 4(18) 2011
Вернуться к номеру
«Старые» и «новые» ингибиторы АПФ: портит ли старый конь борозду?*
Авторы: Радченко А.Д., ННЦ «Институт кардиологии имени академика Н.Д. Стражеско» НАМН Украины, г. Киев
Рубрики: Семейная медицина/Терапия, Кардиология, Терапия
Версия для печати
В последнее время благодаря активному продвижению крупных фармацевтических компаний многие врачи стали получать информацию о значительном преимуществе более «новых» (соответственно более дорогих) иАПФ перед «старыми» (соответственно более дешевыми) и об их «уникальном» механизме действия. Данная статья представляет обзор данных, которые позволяют ответить на такие вопросы: существуют ли различия между иАПФ в степени снижения артериального давления (АД) и влиянии на дополнительные показатели, характеризующие АД? Есть ли «уникальные», т.е. присущие только определенному иАПФ свойства, не зависящие от его способности снижать АД? Нужно ли отказываться от назначения «старых» иАПФ в пользу «новых»?
Сделан вывод, что, несмотря на различия в химической структуре и фармакокинетике, большинство иАПФ одинаково эффективны при различной кардиоваскулярной и сопряженной с ней патологии. Существуют менее изученные в больших исследованиях препараты и более изученные. Среди последних так называемые «старые» иАПФ занимают как раз не последнее место. Они в такой же степени снижают АД при сопоставлении в эквивалентных дозах, могут назначаться один раз в сутки (лизиноприл, комбинация «эналаприл + диуретик»), имеют клиническую доказательную базу эффективности у пациентов с артериальной гипертензией (АГ), сахарным диабетом, сердечной недостаточностью (СН) или систолической дисфункцией левого желудочка любой этиологии, нефропатиями. Они способны предупреждать развитие коронарных событий у пациентов с АГ, СН или систолической дисфункцией левого желудочка. Они улучшают прогноз при назначении в первые сутки инфаркта миокарда у пациентов высокого риска, чего нельзя сказать о некоторых «новых» иАПФ. Поэтому отказываться от их применения в настоящее время нет никакого смысла. Тем более это касается Украины — страны с большими экономическими трудностями, в которой пациент сам вынужден приобретать себе лекарства. Именно «старые» иАПФ выпускаются в виде генериков в значительном количестве и имеют соответственно более низкую стоимость.
Ингибиторы АПФ, классификация, показания, проблема выбора.
В настоящее время накопилось множество данных об эффективности ингибиторов ангиотензинпревращающего фермента (иАПФ) при различных сердечно-сосудистых заболеваниях. Эти данные продолжают пополняться результатами новых исследований. Практически нет ни одного патологического состояния в кардиологии, при котором не были бы показаны иАПФ. В то же время благодаря активному продвижению крупных фармацевтических компаний многие врачи стали получать информацию о значительном преимуществе более «новых» (соответственно более дорогих) иАПФ перед «старыми» (соответственно более дешевыми) и об их «уникальном» механизме действия [64]. Так ли это? Данная статья призвана помочь практическому врачу разобраться в потоке информации, которую он получает, и ответить на такие вопросы:
— Существуют ли различия между иАПФ в степени снижения артериального давления (АД) и влиянии на дополнительные показатели, характеризующие АД?
— Есть ли «уникальные», т.е. присущие только определенному иАПФ свойства, не зависящие от его способности снижать АД?
— Нужно ли отказываться от назначения «старых» иАПФ в пользу «новых»?
Сравнение способности иАПФ снижать АД
Всем известно, что основное гемодинамическое действие иАПФ — это способность уменьшать периферическое сопротивление, влиять на натрийурез и таким образом снижать АД, не вызывая существенных изменений частоты сердечных сокращений [1–5, 80]. У нормотензивных и гипертензивных пациентов без сердечной недостаточности (СН) они немного снижают сердечный выброс. В отличие от других вазодилататоров при назначении иАПФ рефлекторная тахикардия обычно отсутствует, возможно, это объясняется их влиянием на чувствительность барорецепторов, стимуляцией вагуса и снижением активности симпатоадреналовой системы. У пациентов с СН иАПФ индуцируют также венозную дилатацию, уменьшая таким образом преднагрузку на сердце.
Cуществует достаточно много исследований, в которых сравнивали антигипертензивную эффективность различных иАПФ. При этом в части из них проводилось сопоставление не совсем адекватных доз. Наиболее полное сравнение антигипертензивной эффективности различных иАПФ представлено результатами метаанализа Cochrane Collaboration 2009 [40]. В этот анализ вошли результаты 92 исследований, в которых изучали эффективность монотерапии различными иАПФ. В целом в этих исследованиях принимали участие 12 954 пациента, средний возраст 54,4 года, средний уровень АД 157,1/101,2 мм рт.ст. Длительность лечения различными иАПФ в среднем составила 6,2 недели. Эффективность иАПФ сравнивалась с таковой плацебо, степень снижения АД при приеме препаратов рассчитывалась так: снижение АД на фоне иАПФ минус снижение АД на фоне плацебо. В среднем на фоне плацебо САД снизилось на 3,2 мм рт.ст., ДАД — на 3,7 мм рт.ст.
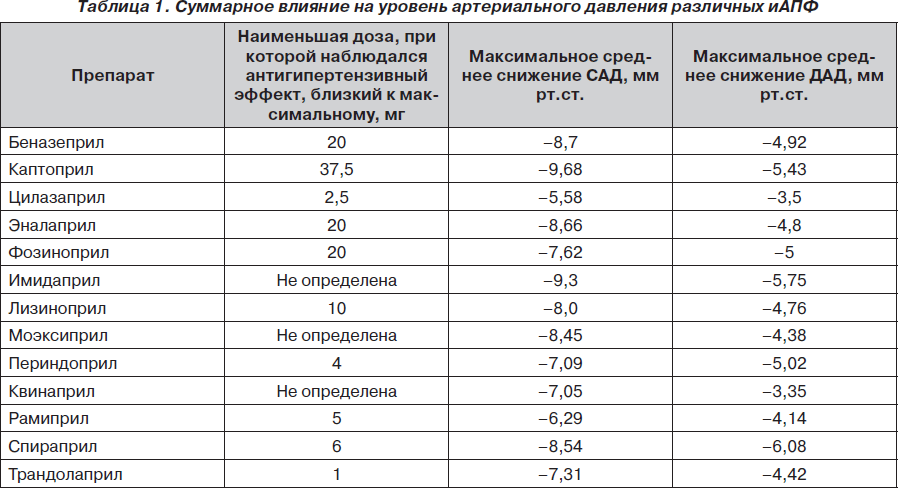
Данные о наиболее эффективной дозе препаратов и степени снижении АД представлены в табл. 1.
Для беназеприла статистически достоверное снижение АД по сравнению с плацебо наблюдалось лишь в дозе 20 мг и более. Каптоприл в любых изучаемых дозах был достоверно более эффективен, чем плацебо, при двух- или трехкратном назначении. Минимальная суточная эффективная доза — 37,5 мг. Для цилазаприла минимальная суточная эффективная доза составила 2,5 мг, для эналаприла — 5 мг, для фозиноприла — 10–20 мг, имидаприла — скорее 20 мг (мало данных), лизиноприла — 10 мг, моэксиприла — 15 мг, периндоприла — 4 мг, квинаприла — скорее 20 мг (мало данных), рамиприла — 5 мг, спираприла — 3–6 мг, трандолаприла — 1 мг. Указанные дозы для некоторых иАПФ отличаются от рекомендованных некоторыми производителями стартовых доз, которые чаще меньше (табл. 1). Это следует учитывать. Стартовые дозы позволяют избежать эффекта первой дозы, но они не всегда позволяют достоверно снизить АД. Для снижения АД нужно назначать эффективные дозы. В табл. 1 указаны наименьшие дозы, которые обеспечивают снижение АД, близкое к максимальному. Для лизиноприла это 10 мг, для рамиприла — 5 мг, для эналаприла — 20 мг. Нельзя назначить 5 мг эналаприла или 2,5 мг рамиприла и ждать существенного антигипертензивного эффекта. Кроме того, необходимо учитывать, что для некоторых иАПФ степень снижения АД может возрастать при увеличении дозы (дозозависимый эффект), например, для лизиноприла с 10 до 80 мг. Для других иАПФ при увеличении дозы не наблюдается существенного снижения АД, как, например, для рамиприла с 5 до 10 мг или для спираприла с 6 до 12 мг.
Как видно из табл. 1, наименьшее влияние на уровень САД имели иАПФ цилазаприл и рамиприл, на уровень ДАД — цилазаприл и квинаприл. Каптоприл и имидаприл оказывали наибольшее влияние на уровень САД, спираприл, имидаприл, каптоприл — на уровень ДАД. Эффект других иАПФ был приблизительно одинаковым.
На рис. 1–4 представлено сравнение различных иАПФ в различных сопоставимых дозах — 1/8, 1/4, 1/2 от максимальной и в максимальной. Как видно из рис. 1–4, в дозе 1/8 от максимальной наиболее эффективным был лизиноприл 10 мг, в дозе 1/4 от максимальной первенство лизиноприла сохранялось, значительно увеличилось снижение АД на рамиприле 5 мг, трандолаприле 1 мг, в дозе 1/2 от максимальной эффективность беназеприла 20 мг, эналаприла 20 мг, фозиноприла 20 мг, имидаприла 10 мг, моэксиприла 15 мг, спираприла 6 мг значительно возросла. А эффективность других иАПФ, в том числе периндоприла 4 мг и рамиприла 10 мг, была ниже. Эффективность монотерапии лизиноприлом 40 мг не изучалась. В максимальных дозах, рекомендуемых производителем, наиболее эффективными были лизиноприл 80 мг, имидаприл 20 мг, периндоприл 8 мг. Эффективность рамиприла 20 мг, эналаприла 40 мг, моэксиприла 30 мг, квинаприла 40 мг не изучалась. Если оценить максимальное снижение АД, которое возможно достигнуть при использовании дозы ≥ 1/2 от максимальной, то наиболее эффективны лизиноприл и имидаприл, наименее эффективен рамиприл (рис. 5).
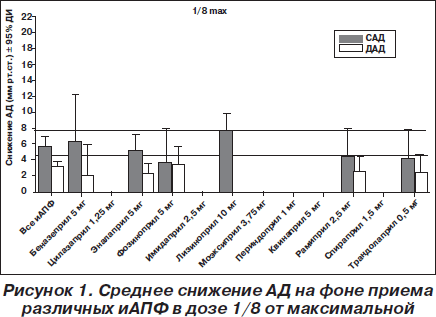
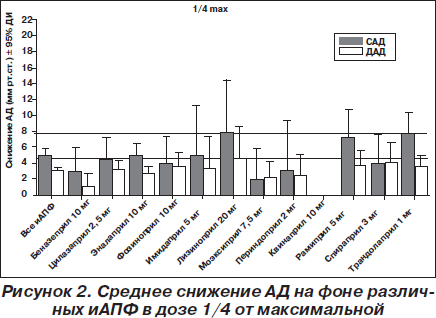
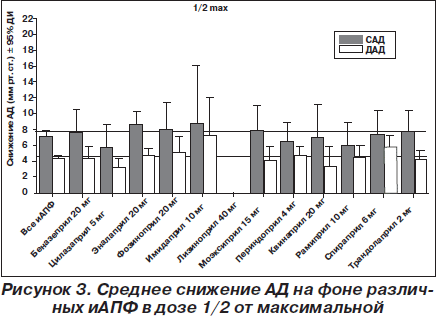
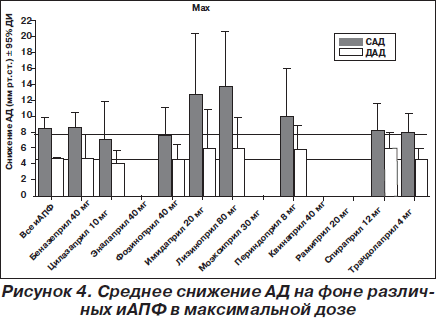
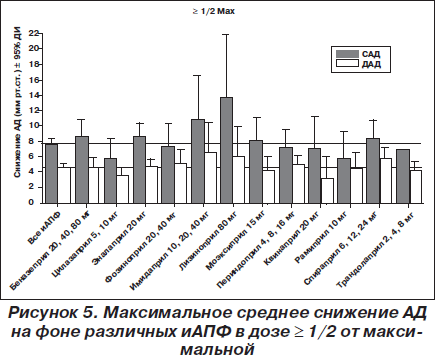
Следует отметить, что, несмотря на указанные незначительные отличия по среднему снижению АД, в отдельных исследованиях эффективность различных иАПФ была значительно выше или ниже. Поэтому в целом можно говорить, что антигипертензивная эффективность иАПФ одинакова и на первый план должна выходить не степень снижения АД, а такие показатели, как соотношение «пик/корыто», вариабельность АД, длительность антигипертензивного эффекта. Поэтому препараты с длительностью действия 24 часа и соотношением «пик/корыто» более 50 %, безусловно, имеют преимущества, так как позволяют увеличить приверженность пациента к лечению и снизить вариабельность АД. Среди таких препаратов есть и «старые» (лизиноприл), и «новые» (рамиприл, периндоприл, трандолаприл).
Дополнительные свойства иАПФ, не зависящие от его способности снижать АД
При краткосрочном назначении иАПФ уменьшается уровень ангиотензина II и альдостерона и повышаются уровни ренина и ангиотензина I. Так как ангиотензин II стимулирует симпатоадреналовую систему, то при назначении иАПФ происходит снижение уровня норадреналина, адреналина и вазопрессина. Дополнительно иАПФ способствуют образованию брадикинина, имеющего вазодилататорные свойства [80]. При длительном лечении иАПФ ангиотензин II и альдостерон возвращаются на прежние уровни за счет активации альтернативных путей (феномен «ускользания»). Однако влияние на образование кининов, простациклина и окиси азота сохраняется, что частично объясняет вазодилататорный, антитромботический и антипролиферативный эффекты иАПФ. Последний проявляется уменьшением сосудистой и кардиальной гипертрофии и экстрацеллюлярного матрикса [71]. ИАПФ также предупреждают апоптоз кардиомиоцитов в перегруженном сердце.
Для иАПФ характерно положительное влияние на почки: они в большей степени расширяют отводящую артериолу, уменьшая внутриклубочковое давление и протеинурию, снижают всасывание натрия в трубочках. Антисклеротическое действие иАПФ опосредуется их способностью влиять на уровни альдостерона, брадикинина, пролиферацию гладкомышечных клеток, функцию эндотелия, активацию и аккумуляцию воспалительных клеток, оксидативный стресс. Кроме того, иАПФ способны модулировать фибринолитический баланс, снижая уровень ангиотензина II и стимулируя тканевый активатор плазминогена 1-го типа. Они также уменьшают агрегацию тромбоцитов, увеличивая образование оксида азота и простациклина [10].
Все эти положительные качества присущи всем иАПФ. Однако между иАПФ существуют отличия в способности проникать внутрь клетки и влиять на внутриклеточную ренин-альдостероновую систему. Некоторые исследователи и фармацевтические компании превозносят эти свойства иАПФ, определяя их как нечто особенное, что делает уникальным некоторые препараты. Но большинство липофильных иАПФ должны обладать способностью легко проникать в клетку. Так, известно, что активный метаболит фозиноприла имеет индекс липофильности 2,0 ЕД, в то время как у периндоприлата он равен 0,872 ЕД, у эналаприлата — 0,108 ЕД [5]. Это значит, что он должен более легко проникать во все органы и ткани организма. В эксперименте показано, что фозиноприлат подавляет активность АПФ в сердечной мышце в большей степени, чем рамиприлат и эналаприлат (K. Huang с соавторами, 2002), что, согласно утверждению исследователей, может лежать в основе более выраженного (по сравнению с другими препаратами группы) кардиопротективного потенциала. Однако клинические исследования показали, что нелипофильный лизиноприл достоверно снижает смертность и риск госпитализаций при СН [80]. «Не слишком липофильные» каптоприл, эналаприл и рамиприл также вошли в руководства по лечению СН [72]. В настоящее время мы не можем говорить, что один иАПФ лучше по каким-то свойствам, чем другой, только на основании данных экспериментальных исследований.
Очень часто, говоря об «уникальных» плейотропных свойствах иАПФ, забывают о влиянии их на уровень АД. Действительно, разница в снижении АД в 2–3 мм рт.ст. может показаться незначительной. Однако это справедливо только в том случае, если речь идет о снижении АД у одного пациента. Когда же в исследование вовлечены сотни или тысячи пациентов с АГ, СН или другими сердечно-сосудистыми заболеваниями, то такая разница между группами с различным лечением оказывается статистически достоверной, и при этом уже нельзя говорить, что снижение АД в 2–3 мм рт.ст. не может обусловить разницу во влиянии на конечные точки [26]. Так, в исследовании VALUE разница в достигнутом САД между группами валсартана и амлодипина составила всего 2,2 мм рт.ст. в пользу амлодипина, что привело к тому, что в группе амлодипина частота развития нефатального инфаркта миокарда была достоверно меньше, а частота развития инсульта имела тенденцию к снижению (Р = 0,08) по сравнению с группой валсартана (S. Julius с соавторами, 2004).
В некоторых исследованиях было показано, что антигипертензивные препараты, одинаково снижая САД и ДАД на плечевой артерии, по-разному влияют на уровень пульсового и центрального (аортального) АД. Так, в исследовании LIFE показана достоверная разница между группами атенолола и лозартана по уровню пульсового АД в конце исследования [27]. А в исследовании К. Hirata с соавторами рамиприл на 5 мм рт.ст. больше снижал АД в аорте, чем атенолол [40]. В исследовании ASCOT комбинация «амлодипин + периндоприл» оказалась более эффективной в снижении аортального давления, чем комбинация «атенолол + тиазид», — разница по аортальному САД составила 4,4 мм рт.ст. [58, 74]. При этом именно лозартан, рамиприл и комбинация «амлодипин + периндоприл» в исследованиях LIFE, НОРЕ и ASCOT обеспечивали достоверное снижение частоты развития конечных точек, что, вполне вероятно, было связано с их положительным влиянием на уровень центрального АД. Безусловно, это не приуменьшает достоинства этих препаратов или комбинаций, однако при существовании разницы по уровню АД нельзя говорить, что эти препараты улучшают прогноз вне зависимости от их влияния на уровень АД.
В настоящее время не существует клинических доказательств, что какие-либо особенности действия тех или иных иАПФ, за исключением их способности снижать АД, обеспечивают им приоритет в назначении. Такие доказательства возможно получить при прямом сравнении различных иАПФ в слепых проспективных рандомизированных исследованиях с сопоставлением по уровню АД, которых до настоящего времени не проводилось.
Нужно ли отказываться от назначения «старых» иАПФ в пользу «новых»?
Из вышесказанного следует, что не существует достоверных различий между иАПФ по их влиянию на уровень АД. Различия по выраженности плейотропных эффектов не имеют доказательной клинической базы для того, чтобы можно было говорить о преимуществах какого-либо отдельно взятого иАПФ. Поэтому в практической деятельности врач должен опираться на существующие руководства по лечению того или иного клинического состояния. Рассмотрим некоторые из них.
Лечение АГ.Для длительного лечения АГ возможно использование любых иАПФ, за исключением короткодействующего каптоприла, который в Украине остается одним из немногих препаратов для купирования гипертензивных кризов [3, 11, 38, 39]. Возможны некоторые предпочтения в назначении тех или иных иАПФ в зависимости от наличия сопутствующей патологии. Так, при заболеваниях печени (цирроз, гепатит с печеночной недостаточностью) предпочтительнее назначение иАПФ с почечным (эналаприл, лизиноприл, периндоприл, беназеприл, квинаприл) или двойным (моэксиприл, рамиприл, фозиноприл, спираприл) путем выведения. При снижении скорости клубочковой фильтрации (< 30 мл/мин) более безопасным является назначение иАПФ с печеночным (трандолаприл) или двойным путем выведения. Однако при условии качественного жесткого лабораторного контроля при обоих состояниях возможно назначение и любых других иАПФ. Гидрофильные иАПФ (лизиноприл) возможно назначать при длительной терапии нестероидными противовоспалительными препаратами [1, 7, 10]. Существуют также доказательства, что у курильщиков лизиноприл реже вызывает кашель, чем другие иАПФ [7]. Согласно руководствам, лизиноприл также эффективен при наличии ретинопатии, мигрени, изолированной систолической гипертензии [11, 13, 17, 60, 78].
Среди многих различных генерических лизиноприлов на украинском рынке представлен и Витоприл компании STADA (Германия). В отделении симптоматических гипертензий ННЦ «Институт кардиологии имени академика Н.Д. Стражеско» изучалась антигипертензивная эффективность данного препарата у пациентов с мягкой и умеренной АГ [6]. Установлено, что лечение Витоприлом в виде моно- или комбинированной терапии с гидрохлортиазидом на протяжении двух месяцев приводило к достоверному снижению уровней офисного САД/ДАД с 164,4 ± 1,2/100,5 ± 0,9 мм рт.ст. до 133,7 ± 1,1/82,3 ± 1,0 мм рт.ст. Целевое АД было достигнуто у 85,2 % пациентов. На фоне лечения Витоприлом наблюдалось достоверное снижение уровней среднесуточного, дневного, ночного САД/ДАД соответственно на 19,2/10,6; 18,8/14,8 и 19,9/5,8 мм рт.ст. Целевое среднесуточное АД (< 120/80 мм рт.ст.) было достигнуто у 63 % пациентов. Витоприл также обеспечивал достоверное снижение величины и скорости утреннего подъема САД и ЧСС, характеризовался низкой частотой возникновения побочных явлений (16,6 %) и частотой отмены (10 %). Витоприл не приводил к достоверным изменениям биохимических показателей, которые изучались.
Таким образом, не существует значимых преимуществ так называемых «новых» иАПФ перед «старыми» в лечении АГ.
Лечение СН. Согласно действующим рекомендациям по лечению СН, иАПФ при их переносимости являются обязательной составляющей ведения пациентов с данной патологией [72]. Эти препараты способствуют улучшению выживаемости больных и уменьшают частоту госпитализаций. В рекомендации Европейского общества кардиологов 2008 года внесены иАПФ, которые имеют наибольшую доказательную базу эффективности при СН: эналаприл, каптоприл, лизиноприл, рамиприл, трандолаприл [72]. Впервые благоприятное влияние эналаприла на прогноз жизни больных с СН продемонстрирован в исследовании CONSENSUS [25, 75]. Это исследование было досрочно прекращено после того, как стало очевидным, что смертность в группе больных, леченных эналаприлом, была на 27 % ниже, чем в контрольной. В последующие годы выполнено несколько десятков рандомизированных исследований (SAVE, AIRE, TRACE, SOLVD, GISSI-3, ATLAS), которые подтвердили результаты исследования CONSENSUS [31, 33, 37, 43, 48, 54, 55, 63, 65, 68, 70, 78, 79, 86, 89]. По сводным данным, применение иАПФ снижает смертность больных с СН в среднем на 23 % и уменьшает общее число случаев смерти и госпитализации в связи с декомпенсацией СН в среднем на 35 % (K. Swedberg et al., 2005).
В исследовании SOLVD-PREVENTION у пациентов с низкой фракцией выброса (менее 40 %) эналаприл предупреждал возникновение клинических проявлений CН [79]. Полученные в ходе исследований ATLAS, GISSI-3, EUCLID результаты дали основание утверждать, что длительная терапия лизиноприлом также эффективно влияет на выживаемость и заболеваемость пациентов на всех этапах развития сердечной недостаточности. При этом в исследовании ATLAS было показано, что при СН назначение лизиноприла в низких дозах сопровождалось достоверно большей вероятностью развития комбинированной конечной точки (смерть от всех причин + госпитализации от всех причин), чем при назначении высоких доз [54]. В исследовании NETWORK при назначении эналаприла 2,5; 5 и 10 мг дважды в день не отмечено достоверной разницы по конечным точкам в группах с различной дозировкой [77]. Не было исследований, которые бы показали разницу в назначении средних и высоких доз иАПФ. Поэтому существующие руководства лишь рекомендуют достигать целевых доз иАПФ при условии их хорошей переносимости. Трандолаприл (исследование TRACE), рамиприл (исследование AIRE) и каптоприл (исследование SAVE) были эффективны у пациентов после инфаркта миокарда при наличии систолической дисфункции левого желудочка. При диастолической дисфункции левого желудочка назначение иАПФ показано при наличии клинических проявлений СН [28, 45, 48, 51, 73, 85]. Нет убедительных доказательств, что какой-то иАПФ имеет преимущества при диастолической дисфункции.
Таким образом, для лечения СН и систолической дисфункции левого желудочка предпочтение следует отдавать иАПФ, которые имеют наиболее убедительные доказательства эффективности, полученные в больших рандомизированных исследованиях и, соответственно, вошедшие в руководства по лечению СН, — эналаприлу, каптоприлу, лизиноприлу, рамиприлу, трандолаприлу и, возможно, фозиноприлу (одобрено FDA). При диастолической дисфункции возможно назначение любых иАПФ [22, 47].
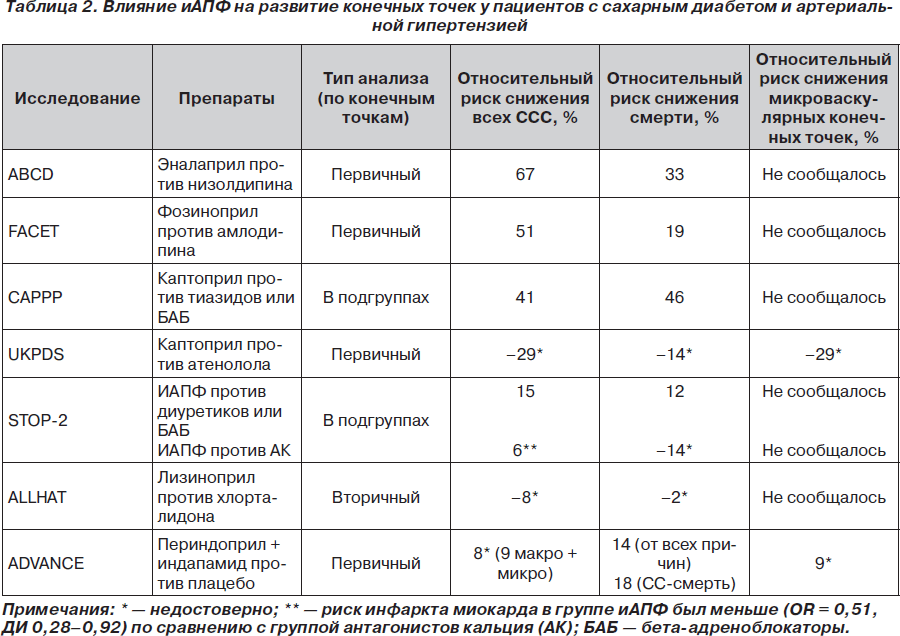
Сахарный диабет. У пациентов с сахарным диабетом иАПФ показаны как препараты первой линии для лечения АГ и диабетической нефропатии (см. раздел ниже). Влияние иАПФ на развитие конечных точек у пациентов с сахарным диабетом и АГ представлено в табл. 2. Как видно из табл. 2, большинство иАПФ, в том числе так называемые «старые», доказали эффективность у больных данной категории при наличии АГ по влиянию на прогноз. У пациентов с сахарным диабетом 1-го типа лизиноприл приводил к уменьшению прогрессирования ретинопатии низкой степени или предупреждал ее возникновение вне зависимости от наличия АГ [17, 76]. Поэтому в показаниях к применению лизиноприла указан сахарный диабет 1-го типа. Уменьшение ретинопатии было также отмечено в исследовании UKPDS при более интенсивном контроле АД [83, 84]. Предупреждение развития микроальбуминурии доказано в исследовании P. Ruggenenti с соавторами для трандолаприла у пациентов с сахарным диабетом и АГ и у пациентов высокого риска для рамиприла [62, 88].
Следует сказать, что ни в рекомендациях Американской ассоциации эндокринологов [8], ни в рекомендациях Европейского общества кардиологов и Европейского общества гипертензии не выделяют преимуществ каких-либо отдельных иАПФ при сахарном диабете, но подчеркивается важность контроля АД. В исследовании ADVANCE было показано, что дополнительное рутинное назначение антигипертензивной терапии в виде комбинации «периндоприл + индапамид» приводит к достоверному снижению риска возникновения макро- и микрососудистых событий на 9 % (но недостоверно отдельно для макро- и для микрососудистых событий), общей смертности — на 14 % и кардиоваскулярной смерти — на 18 %. Кроме того, даже у нормотензивных пациентов с сахарным диабетом использование антигипертензивной терапии способствовало снижению вероятности появления микроальбуминурии на 21 %. В этом исследовании было подтверждено преимущество достижения более низкого (< 135 мм рт.ст.) по сравнению с более высоким (< 140 мм рт.ст.) САД. Однако в исследовании ACCORD BP более интенсивное лечение пациентов с сахарным диабетом (САД < 120 мм рт.ст.) по сравнению с обычным (САД < 140 мм рт.ст.) не привело к достоверному снижению частоты первичной конечной точки (кардиоваскулярных событий), но отмечалось достоверное снижение частоты развития инсульта на 41 %. Поэтому в рекомендациях пока только указывается на необходимость стремиться к достижению уровня САД ближе к 130 мм рт.ст. Это удается редко на монотерапии иАПФ, поэтому часто необходима комбинация. Согласно рекомендациям Американского общества эндокринологов и Американского общества нефрологов, при диабетической нефропатии оптимальной является комбинация иАПФ и диуретика, возможно также комбинировать иАПФ с антагонистами кальция недигидропиридинового ряда [8, 23, 67].
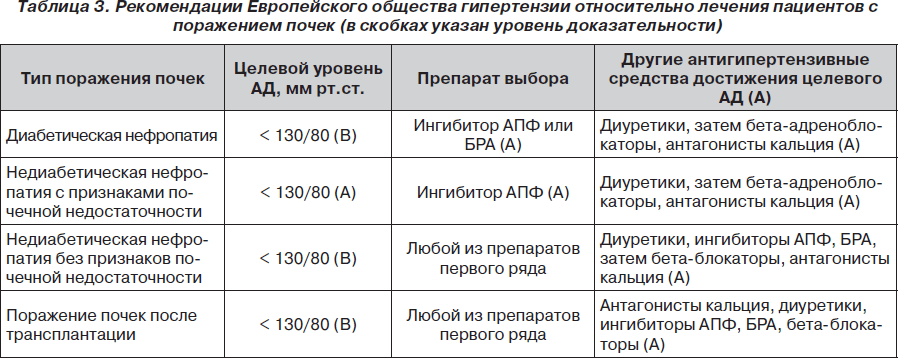
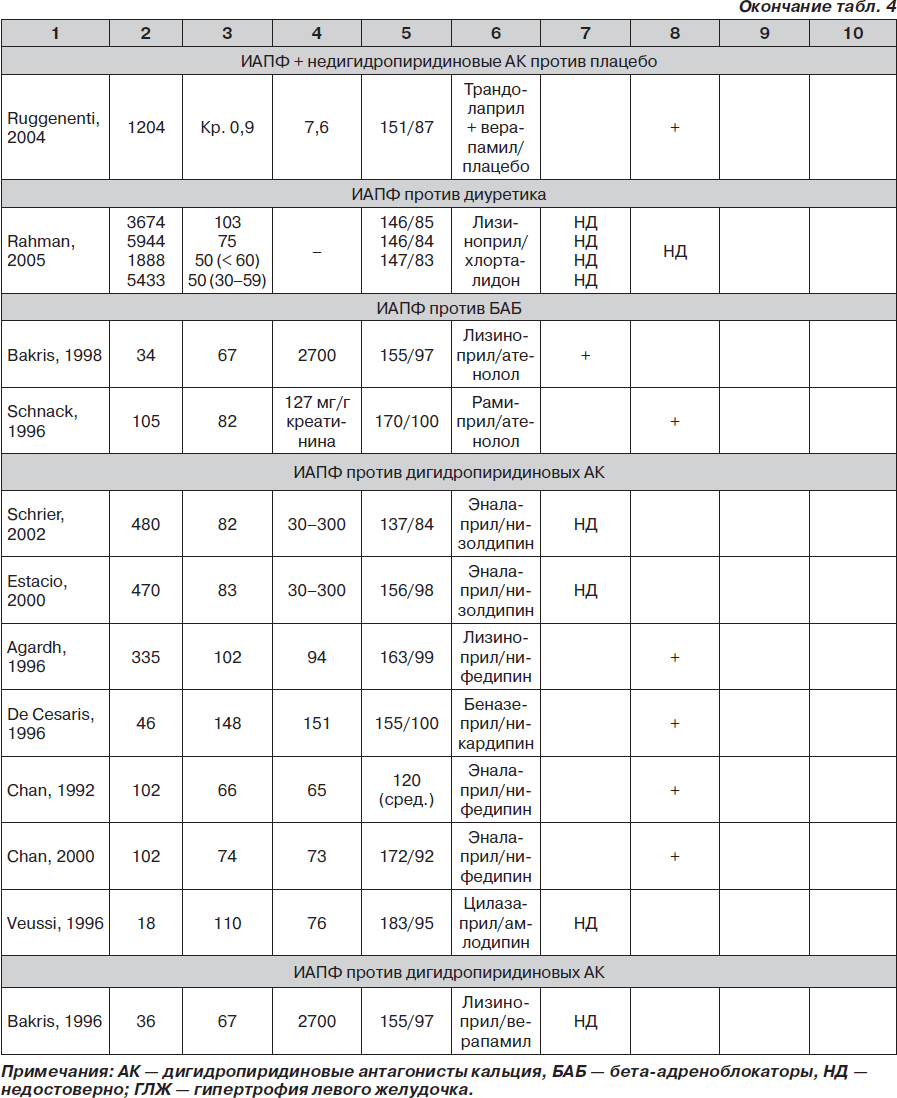
Нефропатия. ИАПФ в настоящее время с успехом применяются в нефрологической практике [13, 15, 50]. Нефропротективный эффект этой группы препаратов, связанный с устранением неиммунных механизмов прогрессирования почечной патологии, остается максимальным в сравнении с другими лекарственными средствами. Применение иАПФ показано как при первично-почечных заболеваниях (гломерулонефритах различного происхождения, первично сморщенной почке), так и при вторичных нефропатиях (особенно при диабетической нефропатии у больных сахарным диабетом), как при сниженной клубочковой фильтрации, так и при нормальной (табл. 3). Нефропротективный эффект иАПФ проявляется на всех стадиях поражения почек:
— на стадии микроальбуминурии (при диабетической нефропатии) возможно остановить прогрессирование патологического процесса в почках;
— на стадии протеинурии возможно стабилизировать фильтрационную функцию почек и затормозить развитие поражения;
— на стадии почечной недостаточности возможно существенно продлить период до проведения диализа или трансплантации почки.
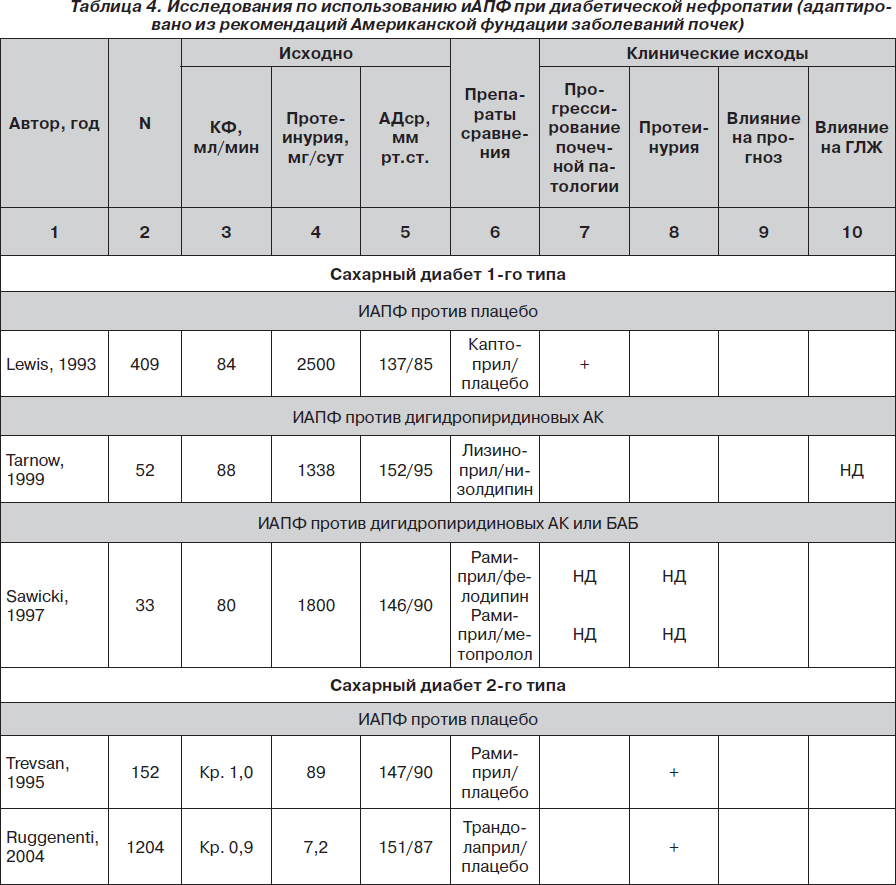
Начало клинического использования иАПФ при поражении почек было положено в 80-е годы XX ст. группами H.-H. Parvіng и S. Bjork, которые исследовали эффективность каптоприла у пациентов с инсулинозависимым сахарным диабетом в сравнении с плацебо и другими антигипертензивными препаратами. В других исследованиях было показано позитивное влияние эналаприла в сравнении с бета-адреноблокаторами и рамиприла у пациентов с сахарным диабетом 1-го типа на процесс снижения уровня гломерулярной фильтрации и развитие протеинурии. В дальнейшем стали появляться работы об эффективности иАПФ при сахарном диабете 2-го типа и нефропатии (табл. 4). Так, в подысследовании MІCRO-HOPE исследования HOPE применение рамиприла на протяжении 4,5 года приводило к достоверному снижению на 25 % частоты развития инфаркта миокарда, инсульта или сердечно-сосудистой смерти. Доказательства влияния на регресс протеинурии были получены для эналаприла, лизиноприла, трандолаприла, фозиноприла, периндоприла и др. У пациентов с систолической дисфункцией левого желудочка в исследовании SOLVD эналаприл предупреждал развитие выраженной протеинурии у больных сахарным диабетом. В исследовании BRILLIANT лизиноприл по сравнению с нифедипином продленного действия приводил к более выраженному уменьшению выделения белка с мочой. В исследовании CALM при почти одинаковом снижении АД лизиноприл в большей степени обеспечивал снижение уровня альбуминурии по сравнению с кандесартаном, а при их комбинации влияние на АД и регресс протеинурии усиливались. В исследовании DETAIL эналаприл не уступал телмисартану по положительному влиянию на функцию почек. В настоящее время в мире проводится исследование у пациентов с диабетической нефропатией VA Nephron-D, в котором сравнивается эффективность лозартана с комбинацией «лозартан + лизиноприл» [32].
При недиабетическом поражении изучение влияния иАПФ началось с исследования T. Hannedouche с соавторами, в котором у 100 пациентов с хронической почечной недостаточностью (уровень креатинина сыворотки 200–400 мкмоль/л) эналаприл в сравнении с бета-адреноблокаторами, несмотря на одинаковый уровень снижения АД, значительно замедлял развитие конечной стадии почечной недостаточности и смерти. Затем в исследовании REІN было продемонстрировано положительное влияние рамиприла на частоту развития конечной стадии почечной недостаточности при недиабетическом поражении почек. Рамиприл также был эффективен у афроамериканцев при гипертензивном нефросклерозе и почечной недостаточности в исследовании AASK [20, 23, 43, 62, 80, 89].
ИАПФ наряду с блокаторами рецепторов ангиотензина II являются средством выбора у пациентов с диабетической нефропатией, так как они предотвращают прогрессирование поражения почек у этой категории больных. При этом у пациентов с сахарным диабетом 1-го типа с АГ и нефропатией преимущество имеют иАПФ, а при 2-м типе — блокаторы рецепторов ангиотензина II. При нефропатиях недиабетической этиологии иАПФ обязательно должны назначаться пациентам со сниженной клубочковой фильтрацией (табл. 3). При отсутствии почечной недостаточности можно назначать любые антигипертензивные препараты.
При назначении иАПФ при нефропатиях следует придерживаться рекомендаций по дозировке (табл. 5). При этом современные рекомендации не отдают предпочтения никаким иАПФ.
Таким образом, в настоящее время нет определенных доказательств, что какой-то иАПФ превосходит другие по влиянию на почки. Есть препараты, более исследованные и менее исследованные, но практически для всех существуют доказательства или большей эффективности в предотвращении или регрессе протеинурии, или не меньшей эффективности, чем у препаратов сравнения.
Ишемическая болезнь сердца. У пациентов с острым инфарктом миокарда показаниями к назначению иАПФ являются передняя локализация инфаркта, обширное поражение, отсутствие реперфузии, систолическая дисфункция левого желудочка или клинические проявления СН, сахарный диабет [18, 35, 40, 45, 46, 49, 85, 89].
Существуют исследования, которые показали эффективность иАПФ при их назначении в первые сутки инфаркта миокарда и в более позднем периоде. При раннем (первые 24–36 часов) краткосрочном назначении отмечалось незначительное благоприятное влияние иАПФ на смертность у пациентов, которые включались в исследование неселективно. Так, в исследовании ISIS-4 58 050 пациентам с острым инфарктом миокарда давали или каптоприл, или плацебо [29, 42]. На протяжении 5 недель достоверно смертность была ниже в группе каптоприла — на 4,9 смерти меньше на 1000 пациентов. У пациентов с перенесенным ранее инфарктом или клиническими проявлениями СН эффективность каптоприла была выше — соответственно на 18 и 14 смертей меньше на 1000 пациентов. При иной, непередней локализации инфаркта не отмечено преимуществ каптоприла. В исследование GISSI-3 было включено 19 394 пациента, которые были рандомизированы получать лизиноприл или плацебо [31, 33–35, 55]. Смертность к 6-й неделе приема была ниже в группе лизиноприла. Разница сохранялась и на этапе 6 месяцев. В исследовании SMILE зофеноприл показал снижение смертности или возникновения тяжелой СН при передней локализации инфаркта миокарда [12]. Метаанализ Myocardial Infarction Collaborative Group подтвердил преимущества раннего назначения иАПФ при остром инфаркте в группах высокого риска (передняя локализация, СН, диабет и др.) [9]. При этом наибольшее количество жизней cпасают уже на протяжении первой недели назначения иАПФ [14].
Благоприятное воздействие иАПФ при назначении их в более поздние (3-и — 10-е cутки) сроки после инфаркта миокарда доказано для каптоприла (исследование SAVE) и трандолаприла (исследование TRACE) у пациентов с систолической дисфункцией левого желудочка и для рамиприла (исследование AIRE) у пациентов с клиническими проявлениями СН.
При стабильной ИБС и относительно низком сердечно-сосудистом риске благоприяное влияние на прогноз было продемонстрировано для периндоприла в исследовании EUROPА — достаточно пролечить 50 пациентов на протяжении 4,2 года для того, чтобы предупредить одно сердечно-сосудистое событие (кардиоваскулярная смертность, инфаркт миокарда или внезапная смерть) [26, 30]. При этом в данное исследование включались пациенты без дисфункции левого желудочка и клинических признаков СН (средний возраст 60 лет). АГ имели только 27 % пациентов, большинство из включенных были мужчинами — 85 %, сахарный диабет был лишь у 11 %. Инфаркт миокарда перенесли 64 %, ангиографически подтвержденную ИБС имел 61 % пациентов, реваскуляризирующие вмешательства перенесли 55 % и только лишь позитивный стресс-тест имели 5 %. В связи с тем что периндоприл был эффективен вне зависимости от наличия сахарного диабета или АГ, многие врачи всем своим пациентам с АГ стали активно назначать только периндоприл, мотивируя это тем, что ИБС — это распространенное заболевание в Украине (согласно статистике, 60 % больных с АГ в Украине имеют и ИБС). При этом забывают, что исследование EUROPА планировалось именно для больных с ИБС без СН, а не для пациентов с АГ и ИБС. Более того, из исследования EUROPА исходно исключались пациенты с уровнем АД более 180/100 мм рт.ст. Средний уровень АД в начале исследования составил 137/82 мм рт.ст. Поэтому трактовать его результаты с позиций антигипертензивной терапии у больных с АГ и ИБС не представляется возможным. Для больных с АГ (в том числе и с ИБС) улучшение прогноза связано прежде всего со снижением АД. При наличии же клинических признаков СН результаты исследования EUROPА вообще не применимы, так как такие пациенты исключались из исследования. Безусловно, СН не исключает возможность назначения периндоприла, который в некоторых исследованиях уменьшал ремоделирование левого желудочка [21]. Однако при этом нельзя a priorі отвергать другие иАПФ, которые доказали благоприятное влияние на прогноз при СН и рекомендованы руководствами.
Учитывать также следует то, что периндоприл в исследовании EUROPA достоверно снижал уровень АД: разница с группой плацебо составила 5/2 мм рт.ст. у всех пациентов, и она была больше в некоторых подгруппах, что не позволяет нам говорить о том, что эффективность периндоприла не зависела от его антигипертензивного эффекта.
Также нельзя забывать и о том, что ИБС должна быть верифицирована. Очень часто диагноз ИБС ставится исходя из возраста пациента, наличия любых болей в области сердца без проведения нагрузочных тестов или коронарографии. В США ИБС имеют 16 млн взрослого населения, а АГ — 65 млн. То есть соотношение АГ к ИБС составляет 4,06. В Украине же в 2009 году было зарегистрировано 11,9 млн больных АГ и 8,7 млн больных с ИБС, то есть соотношение составляет 1,4. Получается, что в Украине значительно больше распространенность ИБС, чем в США. Можно предполагать, что выявление АГ в Украине хуже, однако эпидемиологические исследования говорят, что 33 % украинцев страдают АГ, этот показатель практически не отличается от данных официальной статистики — 31 %. Можно также говорить о расовых различиях: в США велика доля афроамериканцев, которые меньше страдают ИБС и больше АГ. Однако маловероятно, что это даст уж очень большую разницу в распространенности ИБС. Или можно утверждать, что в Украине живут особенные люди, подверженные большому количеству факторов риска ИБС, что сомнительно. Однако можно также говорить, что диагностика ИБС в Украине оставляет желать лучшего. Поэтому мотивировка, что большее количество пациентов с АГ имеют ИБС и в связи с этим им нужно назначать периндоприл, не имеет права на существование.
Несколько отличается от исследования EUROPA исследование НОРЕ [69, 87, 88]. В него включались больные более высокого риска развития сердечно-сосудистых осложнений как с ИБС, так и без ИБС, но с сахарным диабетом или перенесенным инсультом или с заболеваниями периферических артерий в возрасте старше 55 лет, которым назначали или рамиприл, или плацебо. Это исследование было спланировано не для изучения антигипертензивного влияния рамиприла, а для оценки возможностей назначения антигипертензивного препарата у пациентов высокого риска. Было показано снижение частоты возникновения первичной конечной точки (инсульт + инфаркт миокарда + другая сердечно-сосудистая смертность) на 22 %, а при сахарном диабете — на 25 % по сравнению с плацебо. При этом в группе рамиприла отмечалось большее снижение АД — разница составляла от 4/2 до 2/1 мм рт.ст. на различных этапах исследования, что, безусловно, могло играть ведущую роль в уменьшении частоты развития осложнений [69]. В группе пациентов с сахарным диабетом разница по диастолическому АД составила 4 мм рт.ст., что обеспечило снижение частоты возникновения первичной конечной точки на 50 %. Основным выводом данного исследования было то, что дополнительное снижение АД на фоне назначения антигипертензивного препарата обеспечивает у пациентов высокого сердечно-сосудистого риска снижение частоты развития кардиоваскулярных осложнений. Выводы об «уникальности» рамиприла не имеют достаточного подтверждения при наличии разницы по уровню АД. В исследовании ONTARGET у такой же категории пациентов высокого риска телмисартан, который в исследовании TRANSCEND сравнивали с плацебо, по влиянию на конечные точки оказался не менее эффективным, чем рамиприл [87].
C другой стороны, если сравнивать данные об эффективности рамиприла у пациентов с СН, то среди 7105 пациентов, принявших участие в рандомизированных исследованиях по СН, в которых была показана эффективность иАПФ, только 17,2 % принимали рамиприл, а остальные — другие иАПФ [57]. Из 100 000 пациентов в остром периоде инфаркта миокарда, которым назначали иАПФ, рамиприл не получал ни один пациент. В исследовании НОРЕ СН была критерием исключения, а срок после перенесенного инфаркта миокарда составлял в среднем один год. Таким образом, на основании результатов исследования НОРЕ нельзя говорить об эффективности рамиприла у всех специфических категорий пациентов без исключения. Для этого нужны спланированные исследования. Конечно, для врачей удобно иметь «универсальный» препарат, который можно назначить пациенту с любой кардиальной патологией, но исследование НОРЕ не позволяет говорить, что рамиприл является таковым. Безусловно, рамиприл продемонстрировал эффективность у больных с СН в поздние сроки инфаркта миокарда (исследование AIRE), у пациентов с диабетической и недиабетической нефропатией (исследования REIN, ASSK). Однако нельзя отрицать эффективность и других иАПФ или блокаторов рецепторов ангиотензина II при тех же патологиях и возможность их назначения в первые сутки инфаркта миокарда (лизиноприл, каптоприл, валсартан, зофеноприл) в отличие от рамиприла. Один из исследователей в своей статье «Ramipril in Canada: HOPE or НУРЕ?» («Использование рамиприла в Канаде: надежда или назойливая реклама?») так прокомментировал данные о том, что в Канаде значительно выросло назначение рамиприла после публикации результатов исследования НОРЕ [82]: «…это больше пускание пыли в глаза, чем действительно результаты НОРЕ, увеличение числа назначений непропорционально данным, поддерживающим использование этого препарата, и в основном является результатом интенсивного маркетинга» [57].
Следует также отметить, что у пациентов с АГ (особенно высокого риска) назначение «старых» иАПФ приводило к снижению частоты развития коронарных событий, прежде всего инфаркта миокарда. Так, в исследовании АNВP-2 эналаприл по сравнению с диуретиком достоверно уменьшал вероятность развития первого инфаркта миокарда на 32 % (Р = 0,04). В исследование ALLHAT включались пациенты с АГ и одним из факторов риска развития ИБС. Оказалось, что лизиноприл был таким же эффективным в предупреждении первичной конечной точки (инфаркт миокарда или смертность от ИБС), как и амлодипин и хлорталидон [11].
В исследованиях SAVE и SOLVD назначение каптоприла и эналаприла пациентам с систолической дисфункцией левого желудочка приводило к достоверному и значительному снижению частоты возникновения инфаркта миокарда (рис. 6) и нестабильной стенокардии, что позволяет назначать эти иАПФ данной категории больных для профилактики коронарных событий. Иными словами, так называемые «старые» иАПФ также обладают способностью предупреждать возникновение коронарных событий у пациентов, уже имеющих ИБС (в исследование SAVE включались только больные после инфаркта миокарда, а в исследовании SOLVD большинство имели ИБС).
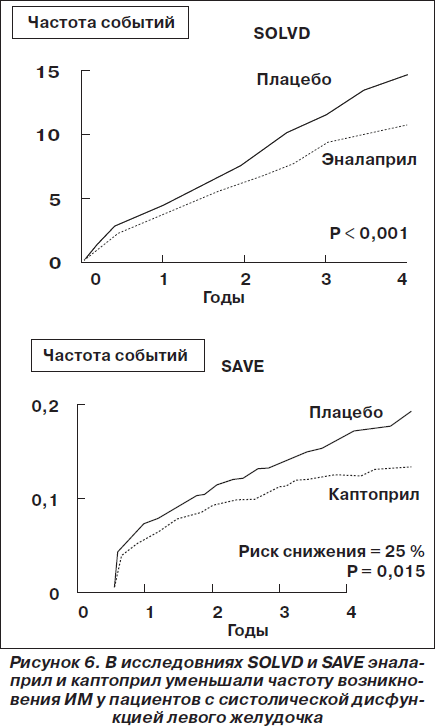
В исследованиях PEACE и QUITE изучали влияние трандолаприла и квинаприла на частоту развития сердечно-сосудистых событий у пациентов с ИБС без СН [80]. Оказалось, что в целом частота развития осложнений у данной категории пациентов очень низкая. Что объяснялось прежде всего включением менее тяжелой категории больных, чем в исследованиях НОРЕ и EUROPA, из-за того что их значительно лучше лечили: проводили полноценную антиангинальную, антигипертензивную, липидоснижающую, антитромбоцитарную терапию и реваскуляризирующие вмешательства (более 70 %). И добавление данных иАПФ не привело к дополнительному благоприятному воздействию. То есть если кроме ИБС у пациента нет другой патологии (сахарный диабет, артериальная гипертензия, СН, асимптомная дисфункция левого желудочка, постинфарктный кардиосклероз) и он получает достаточную терапию, которая в том числе позволяет контролировать АД, то нет необходимости назначать дополнительно иАПФ, согласно действующим рекомендациям. Необходимо сопоставлять риск развития побочных явлений, соотносить затраты/эффективность и использовать дозы и препараты с доказанной эффективностью при этих показаниях.
Существующие рекомендации не исключают назначения так называемых «старых» иАПФ, так как имеются доказательства их эффективности при остром инфаркте миокарда, постинфарктном кардиосклерозе с СН и для предупреждения и лечения диабетической нефропатии. Возможно также назначение пациентам высокого риска телмисартана, который был не хуже, чем рамиприл, в исследовании ОNTARGET, или валсартана после инфаркта миокарда [56]. Если это пациент с АГ, вероятно, что любые иАПФ, снижая АД, будут эффективны для предупреждения возникновения коронарных событий. Тем более что в posthoc анализе исследования САMELOT было показано, что у пациентов со стабильной стенокардией (60 % имели АГ, исходное АД 129/78 мм рт.ст.) и ангиографически подтвержденным коронарным атеросклерозом, не требующим реваскуляризации, которые были рандомизированы получать амлодипин, эналаприл или плацебо на протяжении 2 лет наряду с основной терапией (83 % получали статины, 75 % — бета-адренблокаторы, 95 % — аспирин), эналаприл так же, как и амлодипин, уменьшал вероятность возникновения комбинированной конечной точки (кардиоваскулярная смерть, или инсульт, или инфаркт миокарда) на 29 %. При этом существовала зависимость между прогрессированием атеросклеротической бляшки и снижением АД [52].
Заключение
Таким образом, исходя из вышесказанного, можно сделать вывод, что, несмотря на различия в химической структуре и фармакокинетике, большинство иАПФ одинаково эффективны при различной кардиоваскулярной и сопряженной с ней патологией. Есть препараты, менее изученные в больших исследованиях (например, спираприл) и более изученные. Среди последних так называемые «старые» иАПФ занимают как раз не последнее место. Они в такой же степени снижают АД при сопоставлении в эквивалентных дозах, могут назначаться один раз в сутки (лизиноприл, комбинация «эналаприл + диуретик»), имеют клиническую доказательную базу эффективности у пациентов с АГ, сахарным диабетом, СН или систолической дисфункцией левого желудочка любой этиологии, нефропатиями. Они способны предупреждать развитие коронарных событий у пациентов с АГ, СН или систолической дисфункцией левого желудочка. Они улучшают прогноз при назначении в первые сутки инфаркта миокарда у пациентов высокого риска, чего нельзя сказать о некоторых «новых» иАПФ. Поэтому отказываться от их применения в настоящее время нет никакого смысла. Тем более это касается Украины — страны, в которой существуют немалые экономические трудности, когда пациент сам вынужден приобретать себе лекарства. А именно «старые» иАПФ выпускаются в виде генериков в значительном количестве и имеют соответственно более низкую стоимость. Даже в высокоразвитых странах, например в США, в топ-тройку среди всех назначаемых препаратов, наряду с симвастатином и L-тироксином, входит лизиноприл — 81,3 млн выписанных рецептов по итогам 2009 года [19]. Во многом это благодаря наличию дешевых генерических препаратов лизиноприла и специальных программ по закупке генериков по низким ценам. Иными словами, старая русская пословица «Старый конь борозды не портит» вполне справедлива в данном случае.
1. Бобров В.А., Давыдова И.В., Медведенко О.И. Актуальные вопросы лекарственных взаимодействий в клинической практике. Как выбрать оптимальный ингибитор АПФ для больного, принимающего НПВС? // Укр. мед. часопис. — 2010. — № 1. — С. 43-48
2. Корзун А.И., Кириллова М.В. Сравнительная характеристика ингибиторов АПФ. — Санкт-Петербург: ВМедА, 2003. — 24 с.
3. Майчук Е.Ю., Воеводина И.В. Современные представления об использовании ингибиторов ангиотензинпревращающего фермента для лечения артериальной гипертензии // Русский медицинский журнал. — 2005. — Т. 13(19). — С. 1287-1293.
4. Преображенский Д.В., Сидоренко Б.А. Применение ингибиторов ангиотензинпревращающего фермента при лечении острого инфаркта миокарда // Кардиология. — 1997. — № 3. — С. 100-104.
5. Преображенский Д.В., Сидоренко Б.А., Романова Н.Е., Шатунова И.М. Клиническая фармакология основных классов антигипертензивных препаратов // Consilium Medicum. — 2000. — 2(3); http://old.consilium-medicum.com/media/consilium/n03/099.shtml
6. Радченко Г.Д., Сіренко Ю.М. Досвід застосування лізиноприлу (Вітоприл) у пацієнтів з м’якою та помірною артеріальною гіпертензією // Укр. мед. часопис. — 2009. — № 2. — С. 31-36.
7. Сіренко Ю. Клінічні аспекти застосування лізиноприлу // Ліки України. — 2000. — № 9. — С. 51-54.
8. AACE Diabetes Mellitus Clinical Practice Guidelines Task Force. American Association of Clincal Endocrinologistsmedical Guidelines for Clinical Practice for the Management of Diabetes Mellitus // Endocr. Pract. — 2007. — Vol. 13, Suppl. 1. — P. 1-68.
9. ACE Inhibitor Myocardial Infarction Collaborative Group. Indications for ACE inhibitors in the early treatment of acute myocardial infarction: systematic overview of individual data from 100 000 patients in randomized trials // Circulation. — 1998. — 97. — 2202-1.
10. Alimento M., Campodonico J., Santambrogio G. еt al. The antagonistic effect of aspirin on the expression of prostaglandin participation in the antihypertensive activity of ACE inhibitors // Cardiologia. — 1997. — Vol. 42. — P. 605-610.
11. ALLHAT Officers and Coordinators for the ALLHAT Collaborative Research Group Major outcomes in high-risk hypertensive patients randomized to angiotensin-converting enzyme inhibitor or calcium channel blocker vs diuretic: The Antihypertensive and Lipid-Lowering Treatment to Prevent Heart Attack Trial (ALLHAT) // JAMA. — 2002. — Vol. 288. — P. 2981-2997.
12. Ambrosioni E., Borghi C., Magnani B. The effect of the angiotensin-converting-enzyme inhibitor zofenopril on mortality and morbidity after anterior myocardial infarction. The Survival of Myocardial Infarction Long-Term Evaluation (SMILE) Study Investigators // N. Engl. J. Med. — 1995. — Vol. 332. — P. 80-85.
13. Balazsi I., Takacs J. The effect of lisinopril in hypertensive patients with diabetic nephropathy // Diabetologia Hungarica. — 1999. — Vol. 7. — P. 101-106.
14. Ball S., Hall A., Murray G. Angiotensin-converting enzyme inhibitors after myocardial infarction: indications and timing // J. Am. Coll. Cardiol. — 1995. — Vol. 25. — S42-S46.
15. Casas J.P., Chua W., Loukogeorgakis S. et al. Effect of inhibitors of the renin-angiotensin system and other antihypertensive drugs on renal outcomes: Systematic review and meta-analysis // Lancet. — 2005. — Vol. 366. — P. 2026-2033.
16. Cashin-Hemphill L., Holmvang G., Chan R. et al. Angiotensin converting enzyme inhibition as antiatherosclerotic therapy: no answer yet // Am. J. Cardiol. — 1999. — Vol. 83. — P. 43-47.
17. Chaturvedi N., Sjolie A.K., Stephenson J.M. et al. Effect of lisinopril on progression of retinopathy in normotensive people with type 1 diabetes. The EUCLID Study Group. EURODIAB Controlled Trial of Lisinopril in Insulin-Dependent Diabetes Mellitus // Lancet. — 1998. — Vol. 351. — P. 28-31.
18. Chinese Cardiac Study (CCS-1) Collaborative Group. Oral captopril versus placebo among 14,962 patients with suspected acute MI: a multicenter, randomized, double-blind, placebo-controlled clinical trial // Chin. Med. J. — 1997. — Vol. 110. — P. 834-838.
19. Choudhry N., Shrank W. Four-Dollar Generics — Increased Accessibility, Impaired Quality Assurance // New Engl. J. Med. — 2010. — Vol. 363. — P. 1885-1887.
20. Chua D.Y., Bakris G.L. Diabetes and chronic kidney disease: tragedy and challenge // Blood Purif. — 2004. — Vol. 22. — P. 130-135.
21. Cleland J.G., Tendera M., Adamus J. et al. The perindopril in elderly people with chronic heart failure (PEP-CHF) study // Eur. Heart J. — 2006. — Vol. 27(19). — P. 2338-2345.
22. Cleland J.G. ACE inhibitors for ‘diastolic’ heart failure? reasons not to jump to premature conclusions about the efficacy of ACE inhibitors among older patients with heart failure // Eur. J. Heart Fail. — 2001. — Vol. 3. — P. 637-639.
23. Clinical Practice Guildelines and Clinical Practice Recommendations for diabetes and chronic kidney disease // Am. J. Kidney Disease. — 2007. — Vol. 49, Suppl. — P. 1-180.
24. Cohn J.N., Johnson G., Ziesche S. et al. A comparison of enalapril with hydralazine-isosorbide dinitrate in the treatment of chronic congestive heart failure // N. Engl. J. Med. — 1991. — Vol. 325. — P. 303-310.
25. Collaborative Group Randomised trial of a perindopril-based bloodpressure-lowering regimen among 6105 individuals with previous stroke or transient ischaemic attack // Lancet. — 2001. — Vol. 358. — P. 1033-1041.
26. Daly C., Fox K., Remme W. еt al. The effect of perindopril on cardiovascular morbidity and mortality in patients with diabetes in the EUROPA study: results from the PERSUADE substudy // Eur. Heart J. — 2005. — Vol. 26. — P. 1369-1378.
27. Dahloеf B., Devereux R.B., Kjeldsen S.E., Julius S., Beevers G., de Faire U. et al. Cardiovascular morbidity and mortality in the Losartan Intervention for Endpoint reduction in hypertension study (LIFE): a randomized trial against atenolol // Lancet. — 2002. — Vol. 359. — P. 995-1003.
28. Flather M., Yusuf S., Kшber L., Pfeffer M., Hall A., Murria G. et al. for the ACE-Inhibitor Myocardial Infarction Collaborative Group. Long-term ACE-inhibitor therapy in patients with heart failure or left-ventricular dysfunction: a systematic overview of data from individual patients // Lancet. — 2000. — Vol. 355. — P. 1575-1581.
29. Fourth International Study of Infarct Survival Collaborative Group. ISIS-IV: a randomised factorial trial assessing early oral captopril. Oral mononitrate and intravenous magnesium sulphate in 58050 patients with suspected acute myocardial infarction // Lancet. — 1995. — Vol. 345. — P. 669-685.
30. Fox K.M. EURopean trial On reduction of cardiac events with Perindopril in stable coronary Artery disease Investigators. Efficacy of perindopril in reduction of cardiovascular events among patients with stable coronary artery disease: randomised, double-blind, placebo-controlled, multicentre trial (the EUROPA study) // Lancet. — 2003. — Vol. 362. — P. 782-788.
31. Franzosi M.G., Maggioni A.P., Santoro E. еt al. Cost-effectiveness analysis of early lisinopril use in patients with acute myocardial infarction. Results from GISSI-3 trial // Pharmacoeconomics. — 1998. — Vol. 13(3). — P. 337-346.
32. Fried L., Duckworth W., Zhang J. et al. for VA NEPHRON-D Investigators. Design of Combination Angiotensin Receptor Blocker and Angiotensin-Converting Enzyme Inhibitor for Treatment of Diabetic Nephropathy (VA NEPHRON-D) // Clin. J. Am. Soc. Nephrol. — 2009. — Vol. 4. — P. 361-368.
33. GISSI-3 Investigators GISSI-3: effects of lisinopril and transdermal glyceryl trinitrate singly and together on 6-week mortality and ventricular function after acute myocardial infarction. Gruppo Italiano per lo Studio della Sopravvivenza nell’infarto Miocardico // Lancet. — 1994. — Vol. 343. — P. 1115-1122.
34. Goa K.L., Balfour J.A., Zuanetti G. Lisinopril. A review of its pharmacology and clinical efficacy in the early management of acute myocardial infarction // Drugs. — 1996. — Vol. 52(4). — P. 564-588.
35. Gottlieb S., Leor J., Shotan A., Harpaz D., Boyko V., Rott D. et al. Comparison of effectiveness of angiotensin-converting enzyme inhibitors after acute myocardial infarction in diabetic versus nondiabetic patients // Am. J. Cardiol. — 2003. — Vol. 92. — P. 1020-1025.
36. Gundersen T., Swedberg K., Amtorp O. et al. Absence of effect on exercise capacity of 12-weeks treatment with ramipril in patients with moderate congestive heart failure. Ramipril Study Group // Eur. Heart J. — 1994. — Vol. 15. — P. 1659-1665.
37. Gustafsson I., Kober L., Gustafsson F. Effect of the angiotensin-converting enzyme inhibitor trandopril on mortality and morbidity in diabetis patients with left ventricular dysfunction after acute myocardial infarction. Trace Study Group // J. Am. Coll. Cardiol. — 1999. — Vol. 34. — P. 83-89.
38. Hansson L., Lindholm L., Niskanen L. et al. Effect of angiotensin converting enzyme inhibition compared with conventional therapy on cardiovascular morbidity and mortality in hypertension: the Captopril Prevention Project (CAPPP) randomised trial // Lancet. — 1999. — Vol. 353. — P. 611-616.
39. Hansson L., Lindholm L.H., Ekbom T. еt al. Randomised trial of old and new antihypertensive drugs in elderly patients: cardiovascular mortality and morbidity the Swedish Trial in Old Patients with Hypertension-2 study // Lancet. — 1999. — Vol. 354. — P. 1751-1756.
40. Heran B.S., Wong M.M., Heran I.K., Wright J.M. Blood pressure lowering efficacy of angiotensin converting enzyme (ACE) inhibitors for primary hypertension // The Cochrane Collaboration. Cochrane database of Systematic Reviews. — 2008. — Issue 4. Art.No.:CD003823.DOI:10.1002/14651858.CD003823.pub2.
41. Hirata K., Vlachopoulos C., Adji A., O’Rourke M.F. Benefits from angiotensin-converting enzyme inhibitor «beyond blood pressure lowering»: beyond blood pressure or beyond the brachial artery? [published correction appears in J Hypertens. — 2005. — 23. — 903-904] // J. Hypertens. — 2005. — Vol. 23. — P. 551-556.
42. ISIS-4 (Fourth International Study of Infarct Survival) Collaborative Group ISIS-4: a randomised factorial trial assessing early oral captopril, oral mononitrate, and intravenous magnesium sulphate in 58,050 patients with suspected acute myocardial infarction // Lancet. — 1995. — Vol. 345. — P. 669-685.
43. Jacobsen P., Andersen S., Jensen B.R., Parving H.H. Additive effect of ACE inhibition and angiotensin II receptor blockade in type I diabetic patients with diabetic nephropathy // J. Am. Soc. Nephro. — 2003. — Vol. l14. — P. 992-999.
44. Jong P., Yusuf S., Rousseau M.F. et al. Effect of nealapril on 12 year survival and life expectancy in patients with left ventricular systolic dysfunction: a follow-up study // Lancet. — 2003. — Vol. 361. — P. 1843-1848.
45. Kйber L., Torp-Pedersen C. Clinical characteristics and mortality of patients screened for entry into the Trandolapril Cardiac Evaluation (TRACE) study // Am. J. Cardiol. — 1995. — Vol. 76(1). — P. 1-5.
46. Kingma J.H., van Gilst W.H., Peels C.H. et al. Acute intervention with captopril during thrombolysis in patients with first anterior myocardial infarction. Results from the Captopril and Thrombolysis Study (CATS) // Eur. Heart J. — 1994. — Vol. 15(7). — P. 898-907.
47. Kyriakidis M., Triposkiadis F., Dernellis J. et al. Effects of cardiac versus circulatory angiotensin-converting enzyme inhibition on left ventricular diastolic function and coronary blood flow in hypertrophic obstructive cardiomyopathy // Circulation. — 1998. — Vol. 97. — P. 1342-1347.
48. Kober L., Torp-Pedersen C., Carlsen J.E. et al. for the trandolapril cardiac evaluation (TRACE) study group: a clinical trial of the angiotensin converting enzyme inhibitor trandolapril in patients with left ventricular dysfunction after myocardial infarction // N. Engl. J. Med. — 1995. — Vol. 33. — P. 1670-1676.
49. Latini R., Maggioni A.P., Flather M. et al. ACE inhibitor use in patients with myocardial infarction. Summary of evidence from clinical trials // Circulation. — 1995. — Vol. 92(10). — P. 3132-3137.
50. Mogensen C.E., Neldam S., Tikkanen I. et al. Randomised controlled trial of dual blockade of renin-angiotensin system in patients with hypertension, microalbuminuria, and non-insulin dependent diabetes: The Candesartan And LisinOpril Microalbuminuria (CALM) Study // BMJ. — 2000. — Vol. 321. — P. 1440-1444.
51. Narang R., Swedberg K., Cleland J.G. What is the ideal study design for evaluation of treatment for heart failure? Insights from trials assessing the effect of ACE inhibitors on exercise capacity // Eur. Heart J. — 1996. — Vol. 17. — P. 120-134.
52. Nissen S., Tuzcu E., Libby P. et al. Effect of antihypertensive agents on cardiovascular events in patients with coronary disease and normal blood pressure: the CAMELOT study: a randomized controlled trail // JAMA. — 2004. — Vol. 292. — P. 2217-2225.
53. Northridge D.B., Rose E., Raftery E.D. et al. A multicentre, double-blind, placebo-controlled trial of quinapril in mild, chronic heart failure // Eur. Heart J. — 1993. — Vol. 14. — P. 403-409.
54. Packer M., Poole-Wilson P.A., Armstrong P.W. et al., on behalf of the ATLAS study group. Comparative effects of low and high doses of the angiotensin-converting enzyme inhibitor, lisinopril, on morbidity and mortality in chronic heart failure // Circulation. — 1999. — Vol. 100. — P. 2312-2318.
55. Pedrazzini G., Santoro E., Latini R. et al. GISSI-3 Investigators Causes of death in patients with acute myocardial infarction treated with angiotensin-converting enzyme inhibitors: findings from the Gruppo Italiano per lo Studio della Sopravvivenza nell’Infarto (GISSI)-3 trial // Am. Heart J. — 2008. — Vol. 155(2). — P. 388-394.
56. Pfeffer M.A., McMurray J.J.V., Velasquez E.J. et al. for the Valsartan in Acute Myocardial Infarction Trial Investigators Valsartan, Captopril, or Both in Myocardial Infarction Complicated by Heart Failure, Left Ventricular Dysfunction, or Both // N. Engl. J. Med. — 2003. — Vol. 349. — P. 1893-1906.
57. Pilote L. Ramipril use in Canada: HOPE or HYPE? // JAMC. — 2003. — Vol. 168. — P. 568-569.
58. Poulter N., Wedel H., Dahlof B. et al. Role of blood pressure and other variables in the differential cardiovascular event rates noted in the Anglo-Scandinavian Cardiac Outcomes Trail-Blood Pressure Lowering Arm // Lancet. — 2005. — Vol. 366. — P. 907-913.
59. PROGRESS Collaborative Group Randomised trial of a perindopril-based blood-pressure-lowering regimen among 6105 individuals with previous stroke or transient ischaemic attack // The Lancet. — 2001. — Vol. 358. — P. 1033-1041.
60. Reisin E., Weir M.R., Falkner B. Et al. Lisinopril versus hydrochlorothiazide in obese hypertensive patients: a multicenter placebo-controlled trial. Treatment in Obese Patients With Hypertension (TROPHY) Study Group // Hypertension. — 1997. — Vol. 30(1 Pt 1). — P. 140-145.
61. Report of the American College of Cardiology/American Heart Association Task Force on Practice Guidelines (Committee on Management of Acute Myocardial Infarction) ACC/AHA Guidelines for the Management of Patients With Acute Myocardial Infarction American College of Cardiology; September 1999. Available from: www.acc.org
62. Ruggenenti P., Fassi A., Ilieva A.P. et al. Preventing microalbuminuria in type 2 diabetes // N. Engl. J. Med. — 2004. — Vol. 351. — P. 1941-1951.
63. Rutherford J.D., Pfeffer M.A., Moyй L.A. et al. SAVE Investigators. Effects of captopril on ischemic events after myocardial infarction. Results of the Survival and Ventricular Enlargement trial // Circulation. — 1994. — Vol. 90(4). — P. 1731-1738.
64. Rydйn L., Armstrong P.W., Cleland J.G. et al. Efficacy and safety of high-dose lisinopril in chronic heart failure patients at high cardiovascular risk, including those with diabetes mellitus. Results from the ATLAS trial // Eur. Heart J. — 2000. — Vol. 21. — P. 1967-1978.
65. Shekelle P.G., Rich M.W., Morton S.C. et al. Efficacy of angiotensinconverting enzyme inhibitors and beta-blockers in the management of left ventricular systolic dysfunction according to race, gender, and diabetic status. A meta-analysis of major clinical trials // J. Am. Coll. Cardiol. — 2003. — Vol. 41. — P. 1529-1538.
66. Staessen J.A., Birkenhager W.H. Evidence that new antihypertensives are superior to older drugs // Lancet. — 2005. — Vol. 366. — P. 869-871.
67. Standards of Medical Care in Diabetes–2006. American Diabetes Association // Diabetes Care. — 2006. — Vol. 29, Suppl. 1. — P. S4-42.
68. Study Investigators. Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure. The Acute Infarction Ramipril Efficacy // Lancet. — 1993. — Vol. 342. — P. 821-828.
69. Svensson P., de Faire U., Sleight P. Comparative effects of ramipril on ambulatory and office blood pressure: a HOPE substudy // Hypertension. — 2001. — Vol. 38. — P. 28-32.
70. Swedberg K., Held P., Kjekshus J. et al. Effects of the early administration of enalapril on mortality in patients with acute myocardial infarction. Results of the Cooperative New Scandinavian Enalapril Survival Study II (CONSENSUS II) // N. Engl. J. Med. — 1992. — Vol. 327(10). — P. 678-684.
71. Takai S., Yamamoto D., Jin D. еt al. Inhibition of matrix metalloproteinase-9 activity by lisinopril after myocardial infarction in hamsters // Eur. J. Pharmacol. — 2007. — Vol. 568(1–3). — P. 231-233.
72. Task Force Members. The Task Force for the Diagnosis and Treatment of Acute and Chronic Heart Failure 2008 of the European Society of Cardiology. Developed in collaboration with the Heart Failure Association of the ESC (HFA) and endorsed by the European Society of Intensive Care Medicine (ESICM) // European Heart Journal. — 2008. — Vol. 29. — P. 2388-2442.
73. The Acute Infarction Ramipril Efficacy (AIRE) Study Investigators Effect of ramipril on mortality and morbidity of survivors of acute myocardial infarction with clinical evidence of heart failure // Lancet. — 1993. — Vol. 342. — P. 821-828.
74. The CAFЙ Investigators, for the Anglo-Scandinavian Cardiac Outcomes Trail (ASCOT) Investigators, CAFЙ Steering Committee and Writing Committee. Differential Impact of Blood Pressure-Lowering Drugs on Cantral aortic Pressure and Clinical Outcomes: Principal Results of the Conduit Artery Function Evaluation (CAFЙ) Study // Circulation. — 2006. — Vol. 113. — P. 1213-1225.
75. The Consensus Trial Study Group. Effects of enalapril on mortality in severe congestive heart failure // N. Engl. J. Med. — 1987. — Vol. 316. — P. 1429-1435.
76. The EUCLID Study Group Randomised placebo-controlled trial of lisinopril in normotensive patients with insulin-dependent diabetes and normoalbuminuria or microalbuminuria // Lancet. — 1997. — Vol. 349. — P. 1787-1792.
77. The NETWORK investigators. Clinical outcome with enalapril in symptomatic chronic heart failure, a dose comparison // Eur. Heart J. — 1998. — Vol. 19. — P. 481-489.
78. The SOLVD Investigators Effect of enalapril on survival in patients with reduced left ventricular ejection fractions and congestive heart failure // N. Engl. J. Med. — 1991. — Vol. 325. — P. 293-302.
79. The SOLVD Investigators. Effect of enalapril on mortality and development of heart failure in asymptomatic patients with reduced left ventricular ejection fractions // N. Engl. J. Med. — 1992. — Vol. 327. — P. 685-691.
80. The Task Force on ACE-inhibitors of the European Society of Cardiology. Expert consensus document on angiotensin converting enzyme inhibitors in cardiovascular disease // European Heart Journal. — 2004. — Vol. 25. — P. 1454-1470.
81. The Task force on the Management of Stable Angina Pectoris of the European Society of Cardiology. Guildelines on the management of stable angina pectoris // European Heart Journal. doi:10.1093/eurheartj/ehj001.
82. Tu K., Mamdani M.M., Jacka R.M., Forde N.J., Rothwell D.M., Tu J.V. The striking effect of the Heart Outcomes prevention Evaluation (HOPE) on ramipril prescribing in Ontario // CMAJ. — 2003. — Vol. 168. — P. 553-557.
83. UK Prospective Diabetes Study Group. Efficacy of atenolol and captopril in reducing risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 39 // Br. Med. J. — 1998. — Vol. 317. — P. 713-720.
84. UK Prospective Diabetes Study Group. Tight blood pressure control and risk of macrovascular and microvascular complications in type 2 diabetes: UKPDS 38 // Br. Med. J. — 1998. — Vol. 317. — P. 703-713.
85. Van de Werf et al. for the task force of the management of acute myocardial infarction of the European Society of Cardiology. Management of acute myocardial infarction in patients presenting with ST segment elevation // Eur. Heart J. — 2003. — Vol. 24. — P. 28-66.
86. Vermes E., Ducharme A., Bourassa M.G. et al. Enalapril reduces the incidence of diabetes in patients with chronic heart failure. Insight from the studies of left ventricular dysfunction (SOLVD) // Circulation. — 2003. — Vol. 107. — P. 1291-1296.
87. Yusuf S. From the HOPE to the ONTARGET and the TRANSCEND studies: challenges in improving prognosis // Am. J. Cardiol. — 2002. — Vol. 89. — P. 18A-25A.
88. Yusuf S., Sleight P., Pogue J. et al. Effects of an angiotensin-converting-enzyme inhibitor, ramipril on cardiovascular events in high-risk patients. The Heart Outcomes Prevention Evaluation Study Investigators // New Engl. J. Med. — 2000. — Vol. 342. — P. 145-153.
89. Zuanetti G., Latini R., Maggioni A.P. et al. Effect of the ACE inhibitor lisinopril on mortality in diabetic patients with acute myocardial infarction: data from the GISSI-3 study // Circulation. — 1997. — Vol. 96. — P. 4239-4245.