Журнал «Здоровье ребенка» 3 (30) 2011
Вернуться к номеру
Проблема антимикробной резистентности в терапии острых респираторных заболеваний у детей
Авторы: Шостакович-Корецкая Л.Р. Днепропетровская государственная медицинская академия
Рубрики: Педиатрия/Неонатология
Версия для печати
В последнее время врачам все чаще приходится сталкиваться с лекарственно-устойчивыми возбудителями негоспитальных респираторных инфекций. По данным литературы, основной причиной этого является необоснованная и нерациональная антибиотикотерапия. Для решения проблемы лечения больных с острыми респираторными заболеваниями, вызванными резистентными к стандартной терапии штаммами микроорганизмов, разработана новая форма амоксициллина/клавуланата — Аугментин™ ES. Эффективность и обоснованность применения препарата показана на конкретном клиническом случае из практики педиатра.
Резистентность, антибиотикотерапия, Аугментин™ ES.
На протяжении 2 последних десятилетий значительно увеличилась антимикробная (АМ) резистентность среди многих возбудителей негоспитальной респираторной инфекции. В детской популяции эти инфекции включают острый средний отит (ОСО), острый синусит, фарингит и пневмонию. Многие бактериальные респираторные патогены в разной степени резистентны почти ко всем классам антибиотиков (АБ). C течением времени антибиотики постепенно теряют свой терапевтический потенциал, что является серьезной угрозой для детской популяции и всего населения [1]
Драматическая статистика резистентности
В публикации CDC в «Журнале Американской медицинской ассоциации» (17 октября 2007) представлены дынные о том, что от заболеваний, вызванных MRSA (метициллин-резистентным St.aureus), ежегодно страдает более 94 тыс. людей и умирает около 19 тыс., что значительно больше, чем количество смертей, вызванных эмфиземой легких, ВИЧ/СПИДом, болезнью Паркинсона и др. Тревожат данные американского исследования о том, что у детей носительство MRSA в носоглотке выросло с 0,8 % в 2001 году до 9,2 % в 2004 году [2].
Рост резистентности в мире имеет несколько причин. Использование антибиотиков в кормах сельскохозяйственных животных признано одним из факторов распространения резистентных штаммов (рис. 1). Резистентный энтерококк был обнаружен, например, у 90 % свиней, у 94 % кур. При этом не всегда фактором риска является употребление в пищу мяса животных, в ряде случаев бактерии могут переноситься от животных к людям насекомыми [3].

В некоторых странах лекарственная устойчивость респираторных патогенов приобрела значительные масштабы. В опубликованном в конце 2010 года отчете о резистентности патогенов в странах Европы (Antimicrobial resistance surveillance in Europe, 2009) указано, что в пяти странах континента до 50 % штаммов S.pneumoniae не чувствительны к пенициллину и макролидам [4].
Ситуация в России несколько лучше, однако и она постепенно ухудшается: пневмококк в основном сохраняет чувствительность к пенициллину (90–95 %) и амоксициллину (99–100 %), что позволяет шире использовать эти препараты. Но за период с 1999 по 2005 год процент штаммов со сниженной чувствительностью увеличился с 11,5 до 18,2 % в Южном округе, с 8,6 до 10 % — в Центральном, с 7,1 до 22,3 % — в Уральском, с 4,5 до 14 % — в Москве. Много устойчивых штаммов циркулирует в детских дошкольных учреждениях, особенно в детских домах. Около 1/3 устойчивых к пенициллину штаммов имеют сниженную чувствительность к макролидам, 4–8 % — к цефтриаксону и цефотаксиму, до половины штаммов — к ампициллину [5].
Всегда ли антибиотики назначаются по показаниям?
Ученые находят прямую зависимость между ростом устойчивости бактерий к антибиотикам и нерациональной антибактериальной терапией. Одним из самых частых показаний к назначению антимикробных средств являются острые респираторные вирусные инфекции (ОРВИ). Общеизвестно, что ОРВИ в детском возрасте протекают преимущественно в виде ринита, катаральных форм назофарингита, ларингита, бронхита или трахеита, обусловленных вирусами, при которых антибиотикотерапия не показана. Но в реальной жизни антибиотики при этих заболеваниях применяются, часто необоснованно, несмотря на полученные в клинических исследованиях доказательства отсутствия эффекта антибиотиков в отношении как продолжительности ОРВИ и выраженности симптоматики, так и профилактики бактериальных осложнений. По данным ученых НИИ педиатрии РАМН, при острых респираторных вирусных инфекциях у детей лечение антибиотиками требуется всего в 6–8 % случаев. А на практике антибиотики детям при ОРВИ назначаются в 48 % случаев [6].
В исследовании A.C. Nyquist и соавт. проведен анализ частоты назначений антибиотиков у 531 ребенка при таких заболеваниях, как назофарингит, острая респираторная инфекция, острый бронхит и бронхиолит. Антибиотики назначались чаще всего педиатрами (62 %) и семейными врачами (20 %), реже — врачами общей практики (11 %), терапевтами (3 %) и другими специалистами. Антибиотики были назначены в 44 % случаев заболеваний, трактовавшихся как простудные, в 46 % случаев острых респираторных инфекций, в 72 % случаев острого бронхита (не всегда подтвержденного) [7].
На основании данных Национальных обзоров амбулаторной (NAMCS) и госпитальной помощи (NHAMCS) в США за 1995–2003 гг. отмечается, что, хотя количество детей, получавших АБ в течение 1995–2003 гг., имеет тенденцию к сокращению, врачи предпочитают необоснованное назначение АБ широкого спектра, что приводит к росту АБ-резистентных штаммов, повышает риск развития побочных эффектов у пациентов, а также увеличивает стоимость лечения [8].
В последние десятилетия, по данным ВОЗ (2009), ведущими бактериальными возбудителями респираторных инфекций у детей являются:
— Streptococcus pneumoniae (50 %);
— Haemophilus influenzae (20–30 %);
— Moraxella catarrhalis (10–30 %).
Реже встречаются Staphylococcus aureus и другие бактерии, Klebsiella pneumoniae, нетипируемая Haemophilus influenzae и другие микроорганизмы (Mycoplasma pneumoniae, Chlamydophila pneumoniae, Pseudomonas aeruginosa, Escherichia coli).
Резистентность пневмококка
Поскольку пневмококк является основным возбудителем внебольничных респираторных заболеваний у детей, большой интерес представляет вопрос о темпах развития резистентности пневмококка к антибактериальным препаратам и возможности влиять на эти процессы.
Первое описание устойчивых к пенициллину пневмококков было сделано профессором Х. Корнхофом (Южная Африка) в 1978 году. За 25 лет резистентные штаммы получили широкое распространение, и почти нет места на земле, где можно было бы игнорировать проблему резистентности в лечении пневмококковой инфекции у детей и взрослых. У детей резистентность пневмококка к бета-лактамам и макролидам встречается чаще, чем у взрослых, что отражает сравнительно более продолжительное его носительство в детском возрасте и более частое назначение детям антибиотиков. Исключение составляют только фторхинолоны, которые назначаются детям крайне редко, по жизненным показаниям [9].
На основании серологических реакций с различными капсульными полисахаридными антигенами пневмококки классифицируются в 21 группу, которые включают 90 известных серотипов. Для выявления наиболее значимых в возникновении острых средних отитов серотипов пневмококков было проведено международное исследование, в котором проанализированы случаи отита у 3232 детей из Европы и Америки. Чаще других у детей при ОСО выделяли серотипы 19F, 23F, 14, 6B, 6A, 19A, 9V независимо от возраста ребенка [10].
Так называемые педиатрические серотипы пневмококков, которые обычно встречаются у детей, характеризуются тенденцией к более длительному носительству в носоглотке, чем другие серотипы. Эти штаммы более резистентны к антибиотикам, чем те, которые можно встретить у взрослых носителей.
В современных исследованиях было показано, что, хотя пневмококковые инфекции превалируют у лиц мужского пола (взрослое население), у женщин чаще встречаются резистентные пневмококки, что, вероятно, связано с их более частым заражением устойчивыми штаммами от детей.
Колонизация носоглотки новорожденных происходит быстро, в течение 1-го месяца, через контакт со взрослыми и особенно с детьми. По мере роста и формирования индивидуального иммунного ответа к бактериям новые их серотипы колонизируют респираторный тракт. Этому способствуют условия скученности в детских садах, интернатах. Пик носительства пневмококка отмечается в раннем детском возрасте до 2 лет, а у 20–40 % здоровых детей — периодически на протяжении всей жизни. Носительство пневмококка в закрытых учреждениях достигает 60 % у детей и 5–10 % у взрослых. Преобладание резистентных штаммов среди детей раннего возраста делает данную популяцию опасным «резервуаром» инвазивной пневмококковой инфекции [11].
Отмечается зависимость между частотой выделения резистентных штаммов и предшествующей антибиотикотерапией. Однако для составления полной картины следует также анализировать правильность назначения антибиотика, его дозирование, длительность приема и выполнение рекомендаций врача.
Факты риска резистентности пневмококка:
1. Локализация: резистентность пневмококка чаще наблюдается среди изолятов из респираторного тракта, чем при других инвазивных локализациях.
2. Госпитализация: фактор риска для госпитальных резистентных штаммов, также как дневные стационары по уходу, дома ребенка.
3. Урбанизация: резистентность выше в городах, чем в сельской местности.
4. Возраст: дети до 5 лет, особенно первых 2 лет жизни.
5. Использование антибиотиков: выбор, доза, частота, применение антибиотиков резерва при эмпирической терапии.
6. Пол: женский.
7. Серотипы: педиатрические.
8. Продолжительность: длительное носительство.
9. Контакты: внутрисемейные (с братьями и сестрами), закрытые коллективы.
10. Заболевания: повторные отиты и синуситы.
Накопленные в современной литературе данные и клинический опыт диктуют необходимость изменить парадигму антибактериальной терапии в эпоху растущей резистентности к антибиотикам.
Парадигма (принципы) АБ-терапии в эпоху резистентности
— Учет и оптимизация параметров фармакокинетики (ФК) и фармакодинамики (ФД) при выборе антибиотика.
— Стратегия терапии — эффективная терапия, нацеленная на эрадикацию возбудителя, снижение заболеваемости и смертности, связанной с неадекватным назначением АБ.
— Деэскалация — оптимизация антибактериальной терапии при возможности определения чувствительности патогенов.
— Недопустимость необоснованной, профилактической терапии.
— Прогнозирование успеха/неуспеха терапии — экономическая эффективность.
Таким образом, вооружаясь современными данными, практический врач может прогнозировать эффективность антибактериальной терапии, которую он применяет.
Предикторы эффективности АБ-терапии
Минимальная ингибирующая концентрация (МИК) и минимальная бактериостатическая концентрация до недавнего времени были основными параметрами, используемыми для количественной оценки антибактериальной активности антибиотика.
Хотя эти показатели являются хорошими предикторами взаимодействия между бактерией и антибиотиком, они не в полной мере дают нам информацию о поведении антимикробного препарата в организме человека и о его антимикробной активности.
По фармакодинамическим/фармакокинетическим параметрам все антибиотики можно разделить на 2 группы. Эффективность препаратов первой группы зависит от времени, а второй группы — от концентрации препарата (табл. 1).
Благодаря разным фармакологическим эффектам антибиотиков 1-й и 2-й групп достигают эрадикации возбудителя. Время-зависимый антибиотик 1-й группы) (бета-лактам) должен находиться в достаточной концентрации в месте инфекции на протяжении времени более 40 % интервала между дозами. Так, если анбитиотик назначается два раза в сутки (интервал между дозами 12 часов), то время действия антибиотика (когда его концентрация превышает минимально подавляющую для данного возбудителя) должно продолжаться более 5 часов после каждого приема. Если время эффективной концентрации будет меньше, то применение антибиотика может не привести к полной эрадикации возбудителя. Более того, антибиотик в субоптимальной концентрации будет индуцировать развитие резистентности бактерий.
Для представителей второй группы (аминогликозиды, фторхинолоны, метронидазол и др.) характерна зависимость между эффективностью и величиной отношения максимальной концентрации препарата (Сmax в сыворотке крови) к его минимальной подавляющей концентрации, то есть Сmax/МПК, или величины отношения площади под фармакокинетической кривой (ПФК) к МПК, то есть ПФК/МПК.
Анализируя доступные антибактериальные средства с позиций их фармакокинетических и фармакодинамических параметров, можно выбрать не просто активный в отношении предполагаемого возбудителя препарат (по данным invitro), но и обеспечить эрадикацию возбудителя без риска развития резистентности.
Именно ФК/ФД-параметры используются для разработки международных рекомендаций по выбору антибактериальной терапии респираторной патологии, которая, как правило, на старте проводится эмпирически.
Достижения последних лет в изучении антибиотикорезистентности и возможности прогнозирования эффективности антибактериальной терапии с успехом используются в современных протоколах антибактериальной терапии внебольничной пневмонии у детей в Украине, профессиональными ассоциациями стран Европы, Канады, США (табл. 2).
Антибактериальная терапия внебольничной пневмонии у детей согласно Приказу МЗ Украины № 18 от 13.01.2005
Основные группы антибиотиков, которые могут быть использованы (в ранжированной последовательности):
— полусинтетические пенициллины;
— полусинтетические пенициллины с клавулановой кислотой;
— цефалоспорины;
— макролиды;
— аминогликозиды I–III поколений (применение гентамицина нежелательно в связи с отсутствием чувствительности пневмококка к антибиотику);
— производные метронидазола;
— в отдельных случаях тяжелого течения с угрозой для жизни — фторхинолоны (детям старше 12 лет).
С учетом ФК/ФД-параметров амоксицилин продолжает быть одним из самых активных пероральных антимикробных средств в борьбе с пневмококком и не продуцирующими b-лактамазы штаммами гемофильной палочки. А для борьбы со штаммами гемофильной палочки и моракселлы, продуцирующими b-лактамазы, во всем мире широко используется амоксициллин, защищенный клавулановой кислотой (Аугментин™).
Из приведенных схем лечения видно, что препаратом первой линии в лечении внебольничной пневмонии в подавляющем большинстве случаев является амоксициллин или амоксициллин/клавуланат.
Парентеральные формы цефтриаксона и фторхинолоны также активны в отношении респираторных патогенов, однако фторхинолоны у детей должны применяться с особой осторожностью, принимая во внимание их токсичность и развитие резистентности.
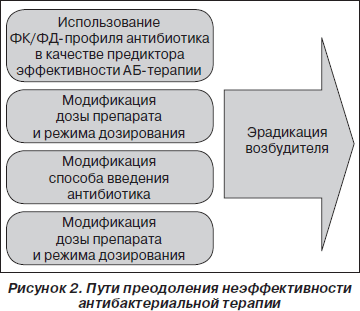
Несмотря на обилие рекомендаций и исторический опыт применения антибактериальной терапии, на практике врачи нередко сталкиваются с отсутствием эффекта от назначенного препарата. Одной из причин неудач антибиотикотерапии может быть развитие резистентности бактерий. При разработке путей преодоления неуспеха терапии в связи с возможной резистентностью пневмококка существует несколько вариантов решения этой проблемы:
1) использование ФК/ФД-профиля антибиотика;
2) модификация дозы препарата (рис. 2).
Современные тенденции микробной резистентности имеют не только негативные аспекты. Так, исследователями было установлено, что по мере все более широкого использования «новых» антибиотиков восстанавливается чувствительность к «старым» антибиотикам вследствие их меньшего использования. Эти факты приводят к убедительному выводу о том, что проблема сдерживания роста резистентности к антимикробным средствам может быть решена путем грамотного подхода к антибиотикотерапии.
Резистентность можно прогнозировать и своевременно предупреждать, сохраняя активность антибиотиков для борьбы с серьезными инфекциями и эпидемиями.
В обычной практике педиатры нередко сталкиваются с рецидивирующими, трудно поддающимися терапии респираторными инфекциями. К сожалению, бактериологическое подтверждение этиологии заболевания в рутинной практике проводится редко, тем более определение чувствительности выделенного штамма к антибиотикам. Вместе с тем в своем выборе врач может опираться на определенные критерии и факторы риска, наличия резистентных штаммов пневмококка в детском возрасте, такие как повторные респираторные заболевания, наличие хронических очагов инфекции, пребывание в закрытых коллективах, частые эпизоды антибиотикотерапии. Необходимые данные можно получить при тщательном сборе анамнеза жизни ребенка и анализе истории болезни.
Для детей из групп риска по инфицированию резистентными штаммами певмококка разработаны специальные дозировки препаратов (повышенные дозы амоксициллина), которые позволяют решить эту проблему и добиться эрадикации патогена.
Ряд исследований, проведенных у детей с носительством резистентного пневмококка, убедительно продемонстрировал, что применение высоких доз амоксициллина (90 мг/сут) в течение 5 дней приводит к лучшим бактериологическим результатам по сравнению с применением 40 мг/сут в течение 10 дней [13].
На основе этих доказательств была разработана новая форма амоксициллина/клавуланата с уникальным соотношением компонентов (14 : 1) — Аугментин™ ES. Применение препарата Аугментин™ ES при эмпирической терапии позволяет достигать высокой бактериологической эффективности не только при лечении инфекции дыхательных путей, вызванных микроорганизмами, продуцирующими бета-лактамазы, но также резистентными штаммами пневмококка.
Таким образом, мы имеем доказательную базу, подтверждающую актуальность и перспективы дальнейшего использования бета-лактамных антибиотиков в эру антибиотикорезистентности.
Случай из практики педиатра
Ребенок 6 лет из школы-интерната был доставлен к врачу с жалобами на высокую температуру, кашель, сопровождающийся болью в груди, одышку.
Из анамнеза жизни известно, что ребенок часто болеет ОРЗ, бронхитами, средним отитом, 3–4 раза в год получает антибиотики. Заболел 4 дня назад, когда повысилась температура до 37,8 °С и появились катаральные симптомы (насморк, кашель). Ребенок получал парацетамол, анаферон детский, теплое питье с позитивной динамикой к 3-му дню болезни. На 4-й день болезни состояние ухудшилось, температура тела повысилась до 39 °С, усилились кашель и одышка при общем относительно сохранном статусе (ребенок активен, сон и аппетит не нарушены). Физикально определялись крепитирующие хрипы в легких справа и укорочение перкуторного звука. ЧД — 30 в 1 мин, ЧСС — 120 в 1 мин. При обследовании: в общем анализе крови лейкоцитоз — до 12 000 в мм3, нейтрофилез. На основании клинико-рентгенологических данных диагностирована пневмония с локализацией в нижней доле справа.
Обоснование терапии. Учитывая то, что ребенок является воспитанником школы-интерната, часто болеет респираторными инфекциями, по поводу которых 3–4 раза в год принимает антибиотикотерапию, он может быть отнесен к группе риска наличия резистентного штамма пневмококка.
Принимая во внимание тот факт, что ребенок в течении года неоднократно переносил инфекции разной локализации, нельзя исключить присутствие бактерий, продуцирующих бета-лактамазы (гемофильная палочка или моракселла).
В условиях эмпирического назначения стартовой терапии пневмонии для покрытия всех возможных в данной ситуации патогенов выбор был сделан в пользу защищенного клавулановой кислотой высокодозного амоксициллина (Аугментин™ES90/6,4 мг/кг/сут в два приема) в течение 10 дней. По окончании лечения были констатированы разрешение пневмонии, нормализация лабораторных показателей и состояния ребенка.
Выводы
Антимикробная терапия была и остается одним из выдающихся достижений в медицине. В то же время проблема бактериальной резистентности, возникшая как ответ на применение антибиотиков, может значительно ограничить наши возможности в лечении инфекционных заболеваний, особенно в педиатрии. Для сдерживания роста резистентности и преодоления неэффективности антибиотикотерапии врач должен следовать в своей практике принципам, которые прошли проверку с позиций доказательной медицины:
1. Разумное использование антибиотиков (только для лечения бактериальных инфекций) может значительно уменьшить риск резистентности к антибиотикам.
2. Когда антибиотикотерапия является оправданной, целесообразно использование антибиотиков узкого спектра действия в оптимальной дозе и продолжительности с учетом ФК/ФД-параметров и чувствительности возбудителя, необходимых для его эрадикации.
3. Субингибирующая концентрации антибиотика, которая не приводит к эрадикации, способствует развитию устойчивости возбудителя.
4. Бета-лактамные антибиотики остаются первой линией терапии бактериальных инфекций респираторного тракта у детей.
5. Применение высокодозных форм амоксициллина/клавуланата (Аугментин™ ЕS) позволяет успешно лечить респираторные заболевания, вызванные штаммами возбудителей с различными механизмами резистентности.
Печатается при поддержке компании «ГлаксоСмитКляйн»
1. Якобс М., Даган Р. // Seminars in Pediatric Infectious Diseases. — 2004. — Vol. 15, № 1. — Р. 5-20.
2. Facts about Antibiotic Resistance // Infectious Diseases Society of America; Revised. — May 21 2009. http://www.idsociety.org/Content.aspx?id=5650
3. Ahmad A., Ghosh A., Schal C., Zurek L. Insects in confined swine operations carry a large antibiotic resistance and potentially virulent enterococcal community // BMC Microbiology. — 2011. — 11. — 23.
4. European Centre for Disease Prevention and Control. Antimicrobial resistance surveillance in Europe 2009 // Annual Report of the European Antimicrobial Resistance Surveillance Network (EARS-Net) Stockholm: ECDC; 2010.
5. Таточенко В.К., Бакрадзе М.Д. Значение лекарственной устойчивости микроорганизмов в педиатрической практике // Практика педиатра. — Декабрь 2009. — С. 5-11.
6. Майданник В.Г. и соавт. Две стороны одной медали? Нерациональная антибиотикотерапия и антибиотикорезистентность // Medicus Amicus. — 2005. — № 5.
7. Nyquist A.C. et al. Antibiotic prescribing for children with colds, upper respiratory tract infections, and bronchitis // JAMA. — 1998. — 279. — 875-877.
8. Jeffrey A. Linder et al. Antibiotic Treatment of Children With Sore Throat // JAMA. — 2005 Nov 9. — 294. — 2315-2322.
9. Keith P. Klugman. Risk factors for antibiotic resistance in Streptococcus pneumoniae // South African Medical Journal. — Nov 2007. http://findarticles.com/p/articles/mi_6869/is_11_97/ai_n28533875
10. Hausdorff W.P. et al. Multinational study of pneumococcal serotypes causing acute otitis media in children // Pediatr. Infect. Dis. — 2002 Nov. — 21(11). — 1008-16.
11. Marchisio P., Esposito S., Cavagna R., Principi N. Nasopharyngeal Carriage of Streptococcus pneumonia in Healthy Children: Implication for the Use of Heptavalent Pneumococcal Conjugate Vaccine // Emerging Infectious Diseases. — May 2002. — Vol. 8, № 5. — Р. 479-484.
12. Ostapchuk M. et al. Community-Acquired Pneumonia in Infants and Children // American Family Physician. — 2004 September 1. — Vol. 70, № 5.
13. Dilruba Nasrin, Peter J. Collignon, Leslee Roberts, Eileen J. Wilson, Louis S. Pilotto, Robert M. Douglas. Effect of lactam antibiotic use in children on pneumococcal resistance to penicillin: prospective cohort study // BMJ. — 2002. — 324. — 28.


