Журнал «Здоровье ребенка» 3 (30) 2011
Вернуться к номеру
Аберантна підшлункова залоза у дітей із синтропною патологією органів травлення
Авторы: Бабій І.Л., Платонова О.М., Федчук І.М., Гариничева Т.О., Бєлова Л.Л., Ситнікова В.О., Лєснікова О.М. Одеський національний медичний університет
Рубрики: Педиатрия/Неонатология
Версия для печати
У роботі повідомляється про 4 клінічних випадки аберантної підшлункової залози у дітей — вродженої вади розвитку. Відмічені клінічні, ендоскопічні, гістологічні особливості зазначеної вади.
Аберантна підшлункова залоза, синтропна патологія органів травлення, діти.
Аберантна підшлункова залоза (додаткова, ектопія підшлункової залози, вроджена гетеротопія підшлункової залози, хористома) — вада розвитку підшлункової залози, за якої вузли її тканини розташовані в інших органах. Є повідомлення, що вперше опис додаткової підшлункової залози надав Schulz (1727), який виявив її в дивертикулі Меккеля. За 200 років із часу першого опису було виявлено всього 60 випадків аберантної підшлункової залози, в наступні 20 років — ще 415 [3, 4]. Наразі, за даними патологоанатомів, аберантні осередки тканини підшлункової залози зустрічаються в 3–10 % секцій. В осіб чоловічої статі цю патологію виявляють у 2 рази частіше, ніж у жінок [7]. Ектопія може зустрічатися в різних відділах шлунково-кишкового тракту чи інших внутрішніх органах: найчастіше виявляється в гастродуоденальній зоні (70–85 %), з них у шлунку — 90 %, поодинокі випадки щодо локалізації у жовчному міхурі, дивертикулі Меккеля, селезінці, брижі, пупку, середостінні. Ектопована підшлункова залоза ніякого зв’язку з основною підшлунковою залозою не має. Аберантна підшлункова залоза належить до групи дизонтогенетичних дистопій епітелію з інших органів, які є наслідком порушення його диференціації в ембріональному періоді. Вирізняють 4 гістологічних типи ектопій підшлункової залози залежно від наявності структурних елементів, з яких вона складається: 1-й тип — із залозної тканини, вивідних протоків та острівців; 2-й — із залозної тканини та вивідних протоків (за відсутності острівців); 3-й — із панкреатичних острівців; 4-й — із вивідних протоків [5]. Макроскопічно аберантна підшлункова залоза, за більшістю спостережень, має вигляд поліпозних утворень, зустрічаються також вузликові, кістоподібні, виразкові форми. Зазначають, що за гастробіоптатами необхідно проводити диференційну діагностику з панкреатичною метаплазією слизової оболонки шлунка. На відміну від гетеротопії ділянки метаплазії обмежені тільки слизовою оболонкою і не містять острівців [1].
Клінічно вада тривалий час може не проявлятися, однак у тканині додаткової підшлункової залози можливий перебіг усіх патологічних процесів і їх ускладнень, що притаманні основній. У такій ситуації вона може набувати «масок» гастриту, виразкової хвороби, панкреатиту, холециститу, апендициту та інших захворювань, що значно утруднює діагностику. Вада при значному розмірі чи підвищеній секреторній активності може стати причиною стенозу воротаря шлунка, запалення, виразки, перфорації стінки органа-хазяїна, кровотечі, ілеуса, інвагінації кишечника, обтураційної жовтяниці тощо. Клінічна симптоматика пов’язана із запальними й некротичними змінами в ектопованій залозі. Зустрічаються дані, що аберантна підшлункова залоза може призвести до стискання прилеглих тканин, спричиняти формування виразок шлунку, дванадцятипалої кишки (ДПК). Загрозливе ускладнення — малігнізація, розвиток панкреатичної аденоми та інших пухлин, у тому числі таких, що перебігають із гіперінсулінізмом [5]. Малігнізація додаткової підшлункової залози можлива частіше, ніж основної, що обумовлює необхідність динамічного ендоскопічного спостереження.
Діагноз встановлюють переважно при ендоскопічному дослідженні, рідше ультразвуковому. Остаточно верифікують діагноз ектопії при морфологічному (гістологічному) дослідженні біоптатів.
Щодо лікування, здебільшого рекомендується оперативне видалення додаткової залози: за даними деяких авторів, воно обов’язкове незалежно від клінічної маніфестації, локалізації, розмірів через ризик малігнізації, за іншими — лише у випадках тривалих скарг і виникнення ускладнень [2, 4]. Оперативне втручання часто зумовлює компенсаторну гіпертрофію клітин основної підшлункової залози. Альтернативою хірургічному методу в деяких випадках може стати метод ендоскопічного втручання. В останні роки з’явились повідомлення щодо ефективності застосування пролонгованих синтетичних аналогів соматостатину (ланреотиду) у хворих з аберантною підшлунковою залозою. Утім тривалість такої терапії не обґрунтована методами доказової медицини [7].
Наводимо власні клінічні спостереження.
Пацієнтка К., 11 років, надійшла зі скаргами на болі в животі натще, переважно в епігастральній ділянці, печію, поганий апетит, нудоту, млявість, схильність до запорів, прогресуючі плями вітиліго. Сімейний анамнез у дівчинки обтяжений. Тітка за материнською лінією страждає виразковою хворобою дванадцятипалої кишки, бабусі за материнською лінією у 18 років проведена гастректомія з приводу гострої шлункової кровотечі. Об’єктивно при надходженні до лікарні стан дитини середньої тяжкості. Хвора зниженого харчування (маса 28 кг, ріст 151 см), індекс Кетле 2 — 18,54. Млява, дещо пригнічена. Шкірні покриви бліді, на спині великі ділянки вітиліго. Живіт доступний глибокій пальпації, дещо напружений в епігастральній та пупковій ділянках, симптом Менделя позитивний. Міхурові симптоми негативні. Болючість у точках Дежардена, Мейо-Робсона та зоні Шоффара. Печінка +1 см з-під краю реберної дуги, безболісна при пальпації, еластична. Стул звичайного кольору, оформлений, нерегулярний, схильність до запорів. У загальному аналізі крові — помірний лейкоцитоз (11,0 Г/л), зсув лейкоцитарної формули вліво (п/яд — 8 %). Амілаза (діастаза) сечі — 150,0 г/ч • л (норма 20–160 г/ч • л). Глюкоза крові 5,0 ммоль/л (норма 3,89–5,83 ммоль/л). Глікемічний профіль: через 1 годину — 3,0 ммоль/л, через 2 години — 3,6 ммоль/л. Дихальний уреазний тест на хелікобактеріоз «ХЕЛІК-тест» — позитивний (+).
Проведено ультразвукове дослідження — патологічних змін із боку жовчного міхура та підшлункової залози не виявлено.
За даними фіброезофагогастродуоденоскопії — ознаки ерозивно-катарального рефлюкс-езофагіту 1-го ступеня, дві виразки цибулини ДПК розмірами 0,6 ґ 1,4 см и 0,7 ґ 0,9 см, на стінках цибулини ДПК 10 афтозних ерозій діаметром 1,5–3 мм. В антральному відділі шлунка на великій кривині візуалізується щільне еластичне утворення діаметром 1,2 см, висотою 0,6 см із пупкоподібним утягуванням у центрі, гладкою поверхнею, за кольором не відрізняється від оточуючої слизової оболонки (узята біопсія). Катаральний гіперпластичний (фолікулярний) виражений гастрит. Поверхнево помірно виражений гастродуоденіт. Деформація цибулини ДПК. Деформація й недостатність воротаря. Недостатність кардії помірна. Н.pylori (+). За даними внутрішньошлункової рН-метрії — селективна гіперацидність (на фоні блокаторів Н2-рецепторів).
За даними біопсії — фрагменти слизової оболонки шлунка з хронічним запаленням із помірним ступенем активності, фрагменти фіброзної тканини, дрібні фрагменти аберантної підшлункової залози — переважно з ацинусами і поодинокими вивідними протоками (рис. 1).
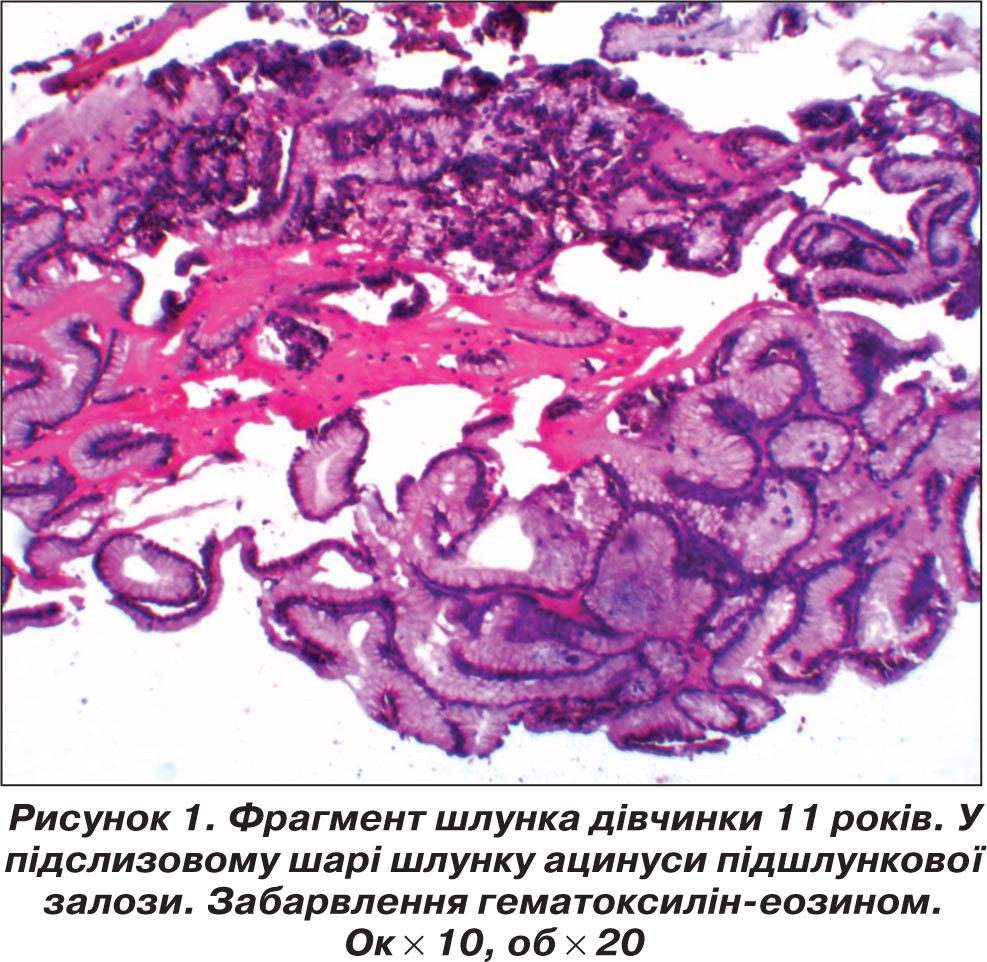
Хворій було виставлено діагноз: виразкова хвороба ДПК, уперше виявлена: 2 гігантські гострі виразки цибулини ДПК із деформацією цибулини дванадцятипалої кишки й воротаря. Гастроезофагеальна рефлюксна хвороба з рефлюкс-езофагітом 1-го ступеня тяжкості. Хронічний гастродуоденіт: нодулярний пангастрит з підвищеною кислотоутворюючою функцією шлунка, асоційований НР, хронічний ерозивний поверхневий дуоденіт. Аберантна підшлункова залоза. Вітиліго.
Крім вищенаведеного спостереження, під нашим наглядом знаходилося ще 3 дівчинки віком 12, 13 та 15 років, у яких при фіброезофагогастродуоденоскопії з приводу скарг на болі в животі було встановлено аберантну підшлункову залозу, що було підтверджено даними біопсії.
Аналізуючи наведені спостереження, слід підкреслити, що в усіх випадках аберантної підшлункової залози пацієнти були жіночої статі. В усіх дітей мала місце синтропна патологія органів травлення (хронічний гастродуоденіт, у 3 із 4 випадків — гастроезофагеальна рефлюксна хвороба, дискінезія жовчовивідних шляхів). Характерно, що у всіх хворих за даними внутрішньошлункової рН-метрії відмічається гіперацидний стан. Ендокринна функція за даними глікемічного профілю та екзокринна функція за результатами ферментної активності не порушені. Щодо аберантної підшлункової залози: ектопія локалізувалась в антральному відділі шлунка у 3 хворих, у препілоричному відділі — в 1 випадку, розміри її коливались від 0,7 до 1,5 см. За даними біопсії спостерігали два випадки аберантної підшлункової залози 2-го типу (залозна тканина і вивідні протоки), два випадки — 4-го типу (вивідні протоки).
Актуальність нашого повідомлення пов’язана з рідкістю уродженої гетеротопії підшлункової залози та недостатньою кількістю друкованих повідомлень щодо клінічних спостережень як у дорослих, так і у дітей.
1. Аруин Л.И., Капуллер Л.Л., Исаков В.А. Морфологическая диагностика болезней желудка и кишечника. — М.: Триада-Х, 1998. — 496 с.
2. Бєлоусов Ю.В. Гастроентерологія дитячого віку: Підручник. — К.: СПД Коляда О.П., 2007. — 440 с.
3. Гребенев А.Л. Аномалии поджелудочной железы // Руководство по гастроэнтерологии: В 3 т. / Под. ред. Ф.И. Комарова, А.Л. Гребенева. — М.: Медицина, 1996. — Т. 3 (гл. 5). — С. 74-81.
4. Маев И.В., Кучерявый Ю.А Аберрантная поджелудочная железа // Клинические перспективы гастроэнтерологии, гепатологии. — 2005. — № 3. — С. 24-30.
5. Самсонов В.А. Опухоли и опухолевидные образования желудка. — М.: Медицина, 1989. — 240 с.
6. Basili E., Allemand I., Ville E., Laugier R. Lanreotide acetate may cure cystic dystrophy in heterotopic pancreas of the duodenal wall // Gastroenterol. Clin. Biol. — 2000. — Vol. 25. — P. 1108-1111.
7. Gastrointestinal and Oesophageal pathology / Ed. by R. Whitehead. — 2nd ed. — London: Churchill Livingstone, 1995.
