Журнал «Травма» Том 13, №1, 2012
Вернуться к номеру
Клеточно-молекулярные механизмы развития асептической нестабильности эндопротеза тазобедренного сустава
Авторы: Сагаловски С., Шенерт М., Отделение ортопедии клиники Медиан, Бад Лаузик, Германия
Рубрики: Травматология и ортопедия
Версия для печати
В обзоре литературы представлены современные взгляды на клеточно-молекулярные механизмы развития асептической нестабильности при эндопротезировании тазобедренного сустава и новые возможности потенциальной терапии.
Summary. In literature review there is presented the contemporary views on cellular and molecular mechanisms development of the aseptic instability development at hip replecement and new possibilities of potential therapy.
Резюме. В огляді літератури наведено сучасні погляди на клітинно-молекулярні механізми розвитку асептичної нестабільності при ендопротезуванні кульшового суглоба та нові можливості потенціальної терапії.
Асептическая нестабильность эндопротеза, механизм развития, лечение, деносумаб, оданакатиб.
Key words: aseptic instability of hip implant, mechanisms of development, therapy, denosumab, odanacatib.
Ключові слова: асептична нестабільність ендопротезу, механізм розвитку, лікування, деносумаб, оданакатіб.
Эндопротезирование тазобедренного сустава в настоящее время является одной из распространенных ортопедических операций, направленных на восстановление нарушенной функции поврежденного органа. С момента внедрения в клиническую практику в 50-е годы прошлого столетия тотальное эндопротезирование играет все возрастающую роль в лечении различных патологических состояний опорно-двигательного аппарата. Количество операций за последние 5 лет увеличилось в Германии и странах Европейского Содружества на 80 % и составляет 175 тысяч в год (Германия) [21, 33]. Ежегодно, по данным экспертной группы Всемирной организации здравоохранения, в мире выполняется до 1 млн 500 тысяч тотальных замещений тазобедренного сустава.
После первичного эндопротезирования, по данным Drees и соавт. [5], благоприятные результаты отмечаются в 85 % случаев, однако по мере изучения отдаленных результатов количество положительных исходов существенно снижается, и это снижение закономерно связано с длительностью срока наблюдения за прооперированными больными. Клиническими наблюдениями установлено, что неудовлетворительные результаты, наблюдаемые в первые годы после операции, в 3 % случаев связаны с техническими погрешностями, в 7 % — с развитием инфекционного процесса, в 6 % — с изменением дислокации имплантированного сустава и в более 75 % случаев потребовалось повторное оперативное вмешательство вследствие возникновения асептического расшатывания (нестабильности) компонентов имплантата [30]. Таким образом, с увеличением количества первичных операций эндопротезирования и сроков наблюдения пациентов растет количество ревизионных оперативных вмешательств. По данным американских авторов, в США процент ревизионных операций достигает 10–15 % от общего числа эндопротезирований [2, 31], в Европе количество подобных вмешательств соответствует 17,5 % [32]. В определенной степени это обусловлено старением населения и ростом заболеваемости артрозами и остеопорозом, способствующими возникновению посттравматических и не связанных с травмой переломов шейки бедренной кости. В результатах, представленных 22 ведущими центрами ортопедии из 12 европейских стран (EUROHIP), показатели ревизионного эндопротезирования в связи с асептической нестабильностью практически не имеют тенденции к снижению, несмотря на постоянное совершенствование конструкций и материалов, техники выполнения операции и вариантов фиксации эндопротеза [7].
Нeсмотря на то что отдельные авторы по-прежнему связывают «выживаемость» имплантатов с качеством материала и их дизайном, по мнению большинства исследователей, значительная роль в развитии асептической нестабильности эндопротеза отводится нарушению процесса ремоделирования костной ткани. Авторы отмечают прямую коррелятивную связь между развитием асептического расшатывания и исходным количественным и качественным состоянием прилежащей к эндопротезу кости, а также величиной ее потери в период стрессового ремоделирования [6].
Изучение особенностей стрессового ремоделирования после тотального эндопротезирования тазобедренного сустава с использованием метода двухэнергетической рентгеновской абсорбциометрии свидетельствует о выраженной потере минеральной плотности костной ткани (МПКТ) в зоне, прилежащей к имплантату [30]. Исследование динамики МПКТ в системе «кость — эндопротез» в период адаптивной перестройки выявило, что на интенсивность потери и прироста прилежащей к эндопротезу костной массы оказывает влияние не только имплантат, но и исходное нарушение метаболизма костной ткани (системный остеопороз), что создает предпосылки к увеличению микроподвижности и тем самым ускоряет развитие асептической нестабильности (рис. 1).
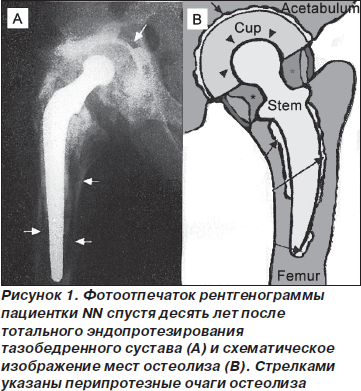
Системный остеопороз — многофакторное заболевание, в основе которого лежат процессы нарушения костного ремоделирования с повышением резорбции костной ткани и снижением синтеза кости [11, 13]. Операция эндопротезирования тазобедренного сустава все чаще выполняется на фоне этого заболевания. Нарушение ремоделирования костной ткани, присущее системному остеопорозу, часто является причиной ранней асептической нестабильности имплантата [5]. Характерные для остеопороза нарушение микроархитектоники трабекул и повышение их хрупкости увеличивают микроподвижность имплантата относительно прилежащей костной массы и оказывают негативное влияние на остеоинтеграцию.
В проведенных сравнительных исследованиях особенностей потери МПКТ в зонах Груена у пациентов с исходным остеопорозом и у больных, оперированных по поводу диспластического или деформирующего артроза и не имеющих изменений показателей МПКТ в телах позвонков поясничного отдела или в шейке бедра, установлено, что спустя 12 месяцев после операции МПКТ в зонах Груена не восстановилась до базовых значений и степень дефицита у больных с остеопорозом была в 2 раза и более выше, чем в контрольной группе [29].
Процессы нарушения костного ремоделирования с повышением резорбции костной ткани и снижением костеобразования, характерные для системного остеопороза, являются результатом нарушения тесного клеточного взаимодействия остеобластов (ОБ) и остеокластов (ОК), берущих начало от предшественников различных клеточных линий: ОБ — из мезенхимальных стволовых клеток, ОК — из макрофагально-моноцитарных клеток костного мозга [36]. ОБ — мононуклеарная клетка, участвующая в процессе образования кости и минерализации клеток костного матрикса. Остеобласты играют фундаментальную роль в модуляции костного ремоделирования и регуляции метаболической активности других клеток костной ткани. ОБ секретируют ряд биологически активных соединений, посредством которых они влияют на процесс созревания клетки-предшественника ОК, превращая его в большую многоядерную клетку, способную участвовать в процессе резорбции, т.е. рассасывания костной ткани, действуя только на минерализованную кость, не изменяя собственно матрикса костной ткани. Созревание и дифференциация ОБ осуществляются под влиянием различных специфических факторов, воздействующих на процесс транскрипции, важнейшим из которых является протеин Cbfa1 (core-binding factor alpha 1; известный также как runt related transcription factor 2; RUNX2) [19]. У мышей с недостаточной функцией Cbfa1 наблюдается существенное замедление процесса костеобразования, не прослеживается созревание остеобластных клеток. Напротив, введение животным рекомбинантного Cbfa1 вызывает экспрессию в неостеогенных клетках генов, присущих ОБ [37]. Значимая роль, выполняемая протеином Cbfa1 (RUNX2) в дифференциации и созревании ОБ, проявляется также в способности белка регулировать функцию многих генов, участвующих в синтезе протеинов костной ткани: коллагена типа 1, остеопонтина, остеокальцина и костного сиалопротеина. Остеопонтин — фосфорилированный кислый гликопротеин, экспрессируется в течение активной стадии пролиферации ОБ и вовлекается в контроль взаимодействия между клеточным и внеклеточным матриксом. В отличие от остеопонтина остеокальцин (костный Gla-протеин) экспрессируется ОБ только в постпролиферативную фазу развития клетки. Он наиболее активен в течение процесса минерализации костной ткани. Считается, что остеокальцин активно участвует в регулировании механизма минерального отложения. Повышение концентрации пептида в плазме крови свидетельствует о завершении дифференциации и активности ОБ.
На рост и функциональную способность ОБ оказывают влияние также паракринные и/или аутокринные факторы, регулирующие активность процессов внутриядерной транскрипции, синтез остеопонтина и остеокальцина. К ним относится ряд факторов роста клеток (фактор роста фибробластов — FGF; инсулиноподобный фактор роста — IGF), модуляторы цитокинов (b-катенин), гормональные биологически активные вещества (глюкокортикоиды, паратгормон). Паратгормон (РТН), секретируемый в основном главными клетками околощитовидной железы, взаимодействует с плазматическим рецептором (PTH-R) ОБ, сопряженным с G-протеином. РТН-рецептор, оперирующий через G-белок, имеет три цепи внеклеточного фрагмента с N-концевым участком, семь трансмембранных фрагментов и внутриклеточную часть рецептора, также представленную тремя петлями полипептидной цепочки с С-концевым участком. При взаимодействии гормона с N-концевым участком рецепторного белка происходит активация внутриклеточной части ГТФ-связующего протеина (G-протеина), приводящей к диссоциации комплекса альфа-бета-гамма-нагруженной ГТФ. Альфа-субъединица активирует два эффекторных белка в системе клеточной сигнальной трансдукции — аденилатциклазу и фосфорилазу С, изменяющих внутриклеточную концентрацию вторичных посредников — циклического аденозинмонофосфата, протеинкиназ типа А и С, ионизированного кальция, а также инозитолтрифосфата и диацилглицерина. Протеинкиназы А и С регулируют скорость внутриклеточных процессов, активируют индукцию экспрессии специфических генов в ядре ОБ, стимулируют пролиферацию клетки, участвуют в процессе высвобождения синтезированных клеткой биологически активных веществ.
В период активной фазы предшественник ОК представляет собой округлую одноядерную клетку моноцитарно-макрофагального ряда костного мозга, которая в последующем под влиянием активных факторов, продуцируемых ОБ, превращается в многоядерную клетку, активный ОК, резорбирующий костную ткань. Предположение, что активация и регуляция ремоделирования костной ткани являются следствием взаимодействия между ОБ и ОК, получило подтверждение в многочисленных исследовательских работах [17, 26, 36, 37]. Значительный прогресс в понимании процессов костного ремоделирования был достигнут с открытием цитокиновой системы RANKL-RANK-OPG [14, 26], играющей ключевую роль в формировании, дифференцировке и активности ОК. Открытие этой системы стало краеугольным камнем для понимания механизмов регуляции костной резорбции, а также других процессов, вовлеченных в локальное ремоделирование кости. Регуляция остеокластогенеза осуществляется в основном при помощи двух цитокинов: лиганда рецептора активатора ядерного фактора каппа-В (NF-kB) — RANKL [38] и остеопротегерина (OPG) [25] на фоне пермиссивного действия макрофагального колониестимулирующего фактора (M-CSF) [20]. RANKL — это гликопротеин, продуцируемый клетками остеобластного ряда и активированными Т-лимфоцитами, принадлежит к суперсемейству лигандов фактора некроза опухоли (TNF) и является главным стимулом для созревания ОК.
Молекулярная основа межклеточного взаимодействия с участием RANKL-RANK-OPG-системы может быть представлена следующим образом (рис. 2): RANKL, экспрессированный на поверхности ОБ, связывается с RANK-рецептором, расположенным на мембранах клеток-предшественников ОК и индуцирует процесс дифференцировки и активации ОК. Одновременно стволовые клетки костного мозга и ОБ высвобождают фактор, стимулирующий образование колоний макрофагов (M-CSF) [20]. Этот полипептидный фактор роста, взаимодействуя с его высокоаффинным трансмембранным рецептором (c-fms), активирует внутриклеточную тирозинкиназу, стимулируя процесс пролиферации и дифференциации клетки-предшественника ОК. Пролиферативная активность M-CSF значительно повышается при воздействии на ОБ паратиреоидного гормона, витамина D3, интерлейкина-1 (IL-1), фактора некроза опухоли и, напротив, понижается под влиянием эстрогенов и остеопротегерина. Эстрогены, взаимодействуя с внутриклеточными рецепторами ОБ, повышают пролиферативную и функциональную активность клетки, одновременно понижая функцию ОК, стимулируя продукцию остеобластом OPG [18]. OPG — растворимый рецептор для RANKL, синтезируемый остеобластными клетками, а также клетками стромы, эндотелиальными клетками сосудов и В-лимфоцитами. Остеопротегерин действует как эндогенный рецептор-ловушка для RANKL, блокируя его взаимодействие с собственным рецептором (RANK), и таким образом угнетает формирование зрелых многоядерных клеток ОК, нарушая процесс остеокластогенеза, понижая активность резорбции костной ткани [40]. Синтезируемый и высвобождаемый остеобластными клетками RANKL является специфическим фактором, необходимым для развития и функционирования остеокластов. RANKL вступает во взаимодействие с тропным к нему рецептором RANK на мембране клетки-предшественника ОК (общий предшественник для ОК и моноцитов/макрофагов), приводя к внутриклеточным каскадным геномным трансформациям (рис. 2). RANK воздействует на ядерный фактор каппа-В (NF-kB) через сопряженный с рецептором протеин TRAF6, который активирует и транслокирует NF-kB из цитоплазмы в клеточное ядро. Накопление активированного ядерного фактора каппа-В повышает экспрессию протеина NFATc1, являющегося специфическим триггером, запускающим процесс транскрипции внутриклеточных генов, формирующих процесс остеокластогенеза [20].
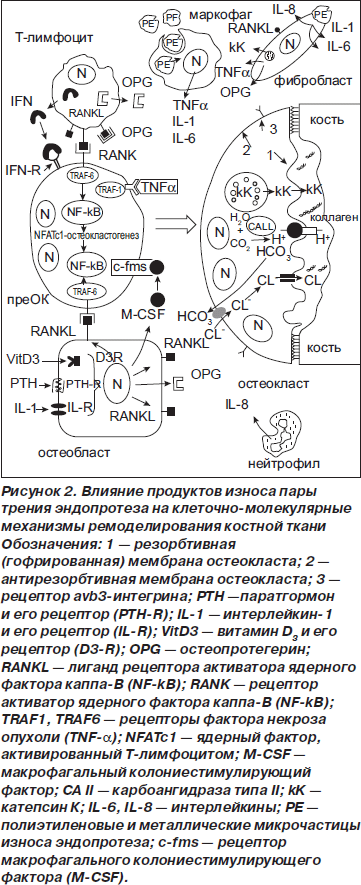
Дифференцированный ОК принимает определенное положение на поверхности кости и развивает специализированный цитоскелет, который позволяет ему создавать изолированную полость резорбции, микросреду между ОК и костью. В этом процессе активное участие принимает интегрин-avb3 [39] из семейства трансмембранных гликопротеидов-рецепторов, состоящих из альфа- и бета-субъединиц. При повышенной активности ОК avb3-интегрин экспрессируется как трансмембранный рецептор клеточной поверхности, легко вступающий во взаимодействие с различными белками внеклеточного матрикса, в частности с коллагеном типа 1. Поэтому avb3-интегрин выполняет ключевую роль в контактном взаимодействии ОК с внеклеточным матриксом. Интегриновый рецептор, связывающийся с коллагеном типа 1, претерпевает конформационные изменения и индуцирует в цитоплазме ОК повышение уровня ионизированного кальция и рН, а также фосфорилирование по тирозину ряда протеинов, играющих роль в контакте ОК с внеклеточным матриксом. Среди этих белков ключевыми участками передачи внеклеточных сигналов является тирозиновая протеинкиназа, сопряженная с цитоплазматическим доменом бета-субъединицы интегрина. Фосфорилирование по тирозину протеинов цитоплазмы ОК делает их способными активировать и вовлекать в последовательную цепь передачи сигналов другим молекулам: ГТФ-связывающим белкам (G-протеинам), цитоплазматическим протеинкиназам и транскрипционным факторам клеточного ядра, что способствует модификации экспрессии специфических генов, проявляющейся в резорбирующей активности прикрепившейся к кости клетки остеокласта. Мембрана ОК, обращенная в образованную клеткой полость, формирует множество складок, преобретает гофрированный вид, что значительно увеличивает резорбирующую поверхность. Гофрированная часть мембраны ОК, обращенная в полость резорбции, обозначается как резорбтивная мембрана в отличие от остальной части — антирезорбтивной мембраны клеточной цитоплазмы. Микросреда созданной полости резорбции подкисляется посредством электрогенной подкачки в нее протонов. Внутриклеточный рН остеокласта поддерживается с участием карбоангидразы II (CA II) посредством обмена ионами HCO3/CL через антирезорбтивную мембрану клетки. Ионы НСО3 выводятся из клетки в экстрацеллюлярное пространство, в то время как ионы хлора поступают из экстрацеллюлярной жидкости в цитоплазму ОК. Ионизированный хлор по анионным каналам гофрированной резорбтивной мембраны проникает в микрополость резорбции, в результате чего рН в резорбтивной полости достигает величины 4,0–4,2. Кислая среда создает условия для мобилизации минеральной фазы кости и формирует оптимальную среду для деградации органического матрикса костной ткани с участием катепсина К, фермента, синтезируемого и высвобождаемого в полость резорбции «кислыми везикулами» остеокласта [28]. Синтез и накопление катепсина К «кислыми везикулами» цитоплазмы ОК осуществляется с участием CTSK-гена и модулируется факторами, влияющими на функцию ОК, включая цитокины (RANKL, TNF, IL-1), гормоны (эстрогены), внутриядерные факторы транскрипции. Так, интерлейкин-1, провоспалительный цитокин, активно стимулирующий резорбцию кости и ингибирующий процесс накопления костной массы, в экспериментах in vivo с использованием клеток линии RAW 264-7 в качестве клеток-предшественников ОК значительно стимулировал экспрессию катепсина К и CA II. Нарушение функции гена, ответственного за кодирование катепсина К, вызывает изменения в процессе костной резорбции и ремоделирования костной ткани, сопровождаемые развитием остеосклероза.
Повышение экспрессии RANKL непосредственно ведет к активации резорбции кости и снижению МПКТ скелета. Введение мышам рекомбинантного RANKL уже к концу первых суток приводило к развитию гиперкальциемии, а к концу третьих — к существенной потере костной массы и снижению показателей МПКТ [38]. Баланс между RANKL и OPG фактически обусловливает количество резорбированной кости и степень изменения МПКТ. В экспериментах на животных установлено, что повышенная экспрессия OPG у мышей приводит к увеличению костной массы, остеопетрозу и характеризуется снижением количества и активности ОК, и напротив, при выключении гена OPG наблюдается понижение МПКТ, существенное повышение количества зрелых, многоядерных ОК, снижение плотности костной ткани и возникновение спонтанных переломов позвонков. Подкожное введение мышам рекомбинантного OPG в дозе 4 мг/кг в сутки в течение семи дней восстанавливало показатели минеральной плотности кости [13]. На модели адъювантного артрита у крыс линии Lewis введение OPG (2,5 и 10 мг/кг/сутки) в течение 9 дней в начальной стадии патологического процесса блокировало функцию RANKL и предотвращало потерю массы костной и хрящевой ткани. Результаты проведенных экспериментов указывают на то, что функция OPG в основном заключается в понижении или значительном «выключении» эффектов, обусловленных RANKL. В настоящее время стало очевидным, что поддержание взаимосвязи между RANKL и OPG является важным условием сохранения равновесия между резорбцией и формированием костной ткани. Сопряженность этих двух процессов, относительные концентрации RANKL и OPG в костной ткани определяют главные детерминанты массы и прочности кости. С момента открытия системы RANKL-RANK-OPG как конечного пути формирования и дифференциации ОК многими исследованиями [38, 40] подтверждена ведущая роль этого клеточно-молекулярного механизма патогенеза костного ремоделирования и возможного его участия в развитии асептической нестабильности эндопротеза, что открывает возможности в поиске новых подходов к профилактике и лечению данного состояния с использованием медикаментозных средств.
Проведенные гистоморфологические исследования подтвердили имеющиеся в литературе данные о том, что одной из причин, приводящих к развитию асептической нестабильности эндопротеза, является остеолиз и металлоз, возникающий на границе комплекса «костная ткань — эндопротез» [6, 8]. Остеолиз возникает в результате асептического воспаления, вызванного продуктами износа составных частей эндопротеза — металла и полиэтилена в узле трения [9]. В ответ на попадание микрочастиц от продуктов трения пар имплантата в ткань развивается ответная реакция с участием многих клеток: макрофагов, фибробластов, нейтрофилов, лимфоцитов, остеобластов и остеокластов, основных клеток, участвующих в процессе ремоделирования костной ткани (рис. 2). Отмечено, что выраженность остеолиза прямо коррелирует с увеличением в окружающей ткани продуктов износа пары трения эндопротеза [6, 16]. При исследовании перипротезных тканей выявлено, что в этой области обнаруживается большое количество фагоцитов и макрофагов, которые известны как активаторы биосинтеза провоспалительных цитокинов, в том числе интерлейкинов (IL-1, IL-6), фактора некроза опухоли, индуцирующих формирование предшественников остеокластов и их дифференцировку. Кроме того, макрофаги, продуцируя интерлейкины, воздействуют на метаболизм ОБ, запуская механизм развития и активации ОК [1]. Активация клеток-предшественников ОК факторами, высвобождаемыми фагоцитами/макрофагами и активированными ОБ, суммарно обеспечивает механизм развития перипротезного остеолиза, резорбцию костной ткани и асептическое расшатывание эндопротеза [16].
Оптимизация интенсивности резорбции и костеобразования в костной ткани, прилежащей к эндопротезу, наиболее актуальна в течение первого года после тотального эндопротезирования, так как стрессовое ремоделирование, являясь реакцией приспособления кости к новым условиям, первоначально проявляется усилением остеолиза. Прогрессивная потеря костной ткани в период стрессового ремоделирования может сопровождаться асептической нестабильностью эндопротеза.
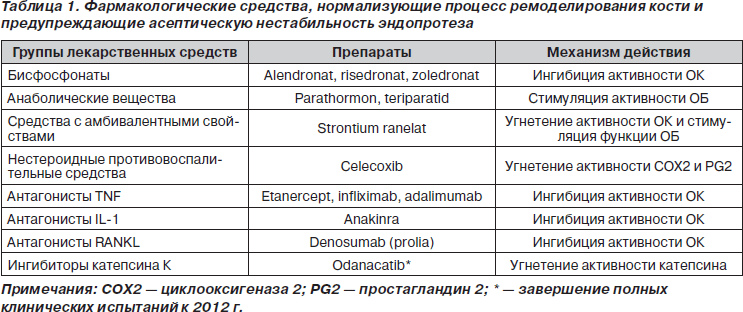
Интенсивность резорбции костной ткани, по мнению многих исследователей [1, 9, 16], является процессом, который можно регулировать различными фармакологическими средствами (табл. 1).
Традиционная патогенетическая терапия включает в свой арсенал препараты, замедляющие костную резорбцию (бисфосфонаты, эстрогены, кальцитонин), медикаменты, стимулирующие костеобразование (паратиреоидный гормон, фториды, андрогены, анаболические стероиды), и препараты многопланового действия (витамин D, статины). Фармакотерапевтическая эффективность этих групп лекарственных средств в достаточной степени представлена в обзорной работе O.V. Glubochenko и соавт. [12].
Результатом разработки новой концепции на основе современного представления о клеточно-молекулярном механизме развития ремоделирования кости стал синтез специфического человеческого моноклонального антитела (изотип иммуноглобулина IgG2; деносумаб, коммерческое наименование препарата рrolia) с высокой степенью аффинности к RANKL [35]. Он создан по технологии XenoMouse, позволяющей получать у мышей человеческие антитела взамен мышиных. В многочисленных лабораторных исследованиях, выполненных in vitro и in vivo, установлено, что деносумаб проявляет высокую способность ингибировать активность RANKL, в результате чего значительно замедляется и ослабляется процесс дифференцировки и активности ОК. Ингибиция активности ОК под воздействием деносумаба приводит к понижению степени резорбции костной ткани у экспериментальных животных [22]. Результаты, полученные при исследовании эффективности деносумаба в лабораторных условиях, получили подтверждение в клинических наблюдениях [27].
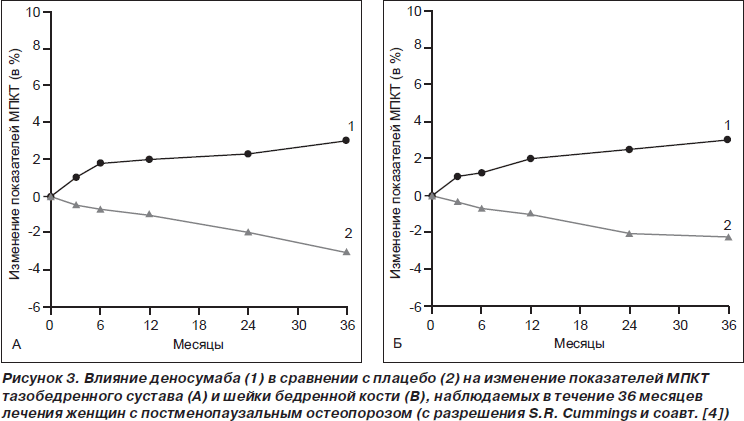
В результате проведенных клинических исследований [4] было доказано, что при назначении деносумаба в дозе 60 мг подкожно один раз в 6 месяцев эффективно подавляется костная резорбция у женщин в период менопаузы, увеличивается МПКТ и значительно снижается риск переломов костей (рис. 3). Данные рандомизированного плацебо-контролируемого изучения, направленного на оценку эффективности и безопасности деносумаба, полученные в наблюдениях 7868 женщин, больных верифицированным остеопорозом, показали снижение риска переломов позвонков на 68 %, переломов проксимального отдела бедренной кости — на 40 % по сравнению с группой лиц, получавших плацебо [4].
Проведенная терапия деносумабом в течение 36 месяцев (больные получали препарат один раз в 6 месяцев) сопровождалась повышением показателей МПКТ поясничного отдела позвоночника на 9,2 %, бедренной кости — на 6,0 %. Проведенное сравнение клинической эффективности деносумаба и алендроната зафиксировало преимущество деносумаба в плане более быстрого и существенного ингибирования процесса костной резорбции, а также значимого повышения показателей МПКТ на всех участках скелета в сравнении с алендронатом [3, 29]. В настоящее время клинически подтверждено, что деносумаб обладает благоприятным профилем долгoсрочной безопасности [23].
Другим потенциальным кандидатом в качестве средства для лечения нарушений процесса ремоделирования кости является оданакатиб (МК-0822) — непептидный ингибитор катепсина К, основного протеолитического фермента ОК. Катепсин К играет ключевую роль в тканевой деструкции, осуществляемой остеокластом, ремоделировании кости и деградации хряща [24]. При резорбции костной ткани после растворения гидроксиапатитов происходит расщепление органических компонентов матрикса с участием катепсина К. В результате действия этого фермента из полости резорбции кости в кровоток попадают большие фрагменты разрушенного коллагена, состоящие из N-телопептидов (NTX) и связанных с ними поперечных пиридиновых мостиков-сшивок, а также С-телопептидов коллагена типа 1 (СТХ). Установлено, что протеолитическая активность катепсина К наиболее высокая при низких значениях рН [24].
В предклинических экспериментах и клинических наблюдениях определена высокая и избирательная, ингибирующая функцию катепсина К способность оданакатиба [10]. При приеме препарата в дозе 50 мг внутрь еженедельно в течение 36 месяцев отмечалось снижение концентрации в плазме крови маркеров резорбции костной массы (СТХ и NTX) на 80 % в сравнении с исходными показателями. Прием оданакатиба 399 женщинами в постменопаузальном периоде с верифицированными признаками остеопороза в течение 36 месяцев понижал риск развития повторных нетравматических переломов проксимального отдела бедренной кости на 8,3 %, позвонков — на 10,7 %. Одновременно отмечалось повышение абсолютных показателей минеральной плотности костной массы шейки бедра и позвонков [34]. По данным American Society for Bone and Mineral Research (ASBMR), международное рандомизированное плацебо-контролируемое исследование, направленное на оценку клинической эффективности и безопасности оданакатиба, назначаемого для лечения и предотвращения переломов, должно завершиться к 2012 году.
Abu-Amer L., Darwech J., Clohisy J.C. Aseptic loosening of total joint replacements: mechanisms underlying osteolysis and potential therapies // Arthritis Res.Ther. — 2007. — Vol. 9 (Suppl. 1). — S. 6.
Bozic K.J.,Kurtz S.M., Lau E. et al. The epidemiology of revision total hip arthroplasty in the United States // J. Bone Joint Surg. Am. — 2009. — Vol. 91, № 1. — P. 128-133.
Brown J.P., Prince R.L., Deal Chad et al. Comparison of the effect of denosumab and alendronate on BMD and biochemical markers of bone turnover in postmenopausal women with low mass: a randomised, blindet, phase 3 trial // J. Bone Miner. Res. — 2009. — Vol. 24, № 1. — P. 153-161.
Cummings S.R., San Martin J., McClung M.R. et al. Denosumab for prevention of fractures in postmenopausal women with osteoporosis // N. Eng. J. Med. — 2009. — Vol. 361, № 8. — P. 756-765.
Drees P., Eckardt A., Gay S. et al. Molecular pathways in aseptic loosening of orthopaedic edoprothesis // Biomed. Technik. — 2008. — Vol. 53, № 3. — P. 93-103.
Drees P., Huber L.C. Molekulare und zellulдre Mechanismen der aseptischen Prothesenlockerung // Rheuma Nachrichten, Zьrich. — 2005. — № 37. — P. 12-17.
Dreinhofer K., Dieppe P., Sturmer T. et al. Indication for total hip replacement comparison of assessments orthopaedic surgeons and referring physicians // Ann. Rheum. Dis. — 2006. — Vol. 65, № 10. — P. 1346-1350.
Filippenko V.A., Deduch N.V., Schkodovskaja N.Y. et al. Clinical and morphological aspects of aseptic loosening of the hip endoprothesis // Orthop. Traumatol. Prosthetics. — 2009. — № 3. — P. 65-69.
Gallo J., Raska M., Mrazek F., Petrek M. Bone remodeling, particle disease and individual susceptibility to periprosthetic osteolysis // Physiol. Res. — 2008. — Vol. 57, № 3. — P. 339-349.
Gauthier J.Y., Chauret N., Cromlish W. et al. The discovery of odanacatib (MK-0822), a selective inhibitor of cathepsin K // Bioorg. Med. Chem. Lett. — 2008. — Vol. 18, № 3. — P. 923-928.
Gehrig L., Lane J., O’Connor M. Osteoporosis: manegment and treatment strategies for orthopaedic surgeons // J. Bone Joint Surgery. — 2008. — Vol. 90, № 6. — P. 1362-1374.
Glubochenko O.V., Glubochenko V.G., Zacharchuk T.V. Contemporary aspects of the treatment of osteoporosis // Clin. and Experim. Pathol. — 2010. — Vol. 9, № 4(34). — P. 137-146.
Hamdy N.A.T. Osteoprotegerin as a potential therapy for osteoporosis // Curr. Reumatol. Res. — 2006. — Vol. 8, № 1. — P. 50-54.
Hofbauer L., Rachner T. Die rolle RANK/RANKL/OPG-signalwegs in Knochenstoffwechsel // Forbildung Osteologie. — 2010. — Vol. 3, № 5. — P. 118-121.
Holding C.A., Findlay D.M., Stamenkov R. et al. The corellation of RANK, RANKL and TNFalpha expression with bone loss volume and polyethylene wear debris around hip implants // Biomaterials. — 2006. — Vol. 27, № 30. — P. 5212-5219.
Iolascon G., Di Pietro D., Capaldo A., Gloria C. Periprosthetic bone density as outcome of therapeutic response // Clin. Cases Miner. Bone Metab. — 2010. — Vol. 7, № 1. — P. 27-31.
Jakob F., Seefried L., Ebert R. Pathophysiology of bone methabolism // Internist. — 2008. — Vol. 49, № 10. — P. 1159-1169.
Kato S. Hormones and osteoporosis update. Estrogen and bone remodeling // Clin. Calcium. — 2009. — Vol. 19, № 7. — P. 951-956.
Kawamura N., Kugimiya F., Oshima Y. et al. Act 1 in osteoblasts and osteoclasts controls bone remodeling // PloS One. — 2007. — Vol. 2, № 10. — P. 1058-1062.
Kitaura H., Zhou P., Novack D.V. et al. M-CSF mediates TNF-induced inflammatory osteolysis // J. Clin. Invest. — 2005. — Vol. 115, № 12. — P. 3418-3427.
Kreutzer J., Schneider M., Schiegel U. et al. Cemented total hip arthroplasty in Germany — an update // Z. Orthop. Ihre Grenzgeb. — 2005. — Vol. 143, № 1. — P. 48-55.
Lewiecki E.M. Denosumab — an emerging treatment for postmenopausal osteoporosis // Expert. Opin. Biol. Ther. — 2010. — Vol. 10, № 3. — P. 467-476.
Moen M.D., Klam S.J. Denosumab: a review of its use in the treatment of menopausal osteoporosis // Drugs. Aging. — 2011. — Vol. 28, № 1. — P. 63-82.
Nagase Y., Tanaka S. Odanacatib (MK-0822) // Clin. Calcium. — 2011. — Vol. 21, № 1. — P. 59-62.
Pivonka P., Zimak J., Smith D.W. et al. Theoretical investigation of the role of the RANK-RANKL-OPG system in bone remodeling // J. Theoretical. Biol. — 2010. — Vol. 262, № 2. — P. 306-316.
Raggatt L.J., Partridge N.C. Cellular and molecular mechanisms of bone remodeling // J. Biol. Chem. — 2010. — Vol. 285, № 33. — P. 25103-25108.
Reid I.R., Miller P.D., Brown J.P. et al. Effects of denosumab on bone histomorphometry: the FREEDOM and STAND studies // J. Bone Miner. Res. — 2010. — Vol. 25, № 10. — P. 2256-2265.
Reves Garcia R., Munoz-Torres M. Cathepsin K: biological aspects and therapeutic possibilities // Med. Clin. (Barc.). — 2008. — Vol. 131, № 6. — 218-220.
Rodionova S.S., Klyushnichenko I.V. The impact of osteoporosis on periprosthetic bone mineral density // Calcif. Tissze Int. — 2007. — Vol. 8, № 1. — P. 145.
Schцnert M., Mayer-Wagner S., Mayer W. et al. Use of (18)F-FDG-Pet in the diagnosis of endoprosthetic loosing of knee and hip implantants // Arch. Orthop. Trauma Surg. — 2010 — Vol. 130, № 10. — P. 1231-1238.
Singh J.A. Epidemiology of knee and hip arthroplasty: a systematic review // Open Orthopaedics J. — 2011. — Vol. 5, № 1. — P. 80-85.
Skutek M., Bourne R.B., MacDonald S.J. International epidemiology of revision THR // Orthoped. Trauma. — 2006. — Vol. 20, № 3. — P. 157-161.
Steel N., Melzer D., Gardner E. et al. Need for and receipt of hip and knee replacement — a national population survey // Pharmacology (Oxford). — 2006. — Vol. 45, № 11. — P. 1437-1441.
Stoch S.A., Wagner J.A. Cathepsin K inhibitors: a novel target for osteoporosis therapy // Clin. Pharmacol. Ther. — 2008. — Vol. 83, № 1. — P. 172-176.
Suigimoto T. Anti-RANKL monoclonal antibody denosumab (AMG 162) // Clin. Calcium. — 2011. — Vol. 21, № 1. — P. 46-51.
Tanaka J., Nakayamada S., Okada Y. Osteoblasts and osteoclasts in bone remodeling and inflammation // Curr. Grug Target Inflam. Allergy. — 2005. — Vol. 4, № 3. — P. 325-328.
Umland E.M. An update on osteoporosis epidemiology and bone physiology // Univer. Tennessee Adv. Stud. Pharmacy. — 2008. — Vol. 5, № 7. — P. 210-214.
Vega D., Maalouf N.M., Sakhaee K. Clinical review: the role of receptor activator of nuclear factor-kappa B (RANK)/RANK ligand/osteoprotegerin: clinical implications // J. Clin. Endocrinol. Metab. — 2007. — Vol. 92, № 12. — P. 4514-4521.
Wadas T.J., Deng H., Sprague J.E., Zheleznyak A. et al. Targeting the avb3 integrin for small-animal PET/CT of osteolytic bone metastases // J. Nucl. Med. — 2009. — Vol. 50, № 11. — P. 1873-1880.
Wagner D., Fahrleitner-Pammer A. Levels of osteoprotegerin (OPG) and receptor activator for nuclear factor kappa B ligand (RANKL) in serum: are they of any help? // Wien. Med. Wochenschr. — 2010. — Vol. 160, № 17–18. — P. 452-457.