Журнал «Здоровье ребенка» 3 (38) 2012
Вернуться к номеру
Эволюция ювенильного анкилозирующего спондилоартрита
Авторы: Прохоров Е.В., Тов И.В., Яковленко А.Ю., Синяченко О.В., Антонова Л.Н., Донецкий национальный медицинский университет им. М. Горького
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Эволюции ювенильного анкилозирующего спондилоартрита в последующем свойственно более частое вовлечение в патологический процесс локтевых и голеностопных суставов, развитие энтезопатий, изменений интраартикулярных рогов менисков, формирование кист Бейкера, хондромных тел и системного остеопороза, а сумма значимости перечисленных признаков превышает аналогичную у пациентов с дебютом болезни во взрослом возрасте в 13 раз, но при этом для ювенильного анкилозирующего спондилоартрита менее характерно поражение позвоночника. Наблюдается возрастной диморфизм результатов использования отдельных групп медикаментозных препаратов и физиотерапевтических средств.
More frequent involvement of elbow and ankle joints, development of enthesopathies, changes in intraarticular meniscal horns, forming of Baker’s cyst, cartilage flaps and systemic osteoporosis are peculiar to juvenile ankylosing spondylitis evolution, and the sum of significance of these signs exceeds 13 times the same in patients with onset in adult stage, but the spine injury is less peculiar to juvenile ankylosing spondylitis. Age dimorphism of results of several drug groups and physiotherapeutic measures is observed.
Еволюції ювенільного анкілозуючого спондилоартриту в подальшому притаманне більш часте втягування в патологічний процес ліктьових і гомілковостопних суглобів, розвиток ентезопатій, змін інтраартикулярних рогів менісків, формування кіст Бейкера, хондромних тіл і системного остеопорозу, а сума значущості перерахованих ознак перевищує аналогічну в пацієнтів із дебютом хвороби в дорослому віці в 13 разів, але при цьому для ювенільного анкілозуючого спондилоартриту менш характерне ураження хребта. Спостерігається віковий диморфізм результатів використання окремих груп медикаментозних препаратів та фізіотерапевтичних засобів.
Ювенильный спондилоартрит, течение, эволюция.
juvenile spondylitis, course, evolution.
ювенільний спондилоартрит, течія, еволюція.
Введение
Анкилозирующий спондилоартрит (АС) относится к тем ревматическим системным заболеваниям, которые наносят огромный медико-социальный и экономический ущерб любому государству [10, 13], значительно ухудшают качество жизни больных в связи с быстрой утратой ими трудоспособности уже в юношеском возрасте [5, 6]. В Украине за счет некачественной диагностики распространенность АС не превышает 3–4 случаев на 10 000 взрослого населения, причем в некоторых областях она еще ниже [1], тогда как в мире АС страдают 50–200 человек на 10 тыс. [7, 9, 14]. Нужно подчеркнуть, что за последние годы в нашей стране все-таки наблюдается рост численности таких больных [2, 3].
Ежегодно повышается интерес исследователей к возрастным особенностям течения заболевания [4], в том числе к проблеме эволюции ювенильного АС [8], но эти вопросы остаются малоизученными. Считается, что формирование ювенильного АС в дебюте болезни относится к прогнознегативным факторам дальнейшего развития патологического процесса [11, 12].
Можно предположить, что выяснение возрастных особенностей течения и эффективности терапии больных АС будет способствовать повышению качества ранней диагностики заболевания, разработке прогностических критериев и рациональной медицинской технологии индивидуальных лечебных мероприятий. Целью и задачей данной работы стала оценка особенностей эволюции клинических, рентгенологических, сонографических и денситометрических признаков течения ювенильного АС, а также эффективности проводимых патогенетических лечебных мероприятий.
Материал и методы
Обследованы 279 больных АС, среди которых было 92 % мужчин и 8 % женщин в возрасте 38,0 ± 0,7 года. Обследованных пациентов в возрасте до 20 лет было 5 %, 20–30 лет — 23 %, 31–40 лет — 30 %, 41–50 лет — 27 %, старше 50 лет — 15 %. Длительность заболевания от первых признаков его манифестации составила 12,0 ± 0,5 года. I и III степень активности АС констатированы в 32 % от общего числа больных, II — в 36 %. Мы распределили обследованных пациентов на две группы — 1-ю (основную), у которых заболевание началось в детском возрасте, и 2-ю (контрольную), куда вошли остальные пациенты с манифестацией АС после 18 лет. В основной группе оказалось 22 % больных в возрасте 28,0 ± 1,3 года, а в контрольной — 78 % в возрасте 41,0 ± 0,7 года (p < 0,001). В дебюте болезни возраст представителей 1-й группы составил 14,0 ± 0,5 года, а 2-й — 29,0 ± 0,6 года. Основная и контрольная группы мало отличались по степени активности патологического процесса.
Поражение грудино-ключичных суставов обнаружено у 4 % от общего числа больных АС, верхнечелюстных — в 5 % случаев, межфаланговых кистей и стоп — по 8 %, пястно-фаланговых, плюснефаланговых и локтевых — по 9 %, лучезапястных — в 10 %, плечевых и тазобедренных — по 36 %, голеностопных — в 14 %, коленных — в 51 %, крестцово-подвздошных — в 95 %, шейного отдела позвоночника — в 65 %, грудного — в 74 %, поясничного — в 87 %. Периферический полиартрит выявлен в 52 % наблюдений, односторонний или двусторонний асимметричный сакроилеит установлен у 25 % от общего числа больных и у 26 % пациентов с поражением крестцово-подвздошных сочленений, двусторонний симметричный — соответственно в 59 и 62 %, анкилозирование этих суставов — по 11 % случаев.
Среди обследованных больных АС тендовагиниты и остеофитоз наблюдались в 28 % случаев, энтезопатии — в 27 %, сужение суставных щелей — в 60 %, субхондральный склероз — в 45 %, остеокистоз — в 35 %, остеоузуры — в 12 %, суставные подвывихи — в 4 %, артикулярные кальцинаты и системный остеопороз — по 23 %, изменения рогов менисков — в 41 %, кисты Бейкера — в 21 %, тела Пеллегрини — Штиды — в 11 %, хондромные тела — в 18 %, тела Гоффа — в 10 %, асептические некрозы костей — в 5 %, эпифизарный остеопороз — в 32 %.
Пациентам выполняли рентгенографию периферических суставов, крестцово-подвздошных сочленений и позвоночника (аппарат Multix-Compact, Siеmens, Германия), артросонографию (аппарат Envisor, Philips, Нидерланды), двухэнергетическую рентгеновскую денситометрию проксимального отдела бедренной кости (аппарат QDR-4500-Delphi, Hologic, США), электрокардиографию (аппараты «МІДАК-ЕК1Т», Украина, и Fukuda Denshi Cardimax-FX326, Япония), эхокардиографию (аппарат Acuson Aspen, Siemens, Германия).
96 % от числа обследованных больных получали в комплексном лечении различные нестероидные противовоспалительные препараты, 34 % — глюкокортикоидные гормоны per os и 15 % — интраартикулярно, 9 % — метотрексат, 57 % — сульфасалазин, 11 % — плаквенил, 19 % — полиферментные смеси системной энзимотерапии (вобэнзим, флогэнзим), 47 % — миорелаксанты (мидокалм, сирдалуд), 13 % — хондромодификаторы (структум, терафлекс, зинаксин), 12 % — антиостеопорозные средства (кальцемин, ранелат стронция), 44 % — магнитотерапию, 18 % — лазеротерапию, 15 % — электрофорез со смесью Парфенова, 12 % — ультравысокочастотную терапию, 9 % — дециметроволновую сверхвысокочастотную терапию, 20 % — сантиметроволновую сверхвысокочастотную терапию. Результаты лечебных мероприятий оценивали спустя 3–23 недели от начала обследования в клинике (в среднем через 11,0 ± 1,2 недели). Под «значительным улучшением» понимали исчезновение жалоб больных и изменений со стороны легких и центральной нервной системы, уменьшение активности патологического процесса на две степени. Обязательным критерием «улучшения» было уменьшение активности заболевания.
Статистическая обработка полученных результатов исследований проведена с помощью компьютерного вариационного, корреляционного, одно- (ANOVA) и многофакторного (ANOVA/MANOVA) дисперсионного анализа (программы Microsoft Excel и Statistica StatSoft, США). Оценивали средние значения (M), их стандартные ошибки (SD), коэффициенты корреляции, критерии дисперсии (D), Стьюдента, Уилкоксона — Рао, Макнемара — Фишера и достоверность статистических показателей (р). Высчитывали также чувствительность, специфичность и значимость отдельных признаков.
Результаты
По данным ANOVA, возраст больных в дебюте заболевания достоверно влияет на частоту поражения локтевых и тазобедренных суставов, а также грудного и поясничного отделов позвоночника. Основная и контрольная группы больных отличаются между собой по частоте воспаления локтевых и голеностопных суставов, сочленений шейного и грудного отделов позвоночника. Перечисленные периферические суставы соответственно в 2,4 и в 7,9 раза чаще вовлекаются в патологический процесс, когда заболевание начинается в детском возрасте, а указанные отделы позвоночника — на 16 и 25 % реже. В результате анализа полученных данных установлено, что эволюционный диморфизм ювенильного АС характеризуется частотой поражения локтевых суставов и грудного отдела позвоночника.
Если у больных основной группы односторонний или двусторонний асимметричный сакроилеит обнаружен в 33 % наблюдений, а двусторонний симметричный в 63 %, то в контрольной — соответственно в 23 и 72 % (различия недостоверны). Необходимо подчеркнуть, что 1-я и 2-я группы также не отличаются между собой по частоте анкилозирования крестцово-подвздошных сочленений (соответственно 8 и 11 %).
В случаях начала болезни в детском возрасте после 18 лет наблюдается достоверно меньшая распространенность поражения позвоночника по сравнению с остальными пациентами, составляющая соответственно 1,870 ± 0,125 и 2,340 ± 0,058. Эволюция болезни с ювенильного АС характеризуется особенностями последующей интегральной тяжести спондилопатии, о чем свидетельствует ANOVA/MANOVA. По данным однофакторного дисперсионного анализа, развитие болезни в детском возрасте определяет выраженность изменений грудного отдела, но не шейного и поясничного. Вместе с тем существуют прямые корреляционные связи тяжести спондилопатии с возрастом детей в дебюте болезни, что относится к шейному, грудному и поясничному отделам позвоночника.
Однофакторный дисперсионный анализ показывает слабое влияние возраста больных в начале заболевания на последующие показатели метакарпального индекса Барнетт — Нордина и индекса минеральной плотности кости. Вместе с тем нужно отметить, что если средние показатели метакарпального индекса у больных основной группы составляют 0,430 ± 0,008 у.е., то в контрольной — 0,450 ± 0,004 у.е. (p = 0,016). В свою очередь, параметры минеральной плотности кости в этих группах мало отличались между собой (соответственно –1,550 ± 0,149 SD и –1,230 ± 0,088 SD).
Эффективность лечения больных основной и контрольной групп практически не разнится. По данным однофакторного дисперсионного анализа, на результаты терапии, независимо от возраста, оказывает существенное влияние применение интраартикулярных глюкокортикоидных гормонов, полиферментных смесей системной энзимотерапии и лазеротерапии.
Обсуждение результатов
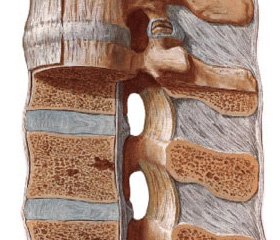
Начало заболевания в ювенильном возрасте оказывает достоверное воздействие на наличие в артикулярных тканях кальцинатов и хондромных тел (рис. 1), о чем свидетельствует дисперсионный анализ. В случаях эволюции АС из ювенильного в 2,2 раза чаще регистрируется развитие энтезопатий во взрослом возрасте, на 24 % больше — изменений рогов менисков, на 23 % — кист Бейкера и интраартикулярных хондромных тел, в 2,4 раза — системного остеопороза. В процессе анализа полученных данных сделано следующее заключение, характеризующее АС, начавшийся в детском возрасте: сумма диагностической значимости таких признаков, как поражение локтевых и голеностопных суставов, развитие энтезопатий, изменений рогов менисков, формирование кист Бейкера, хондромных тел и системного остеопороза, составляет 149,39 %, тогда как в контрольной группе с дебютом во взрослом возрасте — только 11,22 %, т.е. в 13,3 раза меньше.
/042/042_1.jpg)
Дисперсионный анализ свидетельствует о том, что использование сульфасалазина, миорелаксантов, хондромодификаторов и магнитов целесообразно у пациентов с манифестацией АС во взрослом возрасте. Больным после ювенильного АС показаны внутрисуставные введения глюкокортикоидных гормонов, системная энзимо- и лазеротерапия, а остальным пациентам целесообразно дополнительное назначение сульфасалазина, миорелаксантов и хондромодификаторов. Подчеркнем, что наличие анкилозирующего сакроилеита, но только у больных с дебютом АС в детском возрасте, негативно сказывается на результатах патогенетической терапии.
По данным дисперсионного анализа, на результаты лечения больных АС влияет наличие субхондрального склероза и остеокистозa, хотя сказанное относится лишь к пациентам с развитием заболевания после 18 лет. В общей группе обследованных отмечается достоверное воздействие на эффективность терапевтических мероприятий изменений со стороны перикарда, функционального класса сердечной недостаточности (ФКСН) и наличия смешанного типа нарушений функции внешнего дыхания. Если признаки перикардита негативно влияют на результаты лечения и в основной, и в контрольной группе, то от ФКСН и смешанного типа нарушений респираторной функции зависит эффективность лечения только у больных с дебютом болезни во взрослом возрасте.
При эволюции заболевания после ювенильного АС на результаты лечения влияют исходные показатели минеральной плотности кости, а в случаях более позднего развития болезни — поражение почек (мезангиопролиферативный IgA-гломерулонефрит, интерстициальный нефрит, амилоидоз) и центральной нервной системы (дисциркуляторная энцефалопатия, астеновегетативный, кортико-нуклеарный, пирамидный, псевдобульбарный и эпилептиформный синдромы, корковая и мозжечковая атаксия), а также гипертрофия миокарда правого желудочка сердца и дилатация его полости. Нами установлено, что прогнознегативным критерием эффективности лечения пациентов с манифестацией болезни во взрослом возрасте являются параметры легочного сосудистого сопротивления более 230 дин ґ см ґ сек–5 (> M + SD больных).
Выводы
1. Эволюции АС детского возраста в последующем свойственно более частое вовлечение в патологический процесс локтевых и голеностопных суставов, развитие энтезопатий, изменений рогов менисков, формирование кист Бейкера, хондромных тел и системного остеопороза, а сумма диагностической значимости перечисленных признаков превышает аналогичную у пациентов с дебютом болезни во взрослом возрасте в 13 раз, но при этом для ювенильного АС менее характерно поражение позвоночника.
2. Наблюдается возрастной диморфизм результатов использования отдельных групп медикаментозных препаратов и физиотерапевтических средств, но влияние на эффективность лечения эволюции болезни из ювенильного АС отсутствует, а в случаях дебюта патологического процесса во взрослом возрасте отмечается связь эффекта терапевтических мероприятий с характером поражения сердца, почек, легких и центральной нервной системы.
3. Представленные данные будут полезны для ранней диагностики отдельных признаков болезни у пациентов разных возрастных групп и проведения наиболее оптимальной патогенетической терапии, а также для повышения качества диспансерного наблюдения за такой категорией пациентов.
1. Головач І.Ю. Анкілозуючий спондилоартрит (хвороба Бєхтєрєва) // Лікування та діагностика. — 2009. — № 3. — С. 42-53.
2. Масик О.М. Анкілозивний спондилоартрит (хвороба Бехтерева) / О.М. Масик, М.І. Швед, Н.І. Козій. — Тернопіль: ТДМУ, 2007. — 308 с.
3. Панін А.В. Внутрішньосерцева і легенева гемодинаміка у хворих на анкілозивний спондилоартрит // Укр. ревматол. журн. — 2008. — Т. 34, № 4. — С. 73-77.
4. Aggarwal R. Clinical characteristics of patients with ankylosing spondylitis in India / R. Aggarwal, A.N. Malaviya // Clin. Rheumatol. — 2009. — Vol. 28, № 10. — P. 1199-1205.
5. Bergman M.J. Social and economic impact of inflammatory arthritis // Postgrad. Med. — 2006, Spec. No. — P. 5-11.
6. Boonen A. The burden of ankylosing spondylitis / A. Boonen, S.M. van der Linden // J. Rheumatol. Suppl. — 2006. — Vol. 78. — P. 4-11.
7. Burgos-Vargas R. Epidemiology of spondyloarthritis in Mexico / R. Burgos-Vargas, I. Pelaez-Ballestas // Am. J. Med. Sci. — 2011. — Vol. 341, № 4. — P. 298-300.
8. Colbert R.A. Classification of juvenile spondyloarthritis: Enthesitis-related arthritis and beyond // Nat. Rev. Rheumatol. — 2010. — Vol. 6, № 8. — P. 477-485.
9. Evans D.M. Interaction between ERAP1 and HLA-B27 in ankylosing spondylitis implicates peptide handling in the mechanism for HLA-B27 in disease susceptibility / D.M. Evans, C.C. Spencer, J.J. Pointon, Z. Su // Nat. Genet. — 2011. — Vol. 43, № 8. — P. 761-767.
10. Healey E.L. Impact of ankylosing spondylitis on work in patients across the UK / E.L. Healey, K.L. Haywood, K.P. Jordan, A. Garratt // Scand. J. Rheumatol. — 2011. — Vol. 40, № 1. — P. 34-40.
11. Jang J.H. Ankylosing spondylitis: patterns of radiographic involvement — a re-examination of accepted principles in a cohort of 769 patients / J.Y. Jang, M.M. Ward, A.N. Rucker, J.D. Reveille // Radiology. — 2011. — Vol. 258, № 1. — P. 192-198.
12. Sonkar G.K. Is HLA-B27 a useful test in the diagnosis of juvenile spondyloarthropathies? / G.K. Sonkar, S.S. Usha // Singapore Med. J. — 2008. — Vol. 49, № 10. — P. 795-799.
13. Torres T.M. Resource utilisation and cost of ankylosing spondylitis in Brazil / T.M. Torres, M.B. Ferraz, R.M. Ciconelli // Clin. Exp. Rheumatol. — 2010. — Vol. 28, № 4. — P. 490-497.
14. Zochling J. Seronegative spondyloarthritis / J. Zochling, E.U. Smith // Best Pract. Res. Clin. Rheumatol. — 2010. — Vol. 24, № 6. — P. 747-756.

/042/042_2.jpg)