Журнал «Здоровье ребенка» 6 (41) 2012
Вернуться к номеру
Экстрасистолия у детей
Авторы: Пшеничная Е.В., Донецкий национальный медицинский университет им. М. Горького
Рубрики: Педиатрия/Неонатология
Разделы: Медицинское образование
Версия для печати
Актуальность проблемы
Аритмия сердца — одно из наиболее распространенных проявлений болезней сердца и других патологических состояний вне сердечно-сосудистой системы. Экстрасистолия (ЭС) является самым частым нарушением ритма у детей. Согласно данным литературы и собственным наблюдениям, в структуре аритмий она достигает 75 % (Школьникова М.А., 2006; Пшеничная Е.В., 2008), при этом отмечается ее рост за последние десятилетия (Макаров Л.М., 1998; Куприянова О.О., Осколкова М.К., 2004; Нагорная Н.В. с соавт., 2012). Экстрасистолы обнаруживают у детей всех возрастов, включая новорожденных; их выявляют даже пренатально. В ряде случаев ЭС выявляется у здоровых лиц, в том числе занимающихся спортом. В патогенезе экстрасистолической аритмии нередко участвуют различные электрофизиологические феномены, сложным образом сочетающиеся между собой, при взаимном влиянии центральной и вегетативной нервной системы, опосредованном участии других факторов. Вид экстрасистолии в большинстве случаев не позволяет судить о ее клиническом значении и прогнозе у конкретного больного. В связи с этим выбор лечебно-профилактических мероприятий часто оказывается наиболее сложной проблемой, стоящей перед врачом при ведении больного с экстрасистолией.
Общая цель: уметь диагностировать и определить тактику ведения ребенка с экстрасистолией.
Конкретные цели: выделить основные клинические и электрокардиографические признаки экстрасистолии, составить план обследования пациента с экстрасистолией, поставить наиболее вероятный клинический диагноз, определить план лечебно-профилактических мероприятий.
Содержание обучения
Теоретические вопросы
1. Определение экстрасистолии.
2. Этиопатогенез экстрасистолии у детей.
3. Клинико-электрокардиографические признаки экстрасистолии у детей.
4. Современные методы обследования детей с экстрасистолией.
5. Принципы лечения экстрасистолии в детском возрасте.
6. Прогноз клинического течения экстрасистолии у детей.
Ориентировочная основа деятельности
Во время подготовки к занятию необходимо ознакомиться с основными теоретическими вопросами с использованием предложенных источников литературы.
Определение экстрасистолии. Классификация нарушений ритма сердца у детей
Экстрасистола (лат. extra вне + греч. systolē сокращение, сжатие) — нарушение ритма сердца, характеризующееся одиночными или парными преждевременными сокращениями (экстрасистолами) всего сердца или какого-либо его отдела (предсердий или желудочков) в результате возбуждения миокарда, возникшего от импульса, исходящего не из физиологического источника сердечного ритма (синусового узла), а из другого участка миокарда или проводящей системы сердца (гетеротопный источник аритмии).
МКБ Х содержит следующие шифры:
— I 49 — другие нарушения сердечного ритма;
— I 49.1 — преждевременная деполяризация предсердий;
— I 49.2 — преждевременная деполяризация, исходящая из соединения;
— I 49.3 — преждевременная деполяризация желудочков;
— I 49.4 — другая и неуточненная деполяризация.
Этиопатогенез экстрасистолии у детей
Экстрасистолы могут быть врожденными и приобретенными; этиологически обусловленными кардиальными, экстракардиальными и сочетанными факторами.
К кардиальным причинам аритмии относятся врожденные и приобретенные пороки сердца, первичная и вторичная кардиомиопатия, ревмокардит, инфекционный эндокардит, неревматический кардит и другая внутрисердечная патология.
Доказано более частое наличие экстрасистолии у детей с пролапсом митрального клапана и другими малыми структурными аномалиями сердца в сравнении с детьми без таковых.
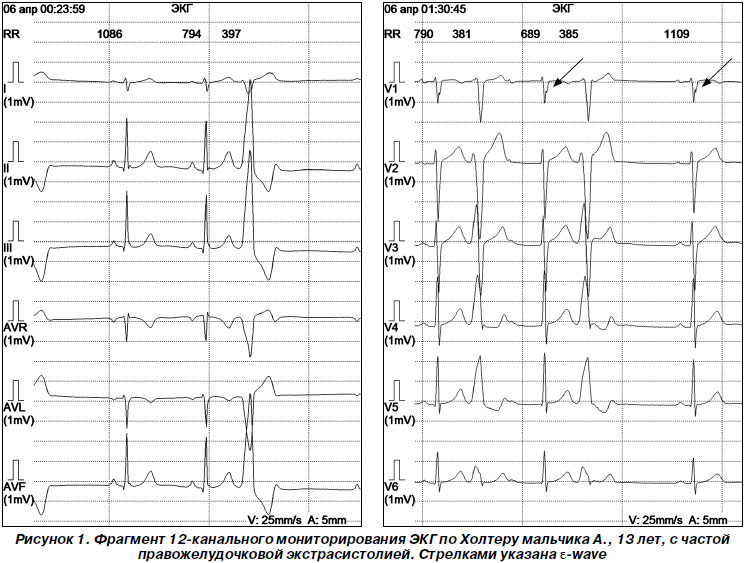
Особую этиологическую группу составляют генетически детерминированные заболевания, при которых аритмии (желудочковая ЭС, желудочковая тахикардия) являются основным клиническим проявлением. Это аритмогенная дисплазия правого желудочка (АДПЖ) — патология мышцы сердца, преимущественно генетически детерминированная, характеризующаяся фиброзно-жировым замещением миокарда правого желудочка, которое может быть как минимальным, выявляемым только при гистологическом исследовании, так и выраженным, с разной степенью вовлеченности в процесс межжелудочковой перегородки и миокарда левого желудочка (Basso C., Corrado D., Marcus F., 2009; Бокерия Л.А., Ревишвили А.Ш., Неминущий Н.М., 2011). В половине случаев заболевание носит семейный характер и является частой причиной внезапной сердечной смерти.
АДПЖ необходимо исключать у каждого больного, имеющего моно- или политопную желудочковую ЭС. В настоящее время для диагностики АДПЖ используют критерии Marcus F. (2010), основанные на данных электрокардиографии, эхокардиографии, МРТ, вентрикулографии, гистологического исследования. Важным ЭКГ-критерием АДПЖ является наличие эпсилон-волны (e-wave) у больных с желудочковыми нарушениями ритма сердца. Эпсилон-волна — это воспроизводимые малоамплитудные сигналы между конечной частью QRS и началом Т в правых грудных отведениях (рис. 1).
Экстрасистолы могут наблюдаться при заболеваниях нервной и эндокринной системы (сахарный диабет, тиреотоксикоз, гипотиреоз), острых и хронических инфекционных процессах, интоксикации, передозировке или неадекватной реакции на лекарственные препараты, дефиците некоторых микроэлементов, в частности магния, калия, селена. До настоящего времени имеются указания на роль очагов хронической инфекции, в частности хронического тонзиллита, в генезе экстрасистолии, однако она до конца не доказана.
Установлено, что ЭС может быть проявлением висцеро-висцеральных рефлексов при холецистите, болезнях гастродуоденальной зоны, гастроэзофагеальном рефлюксе, диафрагмальной грыже и др.
Появление ЭС после выраженных эмоциональных и физических перегрузок объясняют повышением концентрации катехоламинов в крови. На генез экстрасистолии влияют также вегетативная дисфункция и психогенные изменения.
В этиологии ЭС доказана существенная роль перинатальной патологии (неблагоприятное течение беременности и родов, недоношенность, внутриутробная гипотрофия, инфекции плода), приводящей к нарушению морфогенеза и функциональной незрелости проводящей системы сердца. Перинатальные повреждения ЦНС способны нарушить нейровегетативную регуляцию ритма с изменением взаимоотношений симпатических и парасимпатических влияний вегетативной нервной системы, вследствие чего возникает электрическая нестабильность миокарда и проводящей системы сердца, а также снижаются функциональные резервы адаптации симпатоадреналового звена регуляции сердечного ритма.
В тех случаях, когда причину ЭС выявить не удается, ее относят к идиопатической.
Клинико-электрокардиографическая характеристика экстрасистолии у детей
Экстрасистолия у детей нередко протекает бессимптомно, что не позволяет точно установить время ее появления. По нашим данным, около 70 % случаев аритмии выявляют случайно родители или медицинский персонал во время профилактических осмотров или в связи с переносимой или перенесенной респираторной инфекцией. Действительно, доказана связь НРС и респираторных инфекций, что обусловлено возможным наличием кардита, вегетативной дисфункции с гиперактивностью трофотропного аппарата в ранний период реконвалесценции, когда преобладает тонус вагуса на фоне снижения активности симпатоадреналового отдела.
Согласно нашим наблюдениям, многие больные не предъявляют жалоб и не знают о существовании у них ЭС, пока их не информирует об этом врач. При наличии жалоб у ребенка с ЭС наиболее частыми из них являются ощущение перебоев в работе сердца, чувство замирания в сердце, напоминающее ощущение при быстром снижении самолета или в начале движения вниз скоростного лифта; чувство кратковременной (1,0–1,5 с) остановки сердца с последующим ощущением сильного удара сердца в грудную стенку (постэкстрасистолическая потенциация). Иногда описанные ощущения сопровождаются кратковременной (1–2 с) острой болью в области верхушки сердца. В препубертатном и пубертатном периоде нарушения ритма сердца, в том числе экстрасистолия, могут иметь яркую эмоциональную окраску, обусловленную психовегетативными изменениями, и сопровождаться другими кардиальными и экстракардиальными жалобами: болями в области сердца, повышенной возбудимостью, нарушениями сна, метеочувствительностью. Такие проявления, как головокружение, слабость, отмечаются лишь при экстрасистолической аритмии на фоне тяжелого поражения сердца с расстройством гемодинамики.
Аускультативно экстрасистола воспринимается как громкий тон или как два близко отстоящих друг от друга тона, интенсивность первого из которых усилена, а второго — резко ослаблена. Эти тоны возникают в диастоле преждевременно и сопровождаются компенсаторной паузой. Выслушиваемые над сердцем шумы при экстрасистоле иногда исчезают (вследствие недостаточного наполнения желудочков кровью); в ряде случаев, напротив, шум выслушивается только во время экстрасистолического сокращения, что свидетельствует о возникновении турбулентного потока крови в аорте в момент экстрасистолы. Вставочные экстрасистолы аускультативно распознаются как преждевременные сокращения, не сопровождающиеся компенсаторной паузой. При частых политопных экстрасистолах физикальное исследование не всегда позволяет констатировать данное нарушение ритма.
Иногда в момент возникновения экстрасистолы отмечается толчкообразное набухание шейных вен; после экстрасистолы нередко можно видеть или пальпировать единичный усиленный сердечный толчок (следствие постэкстрасистолической потенциации). Выявляются выпадения пульсовых ударов, соответствующие гемодинамически неэффективным ранним экстрасистолам, или преждевременные ослабленные пульсовые удары (при относительно гемодинамически эффективных поздних экстрасистолах), сопровождающиеся удлиненной (компенсаторной) паузой, после которой следует несколько усиленный пульсовый удар. Бигеминия нередко проявляется брадисфигмией, когда до пальпируемой артерии доходят только пульсовые удары, вызванные нормальными сокращениями сердца.
Верификацию ЭС проводят на основании показателей ЭКГ.
Экстрасистолы классифицируются по локализации, степени преждевременности, частоте, последовательности, компенсаторной паузе, а также по особенностям их лабильности при функциональных пробах.
В зависимости от места расположения очага эктопической активности экстрасистолы делят на предсердные, атриовентрикулярные (предсердно-желудочковые, узловые) и желудочковые. В редких случаях наблюдается синусовая экстрасистолия, при которой преждевременное возбуждение возникает в физиологическом водителе ритма сердца — синусово-предсердном узле.
Одним из основных электрокардиографических критериев ЭС является укороченная диастола перед ЭС и компенсаторная пауза после нее. Форма эктопического комплекса зависит от места возникновения ЭС.
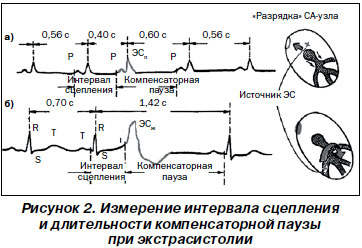
При экстрасистолах, возникающих в желудочках сердца, интервал между пре- и постэкстрасистолическими сокращениями сердца обычно равен времени двух нормальных сердечных циклов; такую компенсаторную паузу называют полной. Компенсаторная пауза после предсердных и предсердно-желудочковых (атриовентрикулярных) экстрасистол короче, чем после желудочковых — неполная компенсаторная пауза (рис. 2).
Предсердная экстрасистолия характеризуется следующими электрокардиографическими признаками:
— преждевременное возникновение и деформация предсердного зубца Р;
— наличие зубца Р перед комплексом QRS;
— морфология и/или полярность зубца Р в ЭС отличается от синусового: для левопредсердной локализации экстрасистолы характерны отрицательные зубцы Р во всех стандартных и левых грудных отведениях; при ЭС из средних и нижних отделов правого предсердия появляется отрицательный Р в отведениях II, III, aVF и положительный зубец Р в I стандартном отведении;
— PR в предсердных ЭС может быть укороченным, удлиненным и нормальным;
— желудочковый комплекс экстрасистолы по конфигурации и продолжительности не отличается от желудочковых комплексов основного ритма;
— компенсаторная пауза неполная, но при аберрантном QRS может быть полной.
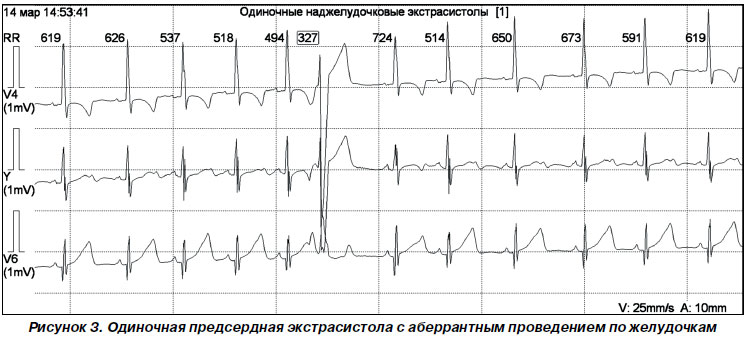
Иногда экстрасистолический комплекс QRST деформируется вследствие аберрантного проведения по желудочкам (если к моменту возникновения экстрасистолы внутрижелудочковая проводимость не восстановилась полностью), напоминая желудочковую экстрасистолу. В таких случаях экстрасистолический зубец Р нередко наслаивается на зубец Т предшествующего нормального комплекса (Т + Р), вызывая его деформацию (рис. 3).
Атриовентрикулярная экстрасистолия по изменениям QRS соответствует предсердной (поэтому их объединяют под общим названием наджелудочковых, или суправентрикулярных, экстрасистол), но отличается от последней изменениями зубца Р, который всегда инвертирован и занимает по отношению к желудочковому комплексу различное положение в зависимости от того, из какой части атриовентрикулярного соединения (верхней или нижней) исходят экстрасистолы. При экстрасистоле, исходящей из верхней части атриовентрикулярного соединения, инвертированный зубец Р предшествует QRS, при этом интервал РQ меньше 0,12 с. При экстрасистоле из нижней части атриовентрикулярного соединения, примыкающей к узлу, зубец Р может наслаиваться на ее желудочковый комплекс, несколько деформируя последний, или регистрироваться сразу вслед за экстрасистолическим желудочковым комплексом (рис. 4).
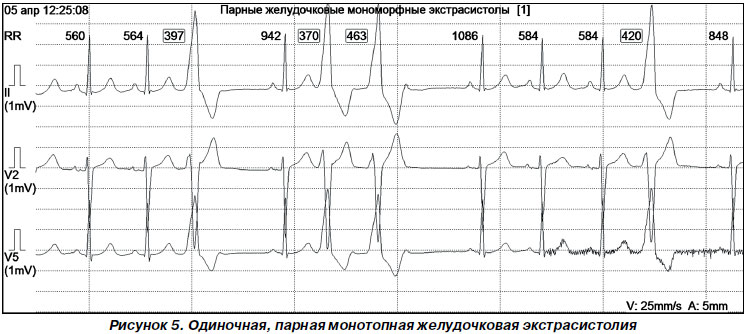
Желудочковая экстрасистолия характеризуется следующими электрокардиографическими признаками (рис. 5):
— зубец Р, предшествующий экстрасистоле, отсутствует (импульс не доходит ретроградно до предсердий) или инвертирован и регистрируется после желудочкового комплекса;
— значительное различие формы желудочкового комплекса экстрасистолы и желудочковых комплексов основного ритма — выраженная деформация и расширение желудочкового комплекса QRS. Комплекс QRS по продолжительности превышает возрастные параметры (более 60 мс у детей до 1 года, более 90 мс у детей от 1 года до 3 лет, более 100 мс у детей 3–10 лет, более 120 мс у детей старше 10 лет);
— расположение сегмента RS-T и зубца Т дискордантно направлению основных зубцов комплекса QRS;
— наличие в большинстве случаев полной компенсаторной паузы.
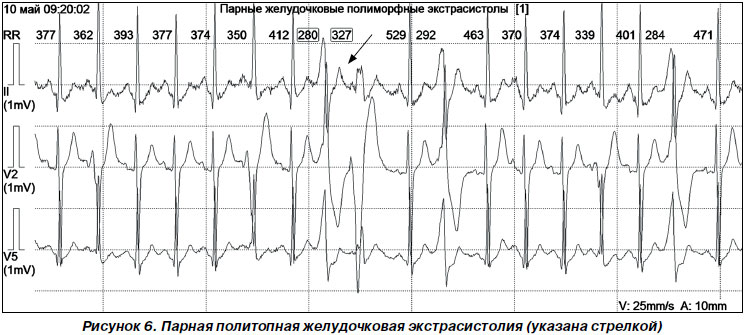
Экстрасистолический желудочковый комплекс QRST обычно напоминает по форме комплекс QRST при блокаде одной из ножек предсердно-желудочкового пучка. Желудочковые экстрасистолы могут быть монотопными (возбуждение возникает в одном эктопическом очаге); в этом случае все экстрасистолические комплексы одинаковы по форме и все интервалы сцепления имеют равную величину. Желудочковые экстрасистолии разделяют в зависимости от локализации на правожелудочковые (наиболее часто у детей из выводного отдела) и левожелудочковые. Правожелудочковые экстрасистолы характеризуются морфологией желудочкового комплекса по типу блокады левой ножки пучка Гиса, левожелудочковые — по типу блокады правой ножки пучка Гиса. Непостоянство интервала сцепления и формы экстрасистолического комплекса свидетельствует о том, что экстрасистолы исходят из разных эктопических очагов (политопная экстрасистолия, рис. 6).
По плотности ЭС могут быть единичными (отдельно расположенными), парными и групповыми. Группу из 3 и более ЭС называют пароксизмом эктопической тахикардии.
Существует аллоритмическая ЭС, то есть чередующаяся с очередными комплексами в правильной последовательности. ЭС, следующая за каждым очередным синусовым комплексом, — бигеминия, группа из трех комплексов, разделенных компенсаторной паузой, — тригеминия (рис. 7), из четырех — квадригеминия и т.д.
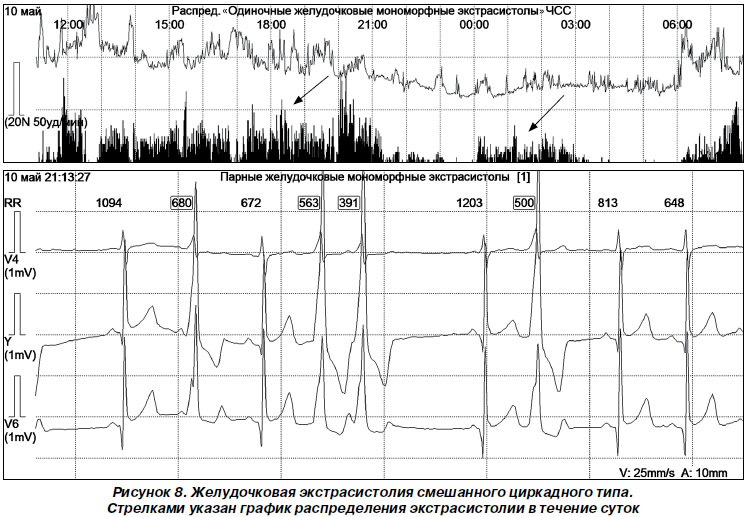
По частоте во время аускультации ЭС делят на редкие (до 5–9 в минуту), средней частоты (от 10 до 15 в минуту), частые (более 15 в минуту). По данным холтеровского мониторирования, частыми считаются экстрасистолы с частотой возникновения более 600 в час или более 15 000 за 24 ч.
Циркадный ритм (тип) ЭС диагностируется в зависимости от периода суток. Выделяют три циркадных типа ЭС: дневной, ночной и смешанный (рис. 8). При дневном типе ЭС регистрируются в период бодрствования, а ночью во время сна исчезают; при ночном — появляются после засыпания.
Все ЭС вегетативного генеза можно разделить на три патогенетических варианта:
1. Лабильные ЭС покоя (вагозависимые).
2. Стабильные ЭС покоя (сочетаннозависимые).
3. ЭС напряжения (симпатикозависимые).
Лабильные ЭС покоя встречаются наиболее часто (в 47,5 %), как правило у детей старшей возрастной группы, их связывают с повышением активности блуждающего нерва. ЭС при этом могут быть частыми, аллоритмическими, групповыми, выявляться в клино- и ортоположении в течение суток.
Стабильные ЭС покоя наиболее характерны для детей младшей возрастной группы, а также для школьников со смешанным типом ВСД и с ваготоническим исходным вегетативным тонусом. Такие ЭС выслушиваются и фиксируются на ЭКГ независимо от положения тела и физической нагрузки, то есть имеется устойчивое сохранение частых ЭС (обычно аллоритмических) в клино- и ортоположении, а также в течение суток (сон и активное бодрствование).
ЭС напряжения чаще регистрируются у детей в пубертатном периоде, характеризуются учащением в ортоположении, их преобладанием в период активного бодрствования, в том числе физической нагрузки, урежением или полным исчезновением в период ночного сна. Особенностью этих ЭС является их появление или сохранение на фоне синусовой тахикардии.
Современные методы обследования детей с экстрасистолией
По своему физическому развитию дети с экстрасистолией не отличаются от сверстников. Поэтому клиническая оценка экстрасистолии должна проводиться обязательно комплексно, с анализом жалоб, анамнеза, состояния сердечно-сосудистой, центральной и вегетативной нервной системы, что имеет важное значение для классификации, выявления генеза, оценки прогноза, составления индивидуальной программы лечения и реабилитации, оценки ее эффективности. Обязательными являются:
— оценка клинико-анамнестических и генеалогических данных;
— оценка вегетативного статуса;
— стандартная электрокардиография;
— холтеровское мониторирование с проведением психологических, физических и лекарственных нагрузочных проб;
— пробы с дозированной физической нагрузкой (тредмил-тест, велоэргометрия);
— допплер-эхокардиографическое обследование;
— исследование уровня электролитов крови, гормонов щитовидной железы; по показаниям — МВ-фракция креатинкиназы, тропонин Т, мозговой натрийуретический пептид;
— обследование на внутриклеточные инфекции;
— нейрофизиологическое исследование и оценка нейротрофической функции;
— чреспищеводная электрокардиография;
Основным методом инструментальной диагностики нарушений ритма сердца является электрокардиография, не теряющая своего значения с течением времени. Взаимоотношение и динамика основных компонентов электрокардиограммы дает клиницисту существенную диагностическую информацию о биоэлектрической активности миокарда, наличии и характеристике аритмии.
Холтеровское мониторирование — длительная регистрация ЭКГ с помощью портативных кардиомониторов в условиях свободной активности обследуемого с последующей дешифровкой записи на специальных автоматических анализирующих системах — является ведущим методом обследования детей с ЭС.
Показаниями к проведению холтеровского мониторирования у детей с ЭС являются:
— выявление нарушений ритма сердца у больных с другой патологией, при которой имеется высокий риск развития аритмии (кардиомиопатия, ПМК с регургитацией, первичная легочная гипертензия, врожденные пороки сердца);
— оценка частоты и комплексности ЭС в суточном цикле;
— определение циркадного ритма аритмии, связи ЭС с нагрузками, субъективными ощущениями;
— оценка эффективности проводимой антиаритмической терапии.
Важной характеристикой экстрасистолии, обусловленной вегетативной дисфункцией, является урежение частоты экстрасистол в ортоположении, при физических нагрузках (тредмил-тест, велоэргометрия), при пробе с атропином, что подтверждает зависимость аритмии от состояния парасимпатического отдела ВНС (лабильные экстрасистолы покоя). При использовании суточного мониторирования ритма сердца отмечается четкая связь частоты экстрасистол с функциональными состояниями детского организма — урежение экстрасистол в период максимальной активности, игры; учащение — в период относительного покоя, в глубоких стадиях сна.
При оценке вегетативного статуса у детей с экстрасистолией, как правило, отмечается преобладание парасимпатического отдела — ваготония — или имеется дистония с превалированием ваготонических признаков (мраморность кожи, повышенное потоотделение, разлитой, красный, возвышающийся дермографизм и др.). Эти дети часто страдают вестибулопатией, повышенной метеозависимостью и метеотропностью. У них имеются другие висцеровегетативные проявления — ночной энурез, дискинезия желудочно-кишечного тракта и/или желчевыводящих путей, гастроэзофагеальный рефлюкс и др.
Проведение допплер-эхокардиографии больным с ЭС необходимо для контроля состояния центральной гемодинамики, изменение которой в виде снижения фракции выброса, появления и прогрессирования дилатации полостей сердца считают признаком развития аритмогенной кардиопатии, показанием к интервенционному лечению.
Исследование ЦНС детей с экстрасистолией, как правило, выявляет негрубую резидуальную симптоматику в виде отдельных микроорганических знаков. Их сочетание с гипертензионно-гидроцефальным синдромом, диагностируемым по краниограммам и эхоэнцефалоскопически, свидетельствует о резидуальном характере органической церебральной недостаточности, в большинстве случаев являющейся результатом неблагоприятного течения беременности и/или родов. Локальная эпилептическая активность на электроэнцефалограмме у больных с экстрасистолией отсутствует.
По нашим наблюдениям, в психологическом статусе этой категории больных характерными были умеренно выраженные тревожные и депрессивные нарушения, ипохондрическая фиксация на состоянии собственного здоровья. Несмотря на эмоциональную лабильность и высокий уровень нейротизма, дети с экстрасистолией хорошо успевали в школе, количество интерперсональных конфликтов у них было меньше, чем при других видах аритмий.
По показаниям в условиях специализированного стационара больным с ЭС применяют специальные методы исследования: поверхностное ЭКГ-картирование (для топической диагностики нарушений ритма), чреспищеводную электрокардиографию. При неинвазивном электрофизиологическом исследовании, благодаря максимальному приближению электродов к левому предсердию, регистрируют высокоамплитудные предсердные потенциалы. Это дает возможность, не прибегая к сложному и опасному методу внутриполостной ЭКГ, исследовать электрический потенциал предсердного комплекса в диагностических целях.
Принципы лечения экстрасистолии у детей
Вопросы лечения экстрасистолии до настоящего времени разработаны недостаточно, в них много спорного, вероятно, из-за разной оценки степени органической «заинтересованности» сердца при экстрасистолии. Необходимо использовать все возможности для постановки этиологического диагноза.
Наличие структурных изменений в сердце, соматической патологии, которые могли стать причиной аритмии, требуют лечения основного заболевания.
Дети с редкой желудочковой экстрасистолией, как правило, не нуждаются в лечении. Важным является динамическое наблюдение пациентов не реже 1 раза в год, а при наличии клинических симптомов ЭС рекомендовано проведение холтеровского мониторирования 1 раз в год в связи с доказанностью сохранения или трансформации ЭС в другую сердечно-сосудистую патологию в последующих возрастных периодах согласно данным Фремингемского исследования.
Важно объяснить больному, что экстрасистолия безопасна, особенно при устранении потенциально значимых аритмогенных факторов: психоэмоционального напряжения, нарушения режима дня, вредных привычек (курение, алкоголь, токсикомания), приема симпатомиметических препаратов. Большое значение имеет здоровый образ жизни: достаточная продолжительность сна, прогулки на свежем воздухе, создание благоприятного психологического климата в семье и школе. Пища должна содержать продукты, богатые калием, магнием (абрикосы, чернослив, печеный картофель, сушеные фрукты), селеном (оливковое масло, морепродукты, сельдь, маслины, бобовые, орехи, гречневая и овсяная крупы, свиное сало) и витаминами.
У детей в периоде новорожденности при отсутствии органической патологии сердца экстрасистолы чаще возникают при наличии пре- или постнатальной гипоксии. Особое значение имеет вскармливание ребенка грудным молоком, содержащим достаточное количество витаминов, минеральных веществ, полиненасыщенных жирных кислот, в том числе омега-3, омега-6. При отсутствии грудного вскармливания необходимо с рождения использовать высокоадаптированные питательные смеси с наличием жизненно важных витаминов, минеральных веществ, микронутриентов.
Дети с лабильной ЭС покоя, нечастой стабильной ЭС покоя не нуждаются в освобождении от уроков физкультуры. Решение о физических нагрузках для детей с частой стабильной ЭС покоя, ЭС напряжения решается индивидуально в зависимости от результатов нагрузочных проб.
При вегетозависимой ЭС в детской аритмологии традиционно используется базисная терапия, целью которой является коррекция и нормализация кардиоцеребральных взаимодействий, нейровегетативных нарушений и восстановление регулирующей функции симпатоадреналовой системы (Белоконь Н.А., Школьникова М.А. 1986). Данные схемы включают в себя ноотропные препараты, мембраностабилизирующие и метаболические средства. При назначении базисной терапии курс лечения должен составлять 3 месяца не менее 2 раз в год. Одновременно назначают не более трех препаратов разных групп.
Ноотропные и ноотропоподобные препараты оказывают трофическое влияние на вегетативные центры регуляции, способствуют усилению метаболической активности клеток, мобилизации энергетических резервов клеток, регуляции корково-подкорковых взаимоотношений, оказывают мягкий и стойкий стимулирующий эффект на симпатическую регуляцию сердца (периферический симпатомиметический эффект), участвуют в активации серотонинергической системы.
Ноофен: 100 мг 2 р/д (до 3–4 лет); 100 мг 2–3 2 р/д (до 6 лет); 100 мг 3–4 р/д (до 10 лет); 200 мг 2–3 р/д (до 14 лет); 250–500 мг 3 р/д (старше 14 лет).
Аминалон: 50 мг — 1/2 т. 2 р/д (до 7 лет); 1 т. 2–3 р/д (старше 7 лет).
Глутаминовая кислота: 50 мг 2 р/д (до 3 лет); 125 мг 2–3 р/д (до 7 лет); 250 мг 3 р/д (до 12 лет); 500 мг 2 р/д (старше 12 лет).
Энцефабол: 25 мг 2 р/д (до 3 лет); 50 мг 2 р/д (до 7 лет); 100 мг 2–3 р/д (старше 7 лет).
Семакс 0,1% р-р (капли в нос): 1 кап. 2 р/д в каждый носовой ход (до 3 лет); 2 кап. 2 р/д (до 7 лет); 3 кап. 2 р/д (до 10 лет); 5 кап. 2 р/д (старше 10 лет).
Пантогам: 50 мг 2 р/д (до 3 лет); 125 мг 2 р/д (до 7 лет); 250 мг 2 р/д (до 10 лет); 500 мг 2 р/д (старше 10 лет).
Оказывают седативное, анксиолитическое действие:
Нейровитан: 1/4–1/2 табл. 1 р/д (от 1 до 3 лет); 1 табл. 1 р/д (от 3 до 7 лет); 1 табл. 1–3 р/д (от 8 до 14 лет); 1 табл. 1–4 р/д (старше 14 лет).
Фенибут: 50 мг 2 р/д (до 3 лет); 125 мг 2 р/д (до 7 лет); 250 мг 2 р/д (до 10 лет); 250 мг 3 р/д (старше 10 лет).
Пикамилон: 10 мг 2 р/д (до 3-х лет); 20 мг 2 р/д (до 7 лет); 50 мг 2 р/д (до 10 лет); 50 мг 3 р/д (старше 10 лет).
Метаболические препараты участвуют во всех видах обмена, восстанавливают нормальную электрическую активность миокарда:
Кардонат: 1 капс. 1 р/д (от 1 до 5 лет); 1 капс. 2 р/д (от 5 до 15 лет); 1–2 капс. 3 р/д (старше 15 лет).
Карнитина хлорид 20% р-р: 4-10 капель 3 р/д (до 1 года); 14 капель 2–3 р/д (от 1 до 6 лет); 28–42 капли 2–3 р/д (от 6 до 12 лет); 0,5–2,0 чайной ложки 2 р/д (старше 12 лет).
Кудесан (коэнзим Q10): 4–10 капель 1 р/д (от 1 до 3 лет); 10–16 капель 1 р/д (от 3 до 7 лет); 16–20 капель 1 р/д (от 7 до 12 лет); 20–60 капель 1 р/д (старше 12 лет).
Милдронат: 250 мг 2 р/д (до 12 лет); 250–500 мг 2 р/д (старше 12 лет).
Препараты калия и магния влияют на метаболические процессы, обладают собственным антиаритмическим действием и потенцируют действие других антиаритмических лекарственных средств:
Магне В6: 10–30 мг/кг/сут в 3 приема (от 1 до 6 лет); 2–6 табл. (1–3 амп.) 3 р/д (от 6 до 12 лет); 6–8 табл. (3–4 амп.) 3 р/д (старше 12 лет).
Панангин: 1–2 табл. 3 р/д.
Аспаркам: 1–2 табл. 3 р/д.
Ритмокор: 1 капс. 3 р/д (от 6 до 12 лет); 1–2 капс. 3–4 р/д (старше 12 лет).
При наличии у ребенка ощущений нарушенного ритма и снижении качества жизни показаны рациональная психотерапия, седативные средства, транквилизаторы или антидепрессанты.
При частой идиопатической желудочковой экстрасистолии необходимо контролировать самочувствие и состояние центральной гемодинамики, изменение которой является показанием к интервенционному лечению.
При радиочастотной катетерной абляции (РЧА) в полость сердца через крупные сосуды вводится специальный электрод, дистальный полюс которого устанавливается в области локализации электрофизиологического субстрата аритмии, ответственного за ее возникновение и/или поддержание. В «зону интереса» наносятся аппликации радиочастотного тока. В результате повреждения миокарда разрушается ключевая зона экстрасистолии, что приводит к невозможности ее возникновения. РЧА эктопического очага показана детям с частой желудочковой экстрасистолией (более 15 000 желудочковых экстрасистол в сутки), сопровождающейся развитием аритмогенной дисфункции миокарда: появлением и нарастанием дилатации полостей сердца, снижением фракции выброса. У детей важно применять максимально щадящий протокол радиочастотных воздействий.
В ближайшем послеоперационном периоде рекомендуют проведение контрольного эхокардиографического исследования, холтеровского мониторирования. Эффективность РЧА желудочковой ЭС составляет, по данным разных авторов, от 83 до 100 % и зависит от типа аритмии, технических возможностей и опыта клиники.
Антиаритмическая терапия у детей имеет существенные ограничения и оправданна только в целях предотвращения развития аритмогенной дисфункции миокарда и при появлении клинических проявлений, обусловленных гемодинамической неэффективностью ЭС. Антиаритмическая терапия с длительностью курса 3–6 мес. должна назначаться детям только при имеющихся ограничениях (чаще всего возрастных) или невозможности проведения радикального лечения — катетерной абляции электрофизиологического субстрата ЭС.
Выбор антиаритмических препаратов остается эмпирическим. При желудочковой ЭС наиболее эффективны следующие препараты:
— амиодарон 5–7–10 мг/кг/сутки (у детей до 1 года — до 15 мг/кг/сут);
— ритмонорм (пропафенон, пропанорм) 10–15 мг/кг/сут;
— атенолол 0,5–1,0 мг/кг/сут;
— конкор 0,1–0,2 мг/кг/сут.
У детей с частой экстрасистолией описана эффективность противосудорожного препарата карбамазепина (финлепсин), обладающего антиаффективным и мембраностабилизирующим свойствами, а также антиаритмической активностью вследствие инактивации входящего натриевого тока. Препарат назначают в дозе 7–10 мг/кг/сут (до 15 мг/кг/сут у детей до 1 года), разделив на 2–3 приема, длительно (до 12 мес.).
Установлено, что при суправентрикулярной форме экстрасистолии эффективны препараты IV класса антиаритмических средств — ингибиторы переноса ионов кальция. Наиболее часто применяемым в аритмологии является изоптин (верапамил, финоптин). Препарат назначают детям в дозе 0,002 г/кг массы тела в сутки в 4 приема.
При одновременном наличии наджелудочковой и желудочковой ЭС более рациональным препаратом является соталол (соталекс) 1–2 мг/кг/сутки.
Подбор антиаритмических препаратов проводят под контролем данных ЭКГ и холтеровского мониторирования с учетом доз насыщения и циркадного характера аритмии. Максимум терапевтического действия лекарственного вещества целесообразно рассчитывать с учетом того, в какие периоды суток максимально выражена желудочковая экстрасистолия. Исключение составляют препараты длительного действия и амиодарон.
Антиаритмическая терапия считается эффективной, если количество желудочковых экстрасистол за сутки уменьшается более чем на 50 %, число парных экстрасистол — не менее чем на 90 %. Эффективность лечения оценивают также по параметрам внутрисердечной гемодинамики по данным эхокардиографии на синусовом ритме и в экстрасистолических комплексах.
Прогноз клинического течения экстрасистолии у детей
Экстрасистолия, особенно желудочковая, нарушает правильность сердечного ритма из-за преждевременности сокращений желудочков, постэкстрасистолических пауз и связанной с этим асинхронности возбуждения миокарда. Однако экстрасистолы, даже частые, как правило, не влияют или мало влияют на гемодинамику, если отсутствуют выраженные диффузные или крупноочаговые поражения миокарда. Это связывают с эффектом так называемой постэкстрасистолической потенциации — увеличением силы следующего за экстрасистолой сокращения. Помимо увеличения силы сокращения имеет значение и компенсаторная пауза (если она является полной), обеспечивающая увеличение конечно-диастолического объема желудочков сердца. При органической патологии миокарда перечисленные механизмы компенсации оказываются несостоятельными, и ЭС может стать причиной снижения сердечного выброса и способствовать развитию застойной сердечной недостаточности.
Прогноз экстрасистолии зависит от наличия или отсутствия органической патологии сердца, электрофизиологических характеристик экстрасистолии (частоты, степени преждевременности, локализации), а также от способности экстрасистолии оказывать отрицательное влияние на кровообращение — гемодинамической эффективности экстрасистолии.
Критериями благоприятного прогноза клинического течения ЭС являются: мономорфная ЭС, исчезающая при физической нагрузке, гемодинамически стабильная (эффективная), не ассоциированная с органической патологией сердца.
Наиболее прогностически неблагоприятны нагрузочные (симпатозависимые), а также ранние и сверхранние желудочковые экстрасистолы, накладывающиеся на нисходящее колено зубца Т, его вершину или восходящее колено, иногда на конечную часть сегмента ST предшествующего нормального комплекса QRS. При злокачественном течении наджелудочковой экстрасистолии возникают мерцательная аритмия и желудочковая тахикардия, которые могут стать причиной летального исхода.
Прогноз в отношении выздоровления при ЭС в большинстве случаев сомнительный. Иногда ЭС спонтанно прекращается на несколько месяцев и даже лет, но в дальнейшем может рецидивировать. Вместе с тем больные сохраняют трудоспособность и высокое качество жизни, если ЭС не обусловлена тяжелой органической патологией миокарда (миокардит, кардиомиопатии, врожденные и приобретенные пороки сердца). Прогноз у детей с ЭС на фоне органической патологии сердца зависит от эффективности лечения основного заболевания и степени контроля аритмии.

Основная
- Аритмии у детей. Атлас электрокардиограмм / Под ред. М.А. Школьниковой. — М.: ИД «Медпрактика-М», 2006. — 148 с.
- Вегетативные расстройства: клиника, лечение, диагностика / Под ред. А.М. Вейна. — М.: Медицинское информационное агентство, 2000. — 752 с.
- Диагностика и лечение нарушений ритма сердца и проводимости у детей: Учебное пособие / Под. ред. М.А. Школьниковой, Д.Ф. Егорова. — СПб: Человек, 2012. — 432 с.
- Конопко Н.Н., Нагорная Н.В., Пшеничная Е.В., Четверик Н.А. Клиническое значение мониторирования ЭКГ по Холтеру в практике педиатра, детского кардиолога и семейного врача // Конспект педіатра. — Ч. 2. — Донецк, 2010. — С. 75-81.
- Макаров Л.М. Холтеровское мониторирование (Руководство для врачей по использованию метода у детей и лиц молодого возраста). — М.: Медпрактика, 2000. — 216 с.
- Школьникова М.А., Березницкая В.В. Диагностика и медикаментозное лечение желудочковых экстрасистолий у детей // Российский вестник перинатологии и педиатрии. — 2008. — № 2. — С. 60-67.
Дополнительная
- Мутафьян О.А. Аритмии сердца у детей и подростков (клиника, диагностика, лечение). — СПб.: Невский Диалект, 2003. — 224 с.
- Мутафьян О.А. Детская кардиология. — М.: ГЭОТАР-Медиа, 2009. — 504 с.
- Приходько B.C., Сенаторова Г.С., Страшок O.I. та ін. Діагностика та лікування дітей з порушеннями серцевого ритму // Методичні рекомендації — Харків, 2003. — 23 с.