Украинский журнал хирургии 2 (17) 2012
Вернуться к номеру
Современные подходы к химиотерапии больных колоректальным раком с метастазами в печень
Авторы: И.Б. Щепотин, Е.А. Колесник, О.В. Васильев, Г.В. Лаврик, А.В. Лукашенко, Р.Я. Палица, Национальный институт рака, Киев
Рубрики: Хирургия
Разделы: Справочник специалиста
Версия для печати
Приведены данные о результатах рандомизированных исследований по изучению эффективности лекарственной терапии у больных метастатическим колоректальным раком (МКРР). Рассмотрены существующие режимы химиотерапии в комплексе с таргетными препаратами: ингибитором сосудистого эндотелиального фактора роста (бевацизумаб) и ингибитором эпидермального фактора роста (цетуксимаб). У больных с прогрессированием заболевания возможно преодоление резистентности к иринотекану и оксалиплатину за счет совместного назначения препаратов с моноклональными антителами. В исследовании BOND-2 изучена комбинация моноклональных антител – бевацизумаба и цетуксимаба – с режимами FOLFOX и FOLFIRI у больных с МКРР (n=2300). Общая выживаемость увеличилась до 27,5 месяцев. Представлены перспективные данные собственных исследований по результатам лечения 52 больных с использованием режимов FOLFOX, XELOX, FOLFIRI, XELIRI, с бевацизумабом или цетуксимабом
Наведені дані про результати рандомізованих досліджень по вивченню ефективності лікарської терапії у хворих метастатичним колоректальним раком (МКРР). Розглянуті існуючі режими хіміотерапії в комплексі з таргетнимі препаратами: інгібітором судинного ендотеліального чинника зростання (бевацизумаб) і інгібітором епідермального чинника зростання (цетуксимаб). У хворих з прогресом захворювання можливе подолання резистентності до ірінотекану і оксаліплатіну за рахунок спільного призначення препаратів з моноклональними антитілами. У дослідженні Bond-2 вивчена комбінація моноклональних антитіл – бевацизумаба і цетуксимаба – з режимами FOLFOX і FOLFIRI у хворих з МКРР (n=2300). Загальна виживаність збільшилася до 27,5 місяців. Представлені перспективні дані власних досліджень за результатами лікування 52 хворих з використанням режимів FOLFOX, XELOX, FOLFIRI, XELIRI, з бевацизумабом або цетуксимабом.
The results of randomized studies for effectiveness of anti-tumor drugs in patients with metastatic colorectal cancer (МCRC) are presented in the article. Chemotherapy regimens in the complex with target agents: anti-VEGF (bevacizumab) and anti-EGFR (cetuximab) – have been considered. After diseases progression duty combined prescription of monoclonal antibodies overcomes resistance is possible for irinotecan and oxaplatin. In the BOND-2 trial monoclonal antibodies – bevacizumab and cetuximab – with FOLFOX and FOLFIRI regimens for MCRC (n=2300) was study. Median survival increased to 27,5 months. The data of the own experience is presented: results of the advanced treatment of 52 MCRC patients, which received FOLFOX, XELOX, FOLFIRI and XELIRI regimens with bevacizumab or cetuximab.
Колоректальный рак, метастазы в печень, химиотерапия, таргетная терапия.
колоректальний рак, метастази в печінку, хіміотерапія, таргетная терапія.
сolorectal cancer, liver matastases, chemotherapy, target therapy.
Вопросы диагностики и лечения колоректального рака (КРР) в последние годы приобретают все большую актуальность. Это связано, в первую очередь, с ростом заболеваемости КРР во всех экономически развитых странах мира. По темпам прироста данная патология находится на третьем, по смертности – на втором месте в структуре онкологических заболеваний [1, 2]. Метастазы в печень наблюдаются в 15-30% случаев на момент диагностики первичного заболевания и в 70% случаев – в процессе его развития, из них у 20% пациентов с II и 50% – с III стадией КРР [3]. За последние 10 лет выбор методов лечения для распространенных форм КРР претерпел значительные изменения. Внедрение в практику мощных цитотоксических и таргетных препаратов вместе с расширением показаний к выполнению хирургических вмешательств позволило в 2 раза повысить выживаемость данной категории больных [4].
Целью настоящего исследования явилось изучение и обобщение данных мировой литературы по вопросу лечения больных КРР с метастазами в печень и представление собственных результатов исследований.
Анализ мировой литературы демонстрирует возрастающий интерес к проблеме комбинированного лечения больных метастатическим КРР (МКРР). Разработка лечебной тактики начинается с решения вопроса о характере и распространенности опухолевого процесса и возможности оперативного лечения. В стратегии лечения больных с метастазами КРР в печень существуют два направления: в случае первично резектабельных метастазов выполняется оперативное вмешательство с адъювантной (±неоадъювантной) лекарственной терапией; в случае нерезектабельных метастазов проводится неоадъювантное лечение с целью перевода новообразование в резектабельную форму.
Резекции печени остаются «золотым» стандартом в лечении метастазов КРР в печень. В результате нескольких ретроспективных серий исследований сравнили продолжительность жизни пациентов с потенциально резектабельными метастазами в печени. От 25 до 55% пациентов после резекции метастазов в печени пережили 5-летний рубеж, ни один из нелеченных пациентов не прожил 5 лет [5, 6]. По данным R. Adam (2007), основанным на изучении базы объединенного международного Интернет Канцер-регистра (2122 больных), общая 5-летняя выживаемость больных МКРР после резекций печени составляет 42%, к прогностически неблагоприятным факторам отнесены: билобарное поражение (р=0,0002), количество метастазов более 3 (р<0,0001), размер наибольшего метастаза превышает 5 см (р=0,03). Представляет интерес тот факт, что неоадъювантная химиотерапия (ХТ) достоверно увеличивает выживаемость только у пациентов с количеством печеночных метастазов более 5 [6].
Необходимо отметить, что с развитием и совершенствованием техники оперативных вмешательств на печени в настоящее время измененились и критерии резектабельности. Множественные метастазы и билобарное поражение не относят к противопоказаниям их радикального лечения. В случае билобарных множественных метастазов часто используется стратегия двухэтапной гемигепатэктомии с использованием химиоэмболизации. Общая 5-летняя выживаемость после двухэтапных резекций печени у больных с билобарными метастазами КРР достигает 42% [5, 7]. Эмболизация правой воротной вены позволяет проводить правостороннюю гемигепатэктомию у пациентов с малым объемом паренхимы левой доли.
Разработаны методики резекции нижней полой и печеночных вен с последующей их реконструкцией. Возможно выполнение комбинированных операций с удалением внепеченочных метастазов. Также не являются более противопоказанием к оперативному вмешательству поражение лимфоузлов ворот печени, границы резекции менее 1 см. Вместе с тем, поражение опухолью регионарных лимфоузлов остается одним из неблагоприятных прогностических факторов при МКРР. По данным R.Adam (2009), 5-летняя общая выживаемость в группе с поражением регионарных лимфоузлов и без такового составила 18 и 53% соответственно (p<0,001), 5-летняя безрецидивная выживаемость — 11 и 23% соответственно (p = 0,004). Установлено, что независимым фактором неблагоприятного прогноза служит поражение чревных лимфоузлов. Резекция печени в сочетании с удалением печеночных лимфоузлов оправдана в тех случаях, когда на фоне неоадъювантной ХТ наблюдается регрессия или стабилизация метастазов в регионарных лимфоузлах, особенно у больных молодого возраста. Напротив, у больных с поражением чревных и/или парааортальных лимфоузлов такой подход нецелесообразен, даже если неоадъювантная ХТ привела к регрессии опухоли [8].
По данным экспертов, определение резектабельности сегодня включает: выполнение R0 резекции (негативные границы резекции), сохранение минимум двух сегментов печени и адекватного количества остаточной печеночной ткани (>20-30%) после резекции, минимальное внепеченочное распространение заболевания. [4]. Тонкая граница между возможностью резекции печени и ее онкологической обоснованностью на сегодняшний день является основной проблемой операбельности больных КРР с метастазами в печень [9].
Несмотря на успехи, достигнутые в хирургическом лечении больных МКРР, для 75-80% единственной реальной возможностью лечения остается ХТ, отказ от которой лишает пациента каких-либо жизненных перспектив. Лекарственная терапия преследует две цели: добиться регрессии опухоли и повысить резектабельность метастазов в печень для полного излечения больного; при невозможности выполнения резекции – стабилизировать опухолевый процесс на максимально возможный период времени при сохранении удовлетворительного качества жизни.
Многие годы КРР считали резистентным к ХТ опухолью. Результаты лечения пациентов с МКРР значительно изменились за последние несколько лет. Медиана выживаемости больных с нерезектабельным метастатическим заболеванием достигла 27 месяцев. Современная доступная лекарственная терапия МКРР базируется на использовании трех групп химиопрепаратов (фторпиримидины, оксалиплатин, иринотекан) и двух биологических препаратов (бевацизумаб, цетуксимаб).
В течение длительного периода времени единственными препаратами, активными при КРР, оставались антиметаболиты из группы фторпиримидинов – 5-фторурацил (5-ФУ) и его производные. В настоящее время 5-ФУ остается базисным препаратом в лекарственной терапии больных МКРР и используется в режиме болюсного (струйного) введения или непрерывной инфузии (22-24 часа). Учитывая специфичность воздействия 5-ФУ в S – фазе клеточного цикла и короткий период полураспада (10-20 минут), режим инфузии предпочтительней. Положительный эффект (число регрессий) монотерапии 5-ФУ наблюдается в 14% случаев при болюсном и в 22% при инфузионном введении с медианой выживаемости 11,3 и 12,1 месяцев соответственно, что подтверждают результаты метаанализа. Дозолимитирующей токсичностьюявляется диарея, стоматит [10]. Кальция фолинат (ФК, лейковорин) является наиболее эффективным биомодулятором фторурацила. Метаанализ 9 рандомизированных исследования (1381 пациентов) показал преимущество использования 5-ФУ/ФК перед монотерапией 5-ФУ, число регрессий составило 23% против 11% [11]. Два наиболее часто используемых режима 5-ФУ/ФК представлены в таблице 1.
Результаты применения режимов De Gramont и Mayo Clinic показали достоверно большую эффективность инфузионного режима: повышение эффекта лечения с 14 до 33% с достоверным увеличением безрецидивной выживаемости с 57 до 62 недель и снижением токсичности 3-4 степени с 24 до 11%, однако статистически достоверных отличий в показателях общей выживаемости не наблюдалось [12].
Причиной создания пероральных форм фторпиримидинов послужило стремление получить препарат, соответствующий по эффективности режиму длительной инфузии 5-ФУ со снижением токсичности и лишенным недостатков в использовании.
Фторафур (тегафур), Урацил+Тегафур (UFТ) используется в суточной дозе 300 мг/м2 в течение 28 дней с интервалом между циклами 7 дней. Сравнение режима клиники Мayo c UFT в двух рандомизированных исследованиях показало равную противоопухолевую активность этих режимов. Эффект лечения составил 11 (12%) для UFT и 15 (9%) при снижении общей токсичности. [13, 14].
Капецитабин (Кселода®) – карбамат фторпиримидина, в результате каскада ферментных реакций в клетках опухоли превращается в 5-ФУ, и практически полностью всасывается из кишечника, за счет чего достигается снижение его системной токсичности. В результате проведенных исследований доказано, что концентрация 5-ФУ в опухоли в 3,2 выше, чем в прилежащих нормальных тканях и в 21, 4 раза выше, чем в плазме крови [15]. Капецитабин используется в суточной дозе 2500мг/м2 в сутки 1-14 дни трехнедельного цикла каждые три недели (с интервалом между циклами 7 дней).
Два крупных рандомизированных исследования (1207 больных) сравнивали эффективность применения режима клиники Mаyo и капецитабина у больных МКРР. Отмечена достоверно большая эффективность капецитабина (р=0,005) при эквивалентном времени до прогрессирования и равноценной выживаемости больных [16, 17].
Сопоставление токсичности двух режимов показало несомненное преимущество капецитабина, который продемонстрировал увеличение профиля безопасности по сравнению с 5-ФУ/ЛВ с достоверным снижением таких побочных явлений как диарея, стоматит, нейтропения 3- 4 степени токсичности [18].
Иринотекан (Кампто®). В основе механизма действия препарата лежит его способность блокировать фермент топоизомеразу I. Последняя участвует в процессе репликации и транскрипции ДНК.
Анализ двух крупных многоцентровых рандомизированных исследования III фазы, выполнявшихся в США и Европе показал, что добавление иринотекана к струйному или инфузионному введению 5-ФУ/ЛВ значительно улучшает непосредственные и отдаленные результаты лечения больных МКРР, существенно снижая риск прогрессирования. Медиана выживаемости после двух линий ХТ составила 14,2-17,4 мес. Дозолимитирующей токсичностью препарата является диарея и нейтропения. [19, 20].
В результате проведенного рандомизированного исследования GERCOR OPTIMOX1 была установлена статистически более высокая эффективность режима FOLFIRI (табл. 2) и во 2 линии терапии: увеличение безрецидивной выживаемости с 2,3 до 3,7 мес. [21].
По данным исследователей, в результате применения различных комбинаций на основе использования иринотекана возможность выполнения резекций печени составила от 31% до 70% [22].
Оксалиплатин (Элоксатин®) – производное платины 3-го поколения. Приводит к формированию платиновых внутринитевых сшивок, которые блокируют репликацию ДНК. Оксалиплатин обладает отсутствием перекрестной резистентности и синергизмом действия с 5-ФУ/ФК, иринотеканом и рядом других противоопухолевых препаратов.
При сравнении режимов 5-ФУ/ФК и FOLFOX4 в качестве 1 линии ХТ МКРР в группе FOLFOX4 была достигнута статистически значимо большая частота объективных эффектов (51% и 22%) и лучшая безрецидивная выживаемость (9,0 и 6,2 мес., р=0,003) [23, 24]. Периферическая сенсорная нейропатия является дозолимитирующей (1-4 степень токсичности встречается у 76-95% пациентов, из них 3-4 степень у 3-16%) и обратимой.
При использовании режима XELOX (табл. 3) в качестве 1 линии ХТ у 96 больных с МКРР эффект получен у 55% и стабилизация на срок более 3 месяцев еще у 32% больных. Медиана времени до прогрессирования составила 7,6 мес., медиана выживаемости превысила 16 мес., более 1 года прожили 72% больных [25].
В исследовании, проведенном Giacchetti S с соавт., терапия оксалиплатином, 5-ФУ/ФК у 151 больного с метастазами КРР в печень, привела к уменьшению более чем на 50% размеров метастазов в 59,6% случаев. В результате оперативные вмешательства на печени были выполнены в 51% случаев. Медиана выживаемости пациентов, которым удалось произвести операцию, составила 48 месяцев, а 5 и 7-летняя выживаемость – 50% и 30% соответственно [24].
В настоящее время в результате использования различных инфузионных режимов 5-ФУ/ФК + оксалиплатин в первой линии терапии МКРР лечебный эффект достигнут в 40-54% случаев с медианой выживаемости от 16 до 21,5 месяцев [26, 27].
В результате использования иринотекан- и оксалиплатин-содержащих режимов ХТ у больных МКРР, в 40-60% случаев достигается объективный эффект и тем самым повышается возможность увеличить число резектабельных больных [28]. Преимущество назначения того или иного режима изучалось в рандомизированных исследованиях. В исследовании GERGOR 220 пациентов МКРР на основе рандомизации больные получали в одной группе лечения в качестве 1 линии режим FOLFIRI, а при прогрессировании в качестве 2 линии – FOLFOX. Во второй группе последовательность была противоположной. Частота объективных эффектов, время до прогрессирования, а также общая выживаемость в сравниваемых группах не различались. Как и ожидалось, режим FOLFIRI ассоциировался с большей частотой нейтропении и алопеции, а FOLFOX был более нейротоксичным [29]. Проведенное в США исследование по изучению качества лечения и стоимости режимов FOLFOX и FOLFIRI также не показало преимуществ одной схемы перед другой [30]. В целом, благодаря последовательному использованию эффективных режимов FOLFIRI и FOLFOX удалось достигнуть медианы выживаемости более 20 месяцев, т.о. доказана целесообразность проведения 2 линии ХТ у больных МКРР. Медиана общей выживаемости больных МКРР при использовании трех активных препаратов (иринотекан, оксалиплатин, 5-ФУ) увеличивается с 18.4 мес. до 31,6 мес. (p<0.01) по сравнению с использованием 5-ФУ + оксалиплатин или 5-ФУ + иринотекан [31].
В последние годы значительный успех в лечении МКРР достигнут при использовании в комплексной терапии таргетных препаратов. В основе таргетной терапии лежит целевое воздействие на определенные клеточные рецепторы или сигнальные пути, передающие информацию в ядро клетки.
Цетуксимаб (Эрбитукс®) – химерическое моноклональное антитело, иммуноглобулин G1, блокирующее рецептор эпидермального фактора роста (EGFR) на поверхности клеток. Этим предотвращается активация внутриклеточных EGFR-зависимых тирозинкиназ и ростовой сигнал не поступает в ядро, индуцирует апоптоз и частично тормозит ангиогенез.
Цетуксимаб вводится в нагрузочной дозе 400 мг/м2 (первая 2-часовая инфузия) с последующими еженедельными инфузиями по 250 мг/м2. Результаты использования различных режимов комбинации цетуксимаб + иринотекан/оксалиплатин + 5-ФУ/ФК в 1-й линии терапии МКРР показали, что объективный эффект лечения составил от 48% до 74% [32]. Дозолимитирующей токсичностью при лечении цетуксимабом является акнеформная сыпь. Обнаружена прямая зависимость эффективности лечения от интенсивности сыпи. На конгрессе ASCO (2007) были приведены следующие данные: медиана времени до прогрессирования составила 3,3 мес. при 0 степени проявления сыпи, 9,1 мес. – при 1-2 степени и 11,3 мес. при 4 степени [33].
В 2008г. были опубликованы результаты двух крупных рандомизированных исследований, подтверждающих эффективность цетуксимаба в сочетании с двумя стандартные режимами ХТ: FOLF1R1 (в исследовании CRYSTAL) и FOLFOX (в исследовании OPUS), в 1 линии терапии МКРР. Было показано статистически значимое увеличение частоты достижения непосредственного эффекта (46–47% при использовании комбинации и 36–39% – без цетуксимаба). Наилучшие показатели выживаемости без прогрессирования были получены для пациентов с метастазами только в печени: 11,4 мес. в группе, получавшей цетуксимаб и 9,2 мес – в контрольной группе. В этом же исследовании было выявлено, что добавление цетуксимаба позволило увеличить частоту выполнения радикальных резекцию печени с 2,5 до 6%. При этом R0 резекцию всех опухолевых очагов удалось выполнить у 4,3% в группе, получавшей цетуксимаб с ХТ, по сравнению с 1,5% в группе, получавшей только ХТ (р=0,0034). Установлено, что за наличие или отсутствие эффекта цетуксимаба может отвечать статус протоонкогена KRAS. Примерно у 40% больных с КРР происходят мутации в гене KRAS, приводящие к синтезу белка, обладающего автономной активностью (т.е. передающего внутриклеточный сигнал без предшествующей стимуляции со стороны EGFR). По понятным причинам у подобных пациентов (с опухолями, несущими мутированный KRAS) блокада EGFR не приводит к приостановке передачи стимулирующих внутриклеточных сигналов. Согласно данным исследований, при мутации KRAS применение препарата оказалось неэффективным, однако среди оставшихся ~60% пациентов (с немутированным, диким KRAS) эффект от назначения цетуксимаба был значимо выше, чем в общей популяции [34, 35].
Согласно данным Е. Van Cutsem в группе больных с диким типом KRAS добавление цетуксимаба к режиму FOLFIRI позволило впервые приблизиться к медиане в 25 мес. (в контрольной группе – 21,0 мес., р=0,2) [36].
Данные исследования CELIM свидетельствуют о том, что добавление цетуксимаба к предоперационной ХТ (FOLFOX/FOLFIRI) у пациентов с МКРР и неоперабельными метастазами в печень и диким типом гена KRAS позволяет достичь общей частоты ответа опухоли на уровне 70% в сравнении с 11% в группе контроля, соответственно резектабельность метастазов в печени увеличилась с 32 до 60% [37].
Таким образом, с одной стороны, данные о прогнозирующей роли KRAS позволяют избавить пациентов с мутированным геном от проведения заведомо неэффективного дорогостоящего лечения, с другой – эффект от назначения цетуксимаба у пациентов с немутированным KRAS оказался значимо больше, чем в общей популяции.
Бевацизумаб (Авастин®) – моноклональное антитело к рецепторам сосудистого эндотелиального фактора роста (VEGF). Клетки аденокарциномы толстой кишки продуцируют избыточное количество VEGF, стимулируя формирование новых капилляров, что улучшает доставку в опухоль кислорода и необходимых для ее роста веществ. Время полужизни антител позволяет применять его 1 раз в 2 нед (5 мг/кг).
У больных с прогрессированием заболевания после назначения иринотекана возможно преодоление резистентности за счет совместного назначения с бевацизумабом. В результате анализа рандомизированных исследований (BEAT) с использованием в различных режимах ХТ бевацизумаба, получены данные об его удовлетворительном профиле безопасности: количество возникших осложнений (кровотечение – 3%, тромбоэмболии – 1%) не превышает таковые в других рандомизированных исследованиях. Использование бевацизумаба у больных МКРР в различных режимах ХТ, включающих оксалиплатин и фторпиримидины (исследование TREE-1/TREE-2, n=360) показали высокую эффективность при низком профиле токсичности. Добавление бевацизумаба позволило повысить общую выживаемость больных с 18,2 до 24,4 месяцев. Медиана времени до прогрессирования увеличилась на 4 месяца [38, 39].
Эффективность лечения бевацизумабом в зависимости от мутации KRAS изучалась в фазе III исследования. Использовали режим IFL +/- бевацизумаб [40]. Медиана безрецидивной выживаемости была значительно выше в группе пациентов с бевацизумабом как с диким KRAS (13,5 и 7,4 мес., p < 0,0001), так и с мутированным KRAS (9,3 и 5,5 мес., p = 0,0008). Положительный ответ на лечение был отмечен в группе с режимом IFL + бевацизумаб с немутированным KRAS (60% и 37,3%, p = 0,006) по сравнению с 43,2% и 41,2% в группе с мутацией. Бевацизумаб проявляет эффективность независимо от статуса KRAS.
В результате анализа проведенных исследований установлено, что использование бевацизумаба у больных МКРР с фторпиримидиновыми режимами ХТ (с включением иринотекана и оксалиплатина и без таковых) статистически достоверно увеличивают общую и безрецидивную выживаемость в 1 (на 4,7 мес.) и 2 (на 2,1 мес.) линии терапии и на 3,1% повышает резектабельность метастазов в печени [41].
Основываясь на результатах проведенного исследования (BOND-2) была изучена комбинация моноклональных антител – бевацизумаба и цетуксимаба – с последовательными режимами FOLFOX и FOLFIRI у больных с МКРР (n=2300). Общая выживаемость увеличилась с 22 до 27,5 месяцев [42]. При изучении комбинации XELOX + бевацизумаб с добавлением цетуксимаба медиана безрецидивной выживаемости была достоверно выше, чем без цетуксимаба и составила 10,7 месяцев [43].
Характеристика молекулярного профиля опухоли является определяющим фактором в выборе и прогнозировании эффективности использования EGFR – ингибиторов с учетом KRAS. В настоящее время продолжается исследование других молекулярных и биохимических маркеров, имеющих отношение к EGFR (BRAF, амфирегулин, эпирегулин, РТen, Vras). Для VEGF-ингибиторов, в частности бевацизумаба, прогностические маркеры не показательны.
Проведенный Golfinopoulos с соавт. метаанализ 242 рандомизированных исследований, включающих 137 различных схем ХТ у больных МКРР с использованием всех пяти лекарственных препаратов, с высокой степенью достоверности показал сравнимую эффективность иринотекан- и оксалиплатин-содержащих режимов. Доказано повышение эффективности лечения при использовании максимального количества лекарственных средств, с включением бевацизумаба и цетуксимаба. [44].
Согласно консенсусу, принятому на Всемирном конгрессе WCGIC (2009) в Барселоне, стратегия 1-й линии ХТ определяется необходимостью проведения агрессивной (или интенсивной) лекарственной терапии. По данным экспертов, в 85% случаев необходимо проведение агрессивной ХТ, которая включает триплет лекарственных препаратов (оксалиплатин или иринотекан + фторпиримидины + цетуксимаб или бевацизумаб). Для целевого назначения таргетных препаратов является обязательным определение мутации KRAS. В случае отсутствия мутации KRAS (дикий тип) назначается препарат цетуксимаб, при невозможности определения мутации KRAS или при ее наличии назначается бевацизумаб. В 15% случаев необходимости в проведении агрессивной ХТ нет. У этой группы пациентов рекомендуется использовать фторпиримидины (предпочтительно пероральные формы – капецитабин, фторафур) с бевацизумабом.
В настоящее время при выборе режима проведения 1-й линии ХТ у больных МКРР целесообразно руководствоваться риск-адаптированными подходами [4]. В клинической практике при принятии решения относительно 1-й линии ПХТ имеет значение мутация KRAS, состояние пациента (статус ECOG) и возможность проведения интенсивной терапии. В соответствии с целью проводимого лечения, можно выделить 3 группы больных:
1) пациенты с нерезектабельными метастазами в печень, потенциально операбельными в случае значительной частичной регрессии – агрессивная лекарственная терапия;
2) пациенты с агрессивно протекающим заболеванием, сопровождающимся симптомами; нуждаются в лечении с целью быстрой регрессии опухоли, требуют срочного проведения интенсивной терапии с перспективой достигнуть максимальной регрессии за короткое время – агрессивная лекарственная терапия;
3) пациенты с небольшой первичной опухолью и множественными метастазами, никогда не подлежащими резекции: лекарственная терапия может включать только фторпиримидины (предпочтительно капецитабин) + бевацизумаб. В случае отсутствия мутации KRAS – цетуксимаб в монотерапии.
Важным является пересмотр цели направленной терапии каждые 1-2 цикла с оценкой максимальной регрессии опухоли.
При наличии нерезектабельного МКРР единственной эффективной альтернативой лечения является ХТ. Учитывая что опухолевый процесс в IV стадии возможно только затормозить в развитии, но не излечить полностью, встаёт вопрос о балансе между необходимостью длительной терапии и предотвращения развития побочных эффектов. Согласно результатам исследования OPTIMOX1, проведённого группой GERCOR, большниство больных, получающих схему FOLFOX вынуждены прекратить лечение до прогрессирования заболевания в связи с высокой нейротоксичностью. Получив такие результаты, группа GERCOR поставила вопрос: возможна ли временная отмена оксалиплатина или ХТ в принципе в целях предотвращения развития серьёзных побочных эффектов и организации перерывов в процессе лечения? C этой целью было организовано второе исследование OPTIMOX2, в котором все пациенты вначале получали режим FOLFOX 6 курсов, затем одной группе продолжалась «поддерживающая» терапия 5-ФУ/ФК, а другой лечение временно прекращалось. При диагностике прогрессирования заболевания и той, и другой группе больных возобновлялась терапия FOLFOX. По результатам исследования, общая выживаемость была достоверно выше в группе пациентов, получавших «поддерживающую» терапию и составила 23,8 месяцев по сравнению с 19,5 месяцами в контрольной группе. Продемонстрированные результаты имеют большое клиническое значение, и показывают необходимость непрерывного лечения больных МКРР. В целях борьбы с нарастающей токсичностью возможны временные переходы на более «лёгкие» схемы ХТ [45].
Однако если в случае нерезектабельных метастазов необходимость проведения ХТ бесспорна, то потребность в ней у пациентов с резектабельными опухолями до сих пор вызывает сомнения. В настоящее время трудно сделать окончательный вывод о целесообразности проведения неоадъювантной ХТ, поскольку результатов клинических исследований в этой сфере пока недостаточно. Тем не менее, по данным исследования EORTC 40983, проведение неоадъювантной ХТ в режиме FOLFOX4 позволяет достичь увеличения показателя 3-летней выживаемости приблизительно на 10% [28]. Следует учитывать, что проведение курса неоадъювантной ХТ не во всех случаях оказывает благоприятное влияние для последующего выполнения резекции, т.к. ХТ гепатотоксична. Таким образом, при операбельной и неагрессивной по своим биологическим свойствам опухоли, которая малосимптомна, высокодифференцирована и поздно прогрессирует после удаления первичной, можно обойтись без неоадъювантной ХТ.
Комбинированный эффект более активных режимов ХТ при метастазах КРР в печень и лучшей хирургической техники привели к возникновению трех консенсусов [9]:
1) число пациентов, подходящих на потенциально радикальную резекцию печени увеличивается.
2) стадия IV в сравнении с I, II, III стадиями КРР является гетерогенной и в существующей сегодня классификации AJCC расценивается слишком упрощенно; принимая во внимание возможности различных терапевтических подходов, нуждается в пересмотре.
3) определение оптимальных точек приложения в лечении пациентов, у которых метастазы в печень могут стать резектабельными, – современная цель клинических исследований. Показатель общей выживаемости, хоть и является наиболее объективным в определении эффективности неоадъювантной ХТ у больных МКРР, может отражать и влияние многих других факторов, поэтому не представляется целесообразным в таком типе исследований. Резектабельность должна стать новым показателем оценки эффективности неоадъювантной лекарственной терапии. Необходимо также принять во внимание то, что показания к резекции печени определяются не только состоянием опухоли пациента, но и квалификацией и «агрессивностью» хирурга.
На сегодняшний день хирурги и онкологи установили себе высокую планку полного излечения больного с метастазами в печень. Считаем, что индикатором реальной эффективности лечения больных КРР с метастазами в печень должна быть не только резектабельность, но и длительность безрецидивного периода после R0 резекции. Применение современных режимов ХТ позволило преодолеть 27-месячную планку медианы общей выживаемости у больных МКРР без резекции метастазов в печени. Согласно мнению большинства экспертов, такое увеличение произошло не за счет какого-нибудь одного цитостатика или одного режима ХТ, а благодаря последовательному использованию всех пяти групп лекарственных препаратов, а также динамическому постоянному обновлению программы лечения.
По данным канцер-регистра Национального института рака за 2005-2009 гг. на лечении в институте находилось 1656 больных КРР, из них в 23% (381) случаев – в IV стадии заболевания. Оксалиплатин- и иринотекан-содержащие режимы использованы у 70% больных в первой или второй линии ХТ. В 18% случаев лечение дополняли биотерапией с использованием таргетных препаратов (бевацизумаб, цетуксимаб), преимущественно во второй линии терапии. У 70% больных лечение носило комбинированный характер: хирургическое вмешательство сочетали с ХТ, в случаях рака прямой кишки - лучевой терапией.
Учитывая повышенный интерес хирургов к вопросам комбинированного лечения и проблеме повышения резектабельности метастазов в печень, мы представляем опыт клиники по проведению лекарственной терапии с включением препаратов таргетного действия.
Материал и методы
Проведен анализ результатов лечения 52 больных КРР c T3-4 N0-2 M1 (метастазы в печень), в возрасте от 42 до 72 лет (средний возраст 56 лет), которые находились на лечении в отделении опухолей брюшной полости Национального института рака в 2005-2009 гг.
В 47 случаях (90%) больным МКРР всвязи с нерезектабельными метастазами в печень выполнены паллиативные операции по удалению первичной опухоли. Потенциально резектабельные метастазы в печень (согласно консенсусу) диагностированы у 17 больных (33%).
Курсы ХТ начинали на 14-21 сутки после операции. Использовали оксалиплатин- и иринотекан-содержащие режимы ХТ: FOLFOX/XELOX (27), FOLFIRI/XELIRI (25). У 31 больных схему лечения дополняли препаратом бевацизумаб 5мг/кг каждые 2 недели (группа I), у 21 пациентов – препаратом цетуксимаб 400мг/м2 – первое введение и 250мг/м2 все последующие еженедельно (группа II). Во всех случаях использовали общепринятые препараты сопровождения (антиеметики, антигистаминные средства и т.д.).
Диагностику осуществляли на основании объективных данных, результатов лабораторных, рентгенологических, эндоскопических, ультразвуковых методов исследования и компьютерной томографии (обязательно у всех пациентов до, в процессе и после окончания лечения), исследование онкомаркера РЭА.
Эффективность ХТ в исследуемых группах оценивалась по изменению суммы размеров измеряемых метастатических очагов в соответствии с критериями REСIST с учетом данных КТ.
Результаты и обсуждение
У 22 из 52 больных первично установленным диагнозом был рак прямой кишки, у 30 – рак ободочной кишки. Метастазы в печень диагностированы в 52 случаях, синхронно – в легкие – 18, яичники – 5, канцероматоз брюшины – в 4 случаях.
Физиологический статус пациентов в соответствии со шкалой ВОЗ составил «0» – 9, «1» – 32, «2» – 11 больных.
При иммуногистохимическом исследовании было выявлено, что 21 пациента имелась положительная экспрессия EGFR, мутантный тип KRAS установлен у 7 больных, дикий – у 10. В 62% случаев имелась гипер-экспрессия VEGF, однако корреляции данных показателей с течением заболевания мы не выявили,
Комбинированные оперативные вмешательства выполнены у 5 пациентов (удаление первичной опухоли в объеме анатомической резекции с удалением метастатических опухолей яичников, большого сальника). Послеоперационных осложнений не было. Количество проведенных циклов лекарственной терапии составило от 3 до 20 (среднее количество циклов = 8). Проведена лекарственная терапия 1 линии у 30 больных, 2 линии – 22 больных. Срок наблюдения за больными составил 9-52 мес. (средний срок – 18 мес.). Умерло 23 пациента от прогрессирования заболевания и 2 пациента по другим причинам (от сопутствующей патологии).
Оптимальным началом ХТ считаем 14-21 сутки после циторедуктивной операции, когда статус пациентов приближается к 1-2 согласно шкале ВОЗ. Почему необходимо соблюдение данного критерия отбора для начала агрессивной ХТ?
По данным исследователей, физикальный статус больных МКРР оказывает влияние на результаты выживаемости после проведения ХТ. Мультивариантный анализ многоцентровых рандомизированных исследований показал, что показатель общей выживаемости у пациентов с статусом ECOG > 2 был значительно меньше, чем при статусе ECOG 0-1 (соответственно 8,5 мес. И 17,3 мес., р <0,0001). Поэтому при выборе агрессивных режимов ХТ необходимо учитывать риск возникновения осложнений у пациентов с низким физикальным статусом [46].
При анализе ближайших результатов лечения больных I группы токсичность 4 степени не наблюдали. У 6 больных отмечали нейтропению 3 степени. Оксалиплатин обладал удовлетворительной переносимостью. Наиболее частым осложнением была периферическая сенсорная нейропатия I-II степени (82% случаев), которая проявлялась в виде парастезий конечностей. Иринотекан обладал также удовлетворительной переносимостью. Дозолимитирующей токсичности не наблюдали. Диарея 3 степени отмечена у 5 пациентов. Регрессия опухоли во всех случаях подтверждена результатами компьютерной томографии (табл. 4).
Медиана времени до прогрессирования составила 10 месяцев. Медиана выживаемости не достигнута. Длительность стабилизации или частичной регрессии после прекращения терапии составила от 3 до 8 месяцев.
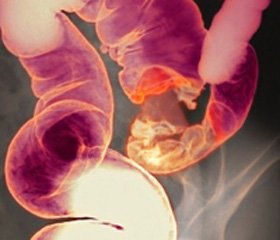
На рисунке 1 (а, б) представлены результаты компьютерной томографии больного Н. до и после комплексного лечения с использованием оксалиплатига, капецитабина и бевазцизумаба.
При анализе ближайших результатов лечения больных II группы токсичность 4 степени не наблюдали. У 4 больных отмечали нейтропению 3 степени. У всех пациентов в большинстве имели место кожные реакции в виде сыпи 2-3 степени, которые требовали терапии сопровождения. В трех случаях сыпь явилась дозолимитирующей.
Медиана времени до прогрессирования в этой группе больных составила 9,5 месяцев. Степень регрессии опухоли (табл. 5) в большинстве случаев зависела от количества проведенных курсов ХТ. Пик ответа опухоли на лечение возникал после 6 циклов лекарственной терапии.
У 47-48% больных обеих групп отмечен высокий эффект терапии в виде частичной регрессии. У 4 пациентов выполнены резекции печени в объеме R0.
Достигнута полная регрессия опухолевых очагов в печени в 6 случаях. В трех случаях выполнена резекция печени, при гистологическом исследовании выявлены элементы аденокарциномы в стадии лечебного патоморфоза. У остальных трех пациентов прогрессирование заболевания возникло в сроки от 7 до 12 месяцев после окончания лечения. С учетом данных других исследователей [4, 5, 26], в случае даже полной регрессии метастазов в печень целесообразно выполнение резекции.
Заключение
Благодаря более активному использованию современных режимов ХТ совместно с препаратами таргетного действия, у ряда пациентов МКРР с первично нерезектабельными метастазами в печень, можно достичь регрессии опухоли до резектабельного состояния, и, тем самым повысить перспективы на длительную выживаемость.
1. Cancer statistics, 2009 / A. Jemal, R. Siegel, E. Ward [et al.] // CA Cancer J. Clin. – 2009. – Vol. 59. – № 4. – Р. 225-249.
2. Рак в Україні, 2007–2008. Захворюваність, смертність, показники діяльності онкологічної служби // Бюл. Національного канцер-реєстру України. – К., 2009. – № 10. – 104 с.
3. Keighley M.R.B. Surgery of the anus, rectum and colon / M.R.B. Keighley, N.S. Williams . – 2nd ed. – London : WB Saunders, 2007. – 340 p.
4. Тoward optimized front-line therapeutic strategies in patients with metastatic colorectal cancer – an expert review from the International Congress on Anti-Cancer Treatment (ICACT) 2009 / R. Adam, D.G. Haller, G. Poston [et al.] // Ann. Oncol. – 2010. – Vol. 21 – №10. – Р. 1093-1096.
5. Treatment of colorectal liver metastases: a review / M. Van den Eynde // Rev. Recent Clin. Trials. – 2009. – Vol. 4. – № 1. – Р. 56-62.
6. Adam R. Developing strategies for liver metastases from colorectal cancer / R. Adam // Semin. Oncol. – 2007 – Vol. 34. – № 2 (suppl. 1). – S. 7-11.
7. Long-term results of two-stage hepatectomy for irresectable colorectal cancer liver metastases / D.A. Wicherts, R. Miller, R.J. de Haas [et al.] // Ann Surg. – 2008. – Vol. 248. – № 6. – Р. 994-1005.
8. Adam R. Is hepatic resection justified after chemotherapy in patients with colorectal liver metastases and lymph node involvement? / R. Adam, T.A. Aloia // J. Clin. Oncol. – 2009. – Vol. 27. – № 8. – Р. 1343-1345.
9. Sobrero A. Resectability of initially unresectable liver metastases from colorectal cancer should not be the primary end point of clinical trials / A. Sobrero, G. Aprile // Gastrointest Cancer Res. – 2009. – Vol. 3. – № 1. – Р. 41-42.
10. Meta-analysis Group In Cancer. Efficacy of intravenous continuous infusion of fluorouracil compared with bolus administration in advanced colorectal cancer // J. Clin. Oncol. – 1998. – Vol. 16. – Р. 301-308.
11. Advanced Colorectal Cancer Meta-Analysis Project. Modulation of fluorouracil by leucovorin in patients with advanced colorectal cancer: evidence in terms of response rate // J. Clin. Oncol. – 1992. – Vol. 10. – Р. 896-903.
12. Randomized trial comparing monthly low-dose leucovorin and fluorouracil bolus with bimonthly high-dose leucovorin and fluorouracil bolus plus continius infusion for colorectal cancer advanced: a French Intergroupe study / A. de Gramont, J.F. Bosset, C. Milan [et al.] // J. Clin. Oncol. – 1997. – Vol. 15. – Р. 808-815.
13. Multicenter phase III study of Uracil/Tegafur and oral Leucovorin versus Fluorouracil and Leucovorin in patients with previously untreated metastatic colorectal cancer / J.Y. Dulliard, P.M. Hoff, J.R. Skillings [et al.] // J. Clin. Oncol. – 2002. – Vol. 20. – № 17. – Р. 3605-3616.
14. Randomized comparative study of Uracil/Tegafur and oral Leucovorin versus Fluorouracil and Leucovorin in patients with previously untreated metastatic colorectal cancer / J. Carmichael, T. Popiela, D. Radstone [et al.] // J. Clin. Oncol. – 2002. – Vol. 20. – № 17. – Р. 3617-3627.
15. Preferential activation of capecitabine in tumor following oral administration to colorectal cancer patient / J. Schuller, J. Cassidy, E. Dumont [et al.] // Cancer Chemother. Pharmacol. – 2000. – Vol. 45. – Р. 291-297.
16. Oral capecitabine compared with intravenous fluorouracil plus leucovorin in patients with metastatic colorectal cancer: result of a large phase III study / E. VanCutsem, C. Twelves, J. Cassidy [et al.] // J. Clin. Oncol. – 2001. – Vol. 19. – Р. 4096-4106.
17. Comparison of oral capecitabine versus intravenous fluorouracil plus leucovorin as first-line treatment in 605 patients with metastatic colorectal cancer: result of a randomized phase III study / P.M. Hoff, R. Ansari, G. Batisti [et al.] // J. Clin. Oncol. – 2001. – Vol. 19. – Р. 2282-2292.
18. Potential regional differences for the tolerability profiles of fluoropyrimidines / D.G. Haller, J. Cassidy, S.J. Clarke [et al.] // J. Clin. Oncol. – 2008. – Vol. 26. – Р. 2118-2123.
19. Irinotecan plus fluorouracil and leucovorin for metastatic colorectal cancer / L.B. Saltz, J.V. Cox, C. Blanke [et al.] // N. Engl. J. Med. – 2000. – Vol. 343. – Р. 905-914.
20. Metastatic colorectal cancer: integrating irinotecan into combination and sequential chemotherapy / J.Y. Douillard, A. Sobrero, C. Carnaghi [et al.] // Ann. Oncol. – 2003. – Vol. 14, suppl 2. – Р. ііі7-12.
21. Efficacy of FOLFIRI-3 (irinotecan D1,D3 combined with LV5-FU) or other irinotecan-based regimens in oxaliplatin-pretreated metastatic colorectal cancer in the GERCOR OPTIMOX1 study / F.C. Bidard, C. Tournigand, T. André [et al.] // Ann. Oncol. – 2009. – Vol. 19. – Р. 4028-4034.
22. Randomized, controlled trial of irinotecan plus infusional, bolus, or oral fluoropyrimidines in first-line treatment of metastatic colorectal cancer:results from the BICC-C study / C.S. Fuchs, J. Marshall, E. Mitchell [et al.] // J. Clin. Oncol. – 2007. – Vol. 25. – № 30. – Р. 4779-4785.
23. Leucovorm ana fluorouracil with or without oxaliplatin as first-line treatment in advanced colorectal cancer / A. de Gramont, A. Figer, M. Seymour [et al.] // J. Clin. Oncol. – 2000. – Vol. 18. – № 16. – Р. 2938-2947.
24. Phase III multicenter randomized trial of oxaliplatin added to chronomodulated fluorouracil-leucovorin as first-line treatment of metastatic colorectal cancer / S. Giachetti, B. Perpoint, R. Zidani [et al.] // J. Clin. Oncol. – 2000. – Vol. 18. – № 1. – Р. 136-147.
25. Randomized phase III study of capecitabin plus oxaliplatin compared with fluorouracil/folinic acid plus oxaliplatin as first-line therapy for metastatic colorectal cancer / J. Cassidy, S. Clarke, E. Diaz-Rubio [et al.] // J. Clin. Oncol. – 2008. – Vol. 26. – № 12. – Р. 2006-2012.
26. Koopman M. The CAIRO and FOCUS studies: Which lesson is to be learned? / M. Koopman, M.T. Seymour, C.J. Punt // Oncologist. – 2009. – Vol. 14. – Р. 192-193.
27. Different strategies of sequential and combination chemotherapy for patients with poor prognosis advanced colorectal cancer (MRC FOCUS): a randomised controlled trial / M.T. Seymour, T.S. Maughan, J.A. Ledermann [et al.] // Lancet. – 2007. – Vol. 370. – Р. 143-152.
28. Nordlinger B. Liver metastases from colorectal cancer: a multidisciplinary approach is necessary / B. Nordlinger, S. Benoist // Bull. Acad. Natl. Med. – 2008. – Vol. 192. – № 1. – Р. 33-43.
29. FOLFIRI Followed by FOLFOX6 or the Reverse Sequence in Advanced Colorectal Cancer: A Randomized GERCOR Study / C. Tournigand, T. Andru, E. Achille [et al.] // J. Clin. Oncol. – 2004. – Vol. 22. – Р. 229-237.
30. Markov model assessing the effectiveness and cost-effectiveness of FOLFOX compared with FOLFIRI for the initial treatment of metastatic colorectal cancer / J.W. Tumeh, P.J. Shenoy, S.G. Moore, J. Kauh, C. A. Flowers // Am. J. Clin. Oncol. – 2009. – Vol. 32. – № 1. – Р. 49-55.
31. The validity of full administration of 5-fluorouracil, irinotecan, and oxaliplatin to unresectable or recurrent colorectal cancer / K. Ishibashi, N. Okada, T. Ishiguro [et al.] // Gan To Kagaku Ryoho. – 2008. – Vol. 35. – № 12. – Р. 2289-2291.
32. Cetuximab and chemotherapy as initial treatment for metastatic colorectal cancer / E. Van Cutsem, C.H. Köhne, E. Hitre [et al.] // N. Engl. J. Med. – 2009. – Vol. 360. – № 14. – Р. 1408-1417.
33. Randomized phase III study of irinotecan and 5-FU/FA with or without cetuximab in the first-line treatment of patients with metastatic colorectal cancer (mCRC): The CRYSTAL trial / E. Van Cutsem, M. Nowacky, S.I. Lang [et al.] // J. Clin. Oncol. – 2007. – Vol. 25. – Р. 164.
34. KRAS status and eficacy in the CRYSTAL study: 1st -line treatment of patient with metastatic colorectal cancer (MCRC) receiving FOLFIRI with or without cetuximab / E. Van Cutsem, I. Lang, G. D’haens [et al.] // Ann. Oncol. – 2008. – Vol. 19. – 8S. – Р. ііі4.
35. KRAS status and efficacy of first-line treatment of patients with metastatic colorectal cancer (mCRC) with FOLFOX with or without cetuximab: the OPUS experience / C. Bokemeyer, I. Bondarenko, J.T. Hartmann [et al.] // J. Clin. Oncol. – 2008. – Vol. 26. – 20S. – Аbst. 4000.
36. The treatment of advanced colorectal cancer: where are we now and where do we go? / Е.Van Cutsem, C.Verslype, I. Demedts // Best Practice & Res Clin Gastroenterol. – 2009. – Vol. 16. – № 2. – Р. 319-330.
37. Tumour response and secondary resectability of colorectal liver metastases following neoadjuvant chemotherapy with cetuximab: the CELIM randomised phase 2 trial / G. Folprecht, T. Gruenberger, W.O. Bechstein [et al.] // Lancet Oncol. – 2010. – Vol. 11. – № 1. – Р. 38-47.
38. Safety and efficacy of first-line bevacizumab with FOLFOX, XELOX, FOLFIRI and fluoropyrimidines in metastatic colorectal cancer: the BEAT study / E. Van Cutsem, F. Rivera, S. Berry [et al.] // Annals of Oncology. – 2009. – Vol. 20. – Р. 1842-1847.
39. Hurwitz H. Bevacizumab in the treatment of metastatic colorectal cancer: safety profile and management of adverse events / H. Hurwitz, S. Saini // Semin. Oncol. – 2006. – Vol. 33. – № 10. – Р. 26-34.
40. The clinical benefit of bevacizumab in metastatic colorectal cancer is independent of K-ras mutation status: analysis of a phase III study of bevacizumab with chemotherapy in previously untreated metastatic colorectal cancer / H.I. Hurwitz, J. Yi, W. Ince [et al.] // The Oncologist. – 2009. – Vol. 14. – Р. 22-28.
41. McCormack P/L. Bevacizumab: A review of its use in metastatic colorectal cancer / P.L. McCormack, S.J. Keam // Drugs. – 2008. – Vol. 68. – № 4. – Р. 487-506.
42. Randomized phase II trial of cetuximab/bevacizumab/irinotecan (CBI) versus cetuximab/bevacizumab (CB) in irinotecan-refractory colorectal cancer / L.B. Saltz, H.J. Lenz, H. Hochster [et al.] // J. Clin. Oncol. – 2005. – Vol. 23. – Р. 3508.
43. Chemotherapy, bevacizumab, and cetuximab in metastatic colorectal cancer / J. Tol, M. Koopman, A. Cats [et al.] // N. Engl. J. Med. – 2009. – Vol. 360. – № 6. – Р. 563-572.
44. Survival and disease-progression benefits with treatment regimens for advanced colorectal cancer: a meta-analysis / V. Golfinopoulos, G. Salanti, N. Pavlidis, J.P.A. Ioannidis // Lancet Oncol. – 2007. – Vol. 8. – Р. 898-911.
45. Can Chemotherapy Be Discontinued in Unresectable Metastatic Colorectal Cancer? The GERCOR OPTIMOX2 Study / B. Chibaudel, F. Maindrault-Goebel, G. Lledo [et al.] // JCO. – 2009. – Vol. 27. – № 34. – Р. 5727-5733.
46. Pooled safety and efficacy analysis examining the effect of performance status on outcomes in nine first-line treatment trials using individual data from patients with metastatic colorectal cancer / D.J. Sargent, C.H. Kohne, H.K. Sanoff [et al.] // J. Clin. Oncol. 2009. – Vol. 7. – № 12. – Р. 1948-1955.

/98/98.jpg)
/99/99.jpg)
/104/104.jpg)
/105/105.jpg)
/106/106.jpg)