Украинский журнал хирургии 3 (18) 2012
Вернуться к номеру
Агрессивный фиброматоз у детей
Авторы: И.П. Журило1, В.К. Литовка2, В.Н. Грона1, И.Н. Иноземцев2, С.В. Веселый1, К.В. Латышов1, А.Ю. Гунькин2, Е.В. Литовка2, 1 Донецкий национальній медицинский университет им. М.Горького,
2 Областная детская клиническая больница, Донецк
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
В клинике детской хирургии с 1985 по 2011 годы лечилось 17 детей с агрессивным фиброматозом в возрасте от 11 месяцев до 16 лет. Опухоли экстраабдоминальной локализации выявлены у 12 (70,6%) больных, интраабдоминальной – у 5 (29,4%). Лечение агрессивного фиброматоза хирургическое. Опухоль склонна к постоянному рецидивированию. По нашим данным, рецидивы при экстраабдоминальной локализации опухоли отмечены у 33,3% больных. При интраабдоминальном расположении очага агрессивного фиброматоза радикальная операция выполнена у 40% пациентов. После повторной операции по поводу рецидива опухоли необходимо проводить полихимиотерапию и лучевую терапию. Больные с агрессивным фиброматозом должны находиться на диспансерном учете. Контрольное ультразвуковое исследование необходимо проводить ежемесячно.
У клініці дитячої хірургії з 1985 по 2011 роки лікувалося 17 дітей з агресивним фіброматозом у віці від 11 місяців до 16 років. Пухлини екстраабдомінальної локалізації виявлені у 12 хворих (70,6%), інтраабдомінальної – у 5 дітей (29,4%). Лікування агресивного фіброматоза хірургічне. Пухлина схильна до постійного рецидивування. За нашим даними, рецидиви за екстраабдомінальною локалізацією пухлини відзначені у 33,3% хворих. За інтраабдомінальному розташуванню осередку агресивного фіброматоза радикальна операція виконана у 40% пацієнтів. Після повторної операції із приводу рецидиву пухлини необхідно проводити поліхіміотерапію та променеву терапію. Хворі з агресивним фіброматозом повинні перебувати на диспансерному обліку. Контрольне ультразвукове дослідження необхідно проводити щомісяця.
In the clinic of Pediatric Surgery from 1985 to 2011 the 17 children with aggressive fibromatosis were cured. The age of children was from 11 months to 16 years. The extraabdominal localization of the tumor were found in 12 patients (70,6%), the intraabdominal localization of the tumor were detected in 5 patients (29,4%). The treatment of aggressive fibromatosis was surgery. The tumor may recur constantly. According to our data, the recurrence of the extraabdominal tumor were observed in 33,3% of patients. When the source of aggressive fibromatosis has the intraabdominal location, the radical surgery was performed in 40% of patients. The polychemotherapy and radiotherapy should be carried out after the second operation for recurrent tumor. The patients with aggressive fibromatosis should be on the dispensary. The control ultrasound should be carried out monthly.
агрессивный фиброматоз, дети
агресивний фіброматоз, діти
aggressive fibromatosis, children
Агрессивный фиброматоз (АФ) – сборная группа новообразований фибробластического и миобластического ряда, которые возникают из сухожилий и фасциально-апоневротических структур, а источником опухолевого роста является фиброцит [1, 8]. В клинической практике, наряду с термином агрессивный фиброматоз, в равной мере употребляется термин десмоид. Реже встречаются следующие синонимы: десмоидная фиброма, глубокий фиброматоз, десмома, инвазивная фиброма, неметастазирующая фибросаркома, мышечно-апоневротический фиброматоз [2, 3, 7].
По своим морфологическим и клиническим особенностям АФ является типичным примером промежуточных (местно агрессивных, «условно злокачественных») опухолей мягких тканей и характеризуется локальными рецидивами, инфильтративным местно-деструирующим ростом, не дающим метастазы [1, 5, 8]. Ежегодно регистрируется от 2 до 4 впервые выявленных случаев АФ на 100000 жителей [7-9].
Клинические проявления АФ определяются локализацией и размерами опухоли. Выделяют абдоминальную и экстраабдоминальную локализацию образований. Этиология АФ не установлена. В возникновении этого заболевания могут играть роль генетические и эндокринные факторы, а также механическая травма [1, 5, 8, 9, 12].
Проблема лечения АФ у детей состоит в наклонности этой опухоли к многократным рецидивам после «радикальных» операций [3, 4, 9]. При этом потенциал инвазивного роста АФ значительно превосходит таковой у многих истинно злокачественных опухолей. Именно резко выраженная способность к инвазии в окружающие ткани предопределяет высокую частоту местных рецидивов этой опухоли, которая достигает 70% [1, 9, 10].
В связи с изложенным, в последние годы для лечения больных с АФ, наряду с оперативным вмешательством, стали шире использовать химиотерапевтические препараты и лучевую терапию. Ряд исследователей отмечает обнадеживающие результаты такого лечения [2, 4, 6, 7].
АФ может развиваться во всех областях человеческого тела, где представлена соединительная ткань. При локализации в конечностях, опухоли, как правило, возникают исключительно на сгибательных поверхностях (передние отделы плеча и предплечья, задние поверхности голени, бедра, ягодичная область). Источником роста опухоли всегда бывают ткани, расположенные глубоко относительно поверхностной фасции [6, 7].
Темпы роста образования обычно медленные, при этом рецидивы новообразования развиваются более бурно, чаще всего в течение нескольких месяцев. Клинически АФ выглядит как плотная, малосмещаемая (реже – несмещаемая) опухоль, расположенная в толще мышечного массива, слегка болезненная при пальпации, размеры ее колеблются от 3-5 до 10-12 сантиметров. В ряде случаев отмечается связь опухоли с надкостницей подлежащих костей.
Клинические проявления АФ абдоминальной локализации также зависят от расположения и распространенности опухолевого процесса. Основными симптомами опухоли считаются ощущение дискомфорта, боли в животе, тошнота, утомляемость, увеличение в размерах живота, периодические подъемы температуры тела. Если опухоль прорастает стенку кишечной трубки, может возникнуть кишечное кровотечение или симптомы «острого живота» [8, 10].
Цель работы – оценить эффективность комплексного лечения агрессивного фиброматоза у детей.
Материал и методы
В клинике детской хирургии Донецкого национального медицинского университета за последние 26 лет лечилось 17 детей с АФ в возрасте от 11 месяцев до 16 лет. Лиц женского пола было – 9, мужского – 8. Опухоли экстраабдоминальной локализации выявлены у 12 (70,6%) больных, интраабдоминальной – у 5 (29,4%). Для подтверждения диагноза использовали ультразвуковое исследование (УЗИ), компьютерную томографию (КТ), магнитно-резонансную томографию.
Результаты и обсуждение
Среди наблюдаемых нами больных с экстраабдоминальной локализацией опухоль располагалась в самых различных местах: ягодичная область (2), предплечье (2), шея (2), лопаточная область (2), плечо (2), по одному пациенту на голени и подмышечной области с переходом на грудную стенку. Давность заболевания у наблюдаемых больных варьировала от нескольких недель (11 детей) до нескольких месяцев (6 пациентов). Приводим одно из наших наблюдений.
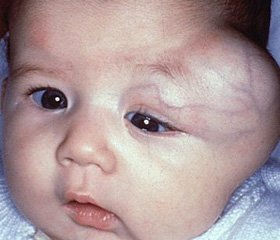
Больной Л., 1 года (история болезни № 13838), поступил в клинику детской хирургии 28.11.2011 г. с жалобами родителей на наличие у ребенка опухолевидного образования в области шеи справа. Болеет с 2-месячного возраста, когда было впервые обнаружено опухолевидное образование до 1 см в диаметре, осмотрен детским хирургом, заподозрена боковая (дермоидная?) киста шеи, рекомендовано наблюдение. Состояние оставалось удовлетворительным, однако опухолевидное образование увеличилось в размерах. С подозрением на тератому, агрессивный фиброматоз госпитализирован в клинику. Общее состояние при поступлении средней тяжести, самочувствие – удовлетворительное. Со стороны внутренних органов без особенностей. Место болезни: в области боковой поверхности шеи, справа, от угла нижней челюсти до яремной ямки, на уровне кивательной мышцы определяется опухолевидное образование, размерами 8´5 см, плотной консистенции, бугристое, не спаянное с кожей, ограничено подвижное, безболезненное. Был обследован, со стороны клинических и биохимических анализов изменений не выявлено. Мультисрезовая КТ (15.11.2011 г.): справа в мягких тканях шеи определяется дополнительное образование овальной формы с ровными, достаточно четкими контурами, размерами 8´6´5 см, по периферии которого в артериальную фазу визуализируется питающие его сосуды. Нижний край образования определяется парастернально (рукоятка грудины). Дифференцировать кивательную мышцу не представляется возможным. Верхний конец образования визуализируется на уровне угла нижней челюсти, книзу от края околоушной слюнной железы. Образование вплотную прилежит к яремной вене, сдавливает её, смещает кзади, также прилежит и деформирует общую сонную, частично наружную и внутреннюю сонные артерии (на протяжении до 1,5 см), смещает их медиально, просвет не суживает. Наружные контуры между образованием и прилегающими к нему сосудами местами четко не прослеживаются, однако, не смотря на деформацию сосудов и сдавление яремной вены, внутренние контуры всех сосудов – ровные, четкие, просвет их выполнен контрастным веществом. Просвет трахеи не сужен, на уровне образования несколько смещен влево. В остальном без патологии (со стороны грудной клетки, брюшной полости). Клинический диагноз: опухоль боковой поверхности шеи справа (тератома?, агрессивный фиброматоз?). 29.11.2012 г. ребенок оперирован.
После обработки операционного поля в косом направлении произведен разрез кожи длиной до 9 см над опухолевым конгломератом. Гемостаз. На всем протяжении рассечена m. platysma. Начато поэтапное выделение опухоли, которая представлена одиночным крупным узлом плотной ткани желтоватого цвета. Постепенно, с соблюдением принципов гемостаза, опухоль полностью выделена из окружающих тканей вплоть до внутренней яремной вены, последняя располагалась вдоль основания опухолевидного образования. Лигированы и пересечены два артерио-венозных пучка, питавших опухолевый узел. Опухоль удалена без нарушения целостности капсулы. Дополнительно удалены 2 лимфатических узла размерами 1´0,8´0,5 см, предлежавших к опухоли. Контроль на гемостаз – кровотечения нет. Послойное ушивание операционной раны наглухо. Интрадермальный шов на кожу. Туалет раны. Асептическая повязка.
Диагноз: рабдомиома (?), агрессивный фиброматоз (?) боковой поверхности шеи справа. Послеоперационный период протекал гладко. Рана зажила первичным натяжением, швы сняты. Заключение патогистологического исследования (№ 11742-63): АФ, в лимфоузлах – гиперплазия лимфоидной фолликулов, гистиоцитоз синусов. 12.12.2011 г. ребенок выписан домой в удовлетворительном состоянии. Был осмотрен через 2 месяца. Жалоб у родителей нет. Клинических и сонографических данных за рецидив опухоли нет.
При локализации АФ в ягодичной области и мягких тканях задней поверхности бедра, серьезную проблему представляет взаимоотношение опухоли к седалищному нерву, который может быть частично или полностью вовлечен в опухолевый процесс. Удаление такой опухоли сопряжено с риском послеоперационного монопареза конечности и возможной нерадикальностью, вследствие технической сложности полного освобождения седалищного нерва от опухоли. В такой ситуации приходится рассчитывать на химиолучевую терапию. В подтверждении сказанного, приводим наше наблюдение.
Ребенок В., 5 лет (история болезни № 9349), поступил в клинику детской хирургии 12.08.2010 г. с жалобами на увеличение в объеме правой ягодицы. Болеет в течение 3-4 недель, когда выявили увеличение ягодицы. Осмотрен хирургом, направлен в клинику. Состояние при поступлении удовлетворительное. Активен, не лихорадит. Со стороны легких и сердца без особенностей. Живот мягкий, безболезненный. Со стороны клинико-лабораторных анализов без особенностей. Место болезни: правая ягодица увеличена в объеме, напряжена. В толще мышечного массива определяется плотная опухоль до 5,0 см в диаметре. В клинике был обследован. УЗИ: в правой ягодичной области лоцируется бугристое образование, размерами 63´40 мм. При ЦДК прослеживается кровоток. Образование исходит, вероятнее всего, из мышечной и соединительной ткани, подкожно-жировой слой не изменен.
Спиральная КТ: в мягких тканях правой ягодичной области, под большой ягодичной мышцей визуализируется мягкотканое образование, размерами 6,8´4,8´8,8 см, неравномерно накапливающее контрастное вещество, больше в периферических отделах. Деструктивных изменений костных структур на уровне исследования не выявлено. Заключение: новообразование мягких тканей правой ягодичной области. Диффузные изменения печени.
18.08.2010 г. операция: дугообразный разрез длиной до 10 см над опухолью в области правой ягодицы. Гемостаз. Рассечена поверхностная фасция и частично большая ягодичная мышца. Тупым и острым путем выделено опухолевидное образование, белесовато-серого цвета, каменисто-хрящевидной плотности, размерами 9´6´4,5 см. Оказалось, что опухоль прорастает седалищный нерв и капсулу тазобедренного сустава, врастает в запирательное отверстие и интимно спаяна с крестцом. По частям удалено до 2/3 опухолевого массива. Гемостаз. Рана ушита до резиново-марлевого выпускника, поставленного к ее дну. Швы на кожу. Асептическая повязка. Макропрепарат: опухоль каменистой, местами хрящевидной плотности, белесовато-серого цвета, гомогенная, с кровоизлияниями. Общий размер удаленной части образования 6´3,5´3,5 см. Послеоперационный период протекал без осложнений. Рана зажила первичным натяжением. Патогистологическое заключение (№ 6401-34): агрессивный фиброматоз. 28.08.10 пациент выписан домой.
08.12.2010 г. ребенок консультирован детским онкологом в национальном институте рака г. Киева. Из-за прорастания опухолью седалищного нерва провести радикальную операцию не представляется возможным. Рекомендовано провести курс полихимиотерапии (ПХТ): метотрексат 30 мг/м2 – 1 раз в неделю (№ 12); винбластин 6 мг/м2 – 1 раз в неделю (№ 12), тамоксифен 10 мг/м2 – ежедневно в течение трех месяцев. Опухолевидное образование уменьшилось в размере. Спустя 1,5 месяца курс ПХТ проведен повторно. Затем проведена телегамматерапия в суммарной дозе 45 Гр. на ложе опухоли. Опухоль уменьшилась до 2 см в диаметре. Мальчик повторно направлен в национальный институт рака для коррекции терапии.
Среди наших пациентов с экстраабдоминальной локализацией после радикальных операций рецидивы отмечены у 4 детей (33,3%), причем у 2 больных е- дважды. Они оперированы повторно, затем был проведен курс ПХТ: метотрексат, винбластин, блеоцин. Одному ребенку назначен курс телегамматерапии в суммарной дозе 60 Гр. Родители одного пациента от химиолучевой терапии отказались. Среди детей с интраабдоминальной локализацией у 4 опухоль располагалась в забрюшинном пространстве с прорастанием брыжейки кишечника. В одном случае опухоль удалена полностью, у двух – частично, у одного ребенка произведена только биопсия опухоли. Еще у 1 больной имел место АФ правого яичника и матки. После удаления опухоли наступило выздоровление. Приводим одно из наших наблюдений пациентов этой группы.
Больной П., 5 лет, поступил в клинику 25.11.1985 г. с жалобами родителей на увеличение в размерах живота ребенка, плохой аппетит. Из анамнеза известно, что в 1982 г. оперирован во Владивостоке по поводу синдрома портальной гипертензии. Произведена спленэктомия, краевая резекция печени, оментогепатодиафрагмопексия. После операции чувствовал себя удовлетворительно, а с августа 1985 г. замечено увеличение в размерах живота, в брюшной полости стало пальпироваться опухолевидное образование, ухудшился аппетит. Обследован по месту жительства, с подозрением на опухоль брюшной полости пациент доставлен в клинику.
При поступлении общее состояние средней тяжести. Кожные покровы бледные. Пониженного питания. Легкие и сердце без особенностей. Пульс до 100 ударов в минуту, удовлетворительных свойств. Живот резко увеличен в объеме, больше в эпигастральной и мезогастральной области, участвует в акте дыхания. Передняя брюшная стенка несколько пастозна, выражен венозный рисунок. По средней линии живота послеоперационный рубец, размером 15´0,5 см. В брюшной полости определяется плотное, бугристое, малоподвижное опухолевидное образование, уходящее верхним краем под печень, а нижним – на 3-4 см ниже пупка. Симптомов раздражения брюшины нет. Анализ крови: Hв – 110 г/л, эр. – 3,4 Т/Л, л. – 10,2 Г/Л, СОЭ – 44 мм/час. Анализ мочи без патологических изменений. Общий белок – 58,7 г/л, трансаминазы в пределах нормы. Диагноз: фибросаркома (лимфосаркома?) брюшной полости с прорастанием в забрюшинное пространство. 18.12.1985 г. после предоперационной подготовки больной оперирован.
В брюшной полости обнаружено плотное, мелкобугристое опухолевидное образование, исходящее из забрюшинного пространства, прорастающее брыжейку кишечника, деформирующее двенадцатиперстную кишку и поджелудочную железу, интимно спаянное с аортой и нижней полой веной, размером 16´12´9 см. На основании макроскопического вида образования высказано предположение в пользу обширной фибросаркомы (фиброматоза?) забрюшинного пространства. Опухоль признана иноперабельной. Произведена биопсия опухоли. Гистологическое заключение: агрессивный фиброматоз с наличием очагов воспаления.
Послеоперационный период протекал гладко. Рана зажила первичным натяжением. С учетом размеров опухоли и наличием воспалительных изменений в ней, решено провести 2 курса лучевой терапии по 85 Гр. с интервалом в 2,5 месяца. После первого курса образование значительно уменьшилось в размерах, а после второго перестало определяться. Больной осмотрен через 1, 2 и 5 лет после операции. Клинически и при обследовании данных, свидетельствующих о рецидиве опухоли, нет.
Выводы
1. Лечение агрессивного фиброматоза только хирургическим методом не всегда является эффективным, так как опухоль склонна к постоянному рецидивированию. По нашим данным, рецидивы при экстраабдоминальном расположении опухоли отмечены у 33,3% больных.
2. При интраабдоминальном расположении агрессивного фиброматоза радикальную операцию удалось выполнить только у 40% пациентов.
3. После повторной операции по поводу рецидива опухоли необходимо проводить химио-лучевую терапию.
4. Больные с агрессивным фиброматозом должны находиться на диспансерном учете, сонографический контроль необходимо проводить ежемесячно.
1. Ашкрафт К.У. Детская хирургия / К.У. Ашкрафт, Т.М. Холдер. – Спб.: ООО «Раритет-М». – 1999. – 400 с.
2. Грона В.Н. Опухоли и опухолеподобные образования у детей / В.Н. Грона, В.К. Литовка, И.П. Журило, К.В. Латышов. – Донецк: Норд-Пресс. – 2010. – 364 с.
3. О десмоидном фиброматозе у детей / В.П. Кононученко, В.К. Литовка, И.П. Журило [и др.] // Проблемні питання педіатріі, та вищої медичної освіти (II випуск): Зб. наукових праць. – Донецьк: Норд-Пресс. – 2008. – С. 164-165.
4. Результаты комбинированного лечения агрессивного фиброматоза у детей / М.С. Лосева, В.И. Ковалев, В.А. Стыков [и др.] // Материалы конф.: Достижения и перспективы детской хирургии. – СПб. – 2002. – С. 145.
5. Агресивний фіброз у дітей / А.А. Переяслов, І.С. Гоменюк, О.О. Трошков, М.П. Локодчак // Хірургія дитячого віку. – 2011. – № 2. – С. 62-65.
6. Low-dose chemotherapy with methotrexate and vinblastine for patients with advanced aggressive fibromatosis / A. Azzarelli, A. Gronchi, R. Bertulli [et al.] // Cancer. – 2001. – Vol. 92. – Р. 1259-1264.
7. Buitendijk S. Pediatric aggressive fibromatosis. A retrospective analysis of 13 patients and review of the literature / S. Buitendijk, C.P. Van de Ven, T.G. Dumans [et al.] // Cancer – 2005. – Vol. 104. – Р. 1090-1099.
8. Fletcher C.D.M. Word Healh Organisation Classification of Tumors. Pathology and Genetics of Tumours of Soft Tissue and Bone. / C.D.M. Fletcher, K.K. Unni, F. Mertens. – IARC: Lyon. – 2002.
9. Aggressive fibromatosis: a challenge for paediatric oncologikal surgery / J. Godzinski, W. Sulka, M. Rapala [et al.] // Pediatr. Blood cancer. – 2003. – Vol. 41. – Р. 278.
10. Surgical management of intra – abdominal desmoids tumors / A.J. Smith, J.J. Lewis, N.B. Merchant [et al.] // Br. J. Surg. – 2000. – Vol. 87. – Р. 776-784.
11. Fibromatosis: benign by name but not necessarily by nature / S. Tolan, J.H. Shanks, M.Y. Lohz [et al.] // Clin. Oncol. – 2007. – Vol. 19. – Р. 319-326.
12. Wong S.L. Diagnosis and management of desmoid tumor and fibrosarcoma / S.L. Wong // J. Surg. Oncol. – 2008. – Vol. 97. – Р. 554-558.