Украинский журнал хирургии 1 (10) 2011
Вернуться к номеру
Первый опыт использования радиохирургии при лечении больных с немелкоклеточным раком легких
Авторы: Ю.П. Спиженко, О.Е. Бобров, Т.И. Чеботарева, А.Л. Леонович, Ю.Н. Лещенко, О.А. Шараевский, С.Н. Лучковский, Центр онкологии и радиохирургии «Киберклиника Спиженко», Украина
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
Проведено проспективное, нерандомизированное исследование, основанное на анализе опыта лечения 28 больных с немелкоклеточным раком легкого (5 женщин и 23 мужчин, в возрасте от 47 до 74 лет). Всего у 28 больных было проведено 76 фракций (операций) по поводу 67 опухолей. Только у 5 больных были одиночные опухоли легкого объемом от 4,6 до 68,8 мл (медиана – 34±2,4 мл). У 19 больных – множественные опухоли легких, объемом от 23,7 до 97,5 мл (медиана – 48±1,8 мл). В группе больных с немелкоклеточным раком легкого и метастазами в головной мозг – у 5 больных был один метастаз, у остальных – от 2 до 12 метастазов. Лечебная изодозная кривая обычно составляла 67-90% от используемой дозы для злокачественных (немелкоклеточных) опухолей легких. Величина разовой дозы при периферическом раке составляла 18,5-20,0 Гр, при центральном раке – 10,5-12,5 Гр (количество фракций от 3 до 5). Доза за одну фракцию при лечении метастазов в легкие достигала 10-15 Гр (количество фракций 3-4). Лечение метастазов немелкоклеточного рака легкого в головной мозг проводили за 1-5 фракций, при величине разовой дозы от 5 до 18 Гр. Полного исчезновения опухоли удалось добиться у 2 больных с периферическим НМРЛ и у 4 больных с одиночными метастазами немелкоклеточного рака легкого в головной мозг. Еще у 13 больных объем опухоли уменьшился, а у 7 – стабилизировался. Ни у одного больного после радиохирургического лечения прогрессирования опухоли не наблюдали.
Було проведено проспективне нерандомізоване дослідження на основі аналізу досвіду лікування 28 хворих з немілкоклітинним раком легенів (5 жінок та 23 чоловіки, віком від 47 до 74 років). Усього у 28 хворих було проведено 76 фракцій (операцій) з приводу 67 пухлин. Тільки у 5 хворих були одиничні пухлини легені об’ємом від 4,6 до 68,6 мл (медіана 34±2,4 мл). У 19 хворих – множинні пухлини легенів, об’ємом від 23,7 до 97,5 мл (медіана – 48±1,8 мл). У групі хворих з немілкоклітинним раком легенів та метастазами в головний мозок – у 5 хворих був один метастаз, у решти – від 2 до 12 метастазів. Лікувальна ізодозна крива зазвичай складала 67-90% дози, що використовувалась для злоякісних (немілкоклітинних) пухлин легенів. Величина разової дози при периферійному раку складала 18,5-20,0 Гр, при центральному раку – 10,5-12,5 Гр (кількість фракцій від 3 до 5). Доза за одну фракцію при лікуванні метастазів в легені сягала 10-15 Гр (кількість фракцій 3-4). Лікування метастазів немілкоклітинного раку легенів в головний мозок проводили за 1-5 фракцій, при величині разової дози від 5 до 18 Гр. Повного зникнення пухлини вдалося досягнути у 2 хворих з периферійним немілкоклітинним раком легенів та у 4 хворих з одиничними метастазами немілкоклітинного раку легенів в головний мозок. Ще у 13 хворих об’єм пухлини зменшився, а у 7 – стабілізувався. У жодного хворого після радіохірургічного лікування прогресування пухлини не спостерігалося.
he prospective non-randomized research has been conducted on the basis of treatment of 28 patients with non-small-cellular lung cancer (5 females and 23 males, aged 47-74). 28 patients were operated on 76 fractions (operations) performed on for 67 tumors. Only five patients had single lung tumors with the volume ranging from 4.6 to 68.8 ml (median – 34 ± 2.4 ml). Nineteen patients had multiple lung tumors with the volume ranging from 23.7 to 97.5 ml (median – 48 ± 1.8 ml). In the group of patients with non-small-cellular lung cancer and with metastases to brain, five patients had one metastasis, the rest had 2-12 metastases. Therapeutic isodose curve usually made up 67-90% of the dose, used for malignant (non-small-cellular) tumors of the lungs. A single dose for peripheral cancer ranged from 18.5 to 20.0 Gy, for central cancer – from 10.5 to 12.5 Gy (the amount of fractions varies from 3 to 5). The dose for one fraction used for the treatment of metastases to the lungs reached 10-15 Gy (3-5 fractions). The treatment of non-small-cellular lung cancer metastases to the brain was conducted during 1-5 fractions with a single dose of 5-18 Gy. Two patients with peripheral non-small-cellular lung cancer and four patients with single metastases of non-small-cellular lung cancer to the brain had a total disappearance of the tumor. Thirteen patients had volume decrease of the tumor; seven patients had this volume stabilized. None of the patients after radiosurgical treatment showed tumor progression.
немелкоклеточный рак легкого, радиохирургия.
немілкоклітинний рак легенів, радіохірургія.
non-small-cellular lung cancer, radiosurgery.
Лечение больных с немелкоклеточным раком легкого (НМРЛ) до настоящего времени остается одной из наиболее сложных проблем онкологии. Прежде всего, это связано с особенностями таких опухолей [1, 5]:
- НМРЛ у 70% больных диагностируют при значительном местном и регионарном распространении (IIIВ стадия и выше).
- НМРЛ малочувствителен к существующим стандартным методам лечения (хирургическому, лекарственному и традиционному лучевому).
Сводные сведения о выживаемости больных с НМРЛ, при стандартном лечении, в стадиях – от 0 (Т1N0M0) до IIА-В (Т1-3N0-1M0) в некоторых странах Европы представлены в таблице.
Как свидетельствуют показатели, приведенные в таблице, большинство больных с НМРЛ, у которых заболевание было диагностировано на достаточно ранних стадиях, после стандартного лечения не переживают даже первого года от установления диагноза, а пятилетняя выживаемость в этой группе больных не превышает 5-11%.
Еще хуже прогноз у больных, диагноз которым устанавливают на более поздних стадиях. Как горько «шутят» американские онкологи – «Если на Пасху больному устанавливают диагноз рака легких, то подарки на Рождество ему покупать не нужно».
Ситуация с НМРЛ в Украине, также далека от удовлетворительной. По данным Бюллетеня Национального канцер-реестра № 10 – «Рак в Украине, 2007-2008» – в первый год от установки диагноза умирают 63,9% больных, а пятилетняя выживаемость составляет только 9,4%.
Именно этим и обусловлена актуальность научных исследований, направленных на поиск путей для улучшения результатов лечения больных с НМРЛ.
В конце ХХ века надежды клиницистов при лечении больных с НМРЛ связывали с включением в комплекс лечебных мероприятий лучевого воздействия – дистанционная лучевая терапия (ДЛТ), эндобронхиальная лучевая терапия (ЭБЛТ), брахитерапия и т.п., однако эти надежды не оправдались. Успехи, несомненно, были, но они оказались более чем скромными. Так, по данным C. Mountain [8], у 152 пациентов с НМРЛ (стадия IIА-В (T1N1M0, T2N1M0, T3N0M0)), которым проводили фракционированную лучевую терапию по «радикальной программе» (с суммарной дозой до 60 Гр) удалось добиться увеличения пятилетней выживаемости на 10%. Еще более скромные результаты были получены C. Peres [13], который пришел к выводу, что – «… лучевая терапия не позволяет добиться полного регресса опухоли, но у 5-10% больных обеспечивает положительный паллиативный эффект, улучшая качество жизни пациента».
В итоге, в начале ХХI века лучевую терапию стали рассматривать, не более чем малоэффективную альтернативу хирургии, у пациентов, которые не могут перенести традиционную операцию из-за тяжести сопутствующей патологии, либо, как сугубо паллиативный метод лечения легочных метастазов, у больных с мультифокальными опухолями [12, 18].
Изменения отношения клиницистов-онкологов к возможностям лучевого воздействия при лечении больных с НМРЛ сегодня связано с разработкой принципов «радиохирургии» и изобретением в 2001 году доктором Джоном Адлером роботизированной радиохирургической системы «CyberKnife». Только эта система позволяет подвести к опухоли тумороцидную дозу излучения при минимальной лучевой нагрузке на прилежащие здоровые органы и ткани [9-11].
С 10 сентября 2009 года в Украине в Центре онкологии и радиохирургии «Киберклиника Спиженко» используется комплекс «CyberKnife® G4». Настоящая работа – первое сообщение о личном опыте радиохирургического лечения больных с НМРЛ.
Материал и методы
Проведено проспективное, нерандомизированное исследование, основанное на анализе опыта лечения в период с 10.09.2009 г. по 9.09.2010 г. – 28 больных с НМРЛ. В представленной группе было 5 женщин и 23 мужчины в возрасте от 47 до 74 лет (медиана возраста – 66,4±1,3 года).
Следует отметить, что среди наблюдавшихся нами пациентов, ни у одного не было действительно ранней стадии НМРЛ. У 5 больных диагноз был установлен при II А-В стадии, а у остальных 23 больных были запущенные мультифокальные опухоли (IV клиническая группа). Срок жизни таких больных, при использовании традиционных методов и технологий, обычно, не превышает нескольких месяцев.
Всего у 28 больных было проведено 76 фракций (операций) по поводу 67 опухолей. Только у 9 больных был первичный НМРЛ. Еще у 7 больных были метастазы в легкие колоректального рака, рака почки, меланомы. Еще одну группу (12 больных) составили больные с НМРЛ и метастазами в головной мозг (48 метастазов).
Только у 5 больных были одиночные опухоли легкого объемом от 4,6 до 68,8 мл (медиана – 34±2,4 мл). У 19 больных – множественные опухоли легких, объемом от 23,7 до 97,5 мл (медиана – 48±1,8 мл). В группе больных с НМРЛ и метастазами в головной мозг – у 5 больных был один метастаз, у остальных – от 2 до 12 метастазов.
Решение о возможности использования радиохирургии принимали после оценки результатов обследования, включавшего компьютерную томографию (КТ), магниторезонансную томографию (МРТ) с ангиопрограммой и гистологическое исследование.
Общее состояние пациентов – неспособность перенести традиционное хирургическое вмешательство из-за дыхательной или сердечной недостаточности, тяжелых сопутствующих заболеваний, мультифокального распространения опухоли – противопоказанием к радиохирургии не является. Также не считали противопоказанием проведение пациенту противоопухолевой терапии.
Противопоказаниями для радиохирургии являются мелкоклеточный рак легких, диаметр опухоли более 8 см, распространение опухоли в средостение, крупные бронхи и сосуды.
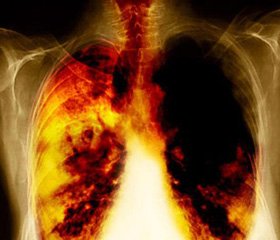
После принятия решения о радиохирургическом вмешательстве пациентам устанавливали (чрескожно, пункционным способом под контролем КТ) золотую рентгенконтрастную метку в «опухоль-мишень»). Спустя 5-7 дней после установки метки, проводили «планирующие» КТ с контрастированием (контраст «Omnipaque 350») и МРТ с последующей объемной 3D-реконструкцией, с определением реальных границ опухоли [10] (рис. 1.).
Планируемый объем «очага-мишени» превышал на 5-8 мм определенные при диагностике размеры опухоли. При этом разрабатывали два плана: один для первичной укладки пациента с ориентацией по костным образованиям позвоночника, для учета и компенсации ротационных смещений (Xsight-spine) (рис. 2.), а второй план – с ориентацией по «метке», введенной в опухоль (Xsight-Lung) (рис. 3.). Амплитуду дыхательных движений контролировали системой «Synchrony». Для этого на пациента надевали специальный жилет со светодиодными датчиками, сигнал от которых улавливала камера «Synchrony», что обеспечивало точное подведение дозы в «мишень» [7].
Дозы и режимы фракционирования были строго индивидуальны для каждого пациента в зависимости от объема опухоли, ее расположения, конфигурации и близости к жизненно-важным структурам. Лечебная изодозная кривая обычно составляла 67-90% от используемой дозы для злокачественных (немелкоклеточных) опухолей легких [5, 6]. Это позволило добиться уверенного покрытия «опухоли-мишени» дозой с конформным (выше 95%) распределением лучевой нагрузки.
Высокая точность подведения дозы к «мишени» (до 0,1 мм при линейных движениях и до 0,1° при ротационных движениях) обеспечивала надежную защиту нормальных тканей и возможность подведения высоких разовых доз.
Величина разовой дозы при периферическом раке составляла 18,5-20,0 Гр, при центральном раке – 10,5-12,5 Гр (количество фракций от 3 до 5). Доза за одну фракцию при лечении метастазов в легкие достигала 10-15 Гр (количество фракций 3-4). Лечение метастазов НМРЛ в головной мозг проводили за 1-5 фракций, при величине разовой дозы от 5 до 18 Гр.
Расчет изодозного распределения и дозного градиента выполняли по алгоритму «Монте Карло», как наиболее точного метода, отражающего дозную нагрузку в патологическом очаге и окружающих тканях.
Результаты и обсуждение
Все больные успешно перенесли лечение в амбулаторных условиях. Осложнение в период освоения методики – пневмоторакс после установки метки – возникло у одного пациента. Это было связано с техническими погрешностями пункции у больного пожилого возраста на фоне эмфиземы легких. Пневмоторакс у него был успешно ликвидирован активным дренированием плевральной полости. Неблагоприятных исходов лечения не наблюдали.
Эффективность тумороцидного воздействия лечения осуществляли по результатам гистологического исследования трепанбиоптата из патологического очага-«мишени» непосредственно по окончанию радиохирургического воздействия (рис. 4, 5.). Контроль за отдаленными результатами лечения осуществляли ежемесячно с использованием физикального осмотра и КТ или МРТ (рис. 6, 7.).
Оценку результатов радиохирургического лечения проводили по трехступенчатой шкале. Хорошими считали результат, когда удавалось добиться исчезновения опухоли, удовлетворительным – если объем опухоли уменьшался или стабилизировался, и плохим – если рост опухоли прогрессировал.
/22/22_2.jpg)
Полного исчезновения опухоли удалось добиться у 2 больных с периферическим НМРЛ и у 4 больных с одиночными метастазами НМРЛ в головной мозг. Еще у 13 больных объем опухоли уменьшился, а у 7 – стабилизировался. Ни у одного больного после радиохирургического лечения прогрессирования опухоли не наблюдали.
Сроки наблюдения за больными составили от 1,5 до 11 месяцев. На 10.09.2010 г. все пролеченные нами больные были живы.
Дискуссия
Радиохирургия – сравнительно молодая технология. От момента изобретения «CyberKnife» прошло только 16 лет, несколько старше его предшественник «Гамма-нож». Но, несмотря на молодость, успехи радиохирургии производят на специалистов-онкологов воистину ошеломляющее впечатление. Значит ли это то, что традиционные хирургические вмешательства отжили свое? И – да, и – нет.
Во-первых, далеко не все клиники, имеющие «CyberKnife» занимаются лечением больных с раком легких. В одних странах это связано с особенностями законодательства в области медицины, запрещающего установку «меток», в других – на первый план выходят чисто экономические причины. Понятно, что владельцы клиник попросту избегают излишних рисков и расходов, связанных с содержанием подразделений для инвазивных вмешательств. Так что клиник, проводящих лечение больных с опухолями паренхиматозных органов, в том числе и легких, в мире не так уж много.
Во-вторых, несмотря на постоянно увеличивающееся число публикаций, подтверждающих высокую эффективность «CyberKnife» при НМРЛ, а также посвященных разработке оптимальных параметров и режимов лечения [4, 5, 14, 16], технология встречает ничем не обоснованное сопротивление «традиционных» онкологов. Но затормозить прогресс, а тем более его остановить, уже вряд ли удастся. Количество клиник, имеющих в своем арсенале «CyberKnife» быстро растет, и приближается к 200, а число пролеченных больных уже превысило 190000.
Наиболее убедительны на сегодняшний день недавно опубликованные данные группы исследователей из отдела онкологии университета в Майами под руководством William T. Brown [2], а также работа Noelle C. van der Voort van Zyp с соавторами [17] из отдела радиационной онкологии «Daniel den Hoed-Erasmus» медицинского центра Роттердама (Нидерланды). Обе группы ученых пришли к выводу о том, что радиохирургия заявила о себе, как высокоэффективная, альтернативная традиционной хирургии технология. Особое значение и перспективы она имеет у больных, для которых обычное хирургическое вмешательство непереносимо.
1. Орлова Р.В. Современное стандартное лечение больных немелкоклеточным раком лёгкого с учётом стадии заболевания / Р.В. Орлова // Практическая онкология. – 2000. – № 3. – С. 43-48.
2. Brown W.T. Lung metastases treated by CyberKnife image-guided robotic stereotactic radiosurgery at 41 months / W.T. Brown, X. Wu, J.F. Fowler, S. Garcia [et al.] // South Med. J. – 2008. – № 101 (4). – Р. 376-382.
3. Cancer incidence in five continents. – Lyon: IARC, Sci. Publ., 1997. – Vol. 7, № 143. – 240 p.
4. Dieterich S. Dynamic tracking of moving tumors in stereotatic radiosurgery / S. Dieterich // Robotic Radiosurgery. – Sunnydale Ca, CyberKnife Society Press, 2005. – Vol. 1. – Р. 51-80.
5. Fowler J.F. A challenge to traditional radiation oncology / J.F. Fowler, W.A. Tome, J.D. Fenwick [et al.] // Int. J. Radiat. Oncol. Biol. Phys. – 2004. – Vol. 60. – Р. 1241-1256.
6. Fritz P. Stereotactic, single-dose irradiation of stage I non-small cell lung cancer and lung metastases / P. Fritz, H.J. Kraus, W. Muhlnickel // Radiat. Oncol. – 2006. – Vol. 1. – Р. 30.
7. Hara R. Stereotactic single high dose irradiation of lung tumors under respiratory gating / R. Hara, J. Itami, T. Kondo // Radiother. Oncol. – 2002. – Vol. 63. – Р. 159-163.
8. Mountain C. Surgery of lung cancer including adjunctive therapy / C. Mountain // Lung cancer. – Amsterdam, 1994. – P. 71-92.
9. Nagata Y. Clinical outcomes of 3D conformal hypofractionated single high-dose radiotherapy for one or two lung tumors using a stereotactic body frame / Y. Nagata, Y. Negoro, T. Aoki // Int. J. Radiat. Oncol. Biol. Phys. – 2002. – Vol. 52. – Р.1041-1046.
10. Nakagawa K. Megavoltage CT-assisted stereotactic radiosurgery for thoracic tumors: original research in the treatment of thoracic neoplasms / K. Nakagawa, Y. Aoki, M. Tago // Int. J. Radiat. Oncol. Biol. Phys. – 2000. – Vol. 48. – Р. 449-457.
11. Okunieff P. Stereotactic body radiation therapy (SBRT) for lung metastases / P. Okunieff, A.L. Petersen, A. Philip // Acta. Oncol. – 2006. – Vol. 45. – Р. 808-817.
12. Pastorino U.B. Long-term results of lung metastasectomy: prognostic analyses based on 5206 cases / U.B. Pastorino, M. Buyse, G. Friedel [et al.] // J. Thorac. Cardiovasc. Surg. – 1999. – Vol. 113. – Р. 37-49.
13. Peres C. Principles and Practice of Radiation Oncology / C. Peres. – Philadelphia: J.P. Lippincott, 1997. – 332 р.
14. Seppenwoolde Y. Accuracy of tumor motion compensation algorithm from a robotic respiratory tracking system: a simulation study / Y. Seppenwoolde, R.I. Berbeco, S. Nishioka // Med. Phys. – 2007. – Vol. 34. – Р. 2774-2784.
15. Survival of Cancer Patients in Europe: The EUROCARE&2 Study. – Lyon: IARC Sci. Publ, I998. – № 151. – 572 p.
16. Timmerman R.D. Stereotatic body radiotherapy in multiple organ sites / R.D. Timmerman, B.D. Kavanagh, L.C. Cho // J. Clin. Oncol. – 2007. – Vol. 25. – Р. 947-952.
17. van der Voort van Zyp N. Stereotactic radiotherapy with real-time tumor tracking for non- small cell lung cancer: Clinical outcome / N. van der Voort van Zyp, C. Prevost Jean-Briac, M.S. Hoogeman // Radiotherapy and Oncology. – 2009. – Vol. 91. – P. 296-300.
18. Venn G.E. Survival following pulmonary metastasectomy / G.E. Venn, S. Sarin, P. Goldstraw // Eur. J. Cardiothorac. Surg. – 1989. – Vol. 3. – Р. 105-109.

/18/18.jpg)
/19/19.jpg)
/20/20.jpg)
/21/21.jpg)
/22/22.jpg)