Журнал «Травма» Том 14, №1, 2013
Вернуться к номеру
Лабораторні маркери прогнозування іммобілізаційного остеопорозу при переломах проксимального відділу стегна у хворих з ожирінням
Авторы: Лоскутова І.В., Рудой Б.С., ДЗ «Луганський державний медичний університет»
Рубрики: Травматология и ортопедия, Эндокринология
Разделы: Справочник специалиста
Версия для печати
Установлено, що при комплексному обстеженні хворих із переломами проксимального відділу стегна на фоні ожиріння слід включати додаткове вивчення імунологічних та біохімічних показників для раннього прогнозування іммобілізаційного остеопорозу в цієї категорії пацієнтів. Доведено доцільність використання імуномодулюючих засобів, гепатопротекторів та донаторів оксиду азоту в комплексному лікуванні хворих з ожирінням при переломі стегна, які перебувають у стані тривалої гіподинамії.
Установлено, что при комплексном обследовании больных с переломами проксимального отдела бедра на фоне ожирения следует включать дополнительное изучение иммунологических и биохимических показателей для раннего прогнозирования иммобилизационного остеопороза у этой категории пациентов. Доказана целесообразность использования иммуномодулирующих средств, гепатопротекторов и донаторов оксида азота в комплексном лечении больных с ожирением при переломе бедра, которые находятся в состоянии длительной гиподинамии.
We found that the complex examination of patients with proximal femur fractures on the background of obesity should include further study of immunological and biochemical parameters for the early prediction of immobilization osteoporosis in these patients. The expediency of the use of immunomodulating agents, hepatoprotectors and nitric oxide donors in complex treatment of obese patients with hip fractures, which are in a state of prolonged physical inactivity, has been proved.
перелом стегна, ожиріння, остеопороз, іммобілізація, гіподинамія, імунологічні та біохімічні показники.
перелом бедра, ожирение, остеопороз, иммобилизация, гиподинамия, иммунологические и биохимические показатели.
hip fracture, obesity, osteoporosis, immobilization, physical inactivity, immunological and biochemical parameters.
Вступ
До факторів, що можуть провокувати розвиток чи прогресування остеопорозу, зараховують іммобілізацію, оскільки зменшується кровотік у кістках та кістковому мозку [4, 5]. Установлено, що пацієнти з обмеженою руховою активністю втрачають у середньому до 1 % маси трабекулярної кістки протягом тижня [10], або відбувається вірогідне зниження мінеральної щільності кісткової тканини у трубчастих кістках на 4,8 % щомісяця [4, 10]. За даними літератури [5] виявлено розвиток остеопенії та локального остеопорозу в умовах післятравматичної іммобілізації кінцівок. Обмеження рухової активності супроводжується стресовою реакцією із супутніми зсувами метаболізму [2, 3, 8], а також формування імунодефіцитних станів [1, 10].
Нещодавно вважали, що медіатори запалення, перш за все тумор-некротизуючий фактор альфа (TNF-a), інтерлейкіни (IL-1b, IL-6) та інші, продукуються лише клітинами запалення (моноцитами, макрофагами). Однак доведено, що вони також синтезуються клітинами м’язів, міокарда та остеобластами [10]. До локальних факторів, які стимулюють активність остеокластів, належать IL-1b,
IL-3, IL-6, IL-11, TNF-a та TNF-b, макрофагальний колонієстимулюючий фактор, гранулоцитомакрофагальний колонієстимулюючий фактор, фактор стовбурових клітин, простагландини. Локальні фактори, які інгібують активність остеокластів, це інтерферон-g, TGF-b, ІL-4, ІL-13 [5, 10].
Клітини жирової тканини є складовою частиною вродженої імунної системи, носієм її рецепторів. Наявність ожиріння додатково навантажує обмін кальцію та сприяє формуванню остеодефіцитних станів у хворих з обмеженою руховою активністю при переломах проксимального відділу стегна, що можна розглядати як фактор поглибленої втрати кісткової тканини [3, 4].
Таким чином, остеопороз має високу соціальну значимість, оскільки призводить до тяжких наслідків та потребує значних економічних витрат на лікування та реабілітацію хворих.
Метою роботи була оцінка комплексного імунологічного та біохімічного обстеження резорбції та формування кісткової тканини у хворих із переломами проксимального відділу стегна на фоні ожиріння.
Зв’язок роботи з науковими програмами, планами, темами. Роботу виконано відповідно до основного плану науково-дослідних робіт ДЗ «Луганський державний медичний університет» за темою «Оптимізація лікування хворих з ожирінням при наявності перелому проксимального відділу стегна» (номер держреєстрації 0112U003853).
Матеріали і методи дослідження
Під спостереженням було 68 хворих із переломами проксимального відділу стегна віком від 35 до 59 років, із них 37 чоловіків (54,4 %) та 31 жінка (45,6 %). За даними клініко-інструментального обстеження в усіх хворих встановлено аліментарно-конституційне ожиріння (Ож) ІІ–ІІІ ступеня [1]. Індекс маси тіла (ІМТ) розраховували за загальноприйнятою методикою [1] згідно з формулою:
ІМТ = маса тіла (кг)/(зріст (м))2.
При значеннях ІМТ 30,0–34,9 кг/м2 діагностували Ож І ступеня, при ІМТ 35,0–39,0 кг/м2 — Ож ІІ ступеня, при ІМТ понад 40,0 кг/м2 — ІІІ ступеня. Із групи дослідження були виключені пацієнти з остеопорозом та остеопенічним синдромом на момент перелому.
Як лікування було обрано хірургічний метод — ендопротезування та остеосинтез металевими конструкціями.
Стан фагоцитарної активності моноцитів (ФАМ) досліджувався оригінальним чашковим методом [11] із використанням живої добової культури Staph. аureus (штам 505) як об’єкта фагоцитозу. При цьому враховувалися такі фагоцитарні показники: фагоцитарне число (ФЧ), фагоцитарний індекс (ФІ), індекс атракції (ІА) та індекс перетравлення (ІП). Дослідження концентрації циркулюючих імунних комплексів (ЦІК) у сироватці крові здійснювалося методом преципітації в розчині поліетиленгліколю з молекулярною масою 6000 Д [12, 13]. Визначали вміст IL-1b, IL-4, IL-6 та TNF-a у сироватці крові. Результати оцінювали за допомогою імуноферментного аналізу на апараті Labline-022 (фірма Labline Diagnostics, Австрія) з використанням наборів виробництва «ProCon» (ООО «Протеиновый контур», Санкт-Петербург, Росія). Дослідження проводились за методиками виробників.
Для оцінки функціонального стану печінки вивчалися [10] біохімічні показники з використанням уніфікованих методів, що включали визначення у крові рівня загального білірубіну, активності сироваткових амінотрансфераз — аланінамінотрансферази (АлАТ) і аспартатамінотрансферази (АсАТ); активності екскреторних ферментів — лужної фосфатази (ЛФ) і g-глутамілтранспептидази (ГГТП); тимолової проби [10].
Рівень середніх молекул (СМ) вивчали за методикою, запропонованою В.В. Ніколайчиком і співавт. [7–9]. Метод визначення кінцевих стабільних метаболітів NО в крові базується на відновленні нітратів (NO3) до нітритів (NO2) з визначенням останніх за реакцією з реактивом Гриса. Оптичну щільність вимірювали на спектрофотометрі СФ-46 (ФЕК) при довжині хвилі 5 нм. Розрахунок кількості нітритів здійснювали за калібрувальним графіком, побудованим за нітритом азоту.
Лабораторне дослідження проводили в динаміці — у першу добу після травми, через тиждень після травми (для виключення впливу гострих післятравматичних наслідків), на 25-ту — 28-му добу і на 55–60-ту добу після травми.
Математичну обробку отриманих даних проводили з використанням пакетів ліцензійних програм Microsoft Office 2003, Microsoft Excel Stadia 6.1/prof та Statistica, враховуючи основні принципи використання статистичних методів у клінічних дослідженнях [6].
Результати та їх обговорення
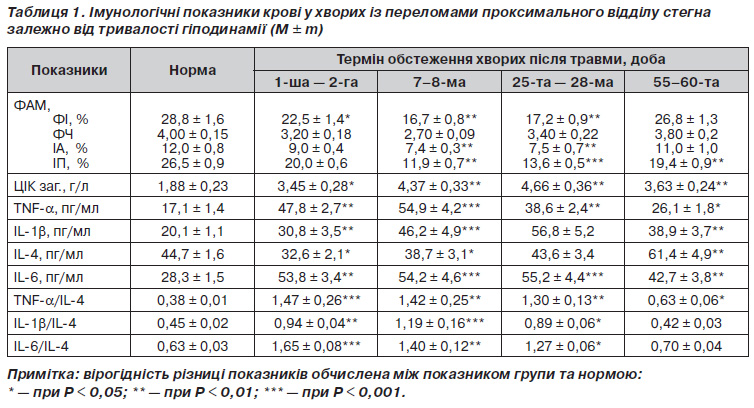
Тривала гіподинамія може суттєво ускладнювати перебіг основного патологічного процесу. Тому проблема раннього прогнозування розвитку іммобілізаційного остеопорозу при переломах стегна у хворих з Ож і проведення у зв’язку з цим лікувально-профілактичних заходів є не тільки медичною, але й соціальною проблемою. У результаті проведеного обстеження хворих із переломами проксимального відділу стегна на фоні Ож було отримано середні показники, що характеризують імунний статус та рівень біохімічних параметрів у даної категорії пацієнтів (табл. 1 і 2).
При проведенні імунологічного дослідження було встановлено, що у хворих із переломами проксимального відділу стегна на фоні Ож до оперативного лікування (у 1-шу добу) було встановлено порушення імунологічних показників (табл. 1). Виявлено зниження показників ФАМ, а саме ФІ — у середньому в 1,27 раза щодо норми (норма 28,8 ± 1,6; Р < 0,05), ФЧ знижено в 1,24 раза (норма 4,0 ± 0,15; Р < 0,05), ІА був помірно знижений в 1,33 раза (норма 12,0 ± 0,8; Р < 0,05), ІП — в 1,38 раза (норма 26,5 ± 0,9 %; Р < 0,05). Загальний рівень ЦІК у сироватці крові становив у середньому 3,45 ± 0,28 г/л, що було в 1,84 раза вище за норму (норма 1,88 ± 0,23 г/л; Р < 0,01). Концентрація ІL-1b була в цей період у 2,38 раза вища за норму (норма 20,1 ± 1,1 пг/мл; Р < 0,01), TNF-a — в 1,8 раза вище за норму (норма 17,1 ± 1,4 пг/мл; Р < 0,01) та ІL-6 — в 1,9 раза вище за норму (норма 28,3 ± 1,5 пг/мл; Р < 0,01). Концентрація протизапального цитокіну ІL-4, навпаки, знижувалася в середньому в 1,37 раза стосовно норми (норма 44,7 ± 1,6 пг/мл; Р < 0,05). Виходячи з цього, коефіцієнти, що відображають співвідношення цитокінів із прозапальною та протизапальною активністю, суттєво збільшувалися: індекс TNF-a/ІL-4 — у середньому у 2,09 раза стосовно норми (Р < 0,01),
ІL-1b/ІL-4 — у 3,87 раза (Р < 0,001), ІL-6/ІL-4 — у 2,62 раза (Р < 0,01). Отже, вивчення цитокінового профілю у хворих із переломами проксимального відділу стегна на фоні Ож виявило збільшення кількості прозапальних цитокінів, але вміст опозиційного протизапального цитокіну вірогідно зменшувався, що викликало суттєвий дефект функціонування цитокінової мережі імунної системи.
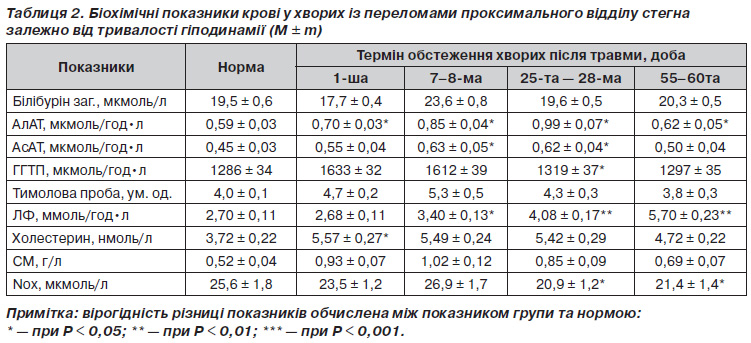
При вивчені функціональних проб печінки встановлено, що в обстежених відзначалися певні зсуви з боку біохімічних показників, що характеризували функціональний стан печінки. Однак вірогідної різниці щодо рівня загального білірубіну у крові протягом періоду спостереження у хворих із переломами проксимального відділу стегна на фоні Ож не було. Зміни ферментативної активності АлАТ, АсАТ, ГГТП та ЛФ у плазмі крові були суттєвими, що свідчить про посилення процесів катаболізму з ушкодженням клітинних мембран при тривалій гіподинамії [10]. При початковому дослідженні активність АлАТ мала тенденцію до підвищення в 1,19 раза (норма 0,59 ± 0,03 мкмоль/год•л; Р > 0,05), АсАТ — в 1,21 раза (норма 0,45 ± 0,03 ммоль/год•л;
Р < 0,05), ГГТП — в 1,27 раза (норма 1286 ±
± 34 мкмоль/год•л; Р < 0,05). Водночас активність ЛФ не виходила за межі норми (2,70 ± 0,11 ммоль/год•л; норма 2,90 ± 0,12 мкмоль/год•л; Р > 0,05). Уміст холестерину в сироватці крові хворих з Ож при переломах проксимального відділу стегна був вищий за норму в 1,5 раза (норма 3,72 ± 0,22 нмоль/л; Р < 0,05), тимолової проби — в 1,17 раза (норма 4,0 ± 0,1 ум.од.; Р < 0,05). За результатами біохімічного дослідження встановлено підвищення концентрації СМ сироватки крові в обстежених у середньому в 1,8 раза (норма 0,52 ± 0,04 г/л; Р < 0,05). У хворих із переломами стегна на фоні Ож рівень нітроксидів (NOх) знаходився на нижній межі (23,5 ± 1,2 мкмоль/мл; норма 25,6 ± 1,8 мкмоль/л; Р > 0,05) (табл. 2).
Отже, у хворих з Ож при переломах проксимального відділу стегна встановлено дестабілізацію імунного гомеостазу — зростання концентрації ЦІК у крові, зниження ФАМ, дисбаланс сироваткових цитокінів за рахунок суттєвого зростання синтезу прозапальних на фоні недостатньої продукції протизапальних.
Повторне обстеження хворих (через 1 місяць) із обмеженою рухової активності з приводу перелому проксимального відділу стегна на фоні Ож виявило погіршення деяких імунологічних та біохімічних показників, що свідчило про порушення процесу кісткової репарації. ФІ був знижений у середньому в 1,67 раза щодо норми (Р < 0,01), тобто нижче від початкового рівня в 1,31 раза (Р < 0,05). Показник ІА у крові хворих на 25–28-й день після перелому стегна був у середньому в 1,62 раза менший за норму і в 1,2 раза стосовно вихідного значення. ФЧ у цей період дослідження вірогідно не змінювалося. Показник ІП в обстежених був нижчий за норму майже вдвічі (Р < 0,01) і менший від початкового рівня в 1,47 раза (Р < 0,01). Було встановлено збільшення загальної концентрації ЦІК у крові до 4,66 ± ± 0,36 г/л, тобто у 2,48 раза вище за норму (Р < 0,01).
Концентрація сироваткового ІL-1b через 1 місяць після травми була вищою за норму у 2,84 раза (Р < 0,001), уміст TNF-a також збільшувався стосовно норми у 2,26 раза (Р < 0,001), рівень ІL-6 — у середньому в 1,95 раза. Рівень зазначених сироваткових цитокінів поступово зростав стосовно початкового рівня (Р < 0,05). Відомо, що IL-1b вважається одним із потужних стимуляторів кісткової резорбції. Цей цитокін продукується макрофагами, що свідчить про його участь у формуванні адекватної імунної відповіді на етапі неспецифічного захисту. Доведено, що він синтезується остеобластами [5]. Водночас TNF-a не лише бере участь у запальних реакціях, але й є молекулярним маркером остеопенії. При Ож TNF-a відіграє важливу роль у підвищенні продукції лептину та IL-6. До того ж TNF-a стимулює активацію ядерного транскрипційного чинника каппа B (kВ), що збільшує продукцію NО — основу запальної реакції в судинній стінці, внутрішньоклітинній адгезії моноцитів і всього каскаду оксидативного стресу [10].
Уміст у сироватці крові ІL-4 на 25-ту — 28-му добу досягав межі норми (Р > 0,05). Виходячи з цих змін вмісту цитокінів у крові, коефіцієнти TNF-a/ІL-4 та ІL-6/ІL-4 були підвищені удвічі (Р < 0,01), зберігався суттєво підвищеним коефіцієнт ІL-1b/ІL-4 — у 3,42 раза щодо норми (Р < 0,01) (табл. 1). У цілому отримані дані дозволяють вважати, що порушення з боку мононуклеарної фагоцитарної системи (МФС) та гуморальної ланки імунного стану мають суттєве значення в патогенезі формування імунних порушень у хворих із переломами проксимального відділу стегна на фоні Ож.
Імунологічне дослідження хворих з Ож при обмеженні рухової активності через 2 місяці після перелому стегна виявило поступове відновлення показників ФАМ, що характеризують функціональну активність МФС. Так, значення ФІ, ФЧ і ІА зростали і досягали нижньої межі норми. Водночас у цей період обстеження показник ІП залишався суттєво нижчим за норму (в 1,37 раза і дорівнював 19,4 ± 0,9 %; Р < 0,01) і вірогідно відрізнявся від початкового рівня (в 1,03 раза; P < 0,05). В обстежених хворих на 55–60-ту добу від отримання травми спостерігалася тенденція до зниження концентрації ЦІК у крові (до 3,63 ± 0,24 г/л) порівняно з попереднім значенням (4,66 ± 0,36 г/л), однак їх рівень залишався значно вищим від початкового вмісту (на 10,5 %; Р > 0,05) та норми (в 1,93 раза; Р < 0,05) (табл. 1).
У хворих з Ож при переломах проксимального відділу стегна (через 2 місяця після травми) поступово зменшувався дисбаланс сироваткових цитокінів у бік підвищення рiвня IL-4 на фоні зниження вмісту цитокінів із прозапальною активністю (TNF-a, IL-1b та IL-6). Концентрація ІL-1b зменшувалася стосовно вихідного значення в 1,23 раза, однак перевищувала значення норми в 1,94 раза (Р < 0,01). Рівень TNF-a був вищий за норму в обстежених пацієнтів в 1,53 раза (Р < 0,01) і вірогідно не змінювався від початкового значення. Уміст ІL-6 залишався підвищеним в 1,51 раза щодо норми (Р < 0,05), хоча був нижчим від початкового рівня в 1,26 раза (Р < 0,05) Доведено, що особи, які страждають від Ож, мають більш високі показники мінеральної щільності кісткової тканини [2].
Рівень ІL-4 у сироватці крові у хворих з Ож через 2 місяці після травми стегна перевищував норму в 1,37 раза (Р < 0,05). Виходячи з цього, коефіцієнти, що відображають співвідношення рівнів цитокінів у крові з прозапальною та протизапальною активністю, були підвищеними. Так, кратність зменшення TNF-a/ІL-4 щодо вихідного значення становила 2,24 раза (Р < 0,01), IL-1b/IL-4 — 2,33 раза (Р < 0,01), IL-6/IL-4 — 2,36 раза (Р < 0,05). Отже, у хворих з Ож після тривалої гіподинамії з приводу перелому проксимального відділу стегна відбувалася нормалізація коефіцієнтів TNF-a/ІL-4 та IL-6/IL-4, хоча індекс IL-1b/IL-4 залишався майже удвічі вищим за норму. Кореляція між концентрацією прозапальних цитокінів TNF-a, ІL-1b та IL-6 та мінеральною щільністю кісток засвідчує роль цитокінів у формуванні іммобілізаційної остеопенії у хворих з Ож при обмеженні рухової активності з приводу перелому стегна.
При повторному вивченні відзначалося поступове зростання активності екскреторних ферментів протягом місяця з тенденцією до нормалізації цих показників через 55–60 діб після травми (табл. 2). Так, активність АлАТ через 1 місяць після травми була в 1,68 раза вища за норму (Р < 0,01), а через 2 місяці відбувалася нормалізація її рівня (Р < 0,01). Аналогічна динаміка відзначалася стосовно показника АсАТ: на 25–28-й день — він в 1,36 раза вищий за норму (Р < 0,01), а на 55–60-ту добу досягав верхньої межі норми. Коливання активності ГГТП та показник тимолової проби у крові обстежених хворих залишалися біля верхньої межі норми. Водночас активність ЛФ та рівень холестерину у крові протягом періоду обстеження поступово зростали. Так, показник ЛФ на 25–28-й день після травми перевищував норму в 1,41 раза (Р < 0,05) і на 55–60-ту добу був удвічі вищим за норму (Р < 0,01). Рівень холестерину у сироватці крові пацієнтів з Ож при тривалій гіподинамії був вищим за норму в 1,43 раза (Р < 0,05) через 1 місяць та в 1,29 раза (Р < 0,05) — через 2 місяці після травми.
Рівень СМ у сироватці крові хворих при обмеженні рухової активності протягом 1 місяця був у середньому в 1,64 раза вищий за норму (норма 0,52 ± 0,03 г/л; Р < 0,05). Концентрація NОх у крові становила 20,9 ± 1,2 мкмоль/л, що було нижче від норми в 1,22 раза (Р < 0,05). Динамічне спостереження довело, що при тривалій гіподинамії з приводу перелому проксимального відділу стегна у хворих з Ож уміст СМ у крові через 2 місяці після травми поступово зменшувався, залишаючись вищим за норму в 1,35 раза (Р < 0,05). Уміст NOх у крові пацієнтів у цей період обстеження становив 21,4 ± 1,4 мкмоль/л, тобто кратність зменшення дорівнювала 1,2 раза (Р < 0,05).
Отже, отримані результати, що були найбільш виражені на 25-ту — 28-му добу після травми, свідчать про несприятливий вплив тривалої гіподинамії на стан органів та систем людини з переломами стегна на фоні Ож.
Лабораторний моніторинг дозволив виявити найбільш інформативні тести оцінки якості регенерації кісткової тканини після хірургічної корекції при переломах проксимального відділу стегна у хворих з Ож. У ранній післяопераційний період (1 міс.), коли рентгенологічна діагностика репаративного остеогенезу ще неінформативна, пропонуємо використовувати вивчення імунологічного статусу та метаболічні показники, що характеризують клініко-функціональний стан організму хворого. Для прогнозування формування іммобілізаційного остеопорозу нами обрано дослідження в динаміці концентрації ЦІК у крові, вмісту сироваткових прозапальних (TNF-a, IL-1b, IL-6) і протизапального (IL-4) цитокінів, рівня СМ у сироватці крові, а також активність ЛФ. Таким чином, вивчення гуморальної ланки імунітету та вираженість синдрому метаболічної інтоксикації у хворих з Ож при переломах проксимального відділу стегна можна використовувати як прогностичні маркери формування іммобілізаційного остеопорозу.
Висновки
1. Комплексне обстеження хворих із переломами проксимального відділу стегна на фоні ожиріння повинно включати додаткове вивчення імунологічних (індекси, що характеризують стан макрофагальної фагоцитуючої системи, концентрації ЦІК у крові, інтерлейкіни-1b, -6, -4 і тумор-некротизуючий фактор a) та біохімічних (екскреторні ферменти — амінотрансферази, лужна фосфатаза, середні молекули у сироватці крові) показників.
2. При тривалій гіподинамії з приводу перелому стегна найбільш вірогідними критеріями прогнозування іммобілізаційного остеопорозу можна вважати стабільно підвищену концентрацію ЦІК та СМ у сироватці крові, а також збереження високого рівня співвідношення IL-1b/IL-4.
3. На підставі отриманих результатів можна рекомендувати включення імуномодулюючих засобів, гепатопротекторів та донаторів оксиду азоту в комплексному лікування хворих з ожирінням при переломі стегна, які перебувають у стані тривалої гіподинамії.
- Бессен Д.Г. Избыточный вес и ожирение / Д.Г. Бессен, Р. Кушнір. — М.: Бином, 2006. — 240 с.
- Динамика медиаторов энергетического обмена и пищевого поведения на фоне терапии ожирения / Г.Е. Волкова, Т.И. Романцова, Т.Г. Вознесенская [и др.] // Ожирение и метаболизм. — 2009. — № 1. — С. 29-36.
- Ожирение — хроническая неинфекционная эпидемия / Н.Е. Вознюк, В.Б. Иванов, А.В. Лосев, С.А. Прилепа // Вестник новых медицинских технологий. — 2006. — Т. ХIII, № 2. — С. 94-96.
- Корж Н.А. Факторы риска остеопороза / Н.А. Корж, Н.В. Дедух // Международный медицинский журнал. — 2007. — № 2. — С. 70-74.
- Котельников Г.П. Лучевая диагностика остеопороза: современное состояние и перспективы / Г.П. Котельников, И.П. Королюк, А.Г. Шехтман // Клиническая геронтология. — № 4. — 2003. — С. 32-36.
- Лапач С.Н. Основные принципы применения статистических методов в клинических испытаниях / С.Н. Лапач, А.В. Чубенко, П.Н. Бабич. — К.: Морион, 2002. — 160 с.
- Николайчик В.В. Способ определения «средних молекул» / В.В. Николайчик, В.М. Моин, В.В. Кирковский // Лаборат. дело. — 1991. — № 10. — С. 13-18.
- Ошакбаев К.П. Взаимосвязь эндогенной интоксикации и избыточной массы тела / К.П. Ошакбаев, Ж.К. Абылайулы // Клиническая медицина. — № 1. — 2005. — С. 53-58.
- Парфенова ГА., Чернядыва И.Ф., Ситина В.К. Средние молекулы — маркер эндогенной интоксикации // Врач. дело. — 1987. — № 4. — С.72-77.
- Поворознюк В.В. Остеопороз та біохімічні маркери метаболізму кісткової тканини // Лабораторна діагностика. — 2002. — № 1. — С. 53-59.
- Фролов В.М. Определение фагоцитарной активности моноцитов периферической крови у больных / В.М. Фролов, Н.А. Пересадин, Л.А. Гаврилова // Лаборат. дело. — 1989. — № 6. — С. 116-118.
- Фролов В.М. Диагностическое и прогностическое значение уровня циркулирующих иммунных комплексов у больных / В.М. Фролов, П.К. Бойченко, Н.А. Пересадин // Врачебное дело. — 1990. — № 6. — С. 116-118.
- Фролов В.М. Исследование циркулирующих иммунных комплексов, их диагностическое и прогностическое значение / В.М. Фролов, В.Е. Рычнев // Лаборат. дело. — 1986. — № 3. — С. 159-161.