Журнал «Травма» Том 14, №2, 2013
Вернуться к номеру
Применение Кеторолака в травматологической практике
Авторы: Макогончук А.В., Винницкий национальный медицинский университет им. Н.И. Пирогова
Рубрики: Ревматология, Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
Целью исследования стала оценка эффективности и безопасности парентеральной и пероральной форм Кеторола при последовательном назначении больным с умеренным и выраженным болевым синдромом при травмах опорно-двигательного аппарата.
В исследование были включены 105 пациентов (60 мужчин и 55 женщин) в возрасте от 30 до 60 лет с различными травмами конечностей.
Общая длительность лечения больного в исследовании составила три дня. На первом этапе лечения больным назначался Кеторол в виде внутривенной инъекции в дозе 60 мг, затем внутримышечно (30 мг два раза в сутки) в течение вторых суток, на третьи сутки — в таблетированной форме в суточной дозе 20–30 мг (10 мг два-три раза в сутки). Во время исследования прием других нестероидных противовоспалительных препаратов, анальгетиков исключался.
По полученным результатам выраженность болевого синдрома до лечения составила в среднем 6,8 балла по NRS. После применения первой дозы парентеральной формы препарата Кеторол выраженность болевого синдрома по NRS значительно снизилась (р < 0,001) и составила в среднем 0,9 балла, что вызвано внутривенным введением препарата. Затем боль возобновилась до уровня слабой, после чего наблюдалось стабильное уменьшение интенсивности болевого синдрома практически до полного его исчезновения в течение 3 суток.
В 1 % случаев наблюдались побочные эффекты: гастралгия на третий день лечения и подъем артериального давления (это побочное явление не требовало отмены препарата и корректировалось назначением антигипертензивных средств). Во всех указанных случаях отмены препарата не требовалось.
Метою дослідження була оцінка ефективності та безпеки парентеральної і пероральної форм Кеторолу при послідовному призначенні хворим із помірним і вираженим больовим синдромом при травмах опорно-рухового апарату.
У дослідження були включені 105 пацієнтів (60 чоловік і 55 жінок) віком від 30 до 60 років із різними травмами кінцівок.
Загальна тривалість лікування хворого в дослідженні становила три дні. На першому етапі лікування хворим призначався Кеторол у вигляді внутрішньовенної ін’єкції в дозі 60 мг, потім внутрішньом’язово (30 мг двічі на добу) протягом другої доби, на третю добу — в таблетованій формі у добовій дозі 20–30 мг (10 мг два-три рази на добу). Під час дослідження прийом інших нестероїдних протизапальних препаратів, анальгетиків виключався.
За отриманими результатами вираженість больового синдрому до лікування становила в середньому 6,8 бала по NRS. Після застосування першої дози парентеральної форми препарату Кеторол вираженість больового синдрому за NRS значно знизилася (р < 0,001) і дорівнювала в середньому 0,9 бала, що викликано внутрішньовенним уведенням препарату. Потім біль відновилася до рівня слабкої, після чого спостерігалося стабільне зменшення інтенсивності больового синдрому практично до повного його зникнення протягом 3 діб.
В 1 % випадків спостерігалися побічні ефекти: гастралгія на третій день лікування і підйом артеріального тиску (дане побічне явище не вимагало відміни препарату і корегувалося призначенням антигіпертензивних засобів). У всіх зазначених випадках необхідності у відміні препарату не було.
The aim of the study was to evaluate the efficacy and safety of parenteral and oral forms of Ketorol in sequential administration to patients with moderate to severe pain syndrome in the injuries of the musculoskeletal system.
The study included 105 patients (60 men and 55 women) aged 30 to 60 years with various injuries of the limbs.
The total duration of treatment in the study was three days. In the first stage of treatment patients were administered with Ketorol intravenous injection at a dose of 60 mg, followed intramuscularly (30 mg twice a day) during the second day, then on the third day in tablet form at a daily dose of 20–30 mg (10 mg 2–3 times a day). During the study the use of nonsteroidal anti-inflammatory drugs, analgesics has been excluded.
According to the obtained results, severity of pain syndrome before treatment averaged 6.8 points by NRS. After the first parenteral dose of Ketorol the severity of pain syndrome by NRS significantly decreased (p < 0.001) and averaged 0.9 points, which is caused by the intravenous administration of the drug. Then the pain returned to the level of mild, after which there was a steady decrease in the intensity of pain syndrome almost to it full disappearance during 3rd day.
Side effects were observed in 1 % of cases: gastralgia on the third day of treatment and the increase of blood pressure (this side effect did not require withdrawal and was corrected by antihypertensive drugs). In all these cases, withdrawal was not required.
Современный арсенал обезболивающих препаратов и методов послеоперационного обезболивания продолжает расти быстрыми темпами. Тем не менее в лечении острого болевого синдрома все еще остается ряд проблемных моментов [4, 5].
Все большее количество травматологических операций, особенно ургентных, в настоящее время выполняется в амбулаторных условиях. Эта ситуация требует периоперационноанальгетического режима, который обладает высокой эффективностью, имеет минимальные побочные эффекты и может быть легко управляем как в хирургическом стационаре, так и вне его [12]. Адекватность управления послеоперационной болью является одним из наиболее важных факторов в определении того, когда пациент может безопасно выписаться из травматологического отделения, и имеет большое влияние на способность пациента возобновить нормальную повседневную деятельность [3, 9]. Периоперационное обезболивание традиционно представлено опиоидными анальгетиками. Тем не менее широкое использование опиоидов связано с различными побочными эффектами, такими как угнетение дыхания, сонливость и седативный эффект, тошнота и рвота, зуд, задержка мочи, непроходимость кишечника и запоры, которые могут задержать выписку из стационара и делают их применение недопустимым в амбулаторных условиях [8, 12]. Поэтому анестезиологи и ортопедытравматологи все чаще обращаются к ненаркотическим обезболивающим средствам в качестве адъювантов для управления болью в периоперационном периоде, чтобы минимизировать негативные последствия наркотических анальгетиков [16, 17]. Мультимодальные или сбалансированные методы анальгезии с применением меньших доз опиоидов в сочетании с неопиоидными анальгетиками, такими как местные анестетики, кетамин, ацетаминофен и нестероидные противовоспалительные препараты (НПВП), становятся все более популярными для профилактики боли после операций и травм [6, 10, 11].
Одним из эффективных представителей этой группы является кеторолак (Кеторол, «Доктор Реддис Лабораторис Лтд.», Индия). Кеторолак представляет собой нестероидный агент с сильным обезболивающим эффектом и умеренной противовоспалительной активностью. Его применяют в виде трометаминовой соли перорально, внутримышечно и внутривенно.
Кеторол активно используется уже более 10 лет [1]. Во время его применения, как и при приеме всех НПВП, возможны побочные реакции, в том числе со стороны желудочнокишечного тракта, поэтому его следует принимать только для кратковременного купирования выраженного болевого синдрома, согласно инструкции. Препарат быстро всасывается, обладает высокой биодоступностью (80–100 %). Около 99 % Кеторола связывается с белками плазмы; основной пусть метаболизм Кеторола — связывание с глюкуроновой кислотой, препарат выводится почками (90 %) и кишечником (10 %). Продолжительность действия препарата — 6–10 часов. Выпускается в двух формах: таблетки для приема внутрь по 10 мг и раствор для парентерального введения, который можно вводить в/в и в/м, в ампулах по 30 мг/1 мл.
Клинические исследования показывают, что эффективность одной дозы кеторолака выше, чем морфина, при умеренной и тяжелой послеоперационной боли, при этом частота возникновения побочных эффектов заметно ниже, чем при использовании морфина или петидина [13, 15]. Внутримышечный кеторолак является единственным парентеральным НПВП, доступным для использования в США в качестве анальгетика. Результаты клинического исследования, проведенного с участием 176 пациентов в медицинской школе Университета Эмори, показали, что анальгетическая эффективность кеторолака была сопоставима с двойной дозой морфина и значительно превосходила плацебо [4]. Эффективность кеторолака также выше по сравнению с аспирином, парацетамолом (ацетаминофен) и другими нестероидными противовоспалительными препаратами. Это может также найти применение при острой скелетномышечной боли, при которой кеторолак также демонстрирует достаточно высокую эффективность. Проведены исследования, чтобы полностью оценить потенциал кеторолака в лечении хронических болевых состояний, в которых он показал высокую эффективность в сочетании с парацетамолом [3].
В 1996 году было проведено двойное слепое рандомизированное многоцентровое исследование с участием 244 больных с умеренной болью после крупных ортопедических операций. Пациенты получали внутримышечно кеторолак (60 мг, затем 30 мг), или внутримышечно меперидин (100 мг), или плацебо каждые 2–6 часов, в зависимости от ситуации в течение 5 дней. Болеутоляющее действие оценивали в течение 6 часов после первого приема исследуемого препарата, а затем каждую ночь перед сном. По оценке и пациентов, и наблюдателей кеторолак значительно лучше переносится, чем меперидин, а число пациентов с зарегистрированными побочными эффектами было ниже, чем больных, получавших меперидин [5].
Таким образом, кеторолак открывает перспективы в качестве альтернативы опиоидным и другим нестероидным анальгетикам в улучшении умеренной и тяжелой послеоперационной боли и с приобретением более широкого клинического опыта может найти свое место в лечении острой мышечной боли и других состояний, сопровождающихся болевым синдромом.
Для изучения эффективности и безопасности препарата Кеторол у пациентов с болевым синдромом при травмах на базе кафедры травматологии и ортопедии Винницкого национального медицинского университета им. Н.И. Пирогова было проведено открытое клиническое исследование.
Целью исследования явилась оценка эффективности и безопасности парентеральной и пероральной форм Кеторола при последовательном назначении больным с умеренным и выраженным болевым синдромом при травмах опорнодвигательного аппарата.
Материал и методы исследования
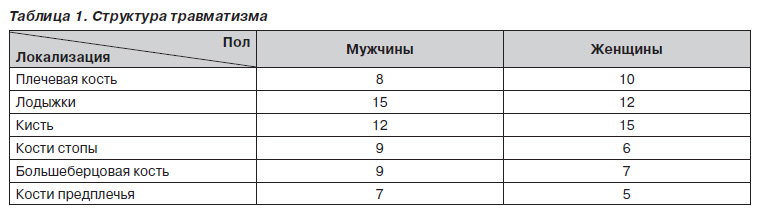
В исследование были включены 105 пациентов (60 мужчин и 55 женщин) в возрасте от 30 до 60 лет. Структура травм представлена в табл. 1. Диагнозы были верифицированы на основании клинических и рентгенологических данных.
Общая длительность лечения больного в исследовании составила три дня. На первом этапе лечения больным назначался Кеторол в виде внутривенной инъекции в дозе 60 мг, затем внутримышечно (30 мг два раза в сутки) в течение вторых суток, на третьи сутки — в таблетированной форме в суточной дозе 20–30 мг (10 мг дватри раза в сутки). Во время исследования прием других НПВП, анальгетиков исключался.
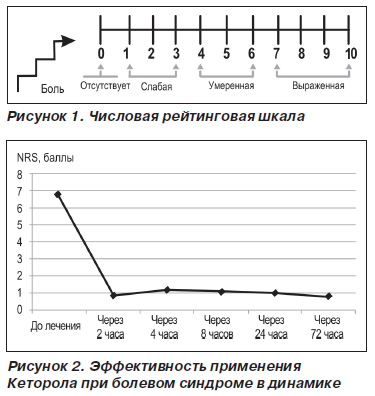
Для оценки эффективности препарата и объективизации оценки болевого синдрома применялась числовая рейтинговая шкала (Numeric Rating Scale, NRS) (рис. 1). Данная шкала является одной из модификаций визуальноаналоговой шкалы, но в то же время она более чувствительна и практична как для пациента, так и для исследователя [18].
Общепринятым стандартом для определения статистически значимого снижения болевого синдрома является 50% его уменьшение [7]. А 30% снижение боли определялось как «значительное улучшение» [14].
Среднее значение интенсивности болевого синдрома составило 6,8 ± 0,1 балла по шкале NRS.
Для статистической обработки материала использовались пакеты программ Statistiсa 6.0 и Microsoft Excel.
Результаты и обсуждение
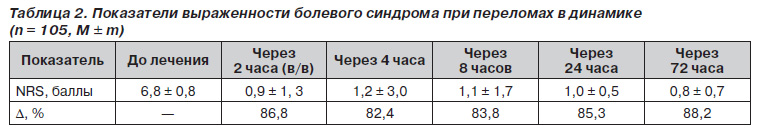
По полученным результатам выраженность болевого синдрома до лечения по NRS составила в среднем 6,8 балла. После применения первой дозы парентеральной формы препарата Кеторол выраженность болевого синдрома по NRS значительно снизилась (р < 0,001) и составила в среднем 0,9 балла, что вызвано внутривенным введением препарата. Затем боль возобновилась до уровня слабой, после чего наблюдалось стабильное уменьшение интенсивности болевого синдрома практически до полного его исчезновения в течение 3 суток. Динамика болевого синдрома во время лечения составила в среднем 86,8; 82,4; 83,8; 85,3 и 88,2 % соответственно по сравнению с начальным уровнем боли (до лечения), что согласно принятым нормативам соответствует статистически значимому снижению интенсивности болевого синдрома (табл. 2).
Наглядно эффективность Кеторола представлена на рис. 2.
Важным этапом исследования является оценка безопасности Кеторола. У 99 % больных отмечалась хорошая и отличная переносимость препарата. У 1 % исследуемых были выявлены побочные эффекты: гастралгия на третий день лечения и подъем артериального давления (возникшее побочное явление не требовало отмены препарата и корректировалось назначением антигипертензивных средств). Во всех указанных случаях отмены препарата не требовалось.
Выводы
Таким образом, Кеторол оказывает достоверно выраженное обезболивающее действие и может быть с успехом использован для раннего эффективного купирования выраженных болевых синдромов, в том числе при переломах, как в стационарной, так и в амбулаторной травматологической практике.
- Стойко Ю.М. Патогенетические аспекты применения нестероидных противовоспалительных препаратов в послеоперационном периоде / Ю.М. Cтойко, В.Г. Гудымович // Медицинский совет. — 2009. — 4. — С. 8892.
- Brown C.R., Moodie J.E., Dickie G., Wild V.M., Smith B.A., Clarke P.J., Evans S.A., Bynum L.J. Analgesic efficacy and safety of singledose oral and intramuscular ketorolac tromethamine for postoperative pain // Pharmacotherapy. — 1990. — 10 (6, Pt 2). — 59S70S.
- Buckley M.M., Brogden R.N. Ketorolac. A review of its pharmacodynamic and pharmacokinetic properties, and therapeutic potential // Drugs. — 1990 Jan. — 39(1). — 86109.
- Chung F., Ritchie E., Su J. Postoperative pain in ambulatory surgery // Anesth. Analg. — 1997. — 85. — 80816.
- DeAndrade J.R., Maslanka M., Reines H.D., Howe D., Rasmussen G.L., Cardea J., Brown J., Bynum L., Shefrin A., Chang Y.L., Maneatis T. Ketorolac versus meperidine for pain relief after orthopaedic surgery // Clin. Orthop. Relat. Res. — 1996 Apr. — 325. — 30112.
- Englbrecht J.S., PogatzkiZahn E.M. Pain management after ambulatory surgery in Germany // Anasthesiol. Intensivmed. Notfallmed. Schmerzther. — 2010 Jan. — 45(1). — 4455; doi: 10.1055/s00291243378. Epub 2010 Jan 20.
- Farrar J.T., Young J.P. Jr, LaMoreaux L., Werth J.L., Poole R.M. Clinical importance of changes in chronic pain intensity measured on an 11point numerical pain rating scale // Pain. — 2001. — 94. — 149158.
- Guignard B., Bossard A.E., Coste C. et al. Acute opioid tolerance: intraoperative remifentanil increases postoperative pain and morphine requirement // Anesthesiology. — 2000. — 93. — 40917.
- Kehlet H., Dahl J.B. Anaesthesia, surgery and challenges in postoperative recovery // Lancet. — 2003. — 362. — 19218.
- Ortiz M.I., MonroyMaya R., SotoRios M., CarrilloAlarcon L.C., PonceMonter H.A., RangelFlores E., LooEstrada J.J., IzquierdoVega J.A., SanchezGutierrez M. Effectiveness of diclofenac, ketorolac and etoricoxib in the treatment of acute pain from ankle fracture // Proc. West Pharmacol. Soc. — 2010. — 53. — 468.
- Paul F. White. The changing role of nonopioid analgesic techniques in the management of postoperative pain // Anesth. Analg. — 2005. — 101. — 522.
- Pierce M.C., Fuchs S. Evaluation of ketorolac in children with forearm fractures // Acad. Emerg. Med. — 1997 Jan. — 4(1). — 226.
- Rawal N., Allvin R., Amilon A. et al. Postoperative analgesia at home after ambulatory hand surgery: a controlled comparison of tramadol, metamizol, and paracetamol // Anesth. Analg. — 2001. — 92. — 34751.
- Rowbotham M.C. What is a «clinically meaningful» reduction in pain? // Pain. — 2001. — 94. — 131132.
- Silvasti M., Svartling N., Pitkanen M., Rosenberg P.H. Comparison of intravenous patientcontrolled analgesia with tramadol versus morphine after microvascular breast reconstruction // Eur. J. Anaesthesiol. — 2000. — 17. — 44855.
- White P.F. Ambulatory anesthesia advances into the new millennium // Anesth. Analg. — 2000. — 90. — 12345.
- White P.F. The role of nonopioid analgesic techniques in the management of pain after ambulatory surgery // Anesth. Analg. — 2002. — 94. — 57785.
- Williamson A., Hoggart B. Pain: a review of three commonly used pain rating scales // Journal of Clinical Nursing. — 2005. — 14. — 798804.