Журнал «Травма» Том 15, №3, 2014
Вернуться к номеру
Порівняльний аналіз геометричних параметрів тривимірних моделей систем «гомілка — апарат зовнішньої фіксації» з різною просторовою орієнтацією опор
Авторы: Гуцуляк В.І., Сулима В.С. - Івано-Франківський національний медичний університет
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
У роботі представлений алгоритм дій щодо створення тривимірних комп’ютерних моделей для черезкісткового остеосинтезу кісток із можливістю візуалізації м’якотканинних структур кінцівок. Використовуючи запропонований алгоритм у програмі Autodesk Inventor 11, створено дві моделі біомеханічних систем: І — «гомілка — апарат зовнішньої фіксації з концентричним розташуванням опор», ІІ — «гомілка — апарат зовнішньої фіксації з ексцентричним розташуванням опор». Результати визначення геометричних параметрів створених моделей показали, що компонування апарату II моделі потребує на 28,9 % менших за радіусом опор і на 29,4–33,3 % коротших черезкісткових елементів порівняно з апаратом І моделі, що зменшує габарити зовнішньої конструкції на 32,4–61,9 %. Проте внаслідок анатомічних особливостей будови гомілки використання опор у формі кілець чи півкілець не в змозі забезпечити адекватної органометричності конструкції.
В работе представлен алгоритм действий для создания трехмерных компьютерных моделей для чрескостного остеосинтеза костей с возможностью визуализации мягкотканных структур конечностей. Используя предлагаемый алгоритм в программе Autodesk Inventor 11, созданы две модели биомеханических систем: І — «голень — аппарат внешней фиксации с концентрическим расположением опор», ІІ — «голень — аппарат внешней фиксации с эксцентрическим расположением опор». Результаты определения геометрических параметров созданных моделей показали, что компоновка аппарата II модели требует на 28,9 % меньших по радиусу опор и на 29,4–33,3 % меньших по длине чрескостных элементов по сравнению с аппаратом І модели, что уменьшает габариты внешней конструкции на 32,4–61,9 %. Тем не менее вследствие анатомических особенностей строения голени использование опор в форме колец или полуколец не в состоянии обеспечить адекватную органометричность конструкции.
This article presents an algorithm of actions while creating three-dimensional computer models for transosseous osteosynthesis with the ability to visualize soft-tissue structures of the limbs. Using the offered algorithm in Autodesk Inventor 11 program, two models of biomechanical systems were created: I — «shin — external fixation device with concentric location of supports», II — «shin — external fixation device with eccentric location of supports». The results of determining geometric parameters of created models showed that the assembling of the model II device requires a 28.9 % smaller radius of the supports and 29.4–33.3 % shorter transosseous elements compared to the model I device that reduces the size of external structures by 32.4–61.9 %. However, due to the anatomy of the shin, the use of supports in the form of rings or semirings are unable to provide an adequate organometric design.
тривимірна модель, апарат зовнішньої фіксації, м’якотканинні структури, алгоритм.
трехмерная модель, аппарат внешней фиксации, мягкотканные структуры, алгоритм.
three-dimensional model, external fixation device, soft-tissue structures, algorithm.
Статья опубликована на с. 18-22
Вступ
Одним із сучасних та найбільш вірогідних методів експериментальних розрахунків властивостей різних конструкцій для використання як у медицині, так і в інших сферах діяльності людини, є метод комп’ютерного тривимірного моделювання, основу якого становить метод кінцевих елементів [1, 2, 6]. Застосування спеціального програмного забезпечення дозволяє розрахувати безліч варіантів біомеханічного впливу різних навантажень на кожний компонент системи та всю систему загалом. Метод дозволяє без значних фінансових витрат, пов’язаних із виготовленням експериментальних взірців та спеціального обладнання для стендових досліджень, виконати комп’ютерне моделювання та наступне віртуальне біомеханічне випробування різних новітніх конструкцій, зокрема систем «кістка — апарат зовнішньої фіксації (АЗФ)» [3–5]. Однак більшість сучасних досліджень систем «кістка — АЗФ» виконують на моделях кісток чи спрощених за конфігурацією трубчатих або циліндричних аналогах із концентричним розташуванням кільцеподібних опор без урахування розміщення м’якотканинних структур [4, 6, 8, 10]. Ексцентричне розташування оточуючих тканин довкола кістки потребує в клінічних умовах особливого компонування рам АЗФ із використанням опор великих діаметрів. Це, на жаль, призводить до послаблення жорсткості фіксації кісткових фрагментів та тривалого дискомфорту для хворого [9, 11]. Більш доречним, з практичного погляду, зокрема для двохкісткових сегментів (гомілки, передпліччя), через їхні анатомічні особливості, є компонування рами АЗФ з ексцентричним розташуванням опор. Не менш важливим є наближення експериментальних моделей апаратів до клінічних умов. Це потребує урахування топографо-анатомічних особливостей сегмента при проведенні черезкісткових елементів, що важко здійснити за відсутності власне м’якотканинних структур. Тому дослідження біомеханіки жорсткості фіксації при черезкістковому остеосинтезі та конструктивних особливостей моделей апаратів з урахуванням розташування м’якотканинних структур сегментів кінцівок залишається маловивченим та актуальним.
Мета роботи: розробити тривимірні комп’ютерні моделі «гомілка — АЗФ» із концентричним та ексцентричним розташуванням опор та провести порівняльний аналіз їхніх геометричних параметрів.
Матеріал і методи
На основі поперечних сканів (із кроком 0,5–1 мм) інтактної гомілки дорослої людини, проведених за допомогою спірального комп’ютерного томографа Siemens Somatom Emotion у програмі Mimix, створені тривимірні моделі кісток та оточуючих м’якотканинних структур із можливістю їх роздільної візуалізації, які трансльовано в програмний комплекс Autodesk Inventor 11 (рис. 1).
У режимі Inspect програми Autodesk Inventor 11 проведено визначення розмірів моделі гомілки на восьми рівнях (рис. 1г). За допомогою інструмента Distance визначали лінійні розміри сегмента в двох взаємно перпендикулярних площинах. Обвід вимірювали за допомогою інструмента Loop.
Розроблений нами покроковий (step-by-step) алгоритм дій дозволив побудувати комп’ютерні тривимірні моделі біомеханічних систем «сегмент — АЗФ» та провести визначення їхніх геометричних параметрів.
Результати та їх обговорення
Алгоритм побудови комп’ютерної тривимірної моделі біомеханічної системи «сегмент (гомілка) — АЗФ» полягає у виконанні таких кроків (step-by-step):
— поетапне створення інтактного анатомічного сегмента, моделей кісток та м’якотканинних структур зі збереженням їх в окремих файлах (Model);
— встановлення сумісних точок чи осей (не менше двох) для моделей кісток та м’якотканинних структур, що забезпечує можливість їх порівняння у файлі складання моделі;
— визначення поздовжньої осі великогомілкової кістки (ВГК);
— моделювання перелому шляхом створення фрагментів кісток та збереження їх в окремих файлах;
— створення файлу складання моделі (Assembly) та вставлення в нього моделей фрагментів кісток;
— орієнтація моделі проксимального фрагмента кістки відносно центру системи координат (із зіставленням площин XY — із фронтальною, XZ — із горизонтальною, YZ — із сагітальною), що забезпечує можливість проведення черезкісткових елементів під заданими кутами та оцінки розкладання векторів сил, що прикладаються до фрагментів кістки при проведенні біомеханічних досліджень;
— встановлення дистального фрагмента кістки відносно проксимального на відстані, що відповідає ширині міжфрагментарної щілини;
— вставлення у файл складання моделі м’якотканинних структур сегмента з забезпеченням їх точної просторової орієнтації щодо кістки шляхом порівняння попередньо встановлених суміжних точок чи осей;
— умовний поділ сегмента шляхом створення «робочих» площин на вісім рівновіддалених рівнів згідно з методом уніфікованого позначення черезкісткового остеосинтезу (МУПЧО) [7];
— надання властивості напівпрозорості м’якотканинним структурам, що забезпечує можливість візуалізації кісткових фрагментів;
— визначення ширини найширшої частини сегмента;
— встановлення поздовжньої осі сегмента в найширшій його частині;
— визначення необхідного типорозміру опор;
— встановлення поздовжньої «робочої» осі для кожної опори, що проходить через її центр;
— встановлення опор АЗФ на необхідних рівнях сегмента шляхом зіставлення поздовжніх осей опор та кістки (сегмента);
— формування кісткових каналів та проведення черезкісткових елементів з урахуванням топографо-анатомічних особливостей вибраного рівня сегмента;
— з’єднання опор між собою та закріплення черезкісткових елементів;
— для проведення біомеханічних досліджень систем «кістка — АЗФ» перед експортом створеної моделі в модуль програми Stress Analysis чи інший програмний комплекс, наприклад ANSYS, необхідно за допомогою команди Suppress — інактивувати м’якотканинні структури сегмента.
Використовуючи запропонований алгоритм, в середовищі програми Autodesk Inventor 11 проведено тривимірне моделювання черезкісткового остеосинтезу при переломах кісток гомілки з використанням АЗФ комбінованого типу з комплекту деталей апарата Г.А. Ілізарова. Типорозмір опор підбирали таким чином, щоб проміжок між шкірними покривами та опорою становив не менше 2 см. Залежно від просторової орієнтації рами апарата довкола фрагментів великогомілкової кістки створено дві тривимірні моделі «гомілка — АЗФ»:
I модель — «гомілка — АЗФ з концентричним розташуванням опор» (рис. 2);
/20/20.jpg)
ІІ модель — «гомілка — АЗФ з ексцентричним розташуванням опор» (рис. 3).
/20/20_2.jpg)
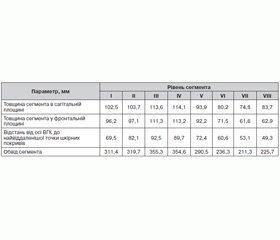
За результатами визначення геометричних параметрів тривимірної моделі гомілки (табл. 1) виявили, що найбільша відстань від осі великогомілкової кістки до найвіддаленішої точки шкірних покривів відповідає IІІ рівню і становить 92,5 мм. Це зумовило вибір опор для І моделі з внутрішнім радіусом 112,5 мм. Найбільша товща сегмента (114,1 мм) відповідає IV рівню в сагітальній площині, що зумовило вибір опор для ІІ моделі з внутрішнім радіусом 80 мм.
Моделювання поперечного перелому обох кісток гомілки проведено на V рівні. Встановлення опор АЗФ відповідно на III, IV та VІ, VII рівнях сегмента проводили шляхом:
— зіставлення поздовжніх осей опор та фрагментів ВГК при побудові І моделі;
— зіставлення поздовжніх осей опор та найширшої частини сегмента при побудові ІІ моделі.
Для можливості проведення порівняльного аналізу моделей черезкісткові елементи проводили на однакових рівнях та позиціях. Представлені моделі відрізняються виключно за діаметром опор, їх просторовою орієнтацією відносно кісткових фрагментів та довжиною використаних черезкісткових елементів.
Тривимірні моделі, розроблені за запропонованим алгоритмом, мають широкий діапазон властивостей, що забезпечує можливість:
— моделювання різних типів переломів кісток;
— використання АЗФ різних типів конструкції;
— різної просторової орієнтації рам апаратів відносно кісткових фрагментів та м’якотканинних структур сегмента;
— визначення оптимального радіуса опор та рівнів їх розташування;
— визначення оптимальних рівнів розташування черезкісткових елементів, їх діаметра та довжини;
— проведення черезкісткових елементів на різних рівнях з урахуванням рекомендованих позицій та позицій доступності згідно з атласом МУПЧО;
— проведення біомеханічних досліджень остеосинтезу.
Результати визначення геометричних параметрів створених моделей систем «гомілка — АЗФ» (табл. 2) показали, що при компонуванні апарата II моделі внутрішній радіус опор становить 80 мм, що на 28,9 % менше порівняно з АЗФ І моделі (112,5 мм). Для фіксації кісткових фрагментів у ІІ моделі використовували консольні черезкісткові елементи довжиною 100 мм, транссегментарні — 180 мм, що відповідно на 33,3 та 29,4 % є коротшими, ніж у І моделі (150 і 255 мм).
Завдяки цьому габарити зовнішньої конструкції у ІІ моделі на ІІІ–VІІ рівнях перевищують латеральний контур гомілки на 33,4–59,9 мм, медіальний — на 41,2–67,5 мм і передній — на 39–43,6 мм, що порівняно з габаритами АЗФ І моделі (60,9–92,6 мм, 74,1–99,8 мм, 102,4–106 мм) відповідно менше на 35,3–48,1 %, 32,4–45,8 % і 58,9–61,9 %. Значні «коливання» показників віддалі від шкірних покривів до контурів АЗФ зумовлені відсутністю органометричності кільцевих опор до анатомічної конфігурації гомілки.
Отже, отримані результати свідчать, що при переломах кісток гомілки ексцентричне розташування кільцевих опор АЗФ є більш раціональним у забезпеченні комфортності для хворого, проте не забезпечує адекватної органометричності конструкції.
Висновки
Створення тривимірних моделей біомеханічних систем «сегмент — АЗФ» для досліджень черезкісткового остеосинтезу слід проводити з візуалізацією м’якотканинних структур кінцівки. Це забезпечує точну просторову орієнтацію рами апарата відносно не тільки кістки, але й шкірних покривів сегмента та можливість проведення черезкісткових елементів з урахуванням топографо-анатомічних особливостей рівня сегмента. При переломах кісток гомілки перевагу слід віддавати ексцентричному розташуванню опор АЗФ, що забезпечує компактність конструкції завдяки зменшенню її габаритів по латеральному, медіальному та передньому контуру відповідно на 35,3–48,1 %, 32,4–45,8 % і 58,9–61,9 % порівняно з концентричним розташуванням опор. Проте внаслідок анатомічних особливостей будови гомілки використання опор у формі кілець чи півкілець не в змозі забезпечити адекватної органометричності конструкції. Вирішення цієї проблеми ми вбачаємо у розробці АЗФ з можливістю адаптації його форми до конфігурації сегмента.
1. Барабаш С.А. Имитационное моделирование деформации фиксирующих устройств как стержневых систем / С.А. Барабаш, А.В. Бушманов // Медицинская информатика. — 2009. — № 1(19). — С. 23-27.
2. Бейдик О.В. Конечно-элементное моделирование жест–кости фиксации костных отломков в аппаратах чрескостного остеосинтеза при лечении диафизарных переломов голени / О.В. Бейдик, К.К. Левченко, А.В. Ткачева // Гений ортопедии. — 2009. — № 1. — С. 24-29.
3. Бур’янов О.А. Метод створення реалістичних скінченно-елементних моделей систем «довга кістка — стрижньовий апарат» / О.А. Бур’янов, А.М. Лакша, Ю.О. Ярмолюк // Матеріали науково-практичної конференції з міжнародною участю «Перший український симпозіум з біомеханіки опорно-рухової системи». — Дніпропетровськ, 2012. — С. 45.
4. Бушманов А.В. Проектирование фиксирующих устройств в травматологии на основе CAD/CAE/CAM-технологий І / А.В. Бушманов // Медицинская информатика. — 2008. — № 1 (15). — С. 3-8.
5. Математичне моделювання діафізарних деформацій довгих кісток / О.А. Тяжелов, Н.Ю. Полєтаєва, К.К. Романенко [та ін.] // Ортопедия, травматология и протезирование. — 2010. — № 3. — С. 61-63.
6. Соловцова Л.А. Программный модуль для расчета прочностных характеристик элементов стержневых устройств / Л.А. Соловцова // Медицинская информатика. — 2008. — № 4(18). — С. 65-71.
7. Соломин Л.Н. Основы чрескостного остеосинтеза аппаратом Г.А. Илизарова / Л.Н. Соломин. — СПб.: ООО «Морсар АВ», 2005. – 544 с.
8. Сравнительный анализ жесткости остеосинтеза, обеспечиваемой чрескостными аппаратами, работающими на основе компьютерной навигации, и комбинированным спице-стержневым аппаратом / Л.Н. Соломин, В.А. Виленский, А.И. Утехин [и др.] // Травматология и ортопедия России. — 2009. — № 2 (52). — С. 20-25.
9. Fragomen A.T. The mechanics of external fixation / A.T. Fragomen, S.R. Rozbruch // HSS J. — 2007. — Vol. 3(1). — P. 13-29. doi: 10.1007/s11420-006-9025-0.
10. Grivas T.B. The use of twin-ring Ilizarov external fixator constructs: application and biomechanical proof-of principle with possible clinical indications / T.B. Grivas, E.A. Magnissalis // J. Orthop. Surg. Res. — 2011. — Vol. 6. — P. 41. doi: 10.1186/1749-799X-6-41.
11. Hybrid external fixation for open severe comminuted fractures of the distal femur / E.G. Hassankhani, F. Birjandinejad, F.O. Kashani, G.G. Hassankhani // Surgical Science. — 2013. — Vol. 4. — P. 176-183. doi: 10.4236/ss.2013.42033.

/19/19.jpg)
/21/21.jpg)