Украинский журнал хирургии 2 (25) 2014
Вернуться к номеру
Роль эндоваскулярных методов в подготовке пациентов с метастатическими опухолями печени к радикальному хирургическому лечению
Авторы: Котенко О.Г., Кондратюк В.А., Федоров Д.А., Гриненко А.В., Коршак А.А., Гусев А.В., Попов А.О., Григорян М.С. – Национальный институт хирургии и трансплантологии имени А.А. Шалимова НАМН Украины, г. Киев, Украина
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
В статье представлены результаты эмболизации воротной вены у пациентов с метастазами колоректального рака в печень перед радикальной обширной резекцией печени.
Цель работы: сравнить непосредственные и отдаленные результаты резекции печени у пациентов, которым выполняли эмболизацию воротной вены в качестве предоперационной подготовки, и пациентов, которым предоперационных эндоваскулярных вмешательств не выполняли.
Материал и методы. Эмболизация воротной вены выполнена у 71 пациента, расчетный остаточный объем печени у которых составлял менее 30 % неповрежденной паренхимы печени. В группу сравнения включены 118 пациентов, которым в связи с достаточным (более 30 %) расчетным остаточным объемом печени предоперационных эндоваскулярных вмешательств не выполняли.
Результаты и обсуждение. У всех пациентов после эмболизации воротной вены наблюдали увеличение расчетного остаточного объема печени на 56,6 ± 14,0 %, что позволило исключить
68 (95,7 %) пациентов из группы повышенного риска и выполнить радикальную резекцию печени у 63 (88,7 %) пациентов. У группы пациентов после эмболизации воротной вены клинико-лабораторные проявления пострезекционной печеночной недостаточности были менее выраженными, чем в группе сравнения. Это объясняется разнесением во времени основных пострезекционных повреждающих факторов — уменьшения объема функционирующей паренхимы печени и портальной гипертензии, вызванной снижением портальной перфузии. Не отмечено значимой разницы 1-, 3- и 5-летней безрецидивной выживаемости у пациентов обеих групп.
Выводы. Эмболизация воротной вены является эффективным мини-инвазивным методом подготовки к радикальной обширной резекции печени пациентов с колоректальными метастазами в печени и повышенным риском пострезекционной печеночной недостаточности.
У статті наведені результати емболізації воротної вени у пацієнтів із метастазами колоректального раку в печінку перед радикальною обширною резекцією печінки.
Мета роботи: порівняти безпосередні та віддалені результати резекції печінки у пацієнтів, яким виконували емболізацію воротної вени як передопераційну підготовку, та пацієнтів, яким передопераційних ендоваскулярних втручань не виконували.
Матеріал і методи. Емболізація воротної вени виконана у 71 пацієнта, розрахунковий залишковий об’єм печінки у яких становив менше 30 % неушкодженої паренхіми печінки. До групи порівняння включені пацієнти, яким у зв’язку з достатнім (більше 30 %) залишковим об’ємом печінки передопераційних ендоваскулярних втручань не виконували.
Результати і обговорення. У всіх пацієнтів після емболізації воротної вени спостерігали збільшення залишкового об’єму печінки на 56,6 ± 14,0 %, що дозволило виключити 68 (95,7 %) пацієнтів із групи підвищеного ризику та виконати радикальну резекцію печінки у 63 (88,7 %) пацієнтів. У групи пацієнтів після емболізації воротної вени клініко-лабораторні прояви пострезекційної печінкової недостатності були менш вираженими, ніж у групі порівняння. Це пояснюється рознесенням у часі основних пострезекційних ушкоджуючих чинників — зменшення об’єму функціонуючої паренхіми печінки й портальної гіпертензії, викликаної пострезекційним зниженням портальної перфузії. Не відмічено значущої різниці 1-, 3- і 5-річної безрецидивної виживаності в пацієнтів обох груп.
Висновки. Емболізація воротної вени є ефективним міні-інвазивним методом підготовки до радикальної обширної резекції печінки пацієнтів з колоректальними метастазами в печінці та підвищеним ризиком пострезекцйної печінкової недостатності.
Expanded liver resection is the only treatment offering a chance of long-term survival of patients with metastatic liver cancer. However, it can be performed in only 10 % of patients, because the future remnant liver is too small, risking severe postoperative liver failure. Preoperative portal vein embolization for these patients may to increase remnant liver volume and give them a chance to radical treatment.
Objective: to compare the immediate and long-term results of liver resection group of patients who underwent endovascular intervention as preoperative preparation and patient groups, which preoperative endovascular treatment was not performed. Contralateral or ipsilateral transhepatic portal accesses were applied, polyvinil particles and coils were used for portal branch occlusion.
Materials and Methods. Preoperative portal vein embolization was performed in 71 patients with the estimated residual liver volume less than 30 % of the intact liver parenchyma. The comparison group included 118 patients who were sufficient (> 30 %) residual liver volume and without preoperative endovascular interventions. Liver function tests including total bilirubin, aspartate aminotransferase, alanine aminotransferase and prothrombin time were performed before portal vein embolization, daily for 5 days thereafter, and before surgery. CT scan volumetric measurements were performed before PVE and before surgery.
Results and Discussion. As a preparation for large hepatic resection, preoperative portal embolization was feasible in all patients. There were no significant deaths. Patients prescribed antibiotics in prophylactic doses, analgesics, anti-inflammatory drugs. In all cases after preoperative portal vein embolization residual liver volume increasing in 56.6 ± 14.0 % was observed. It allowed to exclude 68 (95.7 %) patients from high-risk group and perform radical extensive hepatectomy in 63 (88.7 %) patients. The group of patients after endovascular intervention have less clinical and laboratory markers of postoperative liver failure, than in the comparison group. This is explained by the diversity of post-resection major damaging factors — reducing the volume of functioning liver parenchyma and portal hypertension induced reduction of portal perfusion. There was no significant difference in 1-, 3- and 5-year disease-free survival in both groups of patients: 82, 64, 40 % versus 88, 60, 39 %, respectively.
Conclusion. Preoperative portal vein embolization allows more patients with previously unresectable liver tumors to benefit from resection. This approach preserves sufficient functioning liver parenchyma to prevent postoperative liver failure. By removing the contraindication of an insufficient remnant liver, PVE increases the resectability of colorectal liver metastases with a survival benefit comparable to that obtained with primary liver resection. It can be considered a new neoadjuvant modality in the management of hepatic colorectal metastases. Long-term survival is comparable to that after resection without endovascular preparation.
колоректальные метастазы, резекция печени, эмболизация воротной вены.
колоректальні метастази, резекція печінки, емболізація воротної вени.
colorectal metastases, liver resection, portal vein embolization.
Статья опубликована на с. 22-26
Введение
Радикальная резекция печени у пациентов с колоректальными метастазами печени в настоящее время остается единственной возможностью достигнуть статистически достоверного увеличения продолжительности жизни — от 25 % до 40 % 5-летней выживаемости [1, 2]. Однако подобное вмешательство удается выполнить только у 10 % пациентов с впервые выявленным метастатическим поражением печени [3, 4], причем большинство отказов в радикальном хирургическом лечении связано не с технической невозможностью резекции, а с малым расчетным остаточным объемом печени (РООП), обусловливающим высокий риск послеоперационной печеночной недостаточности [5]. Именно для таких случаев японскими авторами [6] предложена методика предоперационной эмболизации воротных ветвей (ЭВВ) удаляемой части печени, что вызывает компенсаторную гипертрофию РООП и позволяет избежать у таких пациентов фатальной послеоперационной печеночной недостаточности [7].
Целью настоящей работы является определение места ЭВВ в комплексе радикального лечения пациентов с большими метастатическими опухолями в печени и оценка ее влияния на ближайшие и отдаленные результаты хирургического лечения этих пациентов.
Материал и методы
С 2004 по февраль 2014 года обследован 71 пациент с операбельными колоректальными метастазами в печень, у которых радикальная резекция печени была сопряжена с повышенным риском в связи с малым РООП. 58 (81,7 %) из них предварительно выполнена системная химиотерапия (1–5 курсов). Этим пациентам выполнена ЭВВ, они составили основную исследуемую группу.
В течение того же периода 118 пациентам с аналогичным диагнозом выполнена резекция 4 и более сегментов печени без применения ЭВВ. Эти пациенты составили группу сравнения. Неоадъювантная химиотерапия была выполнена 86 (72,9 %) пациентам этой группы. Обе группы пациентов были сравнимы по полу, возрасту, количеству метастазов. Характеристики пациентов представлены в таблице 1.
Всем пациентам обеих групп планировали резекцию как минимум 4 сегментов печени. Основным критерием определения показаний к ЭВВ являлся РООП, который измеряли по данным компьютерной томографии с контрастным усилением. Пациентам назначали ЭВВ, если РООП составлял не более 20 % от общего объема неизмененной паренхимы печени (у пациентов без предшествующей химиотерапии) либо не более 30 % от общего объема неизмененной паренхимы печени (у пациентов с предшествующей химиотерапией).
Техника выполнения ЭВВ в целом соответствовала описанной в литературе. Под комбинированным ультразвуковым и рентгеноскопическим контролем выполняли пункцию ипсилатеральной (59) или контралатеральной (5) портальной ветви. Преимущество отдавали ипсилатеральному портальному доступу, поскольку в этом случае пункционный канал расположен в части печени, подлежащей удалению. При выборе места и направления пункции руководствовались следующими правилами:
— пункционный канал не должен проходить сквозь очаги опухоли либо в непосредственной близости от них;
— в процессе пункции не должны повреждаться крупные сосуды и желчные пути;
— угол пункции портальной ветви должен быть не более 90° против направления кровотока;
— пунктированная портальная ветвь не должна быть деформирована опухолью либо извитой.
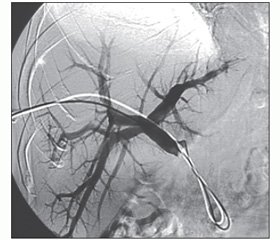
После проведения катетера в ствол воротной вены выполняли портографию и портоманометрию (рис. 1).
Кончик катетера последовательно проводили в целевые сегментарные ветви и выполняли их эмболизацию полиуретановыми эмболами и металлическими спиралями. Конечной точкой считали прекращение либо значительное замедление кровотока в эмболизированной ветви с рефлюксом введенного вручную контрастного вещества в портальную ветвь высшего порядка. После достижения окклюзии всех целевых портальных ветвей выполняли контрольную портоманометрию и портографию (рис. 2), катетер удаляли, в пункционный канал устанавливали эмболизационную спираль.
Распределение пациентов по объему ЭВВ приведено в таблице 2.
Функцию печени оценивали на основании показателей общего билирубина, АЛТ, АСТ, протромбинового времени, общего белка, щелочной фосфатазы. Компьютерную томографию с измерением РООП выполняли до ЭВВ (первичная КТ) и перед хирургическим вмешательством (контрольная КТ), по данным исследований подсчитывали общий объем печени, объем опухоли, объем расчетного печеночного остатка. Показатель РООП (%) представлен в виде коэффициента, отражающего соотношение расчетного остаточного объема паренхимы печени (см3) и общего объема функционирующей паренхимы (см3). Вычисление РООП выполняли следующим образом:
РООП = (объем расчетного печеночного остатка × × 100) / (общий объем печени – объем опухоли).
Процентное увеличение РООП в результате ЭВВ (РООП%) рассчитывали по формуле:
РООП% = (РООП контрольный – РООП исходный) × 100 / РООП исходный.
Результаты представлены в виде среднего значения ± стандартное отклонение, для сравнения применяли t-критерий Стьюдента. Выживаемость подсчитывали по методу Каплана — Мейера, группы сравнивали согласно логранговому критерию. Статистически значимым полагали значение P < 0,05.
Результаты и обсуждение
Технически успешная ЭВВ выполнена у всех пациентов основной группы (71 чел.). У большинства пациентов в течение 2–3 суток после ЭВВ отмечали повышенную температуру, умеренные боли в области печени. Лабораторные показатели перед ЭВВ у всех пациентов были в пределах нормы, на 5-й день после вмешательства отмечено статистически достоверное повышение показателей общего билирубина, АЛТ и АСТ. Изменения показателей общего белка, щелочной фосфатазы, протромбина не являлись статистически достоверными. Перед хирургическим вмешательством все лабораторные показатели функции печени вернулись к базовым значениям. РООП% увеличился с 24,6 ± 6,0 % до 38,2 ± 9,0 %. Таким образом, прирост РООП% составил 56,6 ± 14,0 % (13–69 %). Согласно волюметрическим подсчетам, у 68 пациентов (95,7 %) достигнутый в результате ЭВВ РООП расценен как достаточный для выполнения радикальной резекции печени.
Резекция печени в сроки 20–36 суток после ЭВВ выполнена у 63 пациентов (88,7 %). У 3 (4,2 %) пациентов радикальное вмешательство не выполняли в связи с малым РООП, у 3 (4,2 %) — в связи с прогрессированием опухолевого процесса, у 2 (2,8 %) — в связи с ухудшением общего состояния, не связанного с первичным заболеванием.
За тот же самый период у 118 пациентов с колоректальными метастазами выполнена резекция 4 и более сегментов печени. Таким образом, применение ЭВВ позволило увеличить количество радикальных хирургических вмешательств у этой категории пациентов на 53,4 % (63/118). Динамика лабораторных показателей у пациентов основной группы и группы сравнения отражена в таблице 3.
Согласно полученным лабораторным данным, послеоперационная печеночная недостаточность в основной группе пациентов была выражена в меньшей степени по сравнению с группой пациентов, которым резекцию печени выполняли без предварительной ЭВВ.
Показатели 1-, 3- и 5-летней выживаемости у пациентов основной группы составили соответственно 82, 64 и 40 %, что сопоставимо с аналогичными данными у группы сравнения (88, 60, 39 %).
У всех пациентов основной группы в результате ЭВВ отмечено статистически значимое повышение РООП. Это позволило исключить из группы высокого риска послеоперационной печеночной недостаточности 95,3 % пациентов и выполнить радикальную резекцию печени у 63 (88,7 %) пациентов основной группы. Таким образом, в результате внедрения методики ЭВВ у пациентов с колоректальными метастазами в печень удалось расширить диапазон резектабельности на 53,4 %.
При сравнении результатов послеоперационных исследований отмечено достоверное снижение клинико-лабораторных проявлений пострезекционной печеночной недостаточности в основной группе пациентов, несмотря на то, что РООП перед резекцией печени был достоверно меньше аналогичного показателя в группе сравнения. Это можно объяснить влиянием на результаты резекции печени пострезекционной портальной гипертензии, связанной со скачкообразным снижением портальной перфузии при неизмененном портальном притоке. У пациентов основной группы такое перераспределение портального кровотока возникает непосредственно после ЭВВ, а у пациентов группы сравнения — после резекции печени. Таким образом, методика ЭВВ позволяет не только увеличить процентное соотношение остающейся и удаляемой части печени, но и разнести во времени повреждающие факторы, связанные с радикальной резекцией печени. Таким образом, ЭВВ может быть рекомендована не только пациентам с гранично малым РООП, но и пациентам с другими предикторами послеоперационной печеночной недостаточности (сопутствующие диффузные изменения печени, состояние после множественных курсов химиотерапии).
При изучении отдаленных результатов оперативного лечения не отмечено существенной разницы безрецидивной и отдаленной 1-, 3- и 5-летней выживаемости в сравниваемых группах больных. Таким образом, предоперационная эмболизация воротной вены расширяет возможности радикального лечения, повышает безопасность обширных резекций печени и практически не влияет на отдаленные результаты хирургического лечения у пациентов с колоректальными метастазами в печень.
Выводы
1. Предоперационная эмболизация воротных ветвей удаляемой части печени у пациентов с колоректальными метастазами в печень позволяет увеличить объем остаточной части печени на 56,6 %, что позволило исключить из группы повышенного риска пострезекционной печеночной недостаточности большинство исследованных пациентов и расширить диапазон резектабельности на 53,4 %.
2. Методика ЭВВ позволяет разнести во времени повреждающие факторы, связанные с резким уменьшением объема функционирующей печеночной паренхимы, значительно улучшая непосредственные результаты радикального хирургического лечения у пациентов с предикторами послеоперационной печеночной недостаточности. Наряду с этим не отмечено значимого влияния методики ЭВВ на отдаленные результаты хирургического лечения пациентов с колоректальными метастазами в печень.
1. Long-term survival following resection of colorectal hepatic metastases / Jaeck D., Bachelier P., Guiguet M. [et al.] // Br. J. Surg. — 1997. — Vol. 84. — Р. 977–980.
2. Preoperative portal vein embolization for extension of hepatectomy indications / De Baere T., Roche A., Elias D. [et al.] // Hepatology. — 1996. — Vol. 24. — P. 1386–1391.
3. Resection of colorectal metastases / Scheele J., Stangl R., Altendorf-Hofmann A., Paul M. // World J. Surg. — 1995. — Vol. 19. — P. 59–71.
4. Steele G. Jr. Resection of hepatic metastases from colorectal cancer: biologic perspectives / Steele G. Jr., Ravikumar T.S. // Ann. Surg. — 1989. — Vol. 210. — P. 127–138.
5. Boerma E.J. Research into the results of resection of hilar bile duct cancer / Boerma E.J. // Surgery. — 1990. — Vol. 108. — P. 572–580.
6. Preoperative portal embolization to increase safety of major hepatectomy for hilar bile duct carcinoma: a preliminary report / Makuuchi M., Le Thai B., Takayasu K. [et al.] // Surgery. — 1990. — Vol. 107. — P. 521–527.
7. Right portal vein embolization in preparation for major hepatic resection / Azoulay D., Raccuia J.S., Castaing D., Bismuth H. // J. Am. Coll. Surg. — 1995. — Vol. 181. — P. 267–269.

/23/23.jpg)
/23/23_2.jpg)
/24/24.jpg)
/24/24_2.jpg)