Международный эндокринологический журнал 5 (61) 2014
Вернуться к номеру
Глікований гемоглобін у практиці ендокринолога (огляд літератури і власні дані)
Авторы: Глоба Є.В., Зелінська Н.Б. - Український науково-практичний центр ендокринної хірургії, трансплантації ендокринних органів і тканин МОЗ України, м. Київ
Рубрики: Эндокринология
Разделы: Справочник специалиста
Версия для печати
Стаття присвячена одному з найважливіших показників у діагностиці цукрового діабету — глікованому гемоглобіну (HbA1c). Наведені чинники, що впливають на його значення. Зазначено, що останніми роками у світі досягнутий значний прогрес у стандартизації досліджень HbA1c та продовжується робота щодо оптимізації якості тестування HbA1c у майбутньому.
Статья посвящена одному из важнейших показателей в диагностике сахарного диабета — гликированному гемоглобину (HbA1c). Приведены факторы, которые влияют на его значения. Отмечено, что за последние годы в мире достигнут значительный прогресс в стандартизации исследований HbA1c и продолжается работа по оптимизации качества тестирования HbA1c в будущем.
This article deals with one of the most important factors in the diagnosis of diabetes mellitus — glycated hemoglobin (HbA1c). There are given the factors that may affect its value. It is noted that in recent years the world has made a significant progress in standardizing HbA1c researches, and the work continues in terms of optimization the quality of HbA1c testing in the future.
глікований гемоглобін, діагностика, діти.
гликированный гемоглобин, диагностика, дети.
glycated hemoglobin, diagnosis, children.
Статья опубликована на с. 62-66
Глікований гемоглобін — це гемоглобін, у якому молекула глюкози неферментативно з’єднана з b-кінцевим валіном b-ланцюгів глобіну гемоглобіну А1 (позначається як HbA1c). Уміст HbA1c має пряму кореляцію з рівнем глюкози крові, і, таким чином, його використовують як золотий стандарт для оцінки глікемічного контролю і прогнозу хронічних ускладнень цукрового діабету (ЦД) [1–3].
У нормі концентрація HbA1c становить від 4,4 до 6,1 %, у той час як у хворих на ЦД його рівень залежить від ступеня гіперглікемії і зазвичай перевищує нормальні показники. Глікування — неферментативний процес, що перебігає повільно, протягом усього життя еритроцита (близько 120 днів). HbA1c накопичується в середині еритроцитів і зберігається протягом усього періоду циркуляції еритроцита в кров’яному руслі. HbA1c відображає показники глікемії в попередні 4–12 тижнів [4, 5], з виваженим показником за попередні 4 тижні, за винятком останнього тижня, оскільки саме ці останні показники є оборотними. Нормалізація його рівня в крові відбувається через 4–6 тижнів після досягнення нормального рівня глікемії. Глікогемоглобін HbA1 поділяють на підгрупи залежно від приєднаного вуглеводу (НbА1а, А1b, A1c). HbA1c містить одну молекулу глюкози, він становить 70–90 % глікованої фракції, решта припадає на HbA1а (має форму 1 — з фруктозо-1,6-біфосфатом і форму 2 — з глюкозо-6-фосфатом) і HbA1b (вуглеводний залишок, точно не ідентифікований).
Численні дослідження вимірювання вмісту глюкози традиційними методами підтвердили взаємозв’язок HbA1c з рівнем глікемії пацієнта [1, 2, 6]. Результати досліджень DCCT, проведених в 90-х роках XX ст., підтвердили гіпотези про те, що рівень HbA1c безпосередньо пов’язаний з рівнем глюкози в крові і є найбільш доцільним критерієм при моніторингу ефективності лікування хворих на ЦД [1]. Наприкінці дослідження в 1993 р. вимірювали вміст HbA1c, HbA1 (HbA1а + HbA1b + HbA1c), а також загального глікованого гемоглобіну (GHB). Різноманітність методів, що застосовувалися, призводила до широкої розбіжності результатів і давала значну похибку по одному зразку, зокрема від 10,7 до 17,8 % [7].
На початку 90-х років не існувало єдиної міжнародної узгодженої стандартизації вимірювання HbA1c, що знижувало клінічну ефективність використання даного тесту. Щоб досягти єдиного стандарту і подолати проблеми, пов’язані з його використанням, Міжнародна федерація клінічної хімії (International Federation of Clinical Chemistry and Laboratory Medicine, IFCC) створила в 1993 році робочу групу із стандартизації оцінки HbA1c. Результатом її роботи стала створена в 1996 р. Національна програма із стандартизації досліджень глікованого гемоглобіну (National Glycohemoglobin Standardization Program, NGSP). Більшість виробників приладів і наборів для аналізу крові на HbA1c зобов’язали проходити перевірку на відповідність результатів даним, отриманим референсними методами. Якщо результат перевірки відповідає референсним даним, виробнику видається сертифікат відповідності NGSP. Американська діабетична асоціація (ADA) рекомендує всім лабораторіям використовувати тести для аналізу крові на HbA1c, сертифіковані NGSP. Наявність сертифіката NGSP гарантує можливість порівняти отримані результати з дослідженням DCCT, кореляцію з основними показниками глікемії і можливість використання результатів в умовах проведення науково-дослідних робіт і широкої клінічної практики.
Основними вимогами NGSP є:
— коефіцієнт варіації (CV) нижче від 3 %;
— довірчий інтервал (95%) щодо референс-лабораторії не більше ніж ± 0,75;
— щорічне підтвердження сертифіката NGSP для виробників аналізаторів і наборів реагентів [8].
У дослідженнях DCCT та UKPDS використовувався єдиний метод оцінки HbA1c [1, 2], а саме високоефективної рідинної хроматографії, який став референсним, оскільки в процесі обох досліджень було доведено прогностичну роль рівня HbA1c як критерію оцінки постійної глікемії у розвитку хронічних судинних ускладнень при ЦД 1-го й 2-го типу.
Але після розробки істинного еталонного методу за IFCC [9] вважають, що саме цей метод повинен використовуватися всіма виробниками для застосування в клінічних лабораторіях [10]. У результаті згідно з консенсусом дослідників було розроблено такі настанови:
1. Усі клінічні лабораторії повинні визначати результати HbA1c в одиницях СІ (у ммоль/моль) і похідних одиницях NGSP (у відсотках), використовуючи IFCC-NGSP рівняння (DCCT одиниці). Формули переводу показників HbA1c за IFCC чи DCCT/NGSP такі [11–13]:
HbA1c в одиницях IFCC (ммоль/моль) = 10,93 x HbA1c в одиницях DCCT/NGSP (%) – 23,50;
HbA1c в одиницях DCCT/NGSP (%) = 0,09148 xHbA1c в одиницях IFCC (ммоль/моль) + 2,152;
NGSP (%) = 0,915 x IFCC (ммоль/моль) + 2,15.
2. Таблиці переводу HbA1c в одиниці СІ (IFCC) і в одиниці NGSP повинні бути легко доступні для всіх лікарів (див. http://www.hba1c.nu/eng).
3. У публікаціях рекомендовано повідомляти результати HbA1c як в одиницях СІ (IFCC), так і NGSP/DCCT.
Більшість країн Європи застосовують реєстрацію обох одиниць, але деякі країни (наприклад, Швеція) вже використовують лише одиниці СІ (ммоль/моль) [14].
Моніторинг HbA1c є найкориснішим методом визначення стану метаболічного контролю і єдиним методом отримання інформативних даних, доступних з точки зору їх взаємозв’язку з пізніми мікро- і макроангіопатіями [1, 2]. Однак у HbA1c є обмеження як індикатора стану глікемічного контролю, оскільки він усереднює показники глюкози крові (ГК). HbA1c може бути одним з декількох методів оцінки оптимального глікемічного контролю поряд із задокументованою гіпоглікемією, типом лікування, віком пацієнта і якістю життя. Підвищення рівня HbA1c зумовлює розвиток і прогресування хронічних діабетичних мікро- і макроангіопатій [1, 2]. Цільові показники HbA1c мають статус рекомендованих і встановлюються з очікуванням того, що буде приділено особливу увагу необхідності уникати розвитку тяжких гіпоглікемій (табл. 1, 2). Оскільки тяжкі гіпоглікемії трапляються частіше у хворих з відсутністю чутливості до початкових проявів гіпоглікемії, цільові показники HbA1c можуть бути вищими, коли виникає така нечутливість.
Так, зокрема, за IFCC нормальні показники НbА1с становлять 20–42 ммоль/моль, а у хворих на ЦД цільові показники НbА1с, які визначено як 7 % і 6,5 % за DCCT/NGSP, відповідають показникам 53 і 48 ммоль/моль за IFCC відповідно [11].
Також упродовж 2006–2008 рр. діабетичні асоціації ADA, EASD та IDF провели дослідження з вивчення математичної залежності між HbA1c і середнім рівнем глікемії (СГ) [16–17]. Взаємозв’язок (табл. 3) було підтверджено математичною формулою з використанням лінійного регресійного аналізу: СГ (ммоль/л) = 1,59 x HbA1c – 2,59 [6].
Також калькулятор переводу доступний на сайті http://www.diabetes.co.uk/hba1c–units–converter.html.
Сьогодні тривають дискусії щодо можливості використовувати HbA1c для діагностики ЦД. Зокрема, ADA рекомендує використовувати показник HbA1c ≥ 6,5 % для підтвердження ЦД без проведення будь-яких додаткових тестів, а діапазон 5,7–6,4 % розглядати як такий, що становить ризик розвитку ЦД і потребує додаткового обстеження [18]. Слід зазначити, що при вперше виявленому ЦД 1-го типу із швидким наростанням глікемії в дебюті захворювання може реєструватися відносно невисокий рівень HbA1c, незважаючи на достатню тяжкість клінічних проявів.
Слід пам’ятати про низку чинників, що можуть впливати на показник HbA1c, крім рівня глікемії. До підвищення показника можуть призводити такі з них, як залізодефіцитна анемія, дефіцит В12 і фолієвої кислоти, спленектомія, отруєння свинцем, алкоголь, карбогемоглобін (у пацієнтів з уремією). Хибно занижений уміст HbA1c може відзначатися під час вагітності, при гострих чи хронічних крововтратах, після трансфузій та при гемолітичних і мегалобластних анеміях (унаслідок зниження тривалості життя еритроцитів) (табл. 4).
Наявність патологічних форм гемоглобіну спотворює хід тестування, обумовлює хибно занижені або хибно завищені показники. Тому NGSP рекомендує при виборі методу дослідження HbA1c віддавати перевагу тим, за використання яких мінімізований ефект інтерференції з фракціями гемоглобіну (наприклад, при гемоглобінопатіях — НBs, HbC або при підвищеному вмісті фетогемоглобіну (HbF) і карбоксигемоглобіну (CarbHb)).
Існує безліч аналітичних методів, що дозволяють визначати HbA1c. До таких методів належать капілярний електрофорез (HPLC-CE), рідинна хроматографія, афінна хроматографія, імунологічні і колоночні методики. Вважають, що ні портативні прилади, ні тим більше колонкові методи або застосування аналізаторів, де не використовується референсний метод, не можна застосовувати для діагностики ЦД та інших порушень вуглеводного обміну у зв’язку з високим показником коефіцієнту варіації. На сьогодні для визначення HbA1c найбільшу поширеність в сертифікованих лабораторіях NGSP (понад 95 %) отримав метод високоефективної рідинної хроматографії [8]. Він є референсним методом, що не потребує додаткової інтерпретації результатів, має високу точність і низький CV, не має інтерференції з іншими фракціями гемоглобіну, а високу надійність результатів забезпечує пряме визначення HbA1c. Недоліком даного методу є необхідність придбання спеціалізованого дорогого устаткування. При використанні стандартизованих методів дослідження лабораторія має можливість порівнювати отримані результати з даними, отриманими за допомогою референсних методів. Таке порівняння максимально підвищує вірогідність результатів досліджень. Безперечно, важливим є використання в роботі практикуючого лікаря тільки таких результатів досліджень, які отримані в лабораторіях, що використовують тести для аналізу крові на HbA1c, сертифіковані NGSP.
В Україні з 2004 року створений реєстр дітей, хворих на ЦД, який містить інформацію щодо перебігу ЦД, а саме дату встановлення діагнозу ЦД, вид і дози інсулінів, що отримує дитина, наявність у неї гострих та хронічних ускладнень, а також, зокрема, рівень HbA1c. Згідно з реєстром показник HbA1c змінювався з тенденцією до зниження протягом останніх років (рис. 1).
За результатами аналізу залежності рівня HbA1c від віку пацієнта та тривалості ЦД за даними реєстру було з’ясовано, що найнижчі показники HbA1c у 2012 році спостерігалися за умови тривалості захворювання від одного до п’яти років (p < 0,05), а найвищі — тривалості ЦД до одного року (що пов’язано з природно високим показником при маніфестації ЦД) та 10 років і більше (рис. 2).
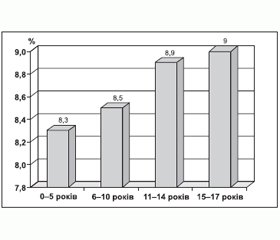
Найнижчі показники HbA1c зафіксовано у дітей віком до п’яти років, а найвищі — у дітей 11–17 років, із вірогідним зростанням показника порівняно з віковою групою 0–5 років (рис. 3). Дана тенденція цілком збігається із світовими даними [20–22].
Отже, тенденції залежності рівня HbA1c від віку пацієнта та тривалості ЦД в Україні серед дітей віком 0–17 років загалом відповідають європейським, але середній рівень HbA1c в Україні дещо вищий за європейські показники за аналогічні роки [21–23].
На закінчення слід зазначити, що останніми роками у світі досягнутий значний прогрес в стандартизації досліджень HbA1c, а NGSP продовжує свою роботу щодо оптимізації якості тестування HbA1c у майбутньому.
1. DCCT. The effect of intensive treatment of diabetes on the development and progression of long-term complications in insulin-dependent diabetes mellitus // N. Engl. J. Med. — 1993. — 329. — P. 977–986.
2. UK Prospective Diabetes Study (UKPDS) Group. Intensive blood-glucose control with sulphonylureas or insulin compared with conventional treatment and risk of complications in patients with type 2 diabetes (UKPDS 33) // Lancet. — 1998. — 352. — P. 837–853.
3. International Expert Committee Report on the Role of the A1c Assay in the Diagnosis of Diabetes // Diabetes Care. — 2009. — Vol. 32(7). — P. 1327–1334.
4. Mortensen H.B., Volund A. Application of a biokinetic model for prediction and assessment of glycated haemoglobins in diabetic patients // Scand. J. Clin. Lab. Invest. — 1988. — 48. — P. 595–602.
5. Phillips P.J., Phillipov G. A1C — frequently asked questions // Australian Family Physician. — 2005. — Vol. 34, № 8. — P. 663–667.
6. Nathan D.M., Kuenen J., Borg R., Zheng H., Schoenfeld D., Heine R.J. for the A1c-Derived Average Glucose (ADAG) Study Group: Translating the hemoglobin A1c assay into estimated average glucose values // Diabetes Care. — 2008. — 31. — P. 1473–8.
7. College of American Pathologists. Electrophoresis/Chromatography Survey 1993, set EC-C. — Northfield, IL: CAP, 1993.
8. Галстян Г.Р. Международные рекомендации по исследованию уровня гликированного гемоглобина HbA1c как диагностического критерия сахарного диабета и других нарушений углеводного обмена // Сахарный диабет. — 2010. — № 4. — С. 57–61.
9. Hoelzel W., Weykamp C., Jeppsson J.O. et al. IFCC reference system for measurement of hemoglobin A1c in human blood and the national standardization schemes in the United States, Japan, and Sweden: a method-comparison study // Clin. Chem. — 2004. — Vol. 50. — P. 166–174.
10. American Diabetes Association, European Association for the Study of Diabetes, International Federation of Clinical Chemistry and Laboratory Medicine, International Diabetes Federation. Consensus statement on the worldwide standardisation of the HbA1c measurement // Diabetologia. — 2007. — Vol. 50. — P. 2042–2043.
11. Goodall I., Shephard M., Tate J. Recommended Changes in HbA1c Reporting Units for Australian Laboratories. Position Statement of the Australasian Association of Clinical Biochemists. — 2010. — 6 р.
12. Weykamp C., John W.G., Mosca A. A review of the Challenging in Measuring Hemoglobin HbA1c // J. Diabetes Sci. Technol. — 2009. — Vol. 3, Issue 3. — P. 436–445.
13. Hanas R., John W.G. On behalf of the International HbA1c Consensus Committee. 2010 Consensus Statement on the Worldwide Standardization of the Hemoglobin A1c Measurement // Diabet Care. — 2010. — 33 (8). — P. 1903–1904.
14. Hanas R., John W.G. 2013 Update on the worldwide standardization of the hemoglobin A1c measurement // Pediatric diabetes. — 2013. — P. 1–2. doi: 10.1111/pedi.12047
15. Алгоритмы специализированной помощи больным сахарным диабетом // Научно-практический медицинский журнал. — 2011. — № 3. — 73 с.
16. Report of the ADA/EASD/IDF Working Group of the HbA1c Assay, London, UK, January 2004 // Diabetologia. — 2004. — 47. — R53–4.
17. Sacks D.B. for the ADA/EASD/IDF Working Group of the HbA1c Assay. Global harmonization of Hemglobin A1c // Clin. Chem. — 2005. — 51. — P. 681–3.
18. The Expert Committee on the Diagnosis and Classification of Diabetes Mellitus: Follow-up report on the diagnosis of Diabetes Mellitus // Diabetes Care. — 2003. — Vol. 26. — P. 3329–3330.
19. Gallagher E.J., Bloomgarden Z.T., Le Roith D. Review of hemoglobin A1c in the management of diabetes // Journal of diabetes. — 2009. — 1. — P. 9–17.
20. Rosenbauer J., Rohrer T., Knerr I., Dost A. et al. Metabolic Control in Children with Type 1 Diabetes // European Endocrinology. — 2010. — 6 (1). — P. 35–38.
21. Carolyn A., Klingensmith G., Petitti D., Rodriguez B. et al. Predictors of Insulin Regimens and Impact on Outcomes in Youth with Type 1 Diabetes: The SEARCH for Diabetes in Youth Study // The Journal of Pediatrics. — 2009. — Vol. 155. — P. 183–189.
22. Nils Krone, Wolfgang Högler and Timothy G. Barrett. Thoughts on paediatric diabetes care in the UK // British Journal of Diabetes & Vascular Disease. — 2009. — 9. — P. 259–267.
23. Lena Hanberger. Quality of Care in Children and Adolescents with Type 1 Diabetes — Patients’ and Healthcare Professionals’ Perspectives. — Linköping, October 2010, 74 р.

/63/63.jpg)
/64/64.jpg)
/65/65.jpg)