Журнал «Травма» Том 16, №3, 2015
Вернуться к номеру
Основные остеосцинтиграфические параметры операбельности при эндопротезировании тазобедренных суставов
Авторы: Ткаченко М.Н. - Национальный медицинский университет имени А.А. Богомольца, г. Киев; Король П.А. - Национальный медицинский университет имени А.А. Богомольца, г. Киев, Киевская городская клиническая больница № 12
Рубрики: Травматология и ортопедия
Разделы: Клинические исследования
Версия для печати
С целью определения основных сцинтиграфических параметров операбельности пациентов с деформирующим остеоартрозом при эндопротезировании тазобедренных суставов методом остеосцинтиграфии исследовано 85 пациентов с деформирующим остеоартрозом тазобедренных суставов в возрасте от 54 до 75 лет. Все пациенты были разделены на три диагностические группы в зависимости от количественных остеосцинтиграфических показателей и клинической картины заболевания.
В результате работы установлено, что эндопротезирование тазобедренных суставов без возникновения послеоперационных осложнений можно проводить только тем пациентам, у которых процент накопления радиофармпрепарата на диагностических остеосцинтиграммах в проекции пораженного остеоартрозом сустава находится в пределах 10–110 %, а в проекции проксимального отдела бедренной кости должен составлять 5–50 % по отношению к симметричной области исследования.
З метою визначення основних сцинтиграфічних параметрів операбельності хворих із деформуючим остеоартрозом при ендопротезуванні кульшових суглобів методом остеосцинтиграфії досліджено 85 хворих на деформуючий остеоартроз кульшових суглобів віком від 54 до 75 років. Усіх хворих розподілено на три діагностичні групи залежно від кількісних остеосцинтиграфічних показників і клінічної картини захворювання.
За результатами роботи встановлено, що ендопротезування кульшових суглобів без виникнення післяопераційних ускладнень можливо проводити тільки тим хворим, у яких відсоток накопичення радіофармпрепарата на діагностичних остеосцинтиграмах у проекції ураженого остеоартрозом суглоба знаходиться у межах 10–110 %, а в проекції проксимального відділу стегнової кістки — 5–50 % щодо симетричної ділянки дослідження.
In order to determine the main scintigraphy parameters for resectability of patients with osteoarthritis deformans during hip replacement using the method of bone scintigraphy, we have examined 85 patients with osteoarthritis deformans of the hip joints aged 54 to 75 years. All patients were divided into three diagnostic groups based on quantitative indicators of bone scintigraphy and clinical pattern of the disease.
The study found that hip replacement without postoperative complications can be carried out only in patients whose percentage of accumulation of radiopharmaceuticals on diagnostic bone scintigrams in the projection of the joint affected by osteoarthritis should be between 10–110 %, and in the projection of the proximal femur should be 5–50 % relative to the symmetric area of the study.
остеосцинтиграфия, эндопротезирование, тазобедренные суставы.
остеосцинтиграфія, ендопротезування, кульшові суглоби.
bone scintigraphy, arthroplasty, hip joint.
Статья опубликована на с. 53-55
Введение
Анализ статистических данных о распространенности остеоартроза показывает, что в разных регионах Европы его частота колеблется от 7 до 25 % взрослого населения. Чаще поражается тазобедренный сустав, что составляет 16,5 % от всей патологии опорно–двигательной системы [6]. Тенденцией последнего времени является уменьшение среднего возраста пациентов с данной патологией. В популяции остеоартроз регистрируется у 3,5 % пациентов в возрасте до 39 лет, а в возрасте после 50 лет их количество значительно возрастает [4].
Эндопротезирование тазобедренных суставов при их патологической нестабильности является актуальным ведущим методом ортопедической коррекции, позволяющим значительно улучшить качество жизни [7, 8]. Несмотря на стойкий комплекс «эндопротез — кость», по различным причинам стабильность в нем нарушается и необходим следующий шаг — ревизионное эндопротезирование. На данном этапе активно изучается диагностическая роль современных дополнительных методов исследования компонентов тазобедренных суставов у пациентов с деформирующим остеоартрозом, которым планируется эндопротезирование тазобедренных суставов [1, 2]. Одним из современных и чувствительных методов для диагностики тазобедренных суставов является остеосцинтиграфия [3, 9].
Как и другие интраскопические методы исследования биологического субстрата, остеосцинтиграфия позволяет дистанционно, без повреждения кожи и нейрон–трофических и гуморальных связей, контролировать состояние различных морфофизиологических систем. Другим характерным свойством метода как способа активной интраскопии является способность использования системного анализа для разнообразных сторон деятельности организма. Вместе с этим обеспечивается возможность формирования обобщающей количественной оценки функционального состояния или морфологического статуса, что не может дать ни один другой способ диагностики [3].
На сегодняшний день в клинической практике активно применяется метод остеосцинтиграфии в диагностике дистрофически–дегенеративных и воспалительных процессов тазобедренных суставов [10]. Одновременно остаются не до конца изученными вопросы определения количественных сцинтиграфических параметров, отражающих степень воспаления в пораженном тазобедренном суставе, которые бы четко свидетельствовали о возможности эндопротезирования без риска возникновения послеоперационных осложнений.
Цель работы: определить основные остеосцинтиграфические параметры операбельности пациентов с деформирующим остеоартрозом при эндопротезировании тазобедренных суставов.
Материал и методы
Остеосцинтиграфию проводили в однодетекторной сцинтилляционной гамма–камере в статическом режиме в передней прямой и боковых проекциях. Для данной методики использовали радиофармпрепарат 99mTc–пирофосфат активностью 550–770 МБк, который вводили пациенту внутривенно. Статическую остеосцинтиграфию осуществляли через 3 часа после введения препарата. Перед исследованием пациенту необходимо было опорожнить мочевой пузырь [5].
Для остеосцинтиграфии использовали многоканальный параллельный коллиматор на 140 кеВ. Оптимальное количество импульсов на кадр составляло 150 тыс.
Обработка результатов исследования на компьютере включала этапы контрастирования, сглаживания, выделения зон интереса с последующим построением гистограмм.
Результаты исследования и их обсуждение
Методом остеосцинтиграфии было исследовано 85 пациентов с деформирующим остеоартрозом, которым планировалось эндопротезирование тазобедренного сустава (57 женщин и 28 мужчин), в возрасте от 54 до 75 лет.
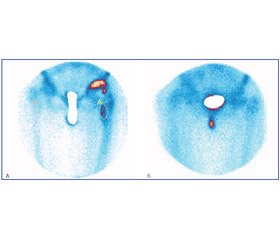
Всем пациентам остеосцинтиграфию проводили за 1–2 дня до эндопротезирования пораженного тазобедренного сустава, а также через 6 месяцев после операции (рис. 1).
По результатам диагностического дооперационного сканирования пациентов распределили на три группы. В первую группу было включено 39 (46 %) пациентов, у которых на диагностических остеосцинтиграммах процент накопления радиофармпрепарата в проекции пораженного сустава составлял 10–110 %, а в проекции проксимального отдела бедренной кости — 5–50 % по сравнению с симметричной областью исследования. Вторую группу составили 29 (34 %) пациентов, у которых процент накопления индикатора в проекции пораженного сустава составлял 110–180 %, а в проекции проксимального отдела бедренной кости — 50–100 %. Третья группа насчитывала 17 (20 %) пациентов с накоплением индикатора в проекции пораженного суставного комплекса больше чем 180 %, а в проекции проксимального отдела бедренной кости — больше чем 100 %.
Всем исследуемым пациентам через 1–2 дня после диагностической остеосцинтиграфии было выполнено эндопротезирование пораженных тазобедренных суставов. Все пациенты прооперированы с установкой цементного или стандартного спейсера. Функциональное состояние пораженного сустава в дооперационный период и после эндопротезирования оценивали по шкале Harris. Через 6 месяцев после эндопротезирования оценивали эффективность оперативного вмешательства по количественным сцинтиграфическим параметрам.
У всех 39 (100 %) пациентов первой диагностической группы на послеоперационных остеосцинтиграммах в проекции суставного комплекса протезированного сустава процент накопления радиофармпрепарата составлял 5–65 %, в проекции проксимального отдела бедренной кости — 5–20 % по сравнению с симметричной областью исследования. Функциональное состояние по шкале Harris улучшилось с 39 ± 4 до 77 ± 5.
У 22 (76 %) пациентов второй диагностической группы через 6 месяцев после протезирования на остеосцинтиграммах процент накопления индикатора в проекции прооперированного сустава составлял 160–250 %, в проекции проксимального отдела бедренной кости — 55–120 % по сравнению с симметричной областью исследования. Функциональное состояние по шкале Harris незначительно улучшилось с 31 ± 2 до 42 ± 4. У 19 (65 %) пациентов второй группы через год после эндопротезирования были диагностированы послеоперационные осложнения в прооперированном суставном комплексе (вывихи головки эндопротеза — у 13 (68 %) пациентов, гнойно–воспалительные осложнения — у 6 (32 %) пациентов).
У 14 (82 %) пациентов третьей группы по данным послеоперационной диагностической сцинтиграфии в проекции протезированного сустава процент накопления радиофармпрепарата составлял 215–380 %, а в проекции проксимального отдела бедренной кости — 90–200 % по сравнению с симметричной областью исследования. Функциональное состояние по шкале Harris ухудшилось с 29 ± 3 до 22 ± 5. У 13 (76 %) пациентов третьей группы через год после эндопротезирования были диагностированы послеоперационные осложнения (гнойно–воспалительные осложнения — у 5 (38 %) пациентов, вывихи головки эндопротеза — у 6 (46 %) пациентов, перипротезный перелом — у 1 (8 %) больного, тромбоэмболия легочной артерии — у 1 (8 %) пациента).
Таким образом, только пациентам первой диагностической группы, у которых не выявлено остеосцинтиграфических и клинических признаков острого воспалительного процесса в пораженном тазобедренном суставе, можно проводить эндопротезирование без риска возникновения послеоперационных осложнений. Пациентам второй и третьей групп в первую очередь необходимо проведение консервативного лечения острого воспалительного процесса в пораженном суставе и лишь затем — эндопротезирование.
Выводы
Основными остеосцинтиграфическими параметрами операбельности больных с деформирующим остеоартрозом, которые позволяют проводить эндопротезирование тазобедренных суставов без риска возникновения после–операционных осложнений, являются следующие:
— процент накопления радиофармпрепарата на диагностических остеосцинтиграммах в проекции пораженного остеоартрозом сустава должен быть в пределах 10–110 % по отношению к симметричной области исследования;
— процент накопления радиофармпрепарата в проекции проксимального отдела бедренной кости должен составлять 5–50 % по отношению к симметричной области исследования.
1. Веснин А.Г. Атлас лучевой диагностики опухолей опорно–двигательного аппарата. — СПб.: Невский диалект, 2009. — P. 87–96.
2. Обобщенная оценка диагностических возможностей радионуклидных исследований / И.Т. Тажединов, Ж.Н. Абдрахмалов, У.К. Джалмукашев, Е.З. Джумашев // Медицинская радиология и радиационная безопасность. — 1999. — Т. 44, № 3. — С. 41–45.
3. Остеосцинтиграфия при системных поражениях опорно–двигательного аппарата: параметры нормы, проблемы визуализации и анализа / Ю.Н. Касаткин, В.В. Поцыбина, Д.И. Левчук // Радиология–практика. — 2003. — № 3. — С. 3134–3137.
4. Ранняя ультразвуковая диагностика остеохондропатии головки бедра / М.Г. Диваков, К.Б. Болобошко // Новости лучевой диагностики. — 1999. — № 2. — С. 12–13.
5. Роль остеосцинтиграфии в дифференциальной диагностике воспалительных процессов коленных суставов / Король П.А., Ткаченко М.Н. // Фундаментальные и прикладные науки сегодня. — 2014. — Т. 1. — С. 53–55.
6. Cовременные возможности сонографии в диагностике патологии тазобедренного сустава / В.П. Дейкало, К.Б. Болобошко // Новости хирургии. — 2006. — Т. 14, № 1. — С. 59–64.
7. Alazraki N.P. et al. Radionuclide imaging in the evaluation of infections and inflammatory disease // Radiol. Clin. North. — 1993. — Vol. 31. — P. 783–794.
8. Kelty N.L. et al. Technical considerations for optimal orthopedic imafing // Semin. Nucl. Med. — 1997. — Vol. 27. — P. 328–33.
9. Savelli G. et al. Bone scintigraphy and the added value of SPECT (single photon emission tomography) in detecting skeletal lesions // Eur. J. Nucl. Med. — 2001. — Vol. 45. — P. 27–37.
10. Scott D.L. et al. The diagnosis and prognosis of early arthritis: rational for new prognostic criteria // Аrthritis Rheum. — 2002. — Vol. 46. — P. 286–290.

/54/54.jpg)