Статья опубликована на с. 11-18
Цитомегаловирусная инфекция (ЦМВИ) — широко распространенная вирусная инфекция, характеризующаяся многообразными проявлениями — от бессимптомного течения до тяжелых генерализованных форм с поражением различных органов и систем. По статистике ВОЗ, генерализованная форма цитомегалии является причиной наибольшего количества летальных случаев в мире после гриппа и ОРВИ [1]. Цитомегаловирус (ЦМВ) — типичный представитель оппортунистических инфекций, манифестирующих с проявлениями клинической картины заболевания на фоне иммунодефицитного состояния. Но вместе с тем сам вирус, кроме значимого патогенного, нередко генерализованного действия, обладает мощным иммуносупрессивным влиянием, обусловливая развитие иммунокомплексных и иммунозависимых заболеваний. Понятие ЦМВИ охватывает проблемы внутриутробного инфицирования, формирования пороков, анте- и постнатального развития патологии сердца и сосудов, органов дыхания, кроветворения, ЦНС, печени, болезней желудочно-кишечного тракта, посттрансплантационных осложнений, онкогенеза, ВИЧ-инфекции, при которой проявления ЦМВИ являются весьма значимыми. Более того, ЦМВИ определена экспертами ВОЗ как СПИД-индикаторная болезнь.
Ранее считалось, что цитомегалия — болезнь новорожденных, но сегодня доказано, что во многих случаях она является причиной болезней и смерти и у взрослых [2]. Сегодня ЦМВИ — самая распространенная из выявленных врожденных инфекционных причин патологии плода и новорожденного. ЦМВ тропен к Т-лимфоцитам, вызывая их значительное повреждение, уступая по разрушающему эффекту только вирусу иммунодефицита человека [3]. Острая первичная ЦМВИ обнаруживается у 1–4 % беременных [4]. При отсутствии специфической терапии генерализованная герпетическая инфекция у новорожденных в 80 % случаев заканчивается летально, а при выживании у 50 % младенцев могут быть тяжелые последствия с поражением различных органов и систем.
Для большинства внутриутробно инфицированных детей характерно латентное течение цитомегаловирусной инфекции. В то же время у 5–18 % инфицированных детей отмечается манифестная врожденная инфекция, характеризующаяся тяжелым течением и нередко заканчивающаяся летально [5]. При исследовании умерших детей (новорожденных и детей раннего возраста) генерализованная цитомегалия обнаруживается у 5–15 %, локализованная — у 10–30 % от общего числа обследованных [6].
Необычайно широкий спектр клинических проявлений ЦМВИ тесно связан с многообразием взаимоотношений между вирусом и макроорганизмом. ЦМВИ может протекать остро (активно), хронически (латентно с рецидивами) и проявляется во врожденной и приобретенной форме. Для цитомегаловирусов характерна способность персистировать в организме с нерегулярной продукцией вирусных частиц и обострениями хронической инфекции, способствуя формированию разнообразной соматической патологии.
Особым свойством ЦМВИ является способность вызывать депрессию практически всех звеньев иммунитета — функции макрофагов, резко угнетать продукцию интерферонов (ИНФ), в первую очередь ИНФ-α. Подавляющее действие вируса на интерферонсинтезирующий механизм клетки связан с угнетением синтеза активирующих белков и протеинкиназы. В ответ на внедрение цитомегаловируса развивается иммунная перестройка в виде снижения реакции лимфоцитов на вирусы в связи с угнетением экспрессии антигена макрофагами, подавлением пролиферативной активности лимфоцитов (что коррелирует с тяжестью клинических проявлений), угнетением фагоцитарной активности и завершенности фагоцитоза.
Многообразие клинических форм ЦМВИ обусловлено способностью вируса к поражению различных тканей и органов. Это дало повод сравнивать цитомегаловирус с многоликим Протеем — мифологическим чудовищем, принимающим облик различных существ.
Врожденная цитомегаловирусная инфекция, являясь самой частой инфекционной фетопатией, представляет значительную проблему из-за возможности реализации тяжелого генерализованного процесса, врожденных пороков развития и потенциального риска формирования хронической патологии. Способность вируса реплицироваться в клетках иммунной системы и индуцировать ее недостаточность является фоном для развития рецидивирующих септических, грибковых и вирусных заболеваний. Повреждение иммунной системы на этапах раннего онтогенетического развития может приводить к формированию необычных иммунных реакций и неадекватности иммунного ответа в позднем онтогенезе. Это проявляется отсроченной патологией, развитием аллергических и аутоиммунных заболеваний [7].
Гематогенно-трансплацентарный путь инфицирования плода ЦМВ по тяжести клинических проявлений является основным. При этом в 10–15 % случаев признаки ЦМВИ проявляются сразу после рождения ребенка. Передача ЦМВИ от матери к плоду возможна в течение всей беременности. Однако последствия инфекции значительно серьезнее при инфицировании в первой половине гестационного периода. Плод может инфицироваться околоплодными водами и при их аспирации и заглатывании, через кожные покровы и конъюнктиву. Восходящий путь инфицирования возможен также при прохождении плодом родового канала, что обусловливает заражение в интранатальном периоде.
В постнатальном периоде новорожденные заражаются в 30 % случаев (данные ВОЗ) от выделений матери, содержащих вирус: слюны, мочи, выделений из гениталий, грудного молока, крови. В настоящее время установлено, что интранатальная (во время родов) или ранняя постнатальная передача ЦМВ происходит в 10 раз чаще, чем трансплацентарная [8].
Наибольший риск внутриутробного ЦМВ-инфицирования плода и развития тяжелых форм заболевания отмечается в тех случаях, когда беременная женщина переносит первичную ЦМВИ. На этом фоне у 5–20 % инфицированных детей отмечается манифестная врожденная ЦМВИ, характеризующаяся тяжелым течением и нередко заканчивающаяся летально. Вместе с тем отсутствие клинических симптомов инфекции при рождении еще не означает дальнейшего благополучия. Впоследствии у 25 % этих детей развиваются серьезные осложнения внутриутробной инфекции, приводящие к инвалидизации и нарушающие качество жизни.
При вторичной инфекции у женщин, серопозитивных к ЦМВ, в период беременности риск инфицирования плода и развития тяжелых форм врожденной ЦМВИ существенно ниже, что обусловлено сформировавшимся анти-ЦМВИ-иммунитетом у перенесших первичную ЦМВИ до беременности. В результате риск внутриутробного инфицирования вирусом цитомегалии при вторичной ЦМВИ во время беременности не превышает 1–2 %, а при инфицировании детей врожденная ЦМВИ протекает преимущественно бессимптомно, манифестные формы заболевания практически не встречаются. В то же время даже при бессимптомном течении врожденной ЦМВИ у 5–15 % детей этой категории в дальнейшем могут отмечаться различные нарушения состояния здоровья.
В постнатальном периоде имеет место разнообразие путей инфицирования ЦМВ: фекально-оральный (бытовой через загрязненные руки, различные предметы обихода, используемые для питья, еды, игр); аспирационный (воздушно-капельный путь передачи); контактный (через поврежденные кожные покровы и мацерированные слизистые оболочки), от медицинского персонала детских учреждений, через предметы ухода за ребенком, инфицирование при переливании крови, трансплантации органов и тканей, половым путем.
Перенесенная первичная ЦМВИ способствует развитию противоцитомегаловирусного иммунитета — у 70 % населения Украины в крови обнаруживаются специфические IgG к ЦМВ. Под воздействием «иммунологического пресса» ЦМВ «прячется, скрывается» в клетках хозяина: внутриклеточное расположение защищает его от иммунного воздействия. Замедляются или полностью прекращаются процессы репликации: вирус «засыпает». При этом дальнейшее его распространение в организме прекращается или резко уменьшается. Этот период инфекционного процесса характеризуется состоянием латенции вируса. Активизация возбудителя в последующем возможна только в тех случаях, когда снижается активность специфического иммунитета, угнетающего его репликацию [9]. При стрессовых ситуациях, интеркуррентных заболеваниях (например, ОРВИ, грипп, обострения хронической патологии и т.д.) вероятна индукция или активизация процессов репликации вируса с дальнейшим его распространением — реактивация ЦМВИ и развитие заболевания.
Основываясь на классификациях клинических форм цитомегаловирусной инфекции у детей, выделяют следующие клинические формы заболеваний, связанных с ЦМВ (табл. 1).
/13.jpg)
Таким образом, для активного течения ЦМВИ характерно острое развитие инфекционного процесса с возможным формированием ЦМВ-обусловленного заболевания. Внутриутробно это аномалии и пороки, ложные (гидронефроз, гидроцефалия) и истинные (пороки сердца, легких и т.д.), воспалительные процессы в ЦНС, печени, сердце (гепатит, фиброэластоз) и т.п. В постнатальном периоде активное течение ЦМВИ клинически может протекать в виде ОРВИ, пневмонии, кардита, гепатита, нефрита, поражений органов кроветворения и др. То есть активное течение ЦМВИ свидетельствует или о первичном инфицировании, или о рецидиве инфекционного процесса. Это подтверждается наличием в сыворотке крови или в секретах (мокрота, смывы со слизистых, слюна, ликвор, моча) антигенов ЦМВ, ДНК, выявляемых методом полимеразной цепной реакции. Определение в крови специфических ЦМВ-IgМ (они быстро исчезают) и IgG менее информативно, хотя наличие IgM и рост в динамике уровня IgG говорят о связях данного заболевания с ЦМВИ.
Если у ребенка, переносящего ЦМВИ (согласно данным анамнеза) или первично обследованного, в крови наличествует только специфический –ЦМВ-IgG, неизменный при динамическом контроле, и отсутствуют ДНК ЦМВ и IgM, то с большой вероятностью можно считать настоящее заболевание ребенка не связанным с ЦМВИ, течение которой в данный момент является латентным и не требует специфического лечения.
Несомненно, что активация персистирующей ЦМВ-инфекции на фоне стрессовых ситуаций, интеркуррентных и вторичных инфекций, травмы и т.д. усугубляет, усложняет и пролонгирует ее течение. Кроме того, персистенция инфекции с ее иммуносупрессивным воздействием определяет вторичное снижение неспецифических факторов защиты с формированием состояний со склонностью к частым и длительным заболеваниям, повышенной предрасположенности к другим вирусно-бактериальным инфекциям. Так, у часто и длительно болеющих респираторными инфекциями детей в 70 % случаев имеет место персистирующая герпесвирусная инфекция, и более чем у трети из них — ЦМВИ. Причем при повторных эпизодах респираторных заболеваний в 67 % случаев наблюдается активация ЦМВИ [11].
Цитомегаловирусная инфекция, наряду с другими герпесвирусами, выявляется в дыхательных путях у детей раннего возраста с повторными (рекуррентными) обструктивными бронхитами — значимым фактором риска развития бронхиальной астмы. Так, при обследовании 136 детей с данной патологией в 36,2 % случаев выявлено активное течение ЦМВИ [12]. Этиотропное лечение ЦМВИ позволило предупредить развитие бронхиальной астмы у 93 % детей данной группы.
Поражающий потенциал ЦМВ огромен: у человека практически нет органа или системы, клеточный аппарат которых не мог бы быть вовлечен вирусом в инфекционный процесс, наблюдается преобладание неспецифических симптомов ЦМВИ над специфическими. Это может быть клиника ОРВИ, тонзиллита, бронхита, пневмонии, энцефалита, кардита, нефрита и т.д. При этом нередко клиническое выздоровление ребенка наступает при проведении стандартной, неспецифической противоцитомегаловирусной терапии. Однако в немалом проценте случаев наблюдается более затяжное течение заболевания у ребенка, резистентность к стандартной терапии, осложнения и рецидивы заболевания. В подобных случаях особое значение приобретает своевременная лабораторная диагностика, направленная на поиск этиологического агента, в частности ЦМВ. В первую очередь эти исследования необходимо проводить у первородящих женщин (при подготовке к беременности, в ее первом триместре и за 2 недели до родов), а также при неблагоприятном исходе предыдущей и при клинической манифестации ЦМВИ во время настоящей беременности.
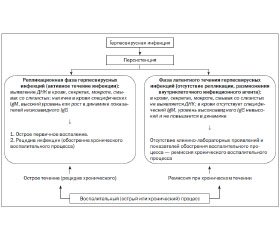
Критерии необходимости проведения специ–фического лечения ЦМВИ, его характер, объем и длительность в первую очередь зависят от активности инфекционного процесса (активный или латентный), состояния систем защиты (склонность к рецидивам — реактивации инфекции), формы (генерализованная — манифестная, локальная) и возраста ребенка (рис. 1).
/14.jpg)
Лечение оппортунистических инфекций, в частности ЦМВ и других герпесвирусов, — это архи–сложная задача в связи с отсутствием в настоящее время однозначно эффективных специфических терапевтических средств, способных на полную эрадикацию возбудителей. Кроме того, преимущественно внутриклеточное существование вирусов делает невозможным достаточно полное проникновение препаратов в клетку, в связи с чем становятся проблематичными нейтрализация и удаление инфекционного агента. Поэтому тактика лечения ЦМВИ направлена в первую очередь на купирование активности инфекционного процесса. Ее характер, в свою очередь, определяется тяжестью и частотой обострений, клиническими проявлениями заболеваний, их осложнениями, а также риском передачи инфекции.
В связи с этим целями и направленностью лечения ЦМВИ является подавление репродукции инфекционного агента в период острых проявлений врожденной или приобретенной инфекции (первичного эпизода заболевания или его обострения — рецидива), профилактика активации латентных форм инфекций, формирование адекватного иммунного ответа с его длительным сохранением с целью блокирования процесса реактивации инфекции в очагах персистенции.
Критериями активности инфекционного процесса (первичного эпизода или его обострения) являются клинические проявления заболевания и, что должно быть обязательным, наличие лабораторных маркеров репликации (активации) герпесвирусов: виремия, антигенемия, ДНК в крови, моче, спинномозговой жидкости, секретах или в мазках и соскобах, обнаружение специфического IgM в сыворотке крови, рост в динамике низкоавидных специфических IgG.
Эффективность лечения любой инфекции в первую очередь связана с наличием средств этиотропной и патогенетически обусловленной терапии. К данной категории препаратов при ЦМВИ относят специфические иммуноглобулины, ациклические нуклеозиды и интерфероны. Формирующийся у инфицированных ЦМВ иммунитет и его реакции направлены прежде всего на нейтрализацию и удаление вируса, его антигенов и пораженных клеток хозяина. Поэтому главенствующую роль в данном процессе, особенно при первичной инфекции или ее рецидиве, играют специфические иммуноглобулины.
Терапия при помощи иммуноглобулинов, тем более специфических, имеет ряд бесспорных преимуществ перед современной химиотерапией. Выделяют две основные формы участия специфических иммуноглобулинов в устранении инфекции: нейтрализация инфекционного агента и иммунный лизис инфекционного агента. Нейтрализация инфекта антителами заключается, с одной стороны, в связывании ими инфекционного фактора в иммунный комплекс, с другой — в препятствовании прикреплению и проникновению его в клетку. Иммунный комплекс, содержащий в себе антитело и антиген (вирус), фиксируется рецептором макрофага с последующим его фагоцитозом и лизисом. С помощью антител происходит также опсонизация инфекта, что в дальнейшем способствует его фагоцитозу. Недостаточная концентрация антител может усиливать репродукцию инфекционных агентов с их патологическим влиянием на хозяина.
Наибольшее распространение и клиническое применение иммуноглобулины получают с момента создания фармакологических форм для внутривенного введения — высокообогащенных гипериммуноглобулинов. Иммуноглобулины IV поколения для внутривенного введения, созданные в 90-е годы прошлого столетия, являются на сегодняшний день максимально безопасными, хорошо переносимыми, наиболее удобными для применения и доказавшими свою эффективность при вирусных инфекциях в случаях их активной репродукции. Биодоступность иммуноглобулинов при внутривенном введении составляет практически 100 %. Специфическая иммуноглобулинотерапия очищенными внутривенными противоцитомегаловирусными препаратами может с успехом применяться даже для лечения инфекций у беременных (в любые сроки беременности), когда противопоказаны многие противоинфекционные средства из-за потенциального эмбриотоксического и тератогенного влияния [13]. Положительное действие противогерпетических иммуноглобулинов отмечено при лечении детей любого возраста с различными проявлениями герпесвирусных инфекций — энцефалитом, офтальмогерпесом, герпетическим стоматитом, герпесом гениталий и кожи.
Широкое применение при ЦМВИ получил Цитобиотект — иммуноглобулин антицитомегаловирусный человека жидкий для внутривенного введения, активность которого обусловлена ЦМВ-нейтрализующим действием данных антител. Цитобиотект оказывает и иммуномодулирующий эффект, влияя на различные звенья иммунной системы человека, повышает неспецифическую резистентность, проявляя антителозависимую клеточную цитотоксичность по отношению к вирусам инфицированной клетки. Применяется для лечения активного течения клинически тяжелых проявлений ЦМВИ у детей любого возраста с иммуносупрессией, в том числе и у новорожденных, или с иммунодефицитом, вызванным различными причинами, в том числе СПИДом. Дозируется из расчета 50–100 ME/кг каждые 2 дня внутривенно капельно до стихания ярких клинических проявлений инфекции. Использование Цитобиотекта в течение нескольких дней практически во всех случаях улучшает течение и прогноз заболеваний, связанных с тяжелой ЦМВИ.
В случаях ассоциации ЦМВИ с другими вирусными или бактериальными инфекциями рекомендуется применение иммуноглобулина человека нормального жидкого для внутривенного введения — Биовен Моно, имеющего иммуноглобулины G к различным инфектам, в т.ч. к группе герпесвирусов, вирусам гриппа, гепатитов, к бактериальным патогенам — стафилококкам, стрептококкам, пневмококкам, кишечной палочке и т.д. Препарат обладает неспецифической активностью, проявляющейся в повышении резистентности к инфекциям. Применяется внутривенно капельно у детей разного возраста из расчета 0,2–0,4 г/кг каждые 3–4 дня.
Эффективным методом лечения ЦМВИ является специфическая химиотерапия ациклическими (атипичными) нуклеозидами, которые поставляют в инфицированную клетку несвойственные ей нуклеозиды, а «неразборчивый» материнский вирус использует их при построении цепей своей дочерней ДНК. В итоге дочерняя ДНК получается дефектной, и вирус расплачивается либо замедлением, либо прекращением процесса копирования. Словом, ациклические нуклеозиды оказывают вирусостатический эффект: в процессе копирования вирусной ДНК псевдонуклеозиды встраиваются в дочерние вирусные ДНК, что приводит к их генетическому дефекту и нежизнеспособности вируса. Таким образом, вирус с дефектной ДНК теряет свои патогенные для человека свойства, становясь к тому же «бесплодным». Основополагающим препаратом данной группы стал ацикловир.
Действие ацикловира складывается из трех основных компонентов:
— высокой специфичности к ферментам герпесвирусов, что обеспечивает его высокую противогерпетическую избирательность и невмешательство в биохимические процессы организма;
— тимидинкиназа герпесвирусов в тысячи раз быстрее, чем клеточная, связывается с ацикловиром, поэтому препарат накапливается только в инфицированных клетках (в остальных клетках его содержание не более 1 %). То есть концентрация ацикловира в инфицированных клетках в 100 раз выше, чем в неинфицированных. Этим объясняется отсутствие в большинстве случаев цитотоксических, тератогенных и мутагенных воздействий препарата;
— ДНК-полимераза вируса «ошибочно» включает фосфорилированный ациклический нуклеозид вместо естественного дезоксигуанозинтрифосфата в концевые участки новых вирусных ДНК, и процесс сборки вирусных ДНК прекращается.
Ацикловир назначается по 200–400 мг 3–5 раз/сут, при необходимости — по 20 мг/кг (до 800 мг на прием) 4 раза/сут. У детей в возрасте до 2 лет применяют в дозе, равной половине дозы для взрослых. Длительность лечения — 5–10 дней. В более тяжелых случаях заболевания возможно про–дление курса лечения и парентеральное введение препарата: внутривенно капельно взрослым и детям старше 12 лет — по 5–10 мг/кг, интервал между введениями — 8 часов; детям в возрасте от 3 месяцев до 12 лет — по 250–500 мг/м2 поверхности тела, интервал между введениями — 8 ч. Для новорожденных доза составляет 10 мг/кг, интервал между введениями — 8 ч.
Сегодня в клинической практике в качестве альтернативы ацикловиру используются валацикловир, фамцикловир и ганцикловир, в которых преодолен основной недостаток ацикловира — низкая биодоступность при пероральном применении.
Наличие в ряде случаев резистентности герпесвирусов к ацикловиру и другим ациклическим нуклеозидам стало серьезной проблемой при лечении конкретного больного ребенка и может непосредственно повлиять на течение и исход заболевания. Это обстоятельство способствовало активным разработкам методов комплексной терапии герпесвирусных инфекций с использованием антивирусных средств в сочетании с иммунотропными препаратами. Особое внимание среди этих препаратов уделяется интерферонам. Широкий спектр физиологических функций интерферонов (противовирусная, радиопротективная, антипролиферативная и иммуномодулирующая) указывает на их контрольно-регуляторную роль в сохранении гомеостаза. Высокая значимость интерферонотерапии наблюдается и при манифестных формах большинства герпесвирусных инфекций, в том числе и ЦМВИ [14]. Широкий спектр противовирусной активности, отсутствие резистентных к интерферону штаммов вирусов предопределили перспективу использования интерферонов как средств этиопатогенетической терапии герпесвирусных инфекций. Высокая противовирусная активность, способность к блокированию размножения и распространения вирусов определили широкое и эффективное применение α- и β-интерферонов при большинстве вирусных инфекций, в т.ч. и при ЦМВИ. Использование индукторов интерфероногенеза при этом весьма ограничено, т.к. в период разгара вирусного заболевания стимуляция интерфероногенеза путем индуцирования их продукции может вызвать срыв компенсаторных возможностей иммунной системы, привести к развитию аллергических и аутоиммунных заболеваний, что связано с повышением продукции многих видов ИНФ, в т.ч. и γ-интерферона, влияющего на активацию иммунных факторов клеточного и гуморального звеньев иммунитета [15]. Выявлено, что на фоне активного течения ЦМВИ у часто и длительно болеющих детей значимое уменьшение в крови уровней α- и β-интерферонов сочеталось с 2–3-кратным увеличением ИНФ-γ, что небезразлично для здоровья ребенка [16].
В связи с этим в педиатрической практике более эффективно и безопасно использование заместительной терапии рекомбинантными α-2β-интерферонами, в т.ч. у новорожденных и недоношенных. Среди препаратов данной группы широкое применение получил отечественный препарат Лаферобион [17]. Препарат обладает комплексным противовирусным, антимикробным, антихламидийным, антипролиферативным и иммуномодулирующим действием [18]. Выпускается в форме ректальных суппозиториев. В состав Лаферобиона входят рекомбинантный α-2β-интерферон (по 150 000 МЕ, 500 000 МЕ, 1 млн и 3 млн МЕ), токоферола ацетат, аскорбиновая кислота и твердый жир. Интерферон, входящий в Лаферобион, производится без использования донорской крови. Среди преимуществ суппозиториев при ОРВИ у детей — лучшая по сравнению с назальными формами интерферонов биодоступность препаратов.
Наличие в комплексе Лаферобиона мембраностабилизирующих компонентов, цитопротекторов — токоферола ацетата и витамина С — обусловливает повышение противовирусной активности интерферона в 10–14 раз путем усиления его иммуномодулирующего действия на Т- и В-лимфоциты. Кроме того, включение в состав Лаферобиона антиоксидантов препятствует окислительному разрушению молекул интерферона и способствует сохранности биологической активности лекарственного продукта.
Методика использования и дозирование Лаферобиона:
— новорожденным, в том числе недоношенным с гестационным возрастом более 34 недель — по 150 000 МЕ 2 раза в сутки;
— недоношенным с гестационным возрастом менее 34 недель — по 150 000 МЕ 3 раза в сутки 5 дней. Перерыв между курсами — 5 дней;
— детям первого года жизни — по 150 000 МЕ 2 раза в сутки;
— от 1 года до 7 лет — 500 000 МЕ 2 раза в сутки;
— 7–14 лет — 1 млн МЕ 2 раза в сутки.
Курс лечения при герпесвирусных инфекциях — 5 дней. Причем во избежание рецидивов имеет смысл проведение в последующем еще 2–3 курсов, между которыми соблюдается 5-дневный интервал.
Принципы лечения при различном течении ЦМВИ представлены в табл. 2.
Демографическая ситуация в Украине, высокий уровень детской смертности и заболеваемости, связанных с внутриклеточными персистирующими инфекциями, в частности герпесвирусными, определяют насущную необходимость пристального изучения этой проблемы. Появление новых диагностических возможностей, лечебных программ позволяет не только активно выявлять инфекции, но и проводить направленную этиотропную и патогенетическую специфическую терапию, предупреждая и купируя развитие вызываемых ими патологических процессов, как острых, так и хронических. В данной работе представлены эффективные подходы к терапии заболеваний, связанных с ЦМВИ.
Список литературы
1. Cunha B.A. Cytomegalovirus pneumonia: community-acquired pneumonia in immunocompetent hosts // Infect. Dis. Clin. North Am. — 2010. — 24 (1). — 147-58.
2. Johansson I., Mаrtensson G., Andersson R. Cytomegalovirus and long-term outcome after lung transplantation in Gothenburg, Sweden // Scand. J. Infect. Dis. — 2010. — 42 (2). — 129-36.
3. Wohl D.A., Kendall M.A., Owens S., Holland G., Nokta M., Spector S.A. The safety of discontinuation of maintenance therapy for cytomegalovirus (CMV) retinitis and incidence of immune recovery uveitis following potent antiretroviral therapy // HIV Clin. Trials. — May-Jun 2005. — 6 (3). — 136-46.
4. A serologic strategy for detecting neonates at risk for congenital cytomegalovirus infection / A. Naessens at al. // Pedat. — 2005. — № 146 (2). — P. 194-197.
5. Congenital cytomegalovirus infection: recent advances in the diagnosis of maternal infection / T. Lazzarotto et al. // Hum. Immunol. — 2004. — № 65 (5). — P. 410-5.
6. Drew W.L. Cytomegalovirus resistance testing: pitfalls and problems for the clinician // Clin. Infect. Dis. — Mar 1 2010. — 50 (5). — 733-6.
7. Орехов К.В. Врожденная цитомегаловирусная инфекция / К.В. Орехов, М.В. Голубева, Л.Ю. Барычева // Детские инфекции. — 2004. — № 1. — С. 49-55.
8. Szenborn L. Significance of diagnostics and treatment in preventing congenital infections with Toxoplasma gondii (Tg), cytome–galovirus (CMV) and parvowirus B19 (PVB19)] // Przegl. Lek. — 2010. — 67 (1). — 54-7.
9. Малашенкова И.К., Дидковский Н.А. Принципы иммунокорригирующей терапии вторичных иммунодефицитов, ассоциированных с хронической вирусно-бактериальной инфекцией // Русский медицинский журнал. — 2002. — Т. 10, № 21. — С. 973-977.
10. Гусева Л.Н., Рогова Л.А., Егорова Н.Ю., Балашова Т.Б. Цитомегаловирусная инфекция (ЦМВИ): классификация и варианты течения // Детские инфекции. — 2003. — № 1. — С. 57-61.
11. Юлиш Е.И., Балычевцева И.В., Висягин В.Б., Кривущев Б.И., Гадецкая С.Г., Ярошенко С.Я., Лютова Т.А., Щур Н.В. Метод дифференцированного похода к лечению и реабилитации часто и длительно болеющих респираторными заболеваниями детей при различном течении персистирующих инфекций // Здоровье ребенка. — 2010. — № 1. — С. 20-29.
12. Юлиш Е.И., Балычевцева И.В., Гадецкая С.Г., Вакуленко С.И. Особенности терапии рецидивирующего обструктивного бронхита у детей раннего возраста, инфицированных внутриклеточными патогенами // Современная педиатрия. — 2007. — № 3 (16). — С. 26-32.
13. Kenneson A., Cannon M.J. Review and meta-analysis ofthe epidemiology of congenital cytomegalovirus (CMV) infection // Rev. Med. Virol. — 2007. — 17 (4). — 253-276.
14. Malmgaard L. Induction and regulation of IFNs during viral infections // J. Interferon Cytokine Res. — 2004. — Vol. 24, № 8. — P. 439-454.
15. Свистушкин В.М., Никифорова Г.Н., Власова Н.П. Возможности лечения больных с острыми респираторными вирусными инфекциями в настоящее время // Лечащий врач. — 2013. — № 1. — С. 34-36.
16. Юлиш Е.И., Чернышева О.Е., Кривущев Б.И., Ярошенко С.Я., Абилова Е.И. Противовирусные средства в лечении и профилактике острых респираторных заболеваний у часто и длительно болеющих детей // Здоровье ребенка. — 2011. — № 6 (33). — С. 95-99.
17. Марушко Ю.В., Мовчан О.С. Клінічні аспекти використання Лаферобіону в педіатрії // Современная педиатрия. — 2012. — № 7. — С. 1-4.
18. Бекетова Г.В. Интерфероны в лечении острых респираторных инфекций у детей // Ліки України. — 2011. — № 3. — С. 106-109.

/13.jpg)
/14.jpg)
/17.jpg)