Статья опубликована на с. 21-30
Здоровий ріст і розвиток дитини в перші 1000 днів життя має надзвичайно важливо значення не лише для виживання та покращення показників здоров’я в ранньому дитинстві, але і для профілактики важливих неінфекційних захворювань старшого віку. Темпи росту людини є найвищими в останній триместр вагітності та в перші місяці життя. Під час останнього триместру вагітності маса дитини збільшується приблизно від 900 до 3400 г, тобто більше ніж утричі. В перші 4 міс. життя доношена дитина подвоює свою масу при народженні, а протягом найближчих 24 міс. її розміри збільшуються удвічі, проте дорослих розмірів вона досягає лише в пізньому підлітковому віці. Водночас мозок дитини набуває величини мозку дорослої людини (приблизно 1200 г) уже у 2 роки. В останньому триместрі вагітності маса мозку збільшується приблизно від 150 г до 400 г, а до шестимісячного віку мозок знову подвоює свої розміри, досягаючи приблизно двох третин величини мозку дорослої людини [1]. Склад і структура мозку також швидко змінюються протягом цього часу [2], і ці зміни продовжують відбуватися в ранньому дитинстві.
Відповідно перинатальний період і раннє дитинство характеризуються високими потребами в енергії і нутрієнтах, насамперед білках, щоб підтримати необхідні темпи росту. Жири, що містяться в грудному молоці та молочних сумішах, також мають надзвичайно важливе значення з кількох причин. Перш за все вони є основним джерелом енергії, щоб підтримувати відповідний ріст і розвиток, забезпечуючи споживання близько половини калорій у вигляді жиру. Однак деякі жирні кислоти (ЖК) на додаток до їх ролі як джерела енергії є важливими компонентами клітинних мембран і/або метаболічними попередниками біологічно активних сполук. Людина не може синтезувати жирні кислоти з подвійними зв’язками в положенні n-6 (ω6) або n-3 (ω3). Ці кислоти є незамінними й їх надходження потрібно забезпечити ззовні через харчові продукти. Важливими похідними незамінних жирних кислот є довголанцюгові поліненасичені жирні кислоти (ДЛПНЖК), що є необхідними для нормального росту і дозрівання багатьох систем організму, однак особливе значення мають для мозку, очей, серцево-судинної й імунної систем. Найважливішими представниками ДЛПНЖК є докозогексаєнова (ДГК) і арахідонова (АК) кислоти, що відіграють важливу роль у формуванні зорової функції і розвитку ЦНС у ранній постнатальний період. Обидві вони переважають серед n-6 і n-3 жирних кислот нервової тканини, а ДГК є основним компонентом мембрани фоторецепторів сітківки ока немовлят. Ендогенний синтез цих жирних кислот може не забезпечувати потреби новонароджених, насамперед недоношених дітей, які не встигають отримати достатньої кількості ДЛПНЖК трансплацентарно.
ДГК і АК наявні в грудному молоці, їх зараховують до біологічно активних сполук, що визначають унікальні властивості цього еталонного природного продукту здорового харчування дітей раннього віку.
Номенклатура та біохімія жирних кислот
Жирні кислоти класифікують за довжиною ланцюга, насиченням або кількістю подвійних зв’язків і просторовою орієнтацією останніх. Відповідно розрізняють коротколанцюгові (< 8 вуглецевих залишків), середньоланцюгові (8–11 залишків), проміжної довжини (12–15 залишків) і довголанцюгові (≥ 16 залишків) ЖК. Насичені ЖК не містять подвійних зв’язків, мононенасичені мають один зв’язок, а поліненасичені — два і більше зв’язки. В ідентичних за кількістю вуглецевих залишків і ступенем насичення ЖК подвійні зв’язки можуть знаходитись в положенні цис- або транс-ізомерів, що впливає на фізичні та біологічні властивості кислот [3].
Характеризуючи ЖК, відповідно до міжнародної номенклатури зазначають кількість вуглецевих залишків і подвійних зв’язків, а також положення першого подвійного зв’язку за порядковим номером вуглецевого залишку, рахуючи від стабільного СН3- (n- або ω-) кінця. Наприклад, олеїнова кислота є мононенасиченою кислотою, молекула якої містить 18 вуглецевих залишків і один подвійний зв’язок між дев’ятим і десятим залишками. Таку структуру описують формулою 18:1n-9.
У людському організмі синтезуються насичені та мононенасичені жирні кислоти, проте не утворюються n-3 і n-6 довголанцюгові поліненасичені жирні кислоти. Попередниками цих сполук є альфа-ліноленова кислота (АЛК), що містить 18 атомів вуглецю, три подвійні зв’язки з першим таким зв’язком у n-3 положенні (С18:3n-3), і лінолева кислота (ЛК), структура якої описується формулою С18:2n-6. Ці жирні кислоти не можуть перетворюватись одна в іншу, тому обидві вони є незамінними й мають обов’язково бути наявними в харчовому раціоні людини.
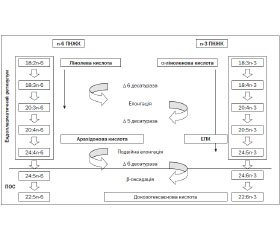
АЛК і ЛК перетворюються на більш ненасичені сполуки з довшим ланцюгом через ферментативне подовження ланцюга (елонгацію) і денасичення (десатурацію). Внаслідок цього процесу з АЛК спочатку утворюється ейкозопентаєнова кислота (С20:5n-3), а далі — ДГК (С22:6n-3). Відповідно ЛК перетворюється на АК (С20:4n-6). В обох типах перетворень беруть участь ті самі ферменти ланцюгового подовження і десатурації, що визначає конкуренцію ферментних субстратів [4] (рис. 1). Іншими словами, утворення певних ДЛПНЖК залежить від співвідношення між n-3 і n-6 кислотами у харчовому раціоні людини. У немовлят темпи ендогенного синтезу ДГК і АК не задовольняють підвищених потреб росту.
Отже, ДГК і АК є важливими компонентами клітинних мембран, особливо в головному мозку, сітківці, серцево-судинній та імунній системах. Крім того, АК є попередником біологічно важливих сигнальних молекул, простагландинів і лейкотрієнів.
Внутрішньоутробне і постнатальне накопичення ДЛПНЖК в організмі дитини
Накопичення ДГК у тканині мозку розпочинається внутрішньоутробно і в другій половині вагітності його можна визначити кількісними методами [5]. Цей процес триває після народження, забезпечуючи досягнення пікової концентрації ДГК (близько 4 г) у дітей віком від двох до чотирьох років [5]. ДГК є також важливим структурним компонентом ліпідів сітківки. Її частка серед усіх жирних кислот зовнішніх сегментів паличок і колбочок перевищує 50 % [6]. На відміну від ДГК інші n-3 ДЛПНЖК у цей період не акумулюються в тканинах мозку і очей. У внутрішньоутробний і післяпологовий періоди у тканинах мозку також збільшується кількість АК.
Ферменти подовження і десатурації для перетворення ПНЖК наявні у печінці плода на ранніх термінах вагітності, але до народження їх активність є низькою [7]. Таким чином, внутрішньоутробно відбувається накопичення n-6 і n-3 ДЛПНЖК, отриманих переважно трансплацентарно, а їх концентрація в пуповинній крові залежить від харчового раціону матері [8]. Новонароджені немовлята здатні синтезувати ДГК і AК незалежно від терміну гестації [9]. Швидкість перетворення АЛК на АК і АЛК на ДГК залежить від генетичних чинників, статі та кількості жирних кислот-попередників, наявних у харчовому раціоні [10]. Водночас, як було зазначено вище, ендогенний синтез цих жирних кислот може не забезпечувати потреби новонароджених, насамперед недоношених дітей, які не встигають отримати достатньої кількості ДЛПНЖК трансплацентарно.
Після народження немовлята отримують АК і ДГК із грудним молоком, що забезпечує переважання вмісту ДГК у тканині мозку порівняно з дітьми на вигодовуванні сумішами, що не містять ДЛПНЖК. У дітей, яких годують сумішами, не збагаченими ДЛПНЖК, темпи синтезу власних ДЛПНЖК із попередників C18 є недостатніми для того, щоб підтримати їх стійкі концентрації у плазмі й еритроцитах [11].
ДЛПНЖК під час вагітності
Наявність активного (проти градієнта концентрації) материнсько-фетального плацентарного транспорту ДГК свідчить про важливе фізіологічне значення цієї кислоти. Активне надходження ДГК із крові матері у кров плода забезпечують специфічні транспортні білки жирних кислот (FATP-1 і –FATP-4) і мембранні білки, що сприяють вибірковому плацентарному захвату саме цієї кислоти [12]. Кількість ДГК, що потрапляє в циркуляцію плода, визначається її вмістом у материнському організмі. Цей показник, у свою чергу, залежить від харчового раціону матері та способу її життя. Саме тому міжнародні рекомендації, розроблені ще у 2001 р., визначали потребу середнього добового споживання ДГК під час вагітності та лактації на рівні 200 мг/добу [13]. Жінки дітородного віку можуть виконати цю рекомендацію, споживаючи одну-дві порції морської риби на тиждень, у тому числі жирних сортів, що є важливим джерелом n-3 ДЛПНЖК. Споживання такої кількості риби звичайно не перевищує допустимих рівнів споживання потенційних забруднювачів навколишнього середовища. Інші джерела n-3 ДЛПНЖК включають збагачені продукти харчування та харчові добавки. Надходження АЛК, що міститься в продуктах харчування і є попередником ДГК, менш ефективне щодо забезпечення оптимального статусу ДГК, ніж безпосереднє споживання цієї кислоти, і є недостатнім для досягнення бажаних рівнів акумуляції ДГК у мозку плода [14].
Ряд досліджень показали, що споживання n-3 ДЛПНЖК з риби, риб’ячого жиру або олії одноклітинних водоростей під час вагітності подовжує тривалість останньої, сприяє народженню дитини з більшою масою і зменшує ризик передчасних пологів. Багатоплідні вагітності та короткий інтервал між вагітностями ще більше підвищують відповідні потреби материнського організму [15]. Міжнародне епідеміологічне дослідження засвідчило, що з вищими концентраціями ДГК у молоці матері та вищим рівнем споживання морепродуктів була пов’язана менша поширеність післяпологової депресії (24,5 % у Південній Африці проти 2 % в Японії) [16].
ДЛПНЖК у період лактації
До складу грудного молока входить лише 20 % поліненасичених жирних кислот, однак ця фракція включає не лише незамінні кислоти (лінолеву й α-ліноленову), але і ДЛПНЖК, частка яких є особливо значною в молозиві. Домінуючими ДЛПНЖК у грудному молоці є ДГК і АК. Уміст АК у молоці є відносно постійним в усіх регіонах світу, тоді як уміст ДГК є варіабельним і більше залежить від харчового раціону і способу життя матері (рис. 2) [17, 18].
Середні популяційні концентрації АК у грудному молоці становлять 0,35–0,7 % загальної кількості жирних кислот, у той час як уміст ДГК коливається від 0,17 до 1,0 % [17]. У матерів, які отримували додаткову ДГК, її вміст у молоці був вищим. Водночас рівень ДГК у молоці вище від 0,8 % загальної кількості жирних кислот мало впливав на збільшення вмісту ДГК у плазмі або еритроцитах немовлят [19].
ДЛПНЖК у молочних сумішах для немовлят
Відомо, що вміст АК і ДГК у плазмі й еритроцитах немовлят, які перебували на грудному вигодовуванні, вірогідно перевищує відповідні показники дітей, яких годували стандартними адаптованими молочними сумішами без ДЛПНЖК. У спробах досягнути статусу ДЛПНЖК дітей на грудному вигодовуванні (за вмістом ДЛПНЖК у плазмі або еритроцитах) немовлят годували сумішами з різними концентраціями і співвідношенням С18 ПНЖК, АЛК і ЛК. Хоча споживання сумішей з вищим співвідношенням АЛК/ЛК забезпечувало незначно вищий уміст ДГК у плазмі й еритроцитах, ці показники все одно не досягали рівня показників дітей на грудному вигодовуванні. Водночас використання сумішей з високим співвідношенням АЛК/ЛК призводило до зменшення концентрацій AК у крові новонароджених [20]. Численні дослідження порівнювали рівні ДЛПНЖК у плазмі й еритроцитах немовлят, яких годували материнським молоком, сумішами, збагаченими ДЛПНЖК, або сумішами без ДЛПНЖК. Рівнів ДГК і АК у дітей на грудному вигодовуванні можна було досягнути лише безпосереднім додаванням обох цих жирних кислот у суміш. Збагачення сумішей лише n-3 ДЛПНЖК без АК може зменшувати вміст АК у крові недоношених [10] і доношених [21] дітей і, отже, негативно впливати на їх фізичний розвиток [22].
Клінічні результати застосування продуктів харчування, збагачених ДЛПНЖК
Харчові ДЛПНЖК і формування зорової функції у немовлят
Немовлята народжуються з незрілою функцією зору, але протягом першого року життя вона стрімко розвивається. Електрофізіологічні методи оцінювання цієї функції, зокрема за допомогою провокованих зорових потенціалів, у дітей раннього віку вважаються найбільш чутливими, а тому їх використання дозволяє виявляти незначні відмінності між групами [23].
Численні дослідження оцінювали вплив забезпечення ДГК на розвиток зорової функції у немовлят. В одному з них вивчали вплив призначення риб’ячого жиру вагітним на ДГК-статус дітей на момент народження і подальше формування зорової функції. Вищий уміст ДГК у крові немовлят був пов’язаний із більш зрілими провокованими зоровими потенціалами у віці 2,5 і 6 місяців [24]. Координація «око — рука» (візуальна моторна інтеграція) у віці 2,5 року також була кращою у дітей, чиї матері отримували високі дози риб’ячого жиру під час вагітності [25]. Декілька досліджень із залученням матерів-годувальниць, які додатково отримували n-3 ДЛПНЖК або плацебо, не виявили відмінностей між відповідними групами, хоча автори продемонстрували вірогідну позитивну кореляцію між гостротою зору і рівнями ДГК у молоці або ДГК статусом малюків [26, 27]. Інші дослідження оцінили вплив збагачення сумішей ДЛПНЖК на розвиток зорової функції у дітей, які отримували такі суміші відразу після народження або пізніше. Частина авторів повідомила про позитивні результати, в той час як інші не знайшли статистично значущих відмінностей залежно від суміші, що споживалась [15]. Водночас у дослідженнях, які не виявили позитивного ефекту збагачення сумішей ДЛПНЖК, використовували продукти з дуже низьким рівнем ДГК.
У двох дослідженнях було оцінено вплив додаткового споживання ДЛПНЖК зі збагаченими сумішами або продуктами прикорму в другому півріччі життя на розвиток зорової функції немовлят. Встановлено поліпшення зору у дітей, яких годували збагаченими продуктами порівняно з дітьми з контрольної групи [28, 29].
У трьох дослідженнях розглянуто потенційні довгострокові переваги годування збагаченими сумішами. Одне з них не засвідчило поліпшення стереозору у дітей віком 4–6 років, які попередньо отримували суміші, збагачені ДЛПНЖК [30]. Друге дослідження не виявило жодних відмінностей між малюками віком 39 місяців, які перебували на грудному вигодовуванні, отримували збагачену або контрольну суміш [31]. У третьому дослідженні протягом 17 тижнів дітей годували трьома різними сумішами (контрольною, збагаченою лише ДГК або АК і ДГК) або грудним молоком, після чого у віці чотирьох років оцінювали зорову функцію й інтелект. Обидва показники були значно гірші в контрольній групі порівняно з дітьми на грудному вигодовуванні, проте таких відмінностей не було в малюків, які отримували дві збагачені суміші [32].
Кокрейнівські огляди 16 досліджень із залученням передчасно народжених дітей [33] і 9 досліджень за участю доношених немовлят [34] не виявили суттєвих зв’язків між збагаченням сумішей ДЛПНЖК, формуванням зорової функції і загальним розвитком дітей раннього віку. Водночас автори зазначили, що недоношені немовлята, залучені у дослідження, були відносно зрілими і здоровими. Існували також значні відмінності між дослідженнями за схемами і методологією оцінювання зорової функції, технологією отримання ДЛПНЖК, їх складом і вмістом у сумішах. Зокрема, у більшості досліджень ефективності сумішей, збагачених ДГК, немовлят контрольної групи годували сумішами, що містили АЛК [35] або низькі концентрації ДГК [36]. Лише в одному дослідженні порівнювали ефективність різних доз ДГК у доношених немовлят за наявності контрольної групи, в якій діти отримували суміш без будь-яких ДЛПНЖК. У немовлят, яких годували сумішами, що містили 0,32; 0,64 або 0,96 % ДГК, виявляли подібну гостроту зору у віці 1 рік, однак вона була вищою, ніж у дітей, які отримували суміш без ДЛПНЖК [37]. Використання більш прискіпливого підходу до оцінки якості досліджень дозволило авторам останнього метааналізу, що загалом включив 16 досліджень і 1949 передчасно народжених і доношених дітей, зробити висновок, що наявні дані доводять суттєвий вплив збагачення сумішей ДЛПНЖК на гостроту зору дітей віком 12 місяців [38].
Харчові ДЛПНЖК і ранній когнітивний розвиток
Беручи до уваги те, що переважаючими n-3 і n-6 жирними кислотами у мозку є ДГК і AК, доцільно передбачити потенційний вплив споживання матір’ю ДГК під час вагітності та в період лактації або збагачення ДЛПНЖК молочних сумішей на когнітивний розвиток немовлят. Проведені в цьому напрямку дослідження використовували різні методи, зокрема тести для оцінки загального (Bayley Scales of Infant Development) і психомоторного (тест Brunet — Lezine) розвитку немовлят, а також більш специфічні обстеження, спрямовані на оцінку розвитку мовлення і здатності вирішувати проблеми. Кожен із зазначених методів оцінює різні компоненти розвитку мозку, а тому суперечливі результати цих досліджень не є несподіваними.
Епідеміологічні дані засвідчили наявність асоціації між високим рівнем споживання риби під час вагітності та темпами постнатального розвитку дитини. Зокрема, йдеться про покращення зорової пам’яті [39], вищий рівень мовного інтелекту й інших поведінкових показників у дітей віком аж до восьми років [40]. У дітей на грудному вигодовуванні віком два місяці ДГК-статус корелював із розвитком мовлення і розуміння в 14 і 18 місяців [41]. Jensen і співавт. [42] оцінювали показники когнітивного розвитку немовлят на грудному вигодовуванні, матері яких протягом чотирьох місяців після пологів додатково отримували ДГК (200 мг/добу) або плацебо (рослинну олію). У 30-місячному віці у дітей, яких годували збагаченим молоком, встановлено значне збільшення індексу психомоторного розвитку, хоча групи не відрізнялись за показниками зорової функції або індексом ментального розвитку.
У подвійному сліпому рандомізованому дослідженні збагачення раціону матері під час вагітності та в період лактації маслом печінки тріски (споживання близько 1,2 г ДГК і 0,8 г ЕПК), забезпечувало перевагу когнітивного розвитку дітей, народжених від цих матерів, у віці чотирьох років у тесті Kaufmann ABC (стандартизований тест оцінки інтелекту) приблизно в 4 бали [43]. Три інших дослідження під час лактації не виявили значного поліпшення когнітивного розвитку дітей [15]. Однак контролювати потенційні фактори впливу у дослідженнях грудного вигодовування і пізнавального розвитку складно.
Суперечливі результати були отримані у дослідженнях із використанням збагачених молочних сумішей. Деякі з них засвідчили значні переваги в когнітивному розвитку дітей, яких годували збагаченими ДЛПНЖК сумішами, тоді як інші дослідження не довели таких переваг [15]. Як і у випадку досліджень, що оцінювали функцію зору, використання сумішей з низьким умістом (< 0,2 %) ДГК, як правило, не забезпечувало досягнення позитивних ефектів.
Раннє споживання ДЛПНЖК може також впливати і на моторний розвиток дітей раннього віку. Самовільна рухова поведінка немовлят, яку називають загальною руховою активністю, свідчить про організацію нервової системи в ранньому віці. Після двох місяців вигодовування сумішами, збагаченими ДЛПНЖК, сумішами, що не містили ДЛПНЖК, або грудним молоком у немовлят, які не отримували ДЛПНЖК, виявляли більший відсоток аномальних самовільних загальних рухів [44]. Однак, діти віком 18 місяців із цих трьох груп не відрізнялись у своєму розвитку за підсумками тесту Bayley або шкали Hempel, яку використовують для стандартизованого виявлення незначних неврологічних дисфункцій. У дітей тримісячного віку, народжених від матерів із недостатнім споживанням АК, виявлялась значно вища аномальна загальна рухова активність [45], а низький статус ДГК при народженні був пов’язаний із меншою кількістю балів за шкалою Hempel у віці 18 місяців [46]. У рандомізованому дослідженні прийом жінками в другій половині вагітності високих доз риб’ячого жиру (добове споживання близько 2,2 г ДГК і 1,1 г ЕПК) покращував візуальну моторну інтеграцію у дітей віком 2,5 року [47]. Отже, як забезпечення в перинатальний період, так і постнатальне споживання ДЛПНЖК можуть сприяти розвитку немовлят.
Незважаючи на наведені відносно оптимістичні ранні результати, останні масштабні дослідження із залученням передчасно народжених немовлят, яких годували збагаченими грудним молоком або сумішами [36, 48], і доношених дітей, матері яких під час вагітності отримували ДГК 800 мг/добу [49], дійшли висновку, що споживання ДГК або більших доз цієї речовини не покращує когнітивний розвиток дітей віком 18 місяців і 8 років. Автори кількох останніх метааналізів зробили такий самий висновок [33, 34, 50]. Водночас у більшості досліджень, включених у згадані метааналізи, когнітивний розвиток дітей оцінювали за допомогою шкали Bayley, що не призначена для таких цілей і показники якої загалом недостатньо корелюють із віддаленим дошкільним розвитком дітей [51]. Натомість на сьогодні існують докази того, що статус ДГК більше впливає на делікатніші особливості формування пізнавальних функцій у дитинстві, такі як увага, пам’ять, швидкість обробки інформації й інші показники інтелектуальної діяльності вищого порядку [35]. Отже, без виконання нової серії досліджень із використанням інших методів оцінки когнітивного розвитку і тривалішим періодом спостереження (до досягнення шкільного віку) робити будь-які висновки про реальний вплив споживання ДЛПНЖК і розумові функції дітей передчасно.
Інші ефекти ДЛПНЖК
Вплив на імунні реакції
Існують свідчення, що споживання ДЛПНЖК у ранньому дитинстві може модулювати імунну відповідь. Частка цих кислот від загальної кількості ЖК в імунних клітинах становить 25 % і функціо–нально вони є найважливішими [52]. Для становлення імунних функцій у новонароджених необхідні ріст і диференціювання імунних клітин. АК є найважливішим структурним компонентом мембран лімфоцитів і необхідна для формування адекватних імунних функцій. Кількісне співвідношення між n-6/n-3 ДЛПНЖК у клітинних мембранах визначає особливості імунної відповіді, перш за все місцевої. Вміст ЖК у фосфоліпідах клітинних мембран усіх клітин дитини, крім нейронів, безпосередньо залежить від складу жирів, що споживаються. Високий уміст ДЛПНЖК у харчовому раціоні відбивається на складі мембранних фосфоліпідів клітин кишечника і визначає їх реакцію на антигенну стимуляцію: n-6 і n-3 ДЛПНЖК по-різному впливають на імунні реакції. Як уже зазначалось, АК (n-6 ДЛПНЖК) є основним метаболічним попередником ейкозаноїдів. Простагландини відіграють особливо важливу роль у модуляції інтенсивності та тривалості запальної й імунної відповідей, забезпечуючи переважно прозапальний ефект. Простагландин E2 (ПГЕ2) модулює імунну відповідь за участі лімфоцитів Th1 і Th2, стимулюючи синтез IgE. Якщо дієта дитини збагачена АК, мембранні фосфоліпіди клітин кишечника також будуть містити підвищену кількість цих кислот. Активація імунних клітин кишечника буде супроводжуватися переважно продукцією ПГЕ2 і підсиленням запальних реакцій, у тому числі алергічних. На відміну від АК ДК пригнічує продукцію ПГЕ2, а також цитокінів, що стимулюють Th2 відповідь, — IL-6, IL-8, –IL-1β, TNF-α. Таким чином, ДГК має протизапальні властивості [53].
У двох рандомізованих дослідженнях вивчали вплив ДЛПНЖК на імунну функцію немовлят. В одному з них недоношені немовлята з 8-го по 42-й день життя отримували збагачену або незбагачену суміші, а їх дані порівнювали з даними дітей, яких годували грудним молоком. Годування сумішшю для недоношених дітей, збагаченою ДЛПНЖК, забезпечувало формування популяцій лімфоцитів, мембранний уміст ДЛПНЖК, продукцію цитокінів і здатність реагувати на антигени, що відповідали показникам немовлят, яких годували грудним молоком, і відрізнялись від показників дітей на штучному вигодовуванні незбагаченою сумішшю [54]. В іншому дослідженні з аналогічним дизайном доношених немовлят годували збагаченою або незбагаченою сумішшю від 2-го до 6-го тижня після пологів. Додавання ДГК і AК зменшувало стимульовану проліферацію лімфоцитів порівняно з відповідним показником у дітей на винятково грудному вигодовуванні. Водночас на відміну від контрольної групи клітинний і цитокіновий профілі у немовлят, які отримували збагачену суміш, були наближеними до профілів дітей на грудному вигодовуванні [55].
Немовлята, народжені вагітними жінками з атопією, які були рандомізовані для отримання високих доз олії морських водоростей у другій половині вагітності, продемонстрували кращу реакцію на антигенний шкірний прик-тест у віці один рік і менш тяжкий атопічний дерматит порівняно з немовлятами, чиї матері отримували плацебо [56].
У норвезькій когорті з 3086 дітей, які перебували під спостереженням протягом 2-го року життя, споживання риби щонайменше 1 раз на тиждень (середній вік дітей на момент включення риби до харчового раціону — 9,1 місяця) вірогідно та суттєво зменшувало шанси виникнення екземи: будь-яка риба — 0,62 (95% довірчий інтервал (ДІ) 0,42–0,91), жирна риба — 0,21 (95% ДІ 0,05–0,86). Асоціації між особливостями харчового раціону матері та виникненням екземи до досягнення дитиною дворічного віку були невірогідними. Автори дослідження зробили висновок, що споживання риби немовлятами протягом першого року життя було важливішим, ніж наявність цього продукту у харчовому раціоні їх матерів під час вагітності [57].
За підсумками іншого когортного дослідження, вигодовування немовлят сумішшю, збагаченою ДГК/АК, асоціювалось зі збільшенням їх віку на момент першого встановлення діагнозу інфекції верхніх дихальних шляхів і найбільш поширених алергічних захворювань, а також меншою частотою цієї патології протягом перших 3 років життя [58].
Вплив на серцево-судинну систему
Захисний вплив n-3 ДЛПНЖК на серцево-судинну систему найкраще продемонстрований і не викликає сумнівів у дорослих.
Споживання молочних сумішей для немовлят, збагачених ДГК й АК, асоціювалось із нижчим артеріальним тиском у дітей віком 6 років [59]. Порівняно з дітьми, яких протягом перших 4 місяців життя годували незбагаченими сумішами, у малюків, які отримували суміші з ДГК і АК, у 6-річному віці були значно нижчими показники середнього артеріального тиску (відмінність середніх показників становила –3,0 мм рт.ст.) і діастолічного артеріального тиску (відмінність середніх показників становила –3,6 мм рт.ст.). Оскільки артеріальний тиск має тенденцію до персистенції з дитинства в доросле життя, ранній вплив харчових ДЛПНЖК може мати довгострокові наслідки щодо зниження артеріального тиску і серцево-судинного ризику.
Два рандомізованих контрольованих дослідження продемонстрували вплив збагачення харчового раціону немовлят ДЛПНЖК на функцію серцево-судинної системи. Щоденне призначення чайної ложки риб’ячого жиру (≈ 1 г ДГК + ЕПК) у віці 9–12 місяців зменшувало вміст тріацилгліцеролу в крові, показники артеріального тиску і частоти серцевих скорочень, а також збільшувало варіабельність серцевого ритму [60, 61].
Отже, сучасні дані свідчать, що збагачення дієти немовлят n-3 ДЛПНЖК оптимізує розвиток серцево-судинної системи, що може зменшувати відповідний ризик у дорослому віці (насамперед щодо розвитку артеріальної гіпертензії).
Шляхи збільшення споживання ДЛПНЖК для матерів і дітей
Численні дослідження оцінювали ефекти і безпеку збагачення харчового раціону вагітних і жінок-годувальниць ДЛПНЖК. У цих дослідженнях використовували тільки ДГК або риб’ячий жир із різним умістом ДГК і EПК. Споживання риби може піддавати організм матері та плода впливу забруднюючих речовин, таких як метил-ртуть, діоксини і поліхлоровані біфеніли, а також збільшувати вміст цих забруднювачів у материнському молоці. З огляду на це для жінок дітородного віку вважається безпечним споживати рибні страви двічі на тиждень [15]. Декілька когортних досліджень засвідчили позитивний взаємозв’язок між високим споживанням морської риби вагітними жінками і поліпшенням когнітивних функцій, вербального інтелекту, тонкої моторної координації і просоціальної поведінки у дітей, що вказує на те, що позитивні ефекти більшого споживання n-3 ДЛПНЖК із морською рибою на розвиток дитини переважують потенційний ризик дії токсичних речовин [13].
Можливі джерела ДЛПНЖК для дітей першого року життя включають грудне молоко, молочні суміші, збагачені ДЛПНЖК, і такі продукти прикорму, як яйця, жирна риба і м’ясо. Безпека має першорядне значення. Олія високого ступеня очищення, отримана з одноклітинних організмів (специфічні види водоростей і грибів), яйця або риба як джерела ДГК і/або AК є прийнятними для використання в молочних сумішах для немовлят і харчових продуктах прикорму, якщо чистота і безпека олії, що використовується, була встановлена. Систематичний огляд впливу збагачення молочних сумішей ДЛПНЖК на фізичний розвиток засвідчив, що збагачення ДГК і АК забезпечує такий самий ріст немовлят, як і під час годування незбагаченими продуктами [62]. Декілька досліджень із молочними сумішами, збагаченими лише ДГК, також продемонстрували адекватне збільшення маси в доношених новонароджених, проте наявних даних недостатньо для остаточних висновків.
Якщо ДЛПНЖК додають до молочних сумішей, поєднане використання ДГК і AК є доцільним. Відносна сталість забезпечення немовлят АК під час грудного вигодовування свідчить про необхідність споживання обох кислот. АК є переважаючою жирною кислотою-попередником ейкозаноїдів, оскільки у високих концентраціях міститься в мембранних фосфоліпідах. АК може бути окисненою за участі трьох різних ферментативних систем: циклооксигеназ (утворюються простагландини і тромбоксани), ліпооксигеназ (утворюються лейкотрієни) і цитохром Р450 монооксигеназ (утворюються 19- і 20-гідроксіейкозотетраєнові кислоти). Ейкозаноїди є надзвичайно важливими біологічно активними сполуками. Наприклад, лише один простагландин (ПГЕ2) впливає на судини, дихальні шляхи, шлунок, нирки, нейтрофіли, лімфоцити і відчуття болю. На сьогодні існує база даних не тільки щодо безпеки, а й ефективності молочних сумішей, що містять АК і ДГК. Усі викладені вище факти разом підтримують необхідність додавання обох кислот, АК і ДГК, якщо суміш збагачується ДЛПНЖК.
Розвиток мозку триває протягом раннього дитинства, що визначає необхідність споживання адекватної кількості ДГК і AК. Із уведенням прикорму діти отримують менше грудного молока або суміші, і загальне харчове надходження ДЛПНЖК може зменшитись, якщо введені продукти не містять їх. Регулярне споживання яєчного жовтка, риби, печінки або інших продуктів харчування, збагачених ДЛПНЖК, може бути доцільним, проте точні потреби у цих речовинах для немовлят другого півроку життя і дітей ясельного віку невідомі. Оскільки споживання ДЛПНЖК може бути корисним для подальшого оптимального неврологічного розвитку, потрібні додаткові дані, які б довели доцільність використання продуктів харчування, збагачених ДГК і AК, у цій віковій групі дітей [15].
Рекомендації щодо споживання ДЛПНЖК для вагітних і годувальниць
Вагітні жінки та матері-годувальниці мають споживати ДГК принаймні 200 мг/добу [15].
Рекомендації щодо споживання ДЛПНЖК для немовлят
Грудне вигодовування є пріоритетним методом харчування здорових дітей. У цьому контексті важливим є також адекватність і збалансованість харчового раціону матерів-годувальниць, у тому числі з регулярним споживанням ДГК. Наявні дані вказують на необхідність збагачення ДГК молочних сумішей для немовлят. Додавання ДГК у кількості щонайменше 0,2 % загального вмісту жирних кислот є необхідним, щоб досягнути важливих функціональних ефектів, однак концентрація ДГК не повинна перевищувати 0,5 % загального вмісту жирних кислот, оскільки дані про безпеку споживання такої кількості ДГК відсутні. Вміст АК має принаймні відповідати аналогічному показнику для ДГК, а концентрація EПК не повинна перевищувати вміст ДГК. Харчовий раціон дитини другого півріччя життя також має містити ДЛПНЖК, але у наш час недостатньо інформації для кількісних рекомендацій щодо їх концентрації у відповідних продуктах харчування [15].
Таким чином, експериментальні та клінічні дані свідчать про важливу роль ДЛПНЖК для здоров’я і розвитку дітей раннього віку, визначаючи фізіологічну доцільність і безпеку збагачення молочних сумішей для немовлят арахідоновою і докозагексаєновою кислотами. Водночас продовжується подальше вивчення оптимальних концентрацій і співвідношень цих речовин у продуктах дитячого харчування.
Список литературы
1. Dobbing J. Quantitative growth and development of human brain / J. Dobbing, J. Sands // Arch. Dis. Child. — 1973. — Vol. 48. — P. 757-767.
2. Georgieff M.K. Nutrition and the developing brain: nutrient priorities and measurement / M.K. Georgieff // Am. J. Clin. Nutr. — 2007. — Vol. 85. — P. 614S-620S.
3. Dietary essential fatty acids in earlypost natal life: long-termoutcomes / R. Uauy, C. Rojas, A. Llanos, P. Mena // Theimpact of maternal nutrition on the offspring / Ed. by G. Hornstra, R. Uauy, X. Yang. — Nestle Nutr. Inst. Workshop Ser., 2005. — Vol. 55. — P. 101-136.
4. Burdge G.C. Conversion of alpha-linolenic acid to longer-chain polyunsaturated fatty acids in human adults / G.C. Burdge, P.C. Calder // Reprod. Nutr. Dev. — 2005. — Vol. 45. — P. 581-597.
5. Martinez M. Polyunsaturated fatty acids in the developing human brain, red cells and plasma: influence of nutrition and peroxisomal disease / M. Martinez // J. World Rev. Nutr. Diet. — 1994. — Vol. 75. — P. 70-77.
6. Stillwell W. Docosahexaenoic acid: membrane properties of a unique fatty acid / W. Stillwell, S.R. Wassall // Chem. and Phys. of Lipids. — 2003. — Vol. 126. — P. 1-7.
7. Long chain polyunsaturated fatty acid formation in neonates: effect of gestational age and intrauterine growth / R. Uauy, P. Mena, B. Wegher [et al.] // Pediatr. Res. — 2000. — Vol. 47. — P. 127-133.
8. Fish oil and folate supplementation of pregnant women and maternal and fetal DHA and EPA plasma levels — a randomized European multicenter trial / S. Krauss-Etschmann, R. Shadid, C. Campoy [et al.] // Am. J. Clin. Nutr. — 2007. — Vol. 85. — P. 1392-1400.
9. The very low birth weight premature infant is capable of synthesizing arachidonic and docosahexaenoic acids from linoleic and linolenic acids / V.P. Carnielli, D.J.L. Wattimena, I.H.T Luijendijk [etal.] // Pediatr. Res. — 1996. — Vol. 40. — P. 169-174.
10. Impact of early dietary intake and blood lipid composition of long-chain polyunsaturated fatty acids on later visual development / D.R. Hoffman, E.E. Birch, D.G. Birch [et al.] // J. Pediatr. Gastroenterol. Nutr. — 2000. — Vol. 31. — P. 540-553.
11. Reduced docosahexaenoic acid synthesis may contribute to growth restriction in infants born to mothers who smoke / C. Agostoni, C. Galli, F. Riva [etal.] // J. Pediatr. — 2005. — Vol. 147. — P. 854-856.
12. Koletzko B. Placental transfer of long-chain polyunsaturated fatty acids (LC-PUFA) / B. Koletzko, E. Larque, H. Demmelmair [et al.] // J. Perinat. Med. — 2007. — Vol. 35. — P. S5-11.
13. Koletzko B. Dietary fat intakes for pregnant and lactating women / B. Koletzko, I. Cetin, J. Brenna // Br. J. Nutr. — 2007. — Vol. 98. — P. 873-877.
14. Brenna J.T. Efficiency of conversion of alpha-linolenic acid to long chain n-3 fatty acids in man / J.T. Brenna // Curr. Opin. Clin. Nutr. Metab. Care. — 2002. — Vol. 5. — P. 127-132.
15. The roles of long-chain polyunsaturated fatty acids in pregnancy, lactation and infancy: review of current knowledge and consensus recommendations / B. Koletzko, E. Lien, C. Agostoni [et al.] // J. Perinat. Med. — 2008. — Vol. 36. — P. 5-14.
16. Hibbeln J.R. Seafood consumption, the DHA content of mothers’ milk and prevalence rates of postpartum depression: a cross-national, ecological analysis / J.R. Hibbeln // J. Affect. Disord. — 2002. — Vol. 69. — P. 15-29.
17. Yuhas R. Human milk fatty acid composition from nine countries varies most in DHA / R. Yuhas, K. Pramuk, E.L. Lien // Li–pids. — 2006. — Vol. 41. — P. 851-858.
18. Docosahexaenoic and arachidonicacid concentration sin human breast milk world wide / J.T. Brenna, B. Varamini, R.G. Jensen [et al.] // Am. J. Clin. Nutr. — 2007. — Vol. 85. — P. 1457-1464.
19. Gibson R.A. Effect of increasing breast milk docosahexaenoic acid on plasma and erythrocyte phospholipid fatty acids and neural indices of exclusively breast fed infants / R.A. Gibson, M.A. Neumann, M. Makrides // Eur. J. Clin. Nutr. — 1997. — Vol. 51. — P. S78-84.
20. A randomized trial of different ratios of linoleic to alphali–nolenic acid in the diet of term infants: effects on visual function and growth / M. Makrides, M.A. Neumann, B. Jeffrey [et al.] // Am. J. Clin. Nutr. — 2000. — Vol. 71. — P. 120-129.
21. Erythrocyte fatty acid composition in term infants fed human milk or a formula enriched with a low eicosapentanoic acid fish oil for 4 months / A. Lapillonne, N. Brossard, O. Claris [et al.] // Eur. J. Pediatr. — 2000. — Vol. 159. — P. 49-53.
22. Lapillonne A. Polyunsaturated fatty acids and infant growth / A. Lapillonne, S.E. Carlson // Lipids. — 2001. — Vol. 36. — P. 901-911.
23. Teller D.Y. First glances: the vision of infants / D.Y. Teller // Investigative Ophthalmology & Visual Science. — 1997. — Vol. 38. — P. 2183-2203.
24. Maternal docosahexaenoic acid supplementation during pregnancy and visual evoked potential development in term infants; a double blind prospective, randomized trial / C.A. Malcolm, D.L. McCulloch, C. Montgomery [et al.] // Arch. Dis. Child. Fetal. Neonatal. Ed. — 2003. — Vol. 88. — P. F383-390.
25. Fish oil supplementation in pregnancy modifies neonatal allergen specific immune responses and clinical outcomes in infants at high risk of atopy: a randomized, controlled trial / J.A. Dunstan, T.A. Mori, A. Barden [et al.] // J. Allergy Clin. Immunol. — 2003. — Vol. 112. — P. 1178-1184.
26. A randomized trial of arachidonic acid dose in formulas containing docosahexaenoic acid in term infants / R.A. Gibson, M. Makrides, J.S. Hawkes [et al.] // Essential fatty acids and eicosanoids: invited papers from the Fourth International Congress. — Ed. by R.A. Riemersma et al. — Champaign, IL: AOCS Press, 1998. — P. 147-153.
27. Maternal fish oil supplementation in lactation: effect on visual acuity and n-3 fatty acid content of infant erythrocytes / L. Lauritzen, M.H. Jorgensen, T.B. Mickelsen [et al.] // Lipids. — 2004. — Vol. 39. — P. 195-206.
28. Visual function in breast-fed term infants weaned to formula with or without long-chain polyunsaturated at 4 to 6 months: a randomized clinical trial / D.R. Hoffman, E.E. Birch, S.C. Yolanda [et al.] // J. Pediatr. — 2003. — Vol. 142. — P. 669-677.
29. Maturation of visual acuity is accelerated in breast-fed infants fed baby food containing DHA-enriched egg yolk / D.R. Hoffman, R.C. Theuer, Y.S. Castaneda [et al.] // J. Nutr. — 2004. — Vol. 124. — P. 2307-2313.
30. Infant nutrition and stereoacuity at age 4–6 years / A. Singhal, R. Morley, T.J. Cole [et al.] // Am. J. Clin. Nutr. — 2007. — Vol. 85. — P. 152-159.
31. Visual, cognitive and language assessments at 39 months: a follow-up study of children fed formulas containing long-chain polyunsaturated fatty acids to 1 year of age / N. Auestad, D.T. Scott, J.S. Janowsky [et al.] // Pediatrics. — 2003. — Vol. 112. — P. e177-83.
32. Visual acuity and cognitive outcomes at 4 years of age in a double-blind, randomized trial of long-chain polyunsaturated fatty acid-supplemented infant formula / E.E. Birch, S. Garfield, Y. Castaneda [et al.] // Early Hum. Dev. — 2007. — Vol. 83. — P. 279-84.
33. Schulzke S.M. Long chain polyunsaturated fattyacid supplementation in preterminfants / S.M. Schulzke, S.K. Patole, K. Simmer // Cochrane Database of Systematic Reviews. — 2011. — Issue 2. — Art. No.: CD000375.
34. Simmer K. Longchain polyunsaturated fatty acid supplementation in infants born at term / K. Simmer, S.K. Patole, S.C. Rao // Cochrane Database of Systematic Reviews. — 2011. — Issue 12. — Art. No.: CD000376.
35. Scholtz S.A. Clinical overview of effects of dietarylong-chain polyunsaturated fattyacids during the perinatal period / S.A. Scholtz, J. Colombo, S.E. Carlson // The importance of immunonutrition. — Eds. M. Makrides, J.B. Ochoa, H. Szajewska. — Nestle Nutr. Inst. Workshop Ser. — 2013. — Vol. 77. — P. 145-154.
36. Neurodevelopmental outcomes of preterminfants fed high-dose docosahexaenoic acid. A randomized controlled trial / M. Makrides, R.A. Gibson, A.J. McPhee [et al.] // JAMA. — 2009. — Vol. 301. — P. 175-182.
37. The DIAMOND (DHA intake and measurement of neural development)study: a double-masked, randomized controlled clinical trial of thematuration of infant visual acuity as a function of the dietary level ofdocosahexaenoic acid / E.E. Birch, S.E. Carlson, D.R. Hoffman [et al.] // Am. J. Clin. Nutr. — 2010. — Vol. 91. — P. 848-859.
38. Qawasmi A. Meta-analysis of LCPUFA supplementation of infant formula and visual acuity / A. Qawasmi, A. Landeros-Weisenberger, M.H. Bloch // Pediatrics. — 2013. — Vol. 131. — P. 262-e272.
39. Maternal fish consumption, hair mercury, and infant cognition in a U.S. cohort / E. Oken, R.O. Wright, K.P. Kleinman [et al.] // Environ. Health Perspect. — 2005. — Vol. 113. — P. 1376-1380.
40. Maternal seafood consumption in pregnancy and neurodevelopmental outcomes in childhood (ALSPAC study): an observational cohort study / J.R. Hibbeln, J.M. Davis, C. Steer [et al.] // Lancet. — 2007. — Vol. 369. — P. 578-585.
41. Innis S.M. Are human-milk long-chain polyunsaturated fatty acids related to visual and neural development in breast-fed infants? / S.M. Innis, J. Gilley, J. Werker // J. Pediatr. — 2001. — Vol. 39. — P. 532-538.
42. Effects of maternal docosahexaenoic acid intake on visual function and neurodevelopment in breastfed term infants / D.L. Jensen, R.G. Voigt, T.C. Prager [et al.] // Am. J. Clin. Nutr. — 2005. — Vol. 82. — P. 125-132.
43. Maternal supplementation with very-long-chain n-3 fatty acids during pregnancy and lactation augments children’s IQ at 4 years of age / I.B. Helland, L. Smith, K. Saarem [et al.] // Pediatr. — 2003. — Vol. 111. — P. e39-44.
44. Long-chain polyunsaturated fatty acids have a positive effect on the quality of general movements of healthy term infants / H. Bouwstra, D.J. Dijck-Brouwer, J.A. Wildeman [et al.] // Am. J. Clin. Nutr. — 2003. — Vol. 78. — P. 313-318.
45. Relationship between umbilical cord essential fatty acid content and the quality of general movements of healthy term infants at 3 months / H. Bouwstra, D.J. Dijck-Brouwer, T. Decsi [et al.] // Ped. Res. — 2006a. — Vol. 59. — P. 717-722.
46. Neurologic condition of healthy term infants at 18 months: positive association with venous umbilical DHA status and negative association with umbilical trans-fatty acids / H. Bouwstra, D.J. Dijck-Brouwer, T. Decsi [et al.] // Ped. Res. — 2006b. — Vol. 60. — P. 1-7.
47. Cognitive assessment of children at age 2(1/2) years after maternal fish oil supplementation in pregnancy: a randomised controlled trial / J.A. Dunstan, K. Simmer, G. Dixon, S.L. Prescott // Arch. Dis. Child. Fetal. Neonatal. Ed. — 2008. –Vol. 93. — P. F45-50.
48. Long-chain polyunsaturated fattyacids and cognition in VLBW infants at8 years: an RCT / A.N. Almaas, C.K. Tamnes, B. Nakstad [et al.] // Pediatrics. — 2015. — Vol. 135. — P. 972-980.
49. Effect of DHA supplementation during pregnancy on maternal depression and neurodevelopment of young children. A randomized controlled trial / M. Makrides, R.A. Gibson, A.J. McPhee [et al.] // JAMA. — 2010. — Vol. 304. — P. 1675-1683.
50. Meta-analysis of long-chain polyunsaturated fatty acid supplementation of formula and infant cognition / A. Qawasmi, A. Landeros-Weisenberger, J.F. Leckman, M.H. Bloch // Pediatr. — 2012. — Vol. 129. — P. 1141-1149.
51. Colombo J. Is the measure the message: the BSID and nutritional interventions / J. Colombo, S.E. Carlson // Pediatrics. — 2012. — Vol. 129. — P. 1166-1167.
52. Dose-related effects of eicosapentaenoic acid on innate immune function in healthy humans: a comparison of young and older men / D. Rees, E.A. Miles, T. Banerjee [et al.] // Am. J. Clin. Nutr. — 2006. — Vol. 83. — P. 331-342.
53. Calder P.C. Dietary modification of inflammation with li–pids / P. Calder // Proceedings of the Nutrition Society. — 2002. — Vol. 61. — P. 345-358.
54. Lower proportion of CD45R0+ cells and deficient interleukin-10 production by formula-fed infants, compared with human-fed, is corrected with supplementation of long-chain polyunsaturated fatty acids / C.J. Field, C.A. Thomson, J.E. Van Aerde [et al.] // J. Pediatr. Gastroenterol. Nutr. — 2000. — Vol. 31. — P. 291-299.
55. Effect of providing a formula supplemented with long-chain polyunsaturated fatty acids on immunity in full-term neonates / C.J. Field, J.E. Van Aerde, L.E. Robinson, M.T. Clandinin // Br. J. Nutr. — 2008. — Vol. 99. — P. 91-99.
56. Dunstan J.A. Does fish oil supplementation in pregnancy reduce the risk of allergic disease in infants? / J.A. Dunstan, S.L. Prescott // Curr. Opin. Allergy Clin. Immunol. — 2005. — Vol. 5. — P. 215-221.
57. Oien T. Do early intake of fish and fish oil protect against eczema and doctor-diagnosed asthma at 2 years of age? A cohort study / T. Oien, O. Storro, R. Johnsen // J. Epidemiol. Community Health. — 2010. — Vol. 64. — P. 124-129.
58. The impact of early nutrition on incidence of allergic manifestations and common respiratory illnesses in children / E.E. Birch, J.C. Khoury, C.L. Berseth [et al.] // J. Pediatr. — 2010. — Vol. 156. — P. 902-906.
59. Long chain polyunsaturated fatty acid supplementation in infant formula and blood pressure in later childhood: follow up of a randomized controlled trial / J.S. Forsyth, P. Willatts, C. Agostoni [et al.] // Br. Med. J. — 2003. — Vol. 326. — P. 953-958.
60. The effect of fish oil supplementation on heart rate in healthy Danish infants / L. Lauritzen, J.H. Christensen, C.T. Damsgaard, K.F. Michaelsen // Pediatr. Res. — 2008. — Vol. 64. — P. 610-614.
61. Fish oil affects blood pressure and the plasma lipid profile in healthy Danish infants / C.T. Damsgaard, L. Schack-Nielsen, K.F. Michaelsen [et al.] // J. Nutr. — 2006. — Vol. 136. –P. 94-99.
62. Supplementation of infant formula with long chain polyunsaturated fatty acids does not influence the growth of term infants / M. Makrides, R.A. Gibson, T. Udell [et al.] // Am. J. Clin. Nutr. — 2005. — Vol. 81. — P. 1094-1101.

/23.jpg)
/24.jpg)