Стаття опублікована на с. 23-29
Захворювання органів шлунково-кишкового тракту (ШКТ) в дитячому віці перебігають динамічно та мають виражену клінічну симптоматику, що можна пояснити постійним напруженням адаптації органів ШКТ до підвищення харчового навантаження, функціональною, ферментативною, імунологічною незрілістю. Незважаючи на чіткий анатомо-фізіологічний розподіл травного тракту на відділи, травлення — це єдиний, цілісний процес, що відбувається завдяки тісним взаємозв’язкам між діяльністю окремих органів. Розлад функцій одного з відділів травного тракту часто спричиняє порушення функції інших органів.
Печінка та кишкова мікрофлора є основними системами, при взаємодії яких здійснюються процеси детоксикації організму. Тому порушення роботи однієї складової призводить до функціональних та структурних змін іншої, що зазвичай не може не відбиватися на загальному стані дитини [1].
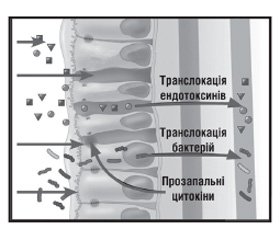
Відомо, що порушення роботи гепатобіліарної системи створюють умови для змін кишкового мікробіоценозу. Порушення функцій гепатоцитів веде до зниження детоксикаційної функції печінки, порушення ентерогепатичної циркуляції жовчних кислот, змін у метаболізмі холестерину. У хворих з хронічними захворюваннями печінки порушення складу нормальної кишкової мікрофлори виявляються практично в 100 % випадків, причому тяжкість клінічних проявів захворювання нерідко прямо пов’язують з вираженістю змін мікроекології кишечника [2]. Це можна пояснити тим, що кишково-печінкова циркуляція пов’язана з мікрофлорою кишечника і модулює її шляхом секреції жовчних кислот, секреторного IgA, муцинів, дефензинів, лізоциму, фосфоліпаз тощо [3, 4]. У нормі ферментація коротколанцюгових жирних кислот, кінцевих компонентів гідролізу, синтез вітамінів і біологічно активних речовин кишковою мікрофлорою забезпечують трофіку слизової оболонки кишечника, підвищують її енергетичний потенціал і стимулюють моторику. При дисбалансі мікрофлори кишечника збільшується кількість потенційно патогенних бактерій, що продукують такі метаболіти, як аміак, ароматичні амінокислоти, сульфіти, ендогенні токсини [5]. Ці речовини сприяють запаленню слизової оболонки, порушенню пристінкового травлення. Як наслідок, порушення функціональних властивостей кишкової стінки, місцевого імунітету й зміни кишкової нормофлори формують можливості для бактеріальної транслокації та патологічного впливу дисбіотичних порушень на печінку [6–8]. Накопичені в просвіті кишечника ендотоксини патогенних бактерій проникають через слизову кишечника в систему кровообігу та ворітну вену й спричиняють ушкодження гепатоцитів. Таким чином виникає порочне коло, при якому порушення роботи одного з органів травлення веде до низки змін в іншому (рис. 1).
/24-1.jpg)
Велике значення у формуванні патологічних змін має стан місцевого кишкового імунітету. Доведено, що кишкова мікрофлора бере участь в активації імунних реакцій і формуванні імунної толерантності макроорганізму. Згідно з науковими дослідженнями, взаємодія мікрофлори й епітеліальних клітин слизової кишечника відбувається за участю кишково-асоційованої лімфоїдної тканини кишечника (GALT). GALT взаємодіє з мікрофлорою через Тоll-рецептори шляхом розпізнавання стабільних патоген-асоційованих молекулярних моделей (PAMPs). Сигнали Тоll-рецепторів активують експресію прозапальних цитокінів, таких як TNF-альфа, ІЛ-6, ІЛ-8 та інших, що призводить до стимуляції адаптивного типу імунітету проти PAMPs [9, 10]. Порушення мікрофлори призводить як до підвищення бактеріального навантаження на печінку, так і до мікробно-індукованої експресії запальних цитокінів, що, в свою чергу, впливає на перистальтику й процеси регенерації слизової кишечника [4].
Отже, формування патології гепатобіліарної системи є складним багатофакторним процесом. –Наукові дослідження останніх десятиріч виявили тісний взаємозв’язок порушень метаболізму ліпідів і перебігу захворювань гепатобіліарної системи. В умовах порушення обміну жовчних кислот, загальних ліпідів і поліненасичених жирних кислот при захворюваннях гепатобіліарної системи [11] визначено вагомий вплив кишкової мікрофлори на перебіг ліпідного обміну. Так, за даними S. Kishino і співавт. (2013), мікрофлора регулює метаболізм поліненасичених жирних кислот шляхом кодування ферменту, що бере участь у їх обміні [12]. Некон’юговані жовчні кислоти (холева та хенодезоксихолева) додатково модифікуються кишковою мікрофлорою для отримання вторинних, менш токсичних жовчних кислот, а погіршення цього процесу корелює з цирозом печінки [13]. За даними S.A. Joyce і співавт. (2014), мікрофлора кишечника, маючи власні ферментативні механізми, впливає на обмін холестерину й системний ліпідний обмін [14]. Порушення обміну жирних кислот у печінці призводить до роз’єднання процесів окислення й фосфорилювання на мембрані мітохондрій, зростає роль ω-мікросомального окислення, що супроводжується пошкодженням гепатоцитів. Вільні жирні кислоти чинять пряму пошкоджуючу дію на гепатоцити, викликаючи апоптоз клітинних структур активацією лізосомального шляху й підвищенням синтезу печінкою фактора некрозу пухлини альфа [15].
Отже, механізми взаємодії печінки та мікробіоти кишечника достатньо вивчені, і з огляду на ці дані вплив на кишкову мікробіоту може бути корисним у лікуванні захворювань печінки.
У корекції дисбіозу перевага надається пробіотикам, ефективність яких доведена численними дослідженнями та метааналізами. За даними Всесвітньої гастроентерологічної асоціації, доведений позитивний імунологічний влив пробіотиків на стан кишкової мікробіоти полягає:
— в aктивації місцевих макрофагів, що підвищують рівень антигенів В-лімфоцитів, а також місцевій й системній секреції ІgА;
— модуляції цитокінового профілю;
— зниженні чутливості до антигенів продуктів харчування.
Також виділено неімунологічні властивості пробіотиків:
— вони сприяють засвоєнню їжі й конкурують з патогенною мікрофлорою за поживні речовини;
— змінюють місцевий рівень рН, що створює несприятливе середовище для патогенних мікро–організмів;
— продукують бактеріоцини для інгібування патогенної мікрофлори;
— нейтралізують супероксидні радикали;
— стимулюють секрецію муцину епітеліальними клітинами;
— підсилюють бар’єрні функції кишечника;
— конкурують з патогенною мікрофлорою за адгезію до кишкового епітелію;
— модифікують вироблені патогенами токсини.
Отже, пробіотики мають ряд корисних властивостей, що важливі для лікування пацієнтів із порушенням мікрофлори та захворюваннями гепатобіліарної системи.
Однак варто зауважити, що, за даними практичних рекомендацій Всесвітньої гастроентерологічної асоціації, слід надавати перевагу пробіотикам з правильним маркуванням, які класифікуються за родом, видом, штамом і буквено-цифровою назвою. Саме ці дані маркування дають можливість оцінити наявність доказів ефективності та безпеки для конкретного пробіотичного штаму, того, що оцінювався в дослідженні. Деякі ефекти не можуть бути відтворені іншим штамом, при іншій технології виробництва або при зменшенні життєздатності штаму [16].
Слід зазначити, що в останній редакції узгоджувального документа Європейського товариства дитячої гастроентерології, гепатології та нутриціології (ЕSPGHAN) 2014 року експерти зробили висновки про переваги пробіотиків, що зареєстровані як лікарські засоби, перед тими, які зареєстровані як харчові добавки, та тими, що використовуються в молочних продуктах [17]. Отже, можна сформулювати три основних вимоги до пробіотика, який слід використовувати в дитячий практиці:
1. Пробіотик повинен мати штам-специфічні докази клінічної ефективності та безпеки.
2. Слід вибирати пробіотик, що зареєстрований як лікарський засіб.
3. Механізми дії пробіотика повинні передбачати влив на ту клінічну ситуацію, при якій він призначається (спектр мікробного антагонізму, створення умов для росту нормальної мікрофлори, можливість підвищення місцевого імунітету тощо).
Усім цим вимогам відповідає лікарський препарат Ентерол® — S.boulardii CNCM I-745 французької компанії Biocodex. Ентерол® — пробіотик з рівнем клінічних доказів А, з підтвердженою поліморфізмом мікросателітних локусів специфічністю штаму, за даними огляду та метааналізу використання S.boulardii, що був опублікований у Всесвітньому журналі гастроентерології (McFarland L., 2010). Саме Ентерол® — ліофілізована форма S.boulardii CNCM I-745 компанії Biocodex — зареєстрований в Інституті Пастера в м. Парижі та має численні докази ефективності й безпеки в оригінальних штам-специфічних дослідженнях.
Висока клінічна ефективність Ентеролу® зумовлена широким спектром властивостей, що надзвичайно важливі для позитивного впливу на кишкову мікробіоту:
— Ентерол® зберігає структуру щільних контактів, що запобігає порушенню бар’єрних властивостей кишечника;
— Ентерол® покращує метаболізм ентероцитів, стимулює вироблення коротколанцюгових жирних кислот, що мають неабияке значення як джерело енергії для ентероцитів та регулюють репарацію слизової оболонки кишечника;
— Ентерол® за рахунок визволення сперміну та спермідину справляє трофічний ефект на слизову оболонку тонкої кишки;
— його ферментативна дія зумовлена підвищенням активності дисахаридаз тонкого кишечника (лактази, сахарази, мальтази);
— антимікробна дія зумовлена здатністю Saccharomyces boulardii пригнічувати ріст патогенних та умовно-патогенних мікроорганізмів і грибів, що порушують біоценоз кишечника, таких як: Clostridium difficile, Clostridium pneumoniae, Staphуlococcus aureus, Pseudomonas aeruginosa, Candida krusei, Candida pseudotropical, Candida albicans, Salmonella typhi, Salmonella enteritidis, Escherichia coli, Shigella dysenteriae, Shigella flexneri, Klebsiella, Proteus, Vibrio cholerae, а також Entamoeba hystolitica, Lambliae, Enterovirus, Rotavirus;
— підсилення неспецифічного імунного захисту відбувається за рахунок підвищення продукції IgA та секреторних компонентів інших –імуноглобулінів.
Враховуючи механізми впливу Ентеролу® на кишкову мікрофлору, що сприяють поліпшенню клінічного стану при порушенні кишкового мікробіоценозу, можливість та безпеку його застосування в дітей, ми обрали саме цей препарат для лікування дітей раннього віку з порушеннями кишкової мікробіоти та захворюваннями гепатобіліарної системи. Отже, метою дослідження було вивчення стану мікрофлори та оцінка ефективності Ентеролу® в дітей з гепатобіліарною патологією.
Матеріал і методи дослідження
У дослідження було залучено 35 дітей раннього віку з вродженими гепатитами. Для встановлення діагнозу хворим проведено клінічне, лабораторне та інструментальне дослідження згідно з сучасними протоколами МОЗ України. Вроджений гепатит діагностували при реалізації захворювання в перші 6 місяців життя [18]. З метою уточнення етіології захворювання визначали маркери TORCH-інфекцій, вірусних гепатитів В і С, за показаннями проводилися реакція Вассермана, дослідження на вірус імунодефіциту людини та інші інфекції. Виключення вроджених порушень обміну з ураженням печінки проводилося після консультації генетика, також використовувались спеціалізовані біохімічні мето–дики.
Усім дітям з вродженими гепатитами призначалось лікування за загальними рекомендаціями: застосування симптоматичної терапії, що включала гепатопротектори, вітамінні препарати; дезінтоксикаційна парентеральна терапія; противірусну терапію препаратом інтерферону альфа-2β у добовій дозі 50 тис. од/кг маси тіла за схемою: 10 днів щодня — доза насичення, а потім через день протягом 6 місяців отримували діти з вірусною етіологією ураження.
Пацієнтів розподілили на 2 групи: 20 дітей основної групи, які крім стандартної терапії отримували препарат Ентерол® 250 мг двічі на добу протягом 14 днів, і 15 дітей групи порівняння, які отримували стандартну терапію. За тяжкістю перебігу й активністю запального процесу в печінці суттєвих міжгрупових розбіжностей не було, не було й вікових та гендерних розбіжностей. Усі пацієнти були включені в аналіз ефективності та переносимості. Тривалість спостереження становила 1 місяць.
Комплекс досліджень включав аналіз анамнестичних даних, клінічний огляд, дані лабораторних досліджень: загальний аналіз крові, біохімічне дослідження крові — рівень некон’югованої і кон’югованої фракцій білірубіну, трансаміназ, лужної фосфатази. За концентрацією трансаміназ оцінювалась активність запального процесу печінки. Мінімальна активність характеризувалась підвищенням трансаміназ до 1,5–2 норм, низька — до 3–5 норм, помірна — до 9 норм и висока — понад 10 норм.
Бактеріологічне дослідження калу проводилося класичним методом, визначали кількість бактерій у фекаліях шляхом засіву серійних розведень на диференціально-діагностичні середовища (Методичні рекомендації № 10-13/3114/1U, 1986 р.). Дисбіоз оцінювали відповідно до класифікації І.Б. Куваєвої і К.С. Ладодо (1991) [19].
Ефективність лікування оцінювали за динамікою зникнення основних клінічних проявів захворювання (загальний стан дітей, порушення апетиту, абдомінальний біль, здуття живота, характер випорожнень) на 7-й і 14-й день спостереження, даними аналізу мікрофлори кишечника на 14-й день лікування. Клініко-біохімічні показники (холестатичний синдром, АЛТ, АСТ, лужна фосфатаза (ЛФ), гаммаглутамілтрансфераза (ГГТ)) у динаміці визначались на 28-й день спостереження.
Результати досліджень оброблені методами статистичного аналізу в ППП Excel і Statistica.
Результати дослідження і їх обговорення
У структурі захворювань гепатобіліарної системи в дітей раннього віку, за даними наших досліджень, вроджений гепатит становить 39,5 % випадків. У структурі вроджених гепатитів переважали гепатити, зумовлені реалізацією TORCH-інфекції (56,3 %). Вірусний гепатит В і С виявлено в 4 дітей (2,3 % — гепатит В і 2,3 % — гепатит С), яких виключили з дослідження. У 39,1 % випадків причини вродженого ураження печінки не виявлено, за ознаками перебігу діагностовано криптогенний гепатит.
Відповідно до розробленого протоколу спостереження наявність основних клінічних симптомів і їх ступінь оцінювались у динаміці на 7-й та 14-й день лікування (табл. 1).
При аналізі впливу проведеного лікування на виділені симптоми оцінювалась їх клінічна та статистична значущість. Клінічна значущість оцінювалася за різницею часток дітей із відповідною симптоматикою в основній (Δро) та контрольній групі (Δрк), клінічна перевага запропонованої методики порівняно зі стандартним методом — за різницею відповідних часток дітей в основнiй і контрольній групах на 14-й день лікування. Для перевірки статистичної значущості використовувалися критерії Стьюдента, Фішера точний та χ2 Пірсона. Результати вважали статистично значущими при pα ≤ 0,05. При розрахунку довірчих інтервалів часток, менших ніж 20 або більше 80 %, через невеликі обсяги груп використовували методику ϕ-Фішера.
Перевірка розподілів хворих у досліджуваних групах за виділеними симптомами розбіжностей не виявила (за критерієм χ2 Пірсона, pα > 0,05).
У пацієнтів основної групи, які отримували Ентерол® у схемі лікування, нормалізація клінічних симптомів та загального стану відбувалася швидше; зменшення/зникнення симптомів на 14-й день лікування відзначено в більшості пацієнтів основної групи. Так, кількість дітей з порушеним загальним станом в основній групі за 14 днів лікування статистично значущо (pα = 0,03) зменшилася на Δро = 35 %: з 14 (70,0 ± 21,4) % до 7 (35,0 ± 22,3) %. Причому в групі контролю статистично та клінічно значущого покращання загального стану не відбулося Δрк = 13,7 %: було 12 [54,5; 96,6] %, стало 10 (66,7 ± 26,1) %.
У результаті лікування в основній групі відзначені позитивні зміни за показниками апетиту та метеоризму. Так, до лікування було 18 [68,2; 99,2] % дітей зі зниженим апетитом, після проведеного лікування їх залишилося 10 (50,0 ± 23,4) %, Δро = 40 %. У групі контролю кiлькiсть дітей зі зниженим апетитом майже не змінилася Δрк = 13,3 %. Тобто в кінці спостереження в дітей групи контролю показники апетиту були гіршими: Δp = 30,0 %.
При оцінці наявності метеоризму після проведеного лікування відзначено зменшення в основній групі кількості дітей з наявністю цього симптому з 17 [68,2; 99,2] % до 6 (30,0 ± 21,4) % (Δро = 55 %, pα = 0,001). Результати вірогідно відрізнялися від групи контролю (Δpк = 50 %, pα = 0,006), у якій не вдалося досягти значущих змін цього показника (Δpк = 6,7 %).
Оцінку абдомінального болю в дітей раннього віку проводили, беручи до уваги немотивований крик і плач дітей. В основній групі в результаті проведеного лікування через 14 днів кiлькiсть дітей з абдомінальним болем значно зменшилася з 18 [68,2; 99,2] % до 11 (55,0 ± 23,0) % (Δро = 35,0 %, pα = 0,02), причому в цій підгрупі сильно вираженого болю не було в жодного пацієнта. У групі контролю майже не відбулося зменшення кiлькостi дітей з вираженим абдомінальним болем (було 14, стало 12 дітей із цим симптомом, Δрк = 13,3 %).
Аналіз характеру випорожнень у динаміці спостереження показав, що діти основної групи досягли значного поліпшення за цими показниками. Так, в основній групі нормалізації випорожнення з клінічною та статистичною значущістю вдалося досягти в більшої кількості дітей, ніж у групі порівняння: 6 (30,0 ± 21,4) %, Δpо = 30,0 % (pα = 0,001), проти 2 [0,9; 36,6] %, Δpк = 13,3 %. У частини дітей в обох групах залишилися розріджені випорожнення, які оцінювались окремо. Встановлено, що в дітей основної групи частота випорожнень зменшилася до трьох-чотирьох разів на добу при значно меншому об’ємі калових мас і патологічних домішок. Такого результату не вдалося –досягти в пацієнтів групи порівняння. У всіх пацієнтів із запором в основній групі проведене лікування сприяло зникненню цього стану зі статистичною та клінічною значущістю (pα = 0,04). При аналізі цього показника в групі контролю статистично та клінічно вірогідних змін у процесі лікування не визначено.
Аналіз мікробіологічного дослідження випорожнень у дітей з гепатитами виявив порушення мікробного спектра товстої кишки. У дітей обох груп стан мікрофлори кишечника відповідав показникам дисбіозу І–ІІІ ступеня, а саме: дисбіоз І ступеня реєструвався в 10 (50,0 %) дітей основної групи та 8 (53,3 %) дітей групи порівняння; дисбіоз ІІ ступеня — у 6 (30,0 %) і 5 (33,3 %) дітей відповідно; у 4 дітей основної групи та 3 дітей групи порівняння діагностовано дисбіоз ІІІ ступеня. У цілому для мікробного пейзажу в дітей з ушкодженням печінки характерні дефіцит біфідобактерій (ББ) (< 107 КУО/г) і лактобактерій (ЛБ) (< 107 КУО/г), підвищення кількості та зміна видового співвідношення умовно-патогенних бактерій. Так, встановлено вірогідне пригнічення біфідобактерій у 55,0 % дітей основної групи і 46,7 % групи порівняння, лактобактерій — у 60,0 і 66,7 % відповідно, кишкової палички — у 45,0 і 60,0 % відповідно, причому її ферментативні властивості змінені в 40,0 і 33,3 % відповідно. Їх кількісне зниження супроводжувалося збільшенням питомої ваги умовно-патогенної флори: Klebsiella, S.аureus, ентерококів. У 13 (65,0 %) дітей основної групи й 11 (73,3 %) дітей групи порівняння встановлена асоціація кількох видів умовно-патогенних мікроорганізмів у різних комбінаціях.
/28-1.jpg)
Зміни мікрофлори після проведеного лікування розцінювалися нами як важливий показник ефективності терапії. Як видно з табл. 2, у дітей, яким був призначений Ентерол®, відмічалася статистично значуща нормалізація показників мікрофлори. У групі порівняння статистичного впливу на показники мікрофлори після лікування не спостерігалося для жодного показника. При порівнянні впливу проведеного лікування на показники мікрофлори між групами встановлено, що більший відсоток нормалізації рівня популяцій ББ досягли пацієнти основної групи (Δpо = 40,0 %, pα = 0,01, проти Δpк = 6,7 % у групі порівняння). Нормалізації рівня ЛБ досягли вдвічі більше пацієнтів в основній групі, ніж у групі порівняння, Δpо = 33,3 % (pα = 0,05). Також на 14-й день лікування в пацієнтів основної групи статистично вірогідно знизилися рівні стафілокока епідермального (Δро = 35,0 %; pα = 0,01) та грибів роду Candida (Δро = 30,0 %; pα = 0,02).
Аналіз клініко-біохімічних показників функціонального стану печінки (АЛТ, АСТ, ЛФ, ГГТ) проводився на 28-й день лікування й виявив позитивні зміни в дітей обох груп із більш вираженою тенденцією до нормалізації в основній групі. Тенденція до більш швидкого поліпшення динаміки холестатичного синдрому відмічена за результатами дослідження в дітей основної групи: рівень загального білірубіну в основній групі знизився на 118,4 ± 89,5 мкмоль/л проти 63,5 ± 24,0 мкмоль/л у групі порівняння (p < 0,1), ЛФ — на 180,0 ± 113,5 од/л проти 96,0 ± 35,5 од/л відповідно (p < 0,1). Для вірогідної оцінки показників функції печінки, активності запального процесу слід продовжити спостереження за біохімічними показниками в динаміці. Алергічних реакцій, побічних ефектів протягом лікування не спостерігалось.
Висновки
1. У дітей раннього віку з гепатитами визначаються клінічно значимі дисбіотичні порушення кишечника.
2. Мікробний пейзаж у дітей з гепатитами характеризується дефіцитом резидентної мікрофлори, підвищенням кількості та зміною видового співвідношення умовно-патогенних бактерій.
3. Включення в схему терапії препарату Ентерол® у дітей зі змінами мікробіоценозу кишечника на тлі захворювань гепатобіліарної системи забезпечує більш швидке усунення диспептичних розладів і поліпшення загального стану пацієнтів порівняно з лікуванням препаратами базисної терапії, досягнення нормалізації рівнів ББ і ЛБ, ефективне зниження рівня умовно-патогенної мікрофлори.
4. Дані дослідження дозволяють рекомендувати Ентерол® дітям із порушенням мікрофлори кишечника в комплексному лікуванні захворювань гепатобіліарного тракту.
Список литературы
1. Чихачева Е., Селиверстов П., Тетерина Л., Добрица В. Микробиоценоз кишечника при хронических заболеваниях печени: диагностика и лечение // Лечащий врач. — 2011. — № 7. — С. 18-21.
2. Закиров И.Г. Дисбактериоз кишечника при хронических вирусных гепатитах. — Казань, 2003. — 86 с.
3. Levi A.C., Borghi F., Petrino R., Bargoni A., Fronticelli C.M., Gentilli S. Modifications of the trophism of intestinal mucosa after intestinal and bilio-pancreatic diversion in the rat // Ital. J. Gastroenterol. — 1991. — 23 (4). — 202-7.
4. Barbosa T., Rescigno M. Host-bacteria interactions in the intestine: homeostasis to chronic inflammation // Wiley Interdiscip. Rev. Syst. Biol. Med. — 2010. — 2. — 80-97.
5. Chen C., Li L., Wu Z., Chen H., Fu S. Effects of lactitol on intestinal microflora and plasma endotoxin in patients with chronic viral hepatitis // J. Infect. — 2007. — 54 (1). — 98-102; doi: 10.1016/j.jinf.2005.11.013.
6. Riordan S.M., Williams R. The intestinal flora and bacterial infection in cirrhosis // J. Hepatol. — 2006. — 45 (5). — 744-57; doi: 10.1016/j.jhep.2006.08.001.
7. Luyer M.D., Buurman W.A., Hadfoune M., Speelmans G., Knol J., Jacobs J.A. et al. Strain-specific effects of probiotics on gut barrier integrity following hemorrhagic shock // Infect. Immun. — 2005. — 73 (6). — 3686-92; doi: 10.1128/IAI.73.6.3686-3692.2005.
8. Rachmilewitz D., Katakura K., Karmeli F., Hayashi T., Reinus C., Rudensky B., et al. Toll-like receptor 9 signaling mediates the anti-inflammatory effects of probiotics in murine experimental colitis // Gastroentero–logy. — 2004. — 126 (2). — 520-8
9. Shaykhiev R., Behr J., Bals R. Microbial patterns signaling via Toll-like receptors 2 and 5 contribute to epithelial repair, growth and survival // PLoS One. — 2008. — 3. — e1393.
10. Chamberlain N.D., Vila O.M., Volin M.V., Vol–kov S., Pope R.M., Swedler W., Mandelin A.M. 2nd, Shahrara S. TLR5, a novel and unidentified inflammatory mediator in rheumatoid arthritis that correlates with disease activity score and joint TNF-alpha levels // J. Immunol. — 2012. — 189. — 475-483.
11. Pitt H.A. Hepato-pancreato-biliary fat: the good, the bad, the ugly // Informa Health care. — 2007. — Vol. 9. — P. 92-97.
12. Kishino S., Takeuchi M., Park S.-B. еt al. Polyunsaturated fatty acid saturation by gut lactic acid bacteria affecting host lipid composition // P. Natl. Acad. Sci USA. — 2013. — 110. — 17808-13.
13. Schnabl B., Brenner D.A. Interactions between the intestinal microbiome and liver diseases // Gastroentero–logy. — 2014. — 146. — 1513-24.
14. Joyce S.A., MacSharry J., Casey P.G. et al. Regulation of host weight gain and lipid metabolism by bacterialbile acid modification in the gut // P. Natl. Acad. Sci USA. — 2014. — 111. — 7421-6.
15. Rahman R., Hammoud G.M., Almashhrawi A.A. et al. Primary hepatocellular carcinoma and metabolic syndrome: an update // World J. Gastrointestinal Onco–logy. — 2013. — Vol. 5. — P. 186-194.
16. Guarner F., Khan A.G., Garisch J. et al. World Gastroente–rology Organisation Global Guidelines: Pro–biotics and prebiotics, October 2011 // J. Clin. Gastro–enterol. — 2012. — 46 (6). — 468-481.
17. Hania Szajewska, Alfredo Guarino, Iva Hojsak, Flavia Indrio, Sanja Kolacek, Raanan Shamir, Yvan Vandenplas, and Zvi Weizman, on Behalf of the ESPGHAN Working Group for Probiotics and Prebiotics, Use of Probiotics for Management of Acute Gastro–enteritis: A Position Paper by the ESPGHAN Working Group for Probiotics and Prebiotics // JPGN. — April 2014. — Vol. 58, № 4.
18. Шабалов Н.П. Неонатология: Учебное пособие: В 2 т. / Шабалов Н.П. — 4-е изд. — Т. 1. — М.: МЕДпресс-информ, 2006. — 608 с.
19. Куваєва І.Б., Ладодо К.С. Мікроекологічні й імунні порушення в дітей. — М., 1991.
20. Vleggaar F.P., Monkelbaan J.F., van Erpecum K.J. Pro–biotics in primary sclerosing cholangitis: a randomized placebo-controlled crossover pilot study // Eur. J. Gastroenterol. Hepatol. — 2008. — 20 (7). — 688-92. doi: 10.1097/MEG.0b013e3282f5197e.
21. Solga S.F. Probiotics can treat hepatic ence–phalopathy // Med. Hypotheses. — 2003. — 61 (2). — 307-13.
22. Rayes N., Seehofer D., Hansen S., Boucsein K., Muller A.R., Serke S. еt al. Early enteral supply of lactobacillus and fiber versus selective bowel decontamination: a controlled trial in liver transplant recipients // Transplantation. — 2002. — 74 (1). — 123-7.
23. Волосовец А.П., Бережной В.В., Кривопустов С.П. Клиническое применение saccharomyces boulardii в современной педиатрии: доказательная база // Современная педиатрия. — 2009. — 12. — 11. — http://medexpert.org.ua

/24-1.jpg)
/27-1.jpg)
/28-1.jpg)