Статья опубликована на с. 47-50
Лечение синдрома холестаза до сих пор остается проблемой. Основной целью коррекции реологических свойств желчи при различных заболеваниях печени и желчевыводящих путей является в первую очередь профилактика возможных осложнений, отмечающихся при длительном холестазе, в виде фиброза и цирроза печени [6, 8, 10].
Препаратом выбора при необструктивном холестазе сегодня является урсодезоксихолевая кислота (УДХК) — третичная желчная кислота, которая применяется в клинической практике для лечения заболеваний гепатобилиарной системы более 40 лет [3, 4].
УДХК представляет собой желчную кислоту, образующуюся в кишечнике и печени, которая составляет 0,1–5 % от общего пула желчных кислот и является нетоксичной вследствие гидрофильности ее молекулы. При лечении препаратами УДХК происходит смещение пропорций составных частей желчи в сторону преобладания УДХК над остальными желчными кислотами. Положительное влияние УДХК связывается с вытеснением токсичных желчных кислот из энтерогепатической циркуляции (путем конкурентного ингибирования всасывания в подвздошной кишке) и предупреждением их повреждающего действия на мембраны. Отмечено ее цитопротекторное действие, обусловленное способностью встраиваться в мембраны гепатоцитов, в результате чего уменьшается продукция антигенов HLA I класса на поверхности гепатоцитов, тем самым предотвращая развитие аутоиммунных реакций. УДХК оказывает желчегонное действие вследствие холегепатического шунта (возвращение из канальцев к синусоидальной мембране через перибилиарные сплетения) [2, 6, 11].
Первые наблюдения терапевтической эффективности УДХК при вирусных гепатитах принадлежат U. Leuschner и соавт. (1981 г.). Авторы отметили снижение активности печеночных трансаминаз, содержания билирубина, уменьшение частоты рецидивов заболевания. В 1990 г. проведено исследование изменения состава желчных кислот и динамики показателей цитолитического и холестатического синдромов в процессе лечения. У больных, получавших УДХК в качестве монотерапии и в комбинации с таурином, достоверное или отчетливое увеличение УДХК в желчи коррелировало с доcтоверным снижением активности печеночных трансаминаз и гамма-глутамилтранспептидазы (ГГТП) в сыворотке крови на 25–30 %. Аналогичное исследование проведено A. Attili и соавт. (1994 г.), в ходе которого было установлено положительное влияние монотерапии УДХК на биохимические показатели и гистологическую активность при хронических вирусных гепатитах В и С. Авторы выявили положительное влияние УДХК на общее состояние больных: значительное уменьшение раздражительности, слабости, утомляемости, кожного зуда. В результате лечения УДХК в течение 8 недель отмечено снижение активности АЛТ, АСТ, ГГТП, ЩФ и содержания в крови билирубина более чем наполовину (40–60 %) [7].
Безопасность и эффективность применения УДХК были подтверждены в многочисленных клинических исследованиях, как при острых и хронических вирусных гепатитах у детей и взрослых, так и при другой патологии печени, сопровождающейся развитием синдрома холестаза [1, 5, 9].
С учетом изложенного нами было проведено исследование при острых вирусных гепатитах (ОВГ) у детей, сопровождающихся синдромом холестаза. Целью настоящего исследования было усовершенствование лечения ОВГ у детей, сопровождающихся синдромом холестаза.
Материал и методы исследования
Исследование проводилось в клинике детских инфекционных болезней Национального медицинского университета (г. Киев) на протяжении 2014–2015 гг. Под наблюдением находилось 40 детей с ОВГ в возрасте от 4 месяцев до 18 лет. Диагноз ОВГ А был установлен у 33 детей, гепатита В — у 4 детей, установить этиологию заболевания у 3 детей не удалось. Всех больных наблюдали и обследовали в течение острого периода болезни.
Для расшифровки этиологического диагноза ОВГ применяли стандартные маркеры вирусных гепатитов: анти-HAV IgM, HBsag, анти-HBc IgM, анти-HCV Ig суммарные. У пациентов, у которых отмечались трудности в расшифровке этиологии ВГ, использовали определение в крови РНК HCV и ДНК HBV с помощью полимеразной цепной реакции.
Функциональное состояние печени изучалось путем исследования активности основных печеночно-клеточных ферментов (аланинаминотрансфераза — АЛТ, аспартатаминотрансфераза — АСТ, щелочная фосфатаза — ЩФ, лактатдегидрогеназа — ЛДГ), ГГТП, тимоловой пробы (ТП), уровня общего билирубина и его фракций.
С помощью рандомизации пациенты были распределены на 2 группы: дети из 1-й группы (контрольная, n = 27) получали базисную терапию ОВГ, больные из 2-й группы (основная, n = 13) получали базисную терапию ОВГ в сочетании с УДХК. В нашей работе мы использовали препарат УДХК оте–чественного производства под коммерческим названием Укрлив®, суспензия. Доза препарата составляла 10 мг/кг/сутки (1 мерная ложка суспензии (5 мл) содержит 250 мг УДХК). Суспензия принималась внутрь вечером перед сном и запивалась небольшим количеством воды. Длительность приема препарата составляла 28 дней. Базисная терапия ОВГ включала: режим, диету, дезинтоксикационную, симптоматическую терапию (спазмолитические препараты при болях в животе). Рандомизация больных по группам исследования была проведена методом случайных чисел.
Статистическая обработка полученных результатов проводилась с использованием современных методов медицинской статистики с помощью MS Excel 2007. Определяли средние показатели (t-тест Student), стандартные отклонения (М ± m). Оценку терапии проводили с помощью метода однофакторного дисперсионного анализа. Разницу частот определяли по методу оценки разницы между частотой появления признака в отдельных сериях наблюдения.
Дизайн исследования: проспективное, рандомизированное, сравнительное, пострегистрационное клиническое исследование в параллельных группах.
Результаты исследования и их обсуждение
В результате исследования диагноз легкой формы ОВГ был установлен у 27,5 % детей (11 детей), среднетяжелой — у 42,5 % (17 детей), тяжелой — у 30 % (12 детей).
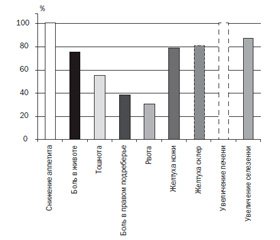
Изучение анамнеза показало, что у всех детей заболевание начиналось остро. Клиника характеризовалась снижением аппетита у 100 % детей, болью в животе — у 75 % (30 детей), тошнотой — у 55 % (22 ребенка), болью в правом подреберье — у 37,5 % (15 детей), рвотой — у 30 % (12 детей). При объективном обследовании пациентов желтуха склер была выявлена у 87,5 % детей (35), желтуха кожи — у 77,5 % детей (31), увеличение размеров печени — у 100 % детей, селезенки — у 87,5 % (35 детей) (рис. 1).
При лабораторном биохимическом обследовании пациентов с ОВГ обнаружено повышение активности АЛТ и АСТ у 100 % больных (40 детей), ЛДГ — у 65 % (26), ГГТП — у 52,5 % (21), ЩФ — у 77,5 % (31), ТП — у 22,5 % (9), билирубина общего — у 87,5 % (35 детей) (рис. 2).
Маркеры синдрома холестаза в виде повышения уровня ЩФ и ГГТП были выявлены у 82,5 % детей.
В динамике наблюдения на 7-й день от начала лечения было установлено, что уже в этот период наметилась определенная тенденция в отличиях частоты встречаемости симптомов ОВГ в группах исследования. Так, снижение аппетита в этот период отмечалось у 96,3 % больных (26 детей) контрольной группы и 61,5 % (8 детей) основной группы (p = 0,013), боль в животе отмечалась у 18,5 % (5 детей) в 1-й группе и у 23,1 % во 2-й группе (3 ребенка), тошнота — у 11,1 % (3 ребенка) в 1-й группе и у 7,7 % (1 ребенок) во 2-й группе, боль в правом подреберье наблюдалась у 40,7 % (11 детей) в 1-й группе и у 23,1 % (3 ребенка) — во 2-й группе, рвота в этот период не отмечалась ни у одного ребенка, желтуха склер наблюдалась у 77,8 % (21 ребенок) пациентов 1-й группы и 69,2 % (9 детей) пациентов 2-й группы; желтуха кожи отмечалась у 37,0 % детей (10) в 1-й группе и у 23,1 % (3 детей) — во 2-й группе (p > 0,05). Увеличение размеров печени и селезенки оставалось у всех детей 1-й и 2-й группы наблюдения на 7-й день от начала лечения.
На 28-й день от начала лечения у детей 2-й группы не регистрировали такие симптомы, как снижение аппетита, боль в животе и правом подреберье, рвота, в то время как у пациентов 1-й группы эти симптомы сохранялись у 11,1; 7,4 и 3,7 % соответственно (p > 0,05). Желтуха склер в этот период отмечалась у 37,0 % (10 детей) в 1-й группе и у 23,1 % (3 ребенка) во 2-й группе, увеличение размеров печени отмечалось у 92,5 % (25) детей 1-й группы и у 76,9 % (10 детей) 2-й группы, увеличение размеров селезенки — у 33,3 % (9 детей) и у 30,1 % (4 ребенка) соответственно (p > 0,05).
Включение в комплексную терапию ОВГ у детей, сопровождающегося холестазом, УДХК способствовало более быстрой нормализации биохимических показателей функционального состояния печени. Так, на 7-й день от начала лечения наметилась положительная тенденция в динамике уровня изучаемых биохимических показателей в исследуемых группах. Показатель активности АЛТ оставался повышенным у 92,5 % (25) детей 1-й группы и у 84,6 % (11) детей 2-й группы, ЩФ — у 77,8 % (21 ребенок) в 1-й группе и у 61,5 % (8 детей) во 2-й группе, ГГТП — у 78,8 % (21 ребенок) в 1-й группе и у 76,9 % (10 детей) во 2-й группе, повышение уровня ЛДГ отмечалось у 85,1 % (23 ребенка) обследованных в 1-й группе и у 84,6 % (11 детей) во 2-й группе, повышение уровня ТП регистрировалось у 22,2 % (6 детей) в 1-й группе и у 48,5 % (3 детей) во 2-й группе (p > 0,05).
На 28-й день от начала лечения уровень общего билирубина в сыворотке крови нормализовался у всех обследуемых детей 2-й группы, активность АЛТ оставалась повышенной у 30,7 % (4 детей), ЩФ — у 23,0 % (3 детей), ГГТП — у 23,0 % (3 детей), ЛДГ — у 23,0 % (3 детей), тогда как у детей 1-й группы активность АЛТ оставалась повышенной у 51,9 % (14 детей), ЩФ — у 37,3,0 % (10 детей), ГГТП — у 40,7 % (11 детей), ЛДГ — у 40,7 % (11 детей) и общий билирубин сыворотки крови — у 11,1 % (3 детей) (p < 0,05).
За время проведения исследования побочных эффектов при применении препарата УДХК –(Укрлив, суспензия) зарегистрировано не было.
Выводы
1. У 82,5 % детей с острыми вирусными гепатитами обнаружен синдром холестаза.
2. Включение в комплексную терапию ОВГ у детей, сопровождающегося холестазом, УДХК –(Укрлив, суспензия) способствует более быстрому регрессу основных симптомов заболевания.
3. Включение в комплексную терапию ОВГ у детей, сопровождающегося холестазом, УДХК (Укр–лив, суспензия) способствует более быстрой нормализации биохимических показателей функционального состояния печени, в первую очередь таких как АЛТ, ЩФ, ГГТП.
Список литературы
1. Выставкина Г.В., Писарев А.Г., Учайкин В.Ф., Чаплыгина Г.В. Лечение Урсосаном холестаза при острых и хронических вирусных гепатитах у детей // Детские инфекции. — 2002. — № 1. — С. 40-42.
2. Кузнецова Е.Л., Широкова Е.Н. Гепатобилиарные транспортеры (OATP2 и BSEP) в ткани печени пациентов с холестатическими заболеваниями печени на фоне проводимой терапии // Рос. журнал гастроэнтерол., гепатол. и колопрокт. — 2007. — № 2. — С. 28-34.
3. Рациональная фармакотерапия заболеваний органов пищеварения: Руководство для практикующих врачей / Под ред. В.Т. Ивашкина. — М.: Медицина, 2003. — 1027 с.
4. Рейзис А.Р., Никитина Т.С., Дрондина А.К. и др. Урсодезоксихолевая кислота как фоновая терапия заболеваний гепатобилиарной системы у детей и подростков // Российский гастроэнтерологический журнал. — 2001. — № 1. — С. 86-91.
5. Рейзис А.Р. Терапия и профилактика хронических гепатитов В и С у детей и подростков // Современные проблемы профилактической педиатрии. — М., 2003. — С. 6-8.
6. Синдром холестаза у детей / Н.А. Коровина, И.Н. Захарова, Н.Е. Малова // Вопросы современной педиатрии. — 2005. — № 3. — С. 39-43.
7. Топорков А.С. Применение урсодезоксихолевой кислоты при хронических вирусных гепатитах // www.consilium-medicum.com/article/7285.
8. Яковенко Э.П., Григорьев П.Я., Агафонова Н.А., Яковенко А.В. Внутрипеченочный холестаз: от патогенеза к лечению // Практикующий врач. — 1998. — № 2. — С. 20-23.
9. Chen W., Liu Y., Glund C. Bile acids for viral hepatitis, 2003 // Cochrane Database Syst. Rev. — 2003. — P. 2.
10. Lazaridis K.N., Gores G.J., Lindor K.D. Ursodeoxycholic acid mechanisms of action and clinical use in hepatobiliary disorders // J. Hepatol. — 2001. — V. 35. — P. 134-146.
11. Lobo-Yeo A., Senaldi G., Portmann В. et al. Class I and class II major histo-compatibility complex antigen expression on hepatocytes: a study in children with liver disease // Hepatology. — 1990. — V. 12. — P. 224-227.

/49-1.jpg)