Статья опубликована на с. 101-107
Несмотря на многочисленные исследования патогенеза, разработку новых лекарственных препаратов, создание специальных программ Всемирной организации здравоохранения, в настоящее время проблема бронхиальной астмы (БА) у детей остается актуальной. Прежде всего это связано с невозможностью взятия под контроль характера течения заболевания [14]. Одной из предполагаемых причин этого является ремоделирование дыхательных путей.
Воспалительный процесс, развивающийся при бронхиальной астме под воздействием специфических и неспецифических факторов, особенно при тяжелом течении заболевания, способствует морфологическим и функциональным изменениям во всех структурах дыхательных путей [3, 18]. Уже в течение первого года персистирующего аллергического воспаления развивается ремоделирование дыхательных путей [10]. Через четыре года после начала заболевания возможно развитие необратимых изменений [2]. Структурные изменения в дыхательных путях, свидетельствующие о ремоделировании, могут происходить в начале патологического процесса, когда на основании клинических данных еще не установлен диагноз бронхиальной астмы [25].
Основными участниками данного патологического процесса являются эпителиальные клетки, базальная мембрана, гладкомышечные элементы, фибробласты и макрофаги [23]. В результате развиваются необратимые морфологические изменения в виде гипертрофии или гиперплазии гладкомышечных элементов, роста и формирования новых сосудов, десквамации эпителия дыхательных путей, гиперплазии бокаловидных клеток, а также накопление коллагена в зонах, расположенных ниже базальной мембраны [20, 21].
Несмотря на то, что в последние годы достигнут определенный прогресс в выявлении основных закономерностей, определяющих ремоделирование дыхательных путей при бронхиальной астме, проблема остается нерешенной [2]. Отсутствуют исследования о роли персистирующих внутриклеточных инфекций при процессах ремоделирования дыхательных путей у детей, а также возможности коррекции патологических изменений при помощи лекарственных средств.
Целью нашей работы явилось определение влияния персистирующих внутриклеточных инфекций на процессы ремоделирования дыхательных путей при бронхиальной астме у детей, а также разработка методов лечения и профилактики хронического воспалительного процесса.
Под нашим наблюдением находилось 328 детей в возрасте от 1 до 15 лет с персистирующей формой бронхиальной астмы. У всех пациентов определялся уровень иммуноглобулинов классов M и G в сыворотке крови, а также ДНК вируса простого герпеса І–ІІ типов, цитомегаловируса, вируса Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе в соскобе слизи со слизистой оболочки ротовой полости и мокроте. В результате полученных данных были выделены 2 группы обследуемых детей. Основную группу (I группа) составили 256 детей с бронхиальной астмой, инфицированных перечисленными внутриклеточными инфекциями, в группу сравнения (ІІ группа) вошли 72 ребенка с бронхиальной астмой, не инфицированные внутриклеточными инфекциями. Группу контроля составили 50 практически здоровых детей.
Активное течение инфекционного процесса, вызываемого внутриклеточными персистирующими возбудителями, определялось по наличию в соскобе со слизистой оболочки ротовой полости и мокроте ДНК возбудителей. По результатам исследования пациенты основной группы были разделены на 2 подгруппы — с активным течением инфекционного процесса, включающей 164 ребенка, и с латентным течением — 92 ребенка.
Нами в сравнении изучены уровни различных медиаторов ремоделирования бронхов в сыворотке крови детей, больных бронхиальной астмой, инфицированных цитомегаловирусом, вирусом простого герпеса І–ІІ типов, вирусом Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе, при активном и латентном течении инфекционного процесса, а также не инфицированных внутриклеточными возбудителями пациентов. В частности, определялись уровни фермента металлопротеиназы 9 (ММР-9), специфического тканевого ингибитора ММР-9 — TIMP-1, трансформирующего фактора роста β (TGF-β), эндотелина-1, аутоантител к коллагену III типа, рассчитывался индекс фиброзирования TIMP-1/ММР-9 (табл. 1, 2).
/102.jpg)
В результате исследования было выявлено, что уровень фермента эндопептидазы ММР-9 в сыворотке крови детей, как инфицированных (основная, или І группа), так и не инфицированных внутриклеточными возбудителями (группа сравнения), был более чем в 2–2,5 раза выше, чем в группе практически здоровых детей. Активность матричных металлопротеиназ является одной из значимых причин, формирующих ремоделирование дыхательных путей. Металлопротеиназы способны гидролизировать все компоненты экстрацеллюлярного матрикса: коллагены, проколлагены, протеогликаны, эластин, фибронектин, ламинин, а также адгезивные и другие белки соединительной ткани, денатурировать фибриллярные коллагены [9, 24]. ММР-9 участвует в ангиогенезе дыхательных путей и способна активировать TGF-β1, приводящий к субэпителиальному фиброзу [22].
Полученные данные свидетельствуют о том, что увеличение уровня сывороточного ММР-9 указывает на дефект гомеостаза экстрацеллюлярного матрикса даже у детей со стабильной, контролируемой астмой, в связи с чем позволяет использовать уровень данного фермента в качестве неинвазивного маркера воспаления и ремоделирования дыхательных путей при бронхиальной астме у детей.
В физиологических условиях металлопротеиназы секретируются в незначительных количествах и регулируются специфическими тканевыми ингибиторами металлопротеиназ (TIMP). Подавление ММР-9 происходит под действием тканевого ингибитора 1-го типа — TIMP-1.
В результате исследования было выявлено, что уровень тканевого ингибитора металлопротеиназ TIMP-1 в сыворотке крови детей, больных бронхиальной астмой, как инфицированных, так и не инфицированных внутриклеточными возбудителями, был более чем в 7 раз выше, чем в группе практически здоровых детей. При активном течении инфекции у пациентов I группы уровень TIMP-1 был выше, чем при латентном течении инфекционного процесса (p < 0,001). Было выявлено статистически значимое отличие данного показателя в основной группе детей при активном течении инфекции и детей группы сравнения (р = 0,004).
Повышение уровня тканевого ингибитора металлопротеиназ TIMP-1 свидетельствует об определенном контроле и регулировании чрезмерной активности ММР-9. Избыток тканевого ингибитора металлопротеиназ-1 в сыворотке крови больных бронхиальной астмой связан с хронической бронхиальной обструкцией [19].
Вследствие таких изменений происходит усугуб–ление процессов ремоделирования дыхательных путей. Поэтому важное значение имеет определение уровня соотношения ММР с ингибитором TIMP (TIMP-1/MMP-9) как маркера фиброза, склероза тканей, влияющего на толщину стенки дыхательных путей у пациентов с бронхиальной астмой, вследствие нарушения баланса между синтезом и деградацией компонентов внеклеточного матрикса в пользу чрезмерной протеолитической активности [12], эмфизематозных изменений в легких [9].
При обследовании детей, больных бронхиальной астмой, было выявлено, что индекс фиброзирования TIMP-1/ММР-9 в сыворотке крови детей, больных бронхиальной астмой, инфицированных внутриклеточными возбудителями, статистически отличался (p < 0,001) от показателей группы здоровых детей. В группе детей, больных бронхиальной астмой и не инфицированных внутриклеточными инфекциями, соотношение TIMP-1/ММР-9 статистически значимо не отличалось от показателей основной группы пациентов (р = 0,061) и практически здоровых детей (р = 0,332). При активном и латентном течении инфекции у пациентов I группы индекс фиброзирования TIMP-1/ММР-9 был практически на одинаковом уровне. Уменьшение мольного соотношения TIMP-1/ММР-9 свидетельствует о повреждении тканей, а избыток TIMP-1, приводящий к увеличению соотношения TIMP-1/ММР-9, отображает ремоделирование дыхательных путей вследствие хронического воспалительного процесса, возникающего при бронхиальной астме у детей, за счет субэпителиального осаждения коллагена [16]. Хронический, длительный дисбаланс TIMP-1/ММР-9 приводит к утолщению дыхательных путей и ограничению воздушного потока, что усугубляет течение бронхиальной астмы у детей [15, 16]. Гиперпродукция ММР-9 и TIMP-1, изученная при инфицировании дыхательных путей вирусом гриппа A H1N1/v, свидетельствовала о подавляющем их действии на возбудитель [8]. Таким образом, повышение уровня ММР-9 и TIMP-1 у детей с бронхиальной астмой, особенно инфицированных внутриклеточными возбудителями, при активном течении инфекционного процесса, может быть также связана с их действием на процессы, способствующие инактивации внутриклеточных возбудителей.
Повышенная выработка металлопротеиназ приводит к высвобождению и активации факторов роста, в частности профибротического трансформирующего фактора роста β-1 (TGFβ-1) [15]. При изучении в ходе исследования в сыворотке крови детей, больных бронхиальной астмой, уровня цитокина TGFβ-1, который рассматривается как иммунопатологическая молекула при заболеваниях, связанных с избыточным фиброзом [25], было выявлено повышение данного фактора роста как в основной группе детей, так и в группе сравнения. Так, в группе детей с бронхиальной астмой, инфицированных внутриклеточными возбудителями, уровень TGFβ-1 практически в 5 раз был выше показателя здоровых детей (p < 0,001). В группе детей, не инфицированных внутриклеточными инфекциями, уровень данного цитокина был в 2 раза выше уровня здоровых детей (р = 0,067). При определении уровня TGFβ-1 в основной группе пациентов при активном и латентном течении внутриклеточных персистирующих инфекций, составившего 18,34 ± 7,82 нг/мл и 10,51 ± 3,34 нг/мл соответственно, было выявлено их статистически значимое различие (p < 0,001). Показатель данного цитокина при активном течении инфекции у детей І группы значимо отличался от показателей группы сравнения (p < 0,001). В случае латентного течения инфекции у пациентов основной группы статистически значимого различия с показателями детей группы сравнения выявлено не было (р = 0,952).
Таким образом, повышенные концентрации TGFβ-1 связаны с прогрессированием фиброза и ремоделированием дыхательных путей у пациентов с бронхиальной астмой, наблюдаемые у наших пациентов. Инфицирование внутриклеточными инфекциями усугубляет этот процесс, особенно в случае активного течения инфекции.
Противовоспалительная активность TGFβ-1 проявляется в супрессии продукции провоспалительных цитокинов, ингибировании активности макрофагов и клеточного деления Т- и В-лимфоцитов и активизации пролиферации фибробластов. Поэтому гиперпродукция TGFβ-1, особенно в основной группе детей, при активном течении инфекционного процесса, обусловлено снижением активации клеток иммунной системы, направленных на ограничение воспалительной реакции, что приводит к поддержанию хронического воспаления и замыкает круг патологических процессов, происходящих в дыхательных путях.
Учитывая тот факт, что в легкие попадает значительное количество патогенов, в том числе и внутриклеточных персистирующих инфекционных агентов, происходит как активация механизмов врожденного иммунитета, так и развитие хронического воспаления, впоследствии приводящего к процессам фиброза, участие в которых принимает TGFβ-1.
Изменения сосудов при бронхиальной астме включают ангиогенез, расширение сосудов, микроваскулярную проницаемость, продукцию факторов роста, адгезию клеток, трансмиграцию и фильтрацию, увеличение кровотока вследствие расширения резистентных артерий и увеличение количества сосудов, коррелирующие со степенью тяжести заболевания [11]. Однако существуют биологически активные вещества, способные вызывать сужение сосудов. К ним относится эндотелин-1, который является наиболее мощным вазоконстриктором и продуцируется сосудистым эндотелием в дыхательных путях при бронхиальной астме под действием ФНО-α. Действие эндотелина-1 многогранно и заключается в способности вызывать бронхоконстрикцию, усиливать реакцию бронхов на ингалируемые антигены, увеличивать приток воспалительных клеток, продукцию цитокинов, участвовать в формировании отека и в процессах ремоделирования дыхательных путей, ускорять хемотаксис, адгезию и активацию нейтрофилов, стимулировать развитие фиброза субэпителиального слоя стенки бронхов и образование хемоаттрактанта для лейкоцитов [11]. Исследования выявили увеличение выработки эндотелина-1 при воспалении, развивающемся при бронхиальной астме, его хронизации, повышении выраженности обструкции дыхательных путей под действием данного пептида [11].
При обследовании наблюдаемых нами детей было выявлено, что уровень эндотелина-1 был статистически значимо выше (p < 0,001) в сыворотке крови детей, больных бронхиальной астмой, как инфицированных, так и не инфицированных внутриклеточными инфекциями, по сравнению со здоровыми детьми. Статистически значимого различия в показателях детей основной группы и группы сравнения выявлено не было (р = 0,147). При активном и латентном течении внутриклеточных персистирующих инфекций показатели эндотелина-1 были практически одинаковыми.
Показателем, определяющим прогноз при бронхолегочной патологии у детей, является уровень аутоантител к коллагену ІІІ типа. В результате хронического воспаления, лежащего в основе ремоделирования дыхательных путей при бронхиальной астме, формируется субэндотелиальный фиброз вследствие нарушения обмена коллагена аутоиммунного характера. Уже на ранних стадиях воспаления можно выявить в интерстиции легких накопление всех типов коллагена с преобладанием коллагена ІІІ типа [13]. До настоящего времени изучение в сыворотке крови уровня аутоантител к коллагену ІІІ типа при бронхиальной астме у детей не проводилось. Данный иммунохимический тест имеет высокую информативность, диагностическую и прогностическую значимость, характеризует воспалительную реакцию на всех ее этапах, в том числе и на ранних, и свидетельствует о ремоделировании дыхательных путей, вызванном дезорганизацией коллагеновых волокон.
В ходе обследования детей с бронхиальной астмой было выявлено, что в основной группе детей и в группе сравнения отмечалось статистически значимое (p < 0,001) повышение уровня аутоантител к коллагену ІІІ типа по сравнению с группой практически здоровых детей. При этом статистическая разница (p < 0,001) отмечалась и среди пациентов из основной группы и группы сравнения, что указывает на влияние внутриклеточного инфицирования на усугубление субэпителиального фиброза у пациентов с бронхиальной астмой. Превалирование показателей при активном течении инфекционного процесса над показателями, определяемыми при латентном течении, также были статистически различны (р = 0,005).
Повышение уровня аутоантител к коллагену ІІІ типа при бронхиальной астме у детей, протекающей на фоне различного течения инфекционного процесса, вызванного внутриклеточными возбудителями и без инфицирования, свидетельствует о дез–организации коллагеновых структур, особенно при активном течении инфекции.
Выявленное влияние длительной персистенции в организме герпесвирусных, хламидофильной и микоплазменной инфекций на процессы ремоделирования дыхательных путей при бронхиальной астме у детей вызывает необходимость разработать новые схемы лечения и усовершенствовать базисную терапию с целью повышения качества жизни ребенка благодаря постоянному контролю над симптомами заболевания, снижения инвалидизации и смертности.
Пациентам основной группы — детям с бронхиальной астмой, инфицированных внутриклеточными инфекциями: герпесвирусными, вызванными вирусом простого герпеса І–ІІ типов, цитомегаловирусной, Эпштейна — Барр-вирусной, в частности, при активной стадии инфекционного процесса стадии, наряду с базисной терапией, включающей ингаляционные кортикостероиды в возрастных дозировках, соответствующих степени тяжести заболевания и бронхолитической терапии (ингаляции β2-агонистов), были включены ациклические (атипичные) нуклеозиды, в частности ацикловир. Доза препарата составила по 100 мг 5 раз в сутки у детей до 2 лет и по 200 мг 5 раз в сутки у детей старше 2 лет в течение 10 дней при острой первичной инфекции и 14 дней при ее рецидивирующем течении.
Выбор препарата ацикловир был обусловлен наличием определенных характеристик, таких как высокая биодоступность, специфичность противовирусного действия, отсутствие канцерогенного действия, способность взаимодействовать только с внутриклеточными включениями-мишенями (вирионами), отсутствие повреждающего влияния на здоровые клетки, хорошее выведение из организма, отсутствие общетоксических свойств, что немаловажно для развивающегося детского организма.
Пациентам основной группы — детям с бронхиальной астмой, инфицированным внутриклеточными инфекциями, протекающими на фоне активной хламидофильной, вызванной Сhlamydophila pneumoniae, и микоплазменной — Mycoplasma pneumoniaе, назначались антибиотики из группы макролидов, в частности азитромицин в возрастной дозировке 10 мг/кг 1 раз в сутки в течение 10 дней при острой первичной инфекции и 14 дней при ее рецидивирующем течении.
Кроме антибактериального эффекта, данная группа антибиотиков обладает противовоспалительным действием за счет ингибирования «окислительного взрыва», кроме того, они способны модулировать цитокиновые реакции, угнетая выработку провоспалительных цитокинов и стимулируя противовоспалительные; снижают образование медиаторов воспаления — простагландинов, лейкотриенов и тромбоксанов. Причем противовоспалительное действие проявляется даже при субтерапевтических концентрациях антибиотиков данной группы и сравнимо с эффектом нестероидных противовоспалительных средств [4]. Еще одной особенностью макролидов является их стимулирующее влияние на фагоцитоз, что происходит за счет их накопления в нейтрофилах и макрофагах, приводящее к усилению фагоцитарной активности и миграции в очаг воспаления. Благодаря способности повышать активность Т-киллеров антибиотики данной группы обладают и иммуномодулирующим действием [5].
Рост резистентности герпесвирусов к действию ациклических нуклеозидов значимо ухудшает эффективность терапии, особенно при рецидивирующем течении инфекции и длительном проведении супрессивной противовирусной терапии [17].
В связи с этим в качестве этиотропной терапии широкое распространение получили флавоноиды, обладающие мощным противовирусным действием, которые используются для подавления размножения герпесвирусов.
Противовирусный препарат, содержащий флавоноиды (протефлазид), разработанный в Украине, как высокоэффективное противогерпетическое средство используется в нашей стране и за рубежом в течение более десяти лет [7].
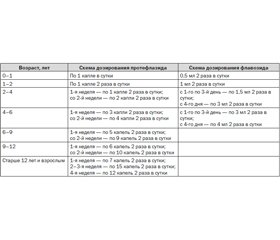
Для детей раннего возраста применяют 2% бесспиртовый раствор препарата флавозид, который может назначаться с рождения. Он не содержит красителей, ароматизаторов, сахара, нетоксичен, хорошо переносится детьми с отягощенным аллергологическим анамнезом [1, 7].
Схема назначения протефлазида (флавозида) представлена в табл. 3. Протефлазид назначали за 15–20 минут до еды с небольшим количеством воды (1–2 столовые ложки) комнатной температуры, флавозид — за 20–30 мин до еды.
Учитывая способность внутриклеточных инфекций влиять на состояние иммунной системы, наличие случаев резистентности к ацикловиру и другим ациклическим нуклеозидам герпесвирусов, что может непосредственно повлиять на течение и исход заболевания, нами в комплекс лечебных мероприятий у наблюдаемых пациентов были включены иммунотропные препараты, в частности интерфероны. Широкий спектр физиологических функций интерферонов (противовирусная, радиопротективная, антипролиферативная и иммуномодулирующая) свидетельствует об их контрольно-регуляторной роли в сохранении гомеостаза.
В результате влияния внутриклеточных персистирующих инфекций на состояние иммунной системы, девиации иммунного ответа в сторону активации клона Т-хелперов второго типа, угнетения клона Т-хелперов первого типа, изменения функционирования системы интерферонов, отрицательной динамики уровней IFN-α в сыворотке крови в комплекс лечения детей основной группы был включен препарат рекомбинантного α2β-интерферона виферон, содержащий 150 000 МЕ интерферона. Назначался детям в возрасте до 7 лет. У детей старше 7 лет использовали виферон, содержащий 500 000 МЕ интерферона. Применялся препарат в виде ректальных свечей два раза в сутки 10 дней ежедневно при острой первичной инфекции. При активном рецидивирующем течении внутриклеточной инфекции препарат назначался в той же дозировке тремя десятидневными циклами с десятидневными интервалами 1–2 раза в год. При латентном течении — по 10 дней 2 раза в год [6].
Таким образом, проведенные исследования выявили влияние персистирующих внутриклеточных инфекций, в частности, цитомегаловирусной, вызванной вирусом простого герпеса І/ІІ типов, вирусом Эпштейна — Барр, Сhlamydophila pneumoniae и Mycoplasma pneumoniaе, особенно при активном их течении, на процессы ремоделирования дыхательных путей при бронхиальной астме. Полученные результаты вызвали необходимость проведения наряду с базисной терапией заболевания этиопатогенетического лечения, в частности, назначение ациклических нуклеозидов или макролидов в зависимости от диагностированной инфекции, иммуномодуляторов и α2β-интерферона с целью уменьшения процессов ремоделирования дыхательных путей, снижения тяжести заболевания и уменьшения инвалидизации.
Список литературы
1. Абатуров О.Є. Імунотропний ефект фітопрепарату «Флавозід®» / О.Є. Абатуров, І.Л. Височина // Современная педиатрия. — 2008. — № 4(21). — С. 99-102.
2. Антипкін Ю.Г., Надточій Т.Г. Сучасні погляди на етіопатогенез, клініко-діагностичні та лікувально-профілактичні особливості перебігу запального процессу при неспецифічних захворюваннях органів дихання у дітей (огляд літератури) // Перинатология и педиатрия. — 2011. — № 1(45). — С. 19-23.
3. Бронхиальная астма: современные концепции диагностики и лечения. Научно-информационный материал. — М., 2011. — 127 с.
4. Веселов А.В. Азитромицин: современные аспекты клинического применения / А.В. Веселов, Р.С. Козлов // Клиническая микробиология и антибикробная химиотерапия. — 2006. — Т. 8, № 1. — С. 18-32.
5. Гадецька С.Г. Особливості перебігу і терапії бронхіальної астми у дітей з респіраторним хламідіозом: Автореф. дис... канд. мед. наук: 14.01.10 / С.Г. Гадецька, 2006. — 20 с.
6. Зайцева С.В., Зайцева О.В. Бронхиальная астма у детей: пути оптимизации терапии // Eлектронний ресурс: http://www.osp.ru/doctor/2001/08/036_print.htm
7. Знаменська Т.К. Лікування герпесвірусних інфекцій (цитомегаловірусної, неонатального герпесу) у дітей першого року життя із застосуванням препарату Флавозід / Т.К. Знаменська, А.О. Писарєв // Здоровье женщины. — 2009. — № 4(40). — С. 60-61.
8. Мироманова Н.А., Жамсуева Д.Р. Значение матриксных металлопротеаз и трансформирующего фактора роста-β1 в развитии осложненных форм гриппа у детей // Врач-аспирант. — 2013. — № 5(60). — С. 16-22.
9. Невзорова В.А., Тилик Т.В., Гилифанов Е.А., Панченко Е.А., Вахрушева С.Е., Тилик В.В. Роль матриксных металлопротеиназ в формировании морфофункционального дисбаланса воздухоносных путей при хронической обструктивной болезни легких // Тихоокеанский медицинский журнал. — 2011. — № 2. — С. 9-13.
10. Недельская С.Н., Ярцева Д.А. Диагностика бронхиальной астмы у детей раннего возраста: возможности, проблемные вопросы, дифференциальная диагностика // Здоровье ребенка. — 2013. — № 2(45). — С. 26-32.
11. Ненартович И.А., Жерносек В.Ф. Ремоделирование бронхов при бронхиальной астме и возможности его коррекции // Рецепт. — 2010. — № 3(71). — С. 77-89.
12. Рукина Д.А., Догадова Л.П., Маркелова Е.В., Абдуллин Е.А., Осыховский А.Л., Хохлова А.С. Иммунологические аспекты патогенеза первичной открытоугольной глаукомы // Русский медицинский журнал. — 2011. — № 4. — С. 162-164.
13. Стройкова Т.Р. Клинико-диагностическое значение аутоантител к коллагену III типа при бронхолегочных заболеваниях у детей: Автореф. дис… на соискание ученой степени кандидата медицинских наук. — Астрахань, 2009. — 20 с.
14. Уманець Т.Р. Клініко-анамнестичні особливості фенотипів бронхіальної астми у дітей // Перинатология и педиатрия. — 2011. — № 2(46). — С. 69-71.
15. Doğu F., Yildiran A., Loğlu D. Serum transforming growth factor-β (TGF-β), matrix metalloproteinase-2 (MMP-2), matrix metalloproteinase-9 (MMP-9) and tissue inhibitors of metalloproteinase (TIMP-1) levels in childhood asthma // Turk. J. Med. Sci. — 2008. — № 38(5). — Р. 415-419.
16. Doherty G.M., Kamath S.V., Courcey F., Christie S.N., Chisakuta A., Lyons J.D. Children with stable asthma have reduced airway matrix metalloproteinase-9 and matrix metalloproteinase-9/tissue inhibitor of metalloproteinase-1 ratio // Clin. Exp. Allergy. — 2005. — № 35(9). — Р. 1168-74.
17. Doward L.C. et al. The development of the herpes symptom checklist and the herpes outbreak impact Questionnaire // Value in Health. — 2009. — Vol. 12(1). — Р. 139-145.
18. Fixman E.D., Stewart A., Martin J.G. Basic mechanisms of development of airway structural changes in asthma // Eur. Respir. J. — 2007. — Vol. 29. — P. 379-389.
19. Hegazy L., Salwa Abu El Hana. Circulating MMP-9 and TIMP-1 in acute exacerbations and after remission induced by oral corticosteroids in asthmatic children // Egypt J. Pediatr. Allergy Immunol. — 2006. — № 4(1). — Р. 23-29.
20. Jeffery P.K. Remodeling and inflammation of bronchi in asthma and chronic obstructive pulmonary disease // Proc. Am. Thorac. Soc. — 2004. — Vol. 1. — P. 176-183.
21. Kanazawa H. Anticholinergic agents in asthma: chronic bronchodilator therapy, relief of acute severe asthma, reduction of chronic viral inflammation and prevention of airway remodeling // Curr. Opin. Pulm. Med. — 2006. — Vol. 12. — P. 60-67.
22. Kraus-Filarska M., Kosinska M., Tomcowicz A. Metalloproteinases and airway remodeling in asthma // Adv. Clin. Exp. Med. — 2007. — Vol. 16, № 3. — Р. 417-423.
23. Nagai H. Immunopharmacological approach to elucidating the mechanism of allergic inflammation // Allerg. Inter. — 2005. — Vol. 54. — P. 251-261.
24. Oikonomidi S., Kostikas K., Tsilioni I. et al. Matrix metalloproteinases in respiratory diseases: from pathogenesis to potential clinical implications // Cur. Med. Chem. — 2009. — Vol. 16, № 10. — Р. 1214-1228.
25. Pohunek P. Pediatric asthma: how significant it is for the whole life? // Paediatr. Respir. Rev. — 2006. — № 7(Suppl.). — Р. 68-69.

/102.jpg)
/103.jpg)
/106.jpg)