Статтю опубліковано на с. 64-69
Вступ
Безпечні, а також успішні результати будь-якого хірургічного лікування залежать від фактичного знання кожної хірургічної структури відповідного регіону. З розвитком лапароскопічного методу для лікування гриж пахвинної ділянки більше уваги приділяється питанням чистої анатомії. Різниця між переднім (відкрита операція) і заднім (ендоскопічним) доступом при пахвинній герніопластиці визначається різними структурами, які повинні бути ідентифіковані під час виконання операції.
На даний час тотальний екстраперитонеальний (ТЕП) ендоскопічний підхід до усунення первинних, двосторонніх, рецидивних пахвинних, стегнових і затульних гриж — найбільш поширених випинань черевної стінки є найбільш обґрунтованим методом лікування. Процедура ТЕП-пластики включає в себе введення ендоскопа в передочеревинний простір Retzius і Bogros після створення за допомогою спеціального балона зони для інсуфляції газу без входження у черевну порожнину. Виконання успішної ТЕП-пластики вимагає досконального знання анатомії таза і пахвинної ділянки, яку ми бачимо на екрані монітора. Якщо погано підготовлений хірург візуалізує пахвинну ділянку ендоскопічно, то він може загубитися і повністю втратити орієнтири очевидної грижі. Результатом є негайна відмова від лапароскопічної пластики. Ще гірше, якщо хірург починає мобілізацію задньої стінки, але не в змозі правильно визначити анатомічні структури, це призводить до травм судин, нервів або внутрішніх органів. За даними літератури, травма кровоносних судин черевної стінки відбувається в 0,2–2 % лапароскопічних операцій [1, 2]. Формування сером або гематом після ТЕП-пластики зустрічається у 2–10 % випадків, що пов’язано з неадекватністю гемостазу і контролем венозної кровотечі під зниженим тиском. 90 % сером зникають самостійно, але 10 % потребують подальшого лікування [1, 3]. Цих ускладнень можна уникнути майже у всіх випадках, розуміючи нормальну анатомію.
Мета: визначити найбільш поширені та важливі елементи судинної анатомії, що призводять до ускладнень під час ТЕП-пластики, і методи запобігання їм.
Матеріал та методи
Було проведено ретроспективний аналіз ретропубікальної лапароскопічної судинної анатомії 32 пацієнтів під час ТЕП-пластики. Усі прооперовані хворі були чоловіками. Середній вік хворих становив 42,9 ± 14,4 року. Усього проведено 25 унілатеральних та 7 білатеральних операцій — 39 гриж, серед яких: 27 косих, 10 прямих пахвинних та 2 стегнові грижі. ТЕП-пластика виконувалася за стандартною технікою з використанням трьох портів, розташованих по серединній лінії нижче від пупка. У цей же період було проведено макроморфометричне дослідження судинної анатомії пахвинної ділянки та передочеревинного простору Retzius та Bogros 17 нефіксованих трупів (всього 34 тазові половини), 15 чоловіків та 2 жінки. Середній вік трупів становив 49,1 ± 13,1 року. Для проведення анатомічного аналізу білатерально у проекції пахвинної зв’язки розсікали шкіру, поверхневу фасцію, передню стінку пахвинного каналу та саму пахвинну зв’язку над стегновою артерією. Виділяли всі гілки зовнішніх клубових судин (ЗКС) на цьому рівні. Потім виконували черезшкірний доступ до ретропубікального простору нижче від пупка без розкриття очеревини і виділяли всі судини у просторі Retzius та Bogros.
Статистичні дані наведено у вигляді середнього зі стандартним відхиленням, а також у вигляді медіани з міжквартильним інтервалом.
Результати та обговорення
Кровотеча може статися під час будь-якої операції, але це стає особливою проблемою під час лапароскопічної герніопластики. При трансабдомінальній преперитонеальній (ТАПП) пластиці анатомічні орієнтири більш чіткі, але під час ТЕП-пластики, знаходячись в обмеженому просторі, хірург спирається виключно на знання анатомії, яке базується на інтерпретації існуючого 2D-зображення на моніторі в уявну 3D-модель у свідомості хірурга, щоб уникнути пошкодження судин, що перешкоджає запланованому алгоритму дій у зв’язку з розвитком кровотечі та можливої конверсії або ускладнень у післяопераційному періоді у вигляді гематом. Особливість методики ТЕП-пластики полягає ще у тому, що перед хірургом стоїть завдання якомога менше використовувати коагуляцію під час створення простору для ендопротеза.
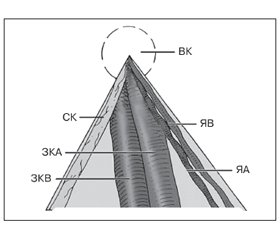
Основними судинами, які можуть створити проблему під час ТЕП-пластики, є ЗКС, нижні епігастральні судини (НЕС), судини сім’яного канатика, м’язові гілки та судини над лобковою дугою (у тому числі судини corona mortis) [1, 2]. Анатомію цих судин та лапароскопічну техніку зупинки кровотечі ми і розглянемо в цій статті. Всі вказані судини знаходяться у судинному просторі, що утворений 2 пластинками поперечної фасції. Між задньою пластинкою поперечної фасції та очеревиною розташований справжній передочеревинний аваскулярний робочий простір для ТЕП-пластики — простір Bogros та медіальніше — простір Retzius. На рисунку 1 наведено схематичне розташування артеріального (рис. 1А) та венозного (рис. 1В) русла ретропубікального заочеревинного простору.
/65.jpg)
Розташування НЕС може варіювати, і їх пошкодження є найбільш поширеною причиною кровотечі під час ТЕП-пластики. По-перше, щоб уникнути травм під час встановлення троакарів, необхідно чітко утримуватись серединної лінії або залишитися достатньо латерально від країв прямих м’язів, при бічному підході розташування троакарів. За нашими даними, що збігаються з даними літератури, треба уникати зони від 4 до 8 см від серединної лінії [2]. Треба мати на увазі, що пацієнт може втратити велику кількість крові, якщо негайно не зупинити кровотечу з цих судин. Якщо після введення троакара виявляється кровотеча, можна використати U-подібні шви з проведенням лігатури за допомогою порожнистої пункційної голки. В 1-му подібному випадку (1/32; 3,1 %) прошивали судини через усі шари, у тому числі через шкіру, при цьому використовували довгу вигнуту голку з лігатурою. При необхідності після зупинки кровотечі додатково на судини можна накласти ендокліпси. При цьому треба пам’ятати, що артеріальне живлення починається з каудальної частини нижніх епігастральних артерій (НЕА).
При створенні передочеревинного простору за рахунок розширення повітряного балона НЕС можуть бути відтягнуті від черевної стінки, відриваючи дрібні гілки. Якщо під час огляду хірург стикається з темним, кривавим полем зору, особливо після очищення камери, треба негайно збільшити інтенсивність світла і встановити 2 троакари по серединній лінії таким чином, щоб сприяти виявленню джерела кровотечі у позаочеревинному просторі шляхом зміни кута огляду або іригації зацікавленої зони. Кровотеча також розвивається при намаганні усунення надлишку жирової клітковини, що фіксована до НЕС і заважає прямому огляду пахвинних ямок. У нашій групі в 1/39 (2,6 %) випадку було зареєстровано пошкодження таких гілок НЕС під час створення поля зору у лівий простір Bogros, при цьому кровотеча була зупинена електрокоагуляцією.
Візуалізація НЕС — ключовий елемент техніки ТЕП-пластики. Такі орієнтири, як окістя лобкової кістки і зв’язки Купера (білого кольору), допомагають хірургу ідентифікувати «судинний кут», створений зверху НЕС, а знизу зовнішньою клубовою веною (ЗКВ). У випадку стегнової грижі ЗКВ будуть приховані за грижовим мішком, який повинен бути мобілізований, щоб вени могли бути візуалізовано.
Також в ідентифікації НЕС може допомогти знання відстані розташування НЕС від серединної лінії. У нашому дослідженні нефіксованих трупів відстань від серединної лінії до НЕС була статистично однакова з обох боків: на рівні верхнього краю симфіза 7,34 ± 0,24 см та на рівні передніх верхніх клубових остей 5,20 ± 0,37 см. У випадку складних рецидивних або невправлюваних гриж, що можуть маскувати нормальну анатомію, хірург повинен почати мобілізацію з ділянки нормальної анатомії і повільно розширювати зону дисекції, щоб можна було визначити звичні орієнтири.
Для адекватної контралатеральної дисекції передочеревинного простору іпсилатеральні НЕС піднімаються вгору (вперед) за допомогою одного з 5-мм тупих дисекторів, у той час як інший дисектор виділяє простір латерально, що теж може спровокувати кровотечу з НЕС. Кровотеча з дрібних м’язових гілок може відбуватися на 1–2 см латеральніше внутрішнього кільця, якщо хірург випадково мобілізує НЕС з розміщенням сітки перед судинами.
Кровотеча з НЕС також може розвиватися в результаті дисекції грижового мішка. У випадку невправлюваної прямої грижі НЕС можуть бути не візуалізовано до тих пір, поки грижовий мішок не буде мобілізований. Слід зазначити, що не треба виконувати лігування і пересічення прямого мішка, бо верхівка сечового міхура може становити частину грижового мішка і буде ушкоджена. Ідентифікація НЕС при ТЕП-пластиці — ключовий момент операції, тому що це необхідно для визначення грижового мішка косої грижі, який розташований латеральніше судин. Це дуже відрізняє техніку ТЕП-пластики від ТАПП-пластики, при якій НЕС разом з прямою і косою грижами очевидні.
У всіх випадках, як правило, ефективною є 2-ручна техніка контролю кровотечі з НЕС, коли один інструмент стискає судини, а інший використовується для лігування, накладання кліпс або коагуляції.
Глибокі огинальні судини клубової кістки (рис. 1) відходять від латерального півкола ЗКС глибше і дещо краніальніше від нижнього краю клубоволобкового тракту, на тому ж рівні або дистальніше початку НЕС. Тому пошкодження цих судин під час ТЕП-пластики малоймовірно.
Зона між сім’явиносною протокою верхньомедіально і тестикулярними судинами супралатерально є так званим «трикутником смерті». Це місце розташування зовнішніх клубових судин (рис. 2).
/66.jpg)
Кровотеча із ЗКC є небезпечним для життя ускладненням [1, 2]. Травма цих судин може відбутися на будь-якій стадії операції після початку мобілізації грижового мішка. Якщо діагностовано кровотечу із ЗКВ, вена повинна бути негайно стиснена для зупинки кровотечі і запобігання емболії СО2. Як варіант може бути встановлений третій порт для лігування отвору у вені, але в обмеженому просторі для кращого визначення місця кровотечі оптимальним є перехід на відкриту операцію. Рішення про конверсію має бути прийнято швидко, якщо кровотечу не вдається зупинити лапароскопічно, але при переході на відкритий доступ необхідно підтримувати стиснення ділянки кровотечі лапароскопічним інструментом. Пошкодження зовнішньої клубової артерії менш ймовірне у зв’язку з її більш міцною стінкою та латеральним розташуванням. Проте техніка зупинки кровотечі є аналогічною. Загальновідомим є той факт, що накладання швів або кліпс, неконтрольована монополярна коагуляція у зоні цього трикутника неприпустимі.
Вінець смерті — corona mortis (CM) являє собою виражений анастомоз між затульними та нижніми епігастральними судинами (рис. 1А). Наявність судин СМ можна легко визначити за затульним отвором, який є анатомічним орієнтиром, що вказує на достатню нижню межу мобілізації передочеревинного простору при ТЕП-пластиці. Пошкодження СМ реєструються у 1,5–2 % і трапляються найчастіше під час мобілізації у зоні зв’язки Купера або фіксації протеза до неї, при цьому судинні структури, як правило, мають діаметр < 2 мм [4]. Існують термінологічні розбіжності в точному визначенні судин СМ. Аберантною затульною артерією (ЗА) слід називати артерію з незвичайним походженням — не від внутрішньої клубової артерії. З іншого боку, додаткова ЗА — анастомоз з типовою ЗА, й у вузькому розумінні це і є СМ [5]. Але для простоти розуміння всі нетипові значимі судинні елементи (від 1 мм в діаметрі) на рівні верхньої лобкової гілки багатьма авторами називаються СМ [6–8]. Згідно з даними Rusu та ін. [6], вони зустрічаються у 80 % випадків. Автори класифікували морфологічні особливості СМ трьох типів (I–III). І. Артеріальна CM (25 %): I.1. ЗА з ЗКА; I.2. ЗА від НЕА (перші дві — абератна ЗА); I.3. Анастомоз ЗА і НЕА (додаткова ЗА); I.4. Лобкові гілки ЗА, за відсутності будь-яких анастомозів з системою НЕА; II. Венозна CM (15 %): II.1. Затульна вена (ЗВ), що впадає у ЗКВ; II.2. ЗВ відтікає у нижню епігастральну вену (НЕВ); II.3. Венозний анастомоз ЗВ і (НЕВ); III — поєднання артеріальної та венозної CM (40 %). Ми також використовуємо цю класифікацію СМ, що складається з дев’яти різних підтипів, які в основному (але не виключно) відповідають різним комбінаціям типів I і II. Kachlík та ін. [3] провели метааналіз більше 4500 тазових половин. Аберантна ЗА була присутня приблизно у 20 % випадків, а додаткова ЗА — в 5 % випадків. Загальна частота артеріальної СМ, за їх даними, становить приблизно 25 % (з судинами більше ніж 1 мм завширшки). За даними M. Ates та ін. [8], частота CM становить 28,4 %, а будь-яких інших артеріальних структур у цій зоні — 45,0 %.
За даними лапароскопічних ТЕП-операцій А. Pellegrino та ін. [4], CM зустрічалася на правій стороні у 60 %, лівій — у 28 % та у 1,5 % — з двох сторін. CM зареєстрований в 52 % випадків. Найчастіше зустрічалася венозна СМ — у 46 %, а потім комбінована венозна й артеріальна, і лише у 8 % — артеріальна СМ. В одному випадку комбінованої СМ була виявлена одна артерія і дві вени. Автори вважають артеріальну СМ діаметром ≥ 2 мм вираженою та < 2 мм — тонкою.
У всіх випадках нашого анатомічного дослідження трупів ми виявляли венозні варіанти СМ між ЗКВ та ЗВ, діаметр цих комунікантних вен становив 2,7 (1,7–4,3) мм. Вони мали вертикальний напрямок до нижньої границі верхньої лобкової гілки до рівня затульного отвору. У 24/34 (70,5 %) випадках типова ЗА мала комунікантну гілку з лобковою гілкою НЕА (рис. 3А), діаметр цієї гілки становив 0,87 (0,5–1,5) мм, у 3/34 (8,8 %) ЗА не мали типового початку від внутрішньої клубової артерії: в 1 випадку — від ЗКА та у 2 — від НЕА (рис. 3В). Хід судин був вертикальний від верхньої лобкової гілки до входу в затульний канал, діаметр аберантної ЗА був 2,1 (2,0–2,3) мм, причому в усіх випадках артерію супроводжувала одна ЗВ діаметром 2,9 (2,7–3,0) мм. В інших випадках артеріальні комунікантні гілки не були виявлені. Середня відстань від комунікантної гілки до тіла симфіза становила 41,1 (33,5–53,5) мм. Венозна дуга над верхньою лобковою гілкою визначалась в усіх випадках в безпосередній близькості від лакунарної зв’язки, але діаметр вен рідко перевищує 1 мм, що не має важливого клінічного значення.
/67.jpg)
Під час ТЕП-пластики тільки у 20/39 (51,3 %) випадках ми визначали анастомоз між НЕА та ЗА, причому діаметр його був меншим, ніж ми виявили у трупів — 0,67 (0,5–1,1) мм. Та лише у 10/39 (25,6 %) тазових половин ми візуалізували чіткі венозні судини, але всі менше ніж 2,0 мм у діаметрі. Менший діаметр судин та зменшення частоти візуалізації вен ми пов’язуємо зі створенням робочої зони підвищеного тиску від 10 до 15 мм рт.ст. Тому дійшли висновку, що узгоджується з даними літератури [3], що венозні структури зони СМ візуалізуються тільки в умовах низького тиску, що необхідно враховувати перед встановленням протеза — зменшити тиск для проведення коагуляції при кровотечі з венозних судин.
Як відомо, кровопостачання сім’яного канатика, яєчка та над’яєчка здійснюється яєчковою та артерією сім’явиносної протоки, які пов’язані між собою дрібними колатералями. Венозна система сформована з лозоподібного сплетення, що переходить у яєчкові вени, та сплетення сім’явиносної протоки. Під час проведення дисекції очеревини над внутрішнім пахвинним кільцем і латеральніше очеревина, як правило, легко відшаровується від сім’яного канатика. Необережна дисекція структур сім’яного канатика може також викликати кровотечу з вищевказаних судин, що може сприяти утворенню гематоми і потенційно спричинити орхіт або атрофію яєчка. Якщо мішок занадто довгий або фіксований до сім’яних судин і сім’явиносної протоки, він може бути розкритий від бічної до присередньої стінки, і таким чином структури сім’яного канатика, у тому числі судини, добре візуалізуються через нижню стінку мішка. Притискання зазвичай зупиняє кровотечу, і діатермія в цьому випадку не завжди потрібна.
Висновки
На жаль, неможливо повністю усунути ускладнення після лапароскопічної герніопластики, але можливо зменшити їх частоту. Досконале знання анатомії та хірургічного доступу, поряд із досконалими лапароскопічними навичками, знижує ймовірність серйозних ускладнень.
У випадку складних рецидивних або невправимих гриж, що можуть маскувати нормальну анатомію, хірург повинен почати мобілізацію з ділянки нормальної анатомії і повільно розширяти зону дисекції, щоб можна було визначити звичні орієнтири. Слід враховувати, що використання балону для дисекції при рецидивних грижах часто призводить до розриву судин та очеревини, тому його використання у таких випадках є обмеженим. Візуалізація НЕС — ключовий елемент техніки ТЕП-пластики, їх чітка ідентифікація сприяє успішному виконанню операції і зменшує ризик розвитку кровотечі.
Вени у зоні лобкової дуги є постійними для кожного пацієнта, але діаметр їх рідко перевищує 1 мм, що не має важливого клінічного значення. Усвідомлення можливості травми аберантних або додаткових затульних судин (corona mortis) під час дисекції простору Bogros у ділянці верхньої лобкової гілки і фіксації сітки до зв’язки Купера допоможе зменшити ризик кровотечі та подальших ускладнень.
/66.jpg)

/65.jpg)
/67.jpg)