Журнал «Здоровье ребенка» 1 (69) 2016
Вернуться к номеру
Новые подходы относительно повышения морфофункциональной готовности к систематическому школьному обучению детей шестилетнего возраста с железодефицитными состояниями
Авторы: Мокия-Сербина С.А., Чечель В.В. - ГУ «Днепропетровская медицинская академия МЗ Украины», г. Кривой Рог
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Мета: підвищення морфофункціональної готовності до систематичного навчання в школі дітей шестирічного віку із залізодефіцитними станами. Пацієнти і методи. У дослідження включено 155 вихованців дитячих дошкільних закладів шестирічного віку із встановленим залізодефіцитним станом і 50 здорових дітей. Пацієнтів розподілили: на основну групу (52 дитини із встановленим латентним дефіцитом заліза і 25 — із залізодефіцитною анемією I ступеня) та групу порівняння (53 дитини з латентним дефіцитом заліза і 25 дітей — із залізодефіцитною анемією I ступеня). Діти із залізодефіцитними станами отримували стандартну феротерапію. В основній групі додатково використовували комбінований препарат багатовекторної дії. Досліджувалися показники: антропометричні (зріст, вага, окружність грудної клітки), дрібна моторика рук, біологічні (зміна молочних зубів, відношення окружності голови до довжини тіла, ступінь окостеніння скелета лівої руки). Результати. Під впливом комбінованої терапії антропометричні показники та дрібна моторика рук відновлювалися до рівня здорових дітей вірогідно швидше. Параметри біологічного розвитку поліпшувалися в порівнюваних групах без статистичної різниці. Висновки. Доповнення феротерапії багатокомпонентним препаратом у дітей шестирічного віку із залізодефіцитними станами сприяє підвищенню їх морфофункціональної готовності до систематичного шкільного навчання.
Цель: повышение морфофункциональной готовности к систематическому обучению в школе детей шестилетнего возраста с железодефицитными состояниями. Пациенты и методы. В исследование включено 155 воспитанников детских дошкольных учреждений шестилетнего возраста с установленным железодефицитным состоянием и 50 здоровых детей. Пациентов разделили: на основную группу (52 ребенка с установленным латентным дефицитом железа и 25 — с железодефицитной анемией I степени) и группу сравнения (53 ребенка с латентным дефицитом железа и 25 — с железодефицитной анемией I степени). Дети с железодефицитными состояниями получали стандартную ферротерапию. В основной группе дополнительно использовали комбинированный препарат мультивекторного действия. Исследовались показатели: антропометрические (рост, вес, окружность грудной клетки), мелкая моторика рук, биологические (смена молочных зубов, отношение окружности головы к длине тела, степень окостенения скелета левой руки). Результаты. Под влиянием комбинированной терапии антропометрические показатели и мелкая моторика рук восстанавливались до уровня здоровых детей достоверно быстрее. Параметры биологического развития улучшались в сравниваемых группах без статистической разницы. Выводы. Дополнение ферротерапии многокомпонентным препаратом у детей шестилетнего возраста с железодефицитными состояниями способствует повышению их морфофункциональной готовности к систематическому школьному обучению.
Objective: to increase morpho-functional readiness for systematic school training of six-year old children with iron deficiency. Materials and methods. The study included 155 six-year old children in preschools with diagnosed iron deficiency and 50 healthy children. Patients were randomized into the basic group (52 children with established latent iron deficiency and 25 persons with iron deficiency anemia I degree) and comparison group (53 children with latent iron deficiency and 25 children with iron deficiency anemia I degree). Children with iron deficiency received standard iron therapy. In the basic group combined drug with multicomponent action was additionally used. There were studied such parameters as anthropometric (height, weight, chest perimeter), fine motor skills of hands, biological (change of first teeth, the ratio of the circumference of the head to the body length, the degree of ossification of the left hand skeleton). Results. Under the combined therapy anthropometric parameters and fine motor hand skills restored to the level of healthy children reliably faster. Parameters ofbiological development improved in both groups with no statistical difference. Conclusions. Iron therapy supplied by multi-component drug in six-year old children with iron deficiency enhances their morpho-functional readiness for systematic school training.
діти, залізодефіцитні стани, морфофункціональний розвиток.
дети, железодефицитные состояния, морфофункциональное развитие.
children, iron deficiency, morpho-functional development.
Статтю опубліковано на с. 25-29
Вступ
Матеріали та методи дослідження
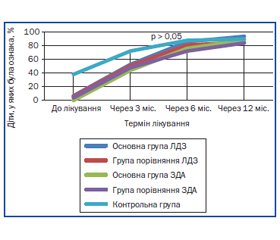
Результати досліджень та їх обговорення
/28.jpg)
Висновки
1. Захарова И.Н. Коррекция дефицита железа: исторические и современные аспекты / И.Н. Захарова, Е.Б. Мачнева // Современная педиатрия. — 2014. — № 8(64). — С. 44-48.
2. Кулакова Е.В. Особенности физического развития детей школьного возраста, воспитывающихся в социально-реабилитационных учреждениях и семье / Е.В. Кулакова, Е.С. Богомолова, Н.И. Дернова // Enviroment & Health. — 2013. — № 2. — С. 35-39.
3. Марушко Ю.В. Проблема діагностики і корекції зниженої толерантності до фізичного навантаження у дітей шкільного віку / Ю.В. Марушко, Т.В. Гищак // Современная педиатрия. — 2014. — № 7(63). — С. 34-40.
4. Реброва О.Ю. Статистический анализ медицинских данных. Применение пакета прикладных программ Statistica / О.Ю. Реброва. — М.: Медиа Сфера, 2012. — 312 с.
5. Сироватко О. Визначення готовності дитини до навчання у школі / О. Сироватко, О. Байер // Психолог. — 2003. — № 13(61). — С. 2-46.
6. Сульженко М.Ю. Профілактика залізодефіцитної анемії в дівчаток-підлітків із доклінічними стадіями дефіциту заліза / М.Ю. Сульженко, Н.М. Головченко // Перинатология и педиатрия. — 2013. — № 4(56). — С. 108-110.
7. Фролова Т.В. Клинические преимущества препарата Кардонат в лечении детей с вегетососудистой дистонией / Т.В. Фролова, О.В. Охапкина // Ліки України. — 2011. — № 2(148). — С. 98-102.
8. Целесообразность использования и оценка эффективности препарата Кардонат в лечении диспластикозависимой патологии у детей с нарушением фибрилогенеза / Т.В. Фролова, О.В. Охапкина, Т.В. Терещенкова [и др.] // Ліки України. — 2009. — № 139. — С. 73-76.
9. Чечель В.В. Особливості фізіологічної готовності дітей старшого дошкільного віку з дефіцитом заліза до систематичного шкільного навчання / В.В. Чечель // Медичні перспективи. — 2013. — Т. XVIII, № 3, ч. 2. — С. 266-271.
10. Юлиш Е.И. Что мы знаем о витаминах? / Е.И. Юлиш // Здоровье ребенка. — 2007. — № 2(5). — С. 110-116.
11. Baker R.D. Clinical Report — Diagnosis and prevention of iron deficiency and iron-deficiency anemia in infants and young children (0-3 years of age) / R.D. Baker, F.R. Greer // Pediatrics. — 2010. — Vol. 126(5). — Р. 1040-1050.
12. Growth Pattern in Anemia Children and Adolescents, aged 12–14 years / S. Kamal, M. Erfan, S.M. Kholoussi [et al.] // J. of American Sciencer. — 2010. — № 6(12). — P. 1636-1646.
13. Iron deficiency anemia: assessment, prevention, and control. A guide for programme managers. — Geneva, World Health Organization, 2001.
14. Role of carnitine in disease / Judith L. Flanagan, Peter A. Simmons, Joseph Vehige [et al.] // Nutrition & Metabolism. — 2010. — Vol. 7. — Р. 30.
1. Zakharova I.N., Machneva E.B. [Correction of iron deficiency: background and current aspects]. Sovremennaya pediatriya. 2014; 8: 44 – 48. Russian.
2. Kulakova E.V., Bogomolova E.S., Dernova N.I. [The physical development features of schoolchildren growing up in social rehabilitation institutions and family]. Enviroment&Health. 2013; 2: 35-39. Russian.
3. Marushko Yu.V., Gishchak T.V. [Diagnostic and correction problem of reduced exercise tolerance in school age children]. Sovremennaya pediatriya. 2014; 7: 34 – 40. Ukrainian.
4. Rebrova O.Yu.[ Statistical analysis of medical data. Application programs STATISTICA package cushioning]. Мoskva: Мediasfera; 2003. Russian.
5. Sirovatko O., Bayer O. [Defining child's readiness to learn at school]. Psikholog. 2003; 13(61): 2-46. Ukrainian.
6. Sul'zhenko M.Yu., Golovchenko N.M. [Preventive ferrotherapy at the preclinical stage of iron deficiency in adolescent girls]. Perinatologiya i pediatriya. 2013; 4: 108 – 110. Ukrainian.
7. Frolova T.V., Okhapkina O.V. [Clinical advantages of Cardonat in treatment of children with vascular dystonia]. Lіki Ukraїni. 2011; 2(148): 98-102. Russian.
8. Frolova T.V., Okhapkina O.V., Tereshchenkova I.I., Berus' A.V.[The assessment of therapeutic efficacy of Cardonat for treatment of dysplastic-dependent pathology in children with fibrillogenesis disorders]. Lіki Ukraїni. 2009; 3(139): 73-76. Russian.
9. Chechel' V.V. [Features of physiological readiness to the systematic schooling of senior preschool children with iron deficiency]. Medichnі perspektivi. 2013; 3: 266-271. Ukrainian.
10. Yulish E.I. [What we know about vitamins?] Zdorov'e rebenka. 2007; 2(5):110-116. Russian.
11. Baker R.D., Greer F.R. Clinical Report – Diagnosis and prevention of iron deficiency and iron-deficiency anemia in infants and young children (0-3 years of age). Pediatrics. 2010; 126 (5): 1040-1050. doi: 10.1542/peds.2010-2576.
12. Kamal S., ErfanM., Kholoussi S.M., Bahgat A.E. Growth Pattern in Anemia Children and Adolescents, aged 12-14 years. J. of American Sciencer. 2010; 6 (12): 1636-1646.
13. Iron deficiency anemia: assessment, prevention, and control. A guide for programme managers. Geneva: World Health Organization; 2001.
14. Flanagan J.L., Simmons P.A., Vehige J., Will M., Garrett Q. Role of carnitine in disease. Nutrition & Metabolism. 2010; 7: 30-0. doi: 10.1186/1743-7075-7-30.

/27_2.jpg)
/27.jpg)