Статтю опубліковано на с. 41-46
Вступ
Наукові уявлення про фізіологічну роль вітаміну D останніми десятиріччями значно поповнилися новими відомостями, що дозволило переглянути погляди на можливість застосування цього вітаміну не лише як регулятора кісткового метаболізму, а й для запобігання розвитку багатьох хвороб, зважаючи на велику кількість позаскелетних ефектів вітаміну D, його багатогранну системну дію на організм [1, 2]. Недостатність або дефіцит холекальциферолу в організмі розглядається як предиктор розвитку багатьох хронічних захворювань, таких як деякі види злоякісних пухлин, автоімунних порушень, цукрового діабету, метаболічного синдрому, артеріальної гіпертензії, атеросклерозу, інфаркту міокарда, ішемічного інсульту, інших хвороб серцево-судинної системи, когнітивних порушень, а також інфекцій внаслідок розвитку вторинних імунодефіцитних станів [4–9].
Передумовою щодо впливу регулюючих властивостей вітаміну D на імунну відповідь стало вивчення на початку 80-років минулого сторіччя рецепторів гена вітаміну D (VDR) у моноцитах крові, а також на активованих Т- і В-лімфоцитах. Крім того, було показано, що на макрофагах експресується фермент CYP27B1, завдяки якому вищевказані клітини мають здатність самі синтезувати 1,25-діоксихолекальциферол (1,25(ОН)2D) з транспортної форми 25-гідрохолекальциферолу (25(ОН)D) [10]. Це стало підґрунтям для вивчення ролі вітаміну D у функціонуванні імунної системи людини.
Було доведено, що гормонально активна форма вітаміну D (1,25(ОН)2D) сприяє диференціації мієлоїдної стовбурової клітини в бік зрілих гранулоцитів, лімфоцитів, моноцитів (макрофагів), що призводить до посилення клітинного імунітету та фагоцитозу. Зрілі макрофаги, активовані g-інтерфероном, здатні синтезувати з 25(ОН)D гормонально активну форму вітаміну D — 1,25(ОН)2D [4].
Поряд із впливом на клітини-попередники мієлоїдного ряду 1,25(ОН)2D взаємодіє зі зрілими моноцитами/макрофагами, що сприяє збільшенню продукції останніми ІЛ-1 та інгібуванню ІЛ-2. Це сприяє проліферації активованих антигеном Т- та В-лімфоцитів, регуляції синтезу імуноглобулінів. Крім того, встановлено, що вітамін D стимулює NK-клітинну активність, що сприяє підвищенню противірусного захисту організму дитини [11].
Причому вплив 1,25(ОН)2D на вказані процеси має дозозалежний ефект. За відсутності або дефіциту вітаміну D в організмі відбувається затримка дозрівання лімфоцитів на стадії лімфобластів, від чого значно страждають процеси імунної відповіді на антигенні подразники. Підтвердженням значущості вітаміну D в імунній регуляції є результати численних експериментальних і клінічних досліджень, що демонструють зв’язок між низькими рівнями вітаміну D і підвищеною сприйнятливістю до різних інфекцій (вірусної, бактеріальної, грибкової етіології), а також до розвитку автоімунної й алергічної патології [12].
Дані, наведені M.C. Magnus et al. (2013), показали, що частота інфекцій нижніх дихальних шляхів у дітей перших трьох років життя (n = 1248) має обернену залежність навіть від рівня 25(ОН)D у сироватці крові їх матерів у періоді вагітності [13]. Необхідно відзначити, що недостатність вітаміну D під час вагітності може сприяти не тільки зниженню імунної відповіді на інфекційні агенти у дітей, але й обумовлювати низькі показники розвитку у них легеневої тканини та зниження їх функціональних характеристик, що також підвищує ризик розвитку інфекцій органів дихання [14].
Маючи на увазі те, що однією з основних функцій вітаміну D є регуляція транспорту кальцію в слизовій оболонці кишечника, ниркових канальцях і кістках, при його дефіциті спостерігається порушення кальцієвого обміну, зниження концентрації цього макроелементу в біологічних рідинах і клітинах, що негативним чином може впливати на активацію імунокомпетентних клітин, яка є кальцій-залежним процесом [15].
При обстеженні школярів України віком 10–17 років виявили, що частота дефіциту вітаміну D становить 88,5 %, недостатність холекальциферолу — 8,9 %, а нормальний рівень за показниками 25(ОН)D3 у сироватці крові реєструється лише у 2,6 %. Аналіз анкет, які заповнювали школярі стосовно їх харчування, показав, що вони не отримували необхідної кількості кальцію та вітаміну D з їжею. Дітям не проводили профілактику дефіциту вітаміну D [15].
Слід зазначити, що у кращому випадку в Україні профілактику дефіциту вітаміну D проводять до року життя дитини.
Сьогодні проблеми, пов’язані з D-гіповітамінозом і порушеннями метаболізму в організмі дитини, зокрема кальцій-фосфорного, залишаються вкрай актуальними.
Слід зазначити, що порушений кальцієвий гомеостаз внаслідок дефіциту вітаміну D найбільш чутливий у періоди інтенсивного росту кісткової тканини: на першому році життя та у періоди першого (5–8 років) та другого (11–18 років) «тяжіння». Саме в ці періоди життя організм дитини потребує надходження вітаміну D, кальцію та мікроелементів, що відіграють активну роль у кальцієвому гомеостазі (магнію, міді, цинку, заліза, кобальту, марганцю) [5].
За результатами досліджень О.М. Лук’янової і співавт. (2006) [16] було встановлено, що у 70 % практично здорових дітей молодшого шкільного віку, які проживали у м. Києві, відзначався знижений рівень кальцію у сироватці крові, у 40 % підвищувалася активність лужної фосфатази за рахунок її кісткового ізоферменту. Вміст 25(ОН)D у всіх обстежених дітей був нижчим за 40 нмоль/л, тоді як при достатній забезпеченості організму цим вітаміном останніми роками його мінімальний рівень повинен становити не менше ніж 75 нмоль/л, максимальний — 150 нмоль/л [8].
В Україні практично відсутні роботи щодо забезпеченості вітаміном D у дітей раннього віку та впливу дефіциту вітаміну D на окремі ланки імунітету. Тому метою роботи було дослідити рівень забезпеченості вітаміном D дітей раннього віку шляхом визначення рівня 25(ОН)D3 у сироватці венозної крові та розробити лікувально-реабілітаційний комплекс для цієї категорії дітей.
Матеріали та методи
У дослідження було включено 60 дітей (28 дівчаток і 32 хлопчики) віком 2–3 роки, які мали часту респіраторну патологію (> 7–8 разів на рік, після початку відвідування дитячого колективу) та 20 здорових дітей такого самого віку, частота респіраторної патології яких становила не більше 2 разів на рік.
У дітей основної та контрольної груп у сироватці венозної крові визначали рівні 25(ОН)D3 за методом радіоконкурентного з’язування після їх екстракції та послідовного хроматографічного розділення в колонках, заповнених окисом алюмінію та сефадексом LH-20 згідно з методом, описаним у літературі [17]. Оцінку D-вітамінного статусу здійснювали відповідно до класифікації M.F. Holick et al. (2011) [4], відповідно до якої дефіцит вітаміну D встановлюється при рівнях 25(ОН)D у сироватці крові нижче за 20 нг/мл (50 нмоль/л), недостатність вітаміну D — при рівнях 25(ОН)D від 20 нг/мл (50 нмоль/л) до 30 нг/мл (75 нмоль/л). Показники 25(ОН)D у сироватці крові дітей від 30 нг/мл (75 нмоль/л) до 50 нг/мл (125 нмоль/л) вважалися нормальними.
З метою оцінки кальцій-фосфорного обміну було вивчено вміст загального кальцію в сироватці та еритроцитах венозної крові за методом D.W. Barron et al. (1957) із застосуванням біотест-наборів «Лахема» (Брно, Чехія); неорганічного фосфору в сироватці та еритроцитах венозної крові — за методом B.C. Dyce et al. (1973); активність лужної фосфатази в сироватці венозної крові — за методом K.S. Motsok et al. (1950) з використанням біотест-наборів фірми «Лахема» (Брно, Чехія).
Для оцінки стану імунної системи дітей використано такі методики:
— лімфоцитарні субпопуляції отриманої свіжої гепаринізованої периферичної крові визначали за методом двокольорової цитофлюориметрії з використанням панелі МКА з набору Immune Monitoring Kit (Becton Dickinson Immunometry Systems, Eremboderm, Бельгія), в яку входять антитіла для виявлення СD45/CD14(Leucogate), IgG1/Ig2 (control), CD/СD19; CD/CD4; CD/CD8; CD-/CD16+CD56+;
— аналіз лімфоцитарних субпопуляцій проводили за допомогою цитофлюориметра FACScan із застосуванням комп’ютерних програм Simul SET і FACScan;
— рівень імуноглобулінів (Ig) G, A, M у сироватці крові та слині визначали за допомогою моноспецифічних сироваток до окремих класів імуноглобулінів виробництва Науково-дослідного інституту епідеміології та мікробіології ім. М.Ф. Гамалеї за методом R. Mancini et al. (1985);
— для визначення секреторного імуноглобуліну А (sIgA) в слині застосовували моноспецифічну сироватку секреторного імуноглобуліну А людини (Науково-дослідний інститут вакцин і сироваток ім. І.І. Мечникова).
Корекцію дефіциту вітаміну D, кальцій-фосфорного обміну та імунних порушень у дітей віком 2–3 роки, які страждали від частих респіраторних захворювань, проводили за розробленим реабілітаційним комплексом, що включав жиророзчинний препарат вітаміну D3 — Вігантол (Vigantol®, виробник Merck KGaA, Німеччина; 1 крапля містить близько 500 МО вітаміну D) по 4000 МО на добу разом із гліцерофосфатом кальцію по 0,25 г тричі на добу впродовж 1 місяця.
Доза препарату вітаміну D3 для дітей віком 2–3 роки була обрана з урахуванням діагностованого дефіциту вітаміну D у цих дітей та відповідала терапевтичній дозі для дітей віком 1–18 років з рівнем 25(ОН)D3 у сироватці крові, нижчим за 20 нг/мл (50 нмоль/л), 3000–5000 МО/д [20].
Після проведеного лікування вітаміном D3 упродовж 1 місяця дітям було запропоновані профілактичні дози холекальциферолу (препарат Вігантол) у дозі 500 МО (1 крапля) 1 раз на добу, з вересня по квітень.
Крім медикаментозної корекції всім дітям був організований раціональний режим доби. Як відомо, режим доби передбачає достатній сон, перебування на свіжому повітрі, своєчасний раціональний прийом їжі, дотримання санітарно-гігієнічних умов життя. Раціональне харчування є одним із головних факторів, що впливають на стан резистентності організму. Тому в раціон дітей включали продукти, що містять підвищену кількість кальцію (молоко, молочнокислі продукти, сир, м’ясо, морську рибу та морепродукти, печінку, гречану та вівсяну каші тощо), вітаміни і різні макро- та мікроелементи (шипшину, яблука, абрикоси, ізюм, курагу, лимони, моркву, помідори, огірки, цибулю, часник, буряк та ін.). Усім дітям призначався також 2-тижневий курс загального масажу, лікувальної фізкультури, водних процедур, що загартовують.
Лікування проводилося на фоні полоскання носа та зіва водним настоєм протизапальних трав (деревій, звіробій).
Дітей обстежували тричі: у листопаді (до лікування), через 3 тижні після проведеного курсу лікування та у квітні.
Математична та статистична обробка була проведена за допомогою Microsoft Excel 2003. При аналізі варіаційних рядів, що відрізнялися за формою від нормального розподілення, використовували непараметричні критерії: χ2 та метод Фішера. У роботі наведені лише вірогідні корелятивні зв’язки (Р < 0,05).
Результати та обговорення
Результати проведеного лабораторного обстеження показали, що у дітей раннього віку, які страждають від частих респіраторних захворювань, уміст у сироватці крові загального кальцію (2,03 ± 0,03 ммоль/л), неорганічного фосфору (1,49 ± 0,02 ммоль/л) істотно знижений, а активність лужної фосфатази (200,0 ± 5,3 Од/л) вірогідно підвищена порівняно з відповідними значеннями у дітей контрольної групи (Са — 2,54 ± 0,05 ммоль/л; Рн — 1,79 ± 0,03 ммоль/л; лужна фосфатаза — 165,2 ± 3,2 Од/л, Р < 0,05 в усіх випадках).
Показники в еритроцитах крові дітей основної групи рівня кальцію (0,21 ± 0,01 ммоль/л) та неорганічного фосфору (2,91 ± 0,03 ммоль/л) були значно зниженими (Са — 0,39 ± 0,03 ммоль/л; Рн — 6,92 ± 0,06 ммоль/л порівняно з дітьми контрольної групи (табл. 1).
На сьогодні відомо, що порушення кальцій-фосфорного гомеостазу знаходиться у прямій кореляційній залежності від забезпеченості організму вітаміном D — 25(ОН)D [18].
У дітей віком 2–3 роки, які страждають від частих респіраторних захворювань, виявляється значне зниження рівнів 25(ОН)D3 в сироватці венозної крові (11,9 ± 0,3 нг/мл), що відповідає дефіциту вітаміну D в організмі, порівняно з показниками 25(ОН)D3 (44,2 ± 3,1 нг/мл, Р < 0,001) у дітей контрольної групи.
Результати аналізу анамнестичних даних дітей з основної та контрольної груп нагляду свідчать про те, що 84,6 % дітей 1-ї групи не споживали морепродуктів, близько 43 % дітей не мали в харчовому раціоні молочних продуктів, упродовж осіннього та зимового періодів діти не отримували полівітамінів, що містять вітамін D, тоді як діти 2-ї групи морепродукти (морську рибу, ікру червону, салати, в які входила морська капуста), молочні продукти споживали у 98,3 % випадків, отримували профілактику гіповітамінозів комплексними вітамінними препаратами з мікроелементами у вікових дозах упродовж осіннього та зимового періодів. Переважна більшість дітей основної групи вела малорухливий спосіб життя: до дитячого садочку їх возили на машинах, мало часу проводили на вулиці, в родинах не займалися спортом, тривалий час діти сиділи за столом, переглядаючи мультфільми. Діти контрольної групи навіть упродовж осіннього та зимового періодів до 2–3 годин проводили на свіжому повітрі, разом з батьками 8 дітей (40 %) відвідували басейн, 7 дітей (35 %) — каток, 3 дитини (15 %) — спортивні танці.
Вивчення показників імунітету в дітей основної групи підтвердило наявність у них порушень клітинного, гуморального та місцевого імунітету різного ступеня тяжкості.
Згідно з отриманими нами даними, в дітей основної групи у періоді поза респіраторною патологією середні показники рівня лейкоцитів, лімфоцитів, CD3+, CD4+CD3+, CD8+CD3+, CD19+-клітин були знижені порівняно з показниками в групі здорових дітей. Причому рівні лейкоцитів, лімфоцитів, CD3+, CD4+CD3+, CD8+CD3+, CD19+-клітин були значно нижчими за нормальні вікові коливання у більшості дітей цієї вікової групи (21 дитина — 70 %). У них же кількість NK-клітин (CD16+CD56+CD3-) мала тенденцію до підвищення (Р < 0,05).
Зниження кількості лейкоцитів, лімфоцитів і CD3+, CD4+CD3+, CD8+CD3+, CD19+-клітин у обстежених дітей викликає настороженість тому, що при такій ситуації в організмі утворюються умови для персистенції вірусів і бактерій, розвитку автоімунних процесів і пухлин.
Підвищення рівня NK-клітин (CD16+CD56+CD3-), які відіграють провідну роль у противірусному та протипухлинному імунітеті, можливо, пов’язано з компенсаторною реакцією організму дитини на постійну персистенцію вірусів, що часто має місце при повторних гострих респіраторних захворюваннях [19].
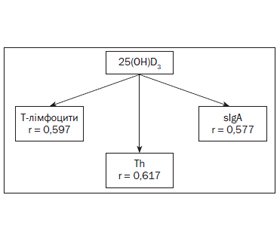
Проведений кореляційний аналіз дозволив встановити наявність вірогідного прямого зв’язку між показниками Т-лімфоцитів, Тh, sIgA в обстежених дітей, з одного боку, та рівнем 25(ОН)D3 у сироватці крові дітей — з іншого (рис. 1). Це дозволяє, певною мірою, говорити про причинний взаємозв’язок між функціональною активністю лімфоцитів, місцевого імунітету слизових оболонок (sIgA) та рівнем 25(ОН)D3 у дітей, які страждають від частих респіраторних захворювань.
Отже, підтверджуються дані літератури про те, що при дефіциті вітаміну D в організмі дітей знижується кількість Т-лімфоцитів, Тh, sIgA, що сприяє формуванню в дітей вторинних імунодефіцитних станів, розвитку частих респіраторних захворювань та їх ускладненого перебігу.
З урахуванням цих досліджень та даних про механізми вторинних порушень імунітету у дітей, які страждають від частих повторних гострих респіраторних вірусних інфекцій (ГРВІ), можна припустити, що до цього патологічного процесу залучені дефіцит вітаміну D і солей кальцію, порушення функціонального стану органів-мішеней для вітаміну D та залоз, що продукують кальцій-тропні гормони.
Маючи на увазі вищевикладене, вважали за доцільне з метою корекції дефіциту вітаміну D та вивчення впливу такої корекції на вторинні імунодефіцитні стани у дітей 2–3-річного віку, які страждають від частих респіраторних захворювань, застосовувати вищенаведений («Матеріали та методи») лікувально-реабілітаційний комплекс.
Слід відзначити, що в жодному випадку застосування розробленого медикаментозного комплексу не було виявлено негативної або побічної дії препаратів. При оцінці ефективності реабілітаційного лікування враховували показники кальцію, неорганічного фосфору в сироватці та еритроцитах венозної крові, активність лужної фосфатази, рівні 25-оксивітаміну D, показники клітинного, гуморального, місцевого імунітету.
Відповідно до поставлених завдань у 60 дітей віком 2–3 роки із частими респіраторними захворюваннями не раніше ніж через 3 тижні після перенесеного останнього гострого патологічного процесу досліджувалися вищезазначені показники, як правило, через 2 доби після закінчення місячного курсу корегуючого медикаментозного лікування. Отримані дані порівнювали з результатами контрольних досліджень, які виконані у 20 здорових дітей раннього віку.
Після лікування у дітей основної групи відзначалося зменшення проявів симптомокомплексу хронічної неспецифічної інтоксикації: зменшилися втомлюваність, пітливість, головний біль, емоційна лабільність, міалгії, артралгії, покращився апетит.
У всіх дітей, які страждали від частих гострих респіраторних захворювань, покращився колір шкіряних покривів, зменшилася блідість шкіри обличчя та синява під очима. Збільшені до розмірів горошини регіональні лімфатичні вузли (задньошийні, підщелепні, пахвинні) після лікування зменшилися та стали більш щільними на дотик. У всіх дітей мало місце покращення стану серцево-судинної та дихальної систем: нормалізувався артеріальний тиск (у 58 дітей (96,7 %) до лікування була тенденція до гіпотонії та тахікардії); частота пульсу та дихання відповідала віковим нормам; за даними електрокардіограми покращилися показники метаболізму в серцевому м’язі.
Результати проведеного лабораторного обстеження показали, що у дітей основної групи вміст загального кальцію, неорганічного фосфору, 25(ОН)D3, активність лужної фосфатази в сироватці крові після лікування практично не відрізнялися від контрольних показників у здорових дітей раннього віку (Р > 0,05).
Виявлено, що підвищення до нормальних рівнів 25-оксихолекальциферолу в крові дітей раннього віку основної групи сприяло нормалізації рівнів кальцію, неорганічного фосфору, активності лужної фосфатази в сироватці крові.
Нормалізація рівнів кальцію та неорганічного фосфору спостерігалася і в еритроцитах крові дітей, які отримали лікування (Р > 0,05) (табл. 1).
Отже, з клінічним покращенням стану здоров’я дітей, які страждали від частих гострих респіраторних захворювань, мала місце нормалізація гомеостазу кальцію та систем його регуляції в організмі дитини.
Цілеспрямоване вивчення стану клітинного гуморального та місцевого імунітету у дітей основної групи після лікування довело, що розроблений комплекс позитивно впливає на показники імунної системи. Зокрема, у дітей, які страждали від частих гострих респіраторних захворювань, після лікування нормалізувалися показники гуморального імунітету, а саме: рівні IgG, IgA, IgM у сироватці крові не відрізнялися від контрольних величин у здорових дітей раннього віку (Р > 0,05).
З огляду на отримані дані комплекс реабілітаційних заходів сприяв позитивному ефекту також на стан клітинної ланки імунітету. Так, у дітей, яким проведено лікування, спостерігалася нормалізація рівня В-лімфоцитів (CD19+) та NK-клітин (CD16+CD56+/CD3–) у венозній крові, їх показники майже не відрізнялися від таких у здорових дітей (Р > 0,05).
Проте рівні лейкоцитів, лімфоцитів, Т-лім-фоцитів та їх субпопуляцій у венозній крові хоча і мали тенденцію до підвищення, але повної нормалізації цих показників імунітету не відбувалося (Р < 0,05).
Вивчення місцевого імунітету в обстежених дітей після лікування показало, що рівні IgA та sIgA в слині підвищилися, але повної нормалізації цих показників місцевого імунітету також не спостерігалося (Р < 0,05).
Отже, на підставі проведених досліджень у дітей раннього віку, які страждають від частих респіраторних захворювань, можна зробити висновок про те, що лікувальний комплекс сприяв зміцненню здоров’я дітей, виражено впливав на нормалізацію кальцієвого гомеостазу та імунних порушень в організмі дитини. Незважаючи на те, що після лікування у дітей основної групи відбулася нормалізація рівня вітаміну D за показниками 25(ОН)D3 в організмі, повної нормалізації клітинного та місцевого імунітету в обстежених дітей не спостерігалося.
Відсутність повної нормалізації показників клітинного та місцевого імунітету в обстежених дітей раннього віку, які страждають від повторних гострих респіраторних захворювань, після одного місяця корегуючого лікування, можливо, крім іншого, пояснюється тим, що вітамін D проявляє свій імуномодулюючий вплив на рівні геному клітин, повільно нормалізуючи обмін речовин в організмі.
Діти основної групи після нормалізації D-вітамінного та кальцій-фосфорного обмінів, тобто після проведення лікувального курсу, продовжували отримувати вітамін D у дозі 1 крапля (500 МО/д) до квітня місяця (профілактична доза вітаміну D для цієї вікової групи). Крім того, всі діти дотримувалися правильно організованого режиму доби, раціонального харчування, виконували лікувальну гімнастику і водні процедури, що загартовували.
Слід зазначити, що від початку першого курсу лікування і до квітня (3-й етап обстеження) минули 4 місяці. За цей період із 60 дітей основної групи захворіло на ГРВІ 12 (20 %) дітей. Причому 6 з них за цей період перенесли ГРВІ 2 рази.
Вивчення стану імунітету у дітей основної групи у квітні показало, що в них відбулася нормалізація показників місцевого та клітинного імунітету. Так, рівні IgA, sIgA в слині та лейкоцитів, лімфоцитів, Т-лімфоцитів та їх субпопуляцій у сироватці крові не відрізнялися від контрольних показників у здорових дітей (Р > 0,05).
Отже, результати клініко-лабораторних досліджень свідчать про те, що дітям раннього віку, які страждають від частих респіраторних захворювань, з метою зміцнення їх здоров’я, нормалізації імунних порушень, кальцієвого гомеостазу можна рекомендувати призначати комплекс реабілітаційного лікування, що включає раціональне харчування, збагачене продуктами, які містять повноцінний білок, вітаміни, мікро- та макроелементи, правильно організований режим, загальний масаж і лікувальну фізкультуру, водні процедури, що загартовують, а також корегуюче медикаментозне лікування — препарати вітаміну D та кальцію.
Висновки
1. Динамічні клінічні спостереження та результати лабораторного обстеження свідчать про те, що одним із механізмів розвитку вторинних імунодефіцитних станів у дітей є дефіцит вітаміну D в організмі.
2. Зважаючи на дані кореляційного аналізу, визначення рівня 25(ОН)D3 у сироватці крові можна використовувати як додатковий критерій порушень в імунній системі у дітей (формування вторинного імунодефіцитного стану).
3. Для корекції дефіциту вітаміну D у дітей раннього віку, які страждають від частих респіраторних захворювань та потребують імунореабілітації, призначення масляного розчину вітаміну D (препарат Вігантол) у терапевтичній дозі 4000 МО/д (при рівні 25(ОН)D3 у сироватці крові < 20 нг/мл) разом із препаратами кальцію у вікових дозах упродовж 1 місяця сприяє нормалізації D-вітамінної забезпеченості організму, кальцій-фосфорного обміну. На показники клітинної та місцевої ланок імунітету препарати вітаміну D та кальцію впливають поступово, нормалізація відбувається при досягненні рівнів 25(ОН)D3 в сироватці крові від 30 нг/мл до 50 нг/мл та при продовженні вживання холекальциферолу у профілактичних дозах 500 МО/д протягом декількох місяців.
4. Для запобігання появі дефіциту вітаміну D, що може супроводжуватись розвитком вторинних імунодефіцитних станів, дітям усіх вікових груп (від народження до 18-літнього віку) рекомендовано вживання масляного розчину вітаміну D у профілактичних дозах («Методичні рекомендації» [20]).
/44.jpg)

/45.jpg)