Статтю опубліковано на с. 5-10
Вступ
За даними Всесвітньої організації охорони здоров’я, від хронічних облітеруючих захворювань артерій нижніх кінцівок страждає 5 % населення земної кулі.
Враховуючи велику кількість випадків захворювання на хронічну ішемію нижніх кінцівок, що зумовлює високий відсоток летальності та інвалідизації пацієнтів, необхідний пошук нових методів лікування цієї хвороби [3, 8].
Критична ішемія нижніх кінцівок є основним показанням до первинної реконструктивної операції, оскільки лише відновлення магістрального кровотоку може зберегти кінцівку та покращити якість життя пацієнтів [2]. Однак результати хірургічної реваскулярізації на сьогодні не можна визнати задовільними. Останніми роками зауважено чітку тенденцію до зростання кількості хворих із мультифокальним ураженням, із незадовільними «шляхами відтоку» та кальцинозом артеріального русла. Виконати пряму реконструкційну операцію в таких умовах можливо лише в 49,5–58 % випадків. У першу чергу це стосується гомілкових сегментів, судинне русло яких не відповідає різко збільшеному об’єму крові, що надходить після реваскулярізації [9]. Відсутність умов для виконання реконструкційної операції при атеросклеротичних оклюзійно-стенотичних ураженнях стегново-підколінно-гомілкового сегмента змушує хірургів розробляти і впроваджувати непрямі хірургічні методи реваскуляризації, спрямовані на покращення колатерального кровообігу, збільшення об’єму мікроциркуляторного русла, стимуляції неоангіогенезу [4, 7].
При виявленні поширеного ураження підколінної артерії та початкових відділів гомілкових артерій перевагу слід вiддавати методам непрямої реваскуляризації, що включає створення в субфасціальному просторі автоекстравазатів, остеотрепанації або відщеплення великогомілкової кістки, пересадку великого чепця, кісткового мозку та стовбурових клітин. Сама ідея непрямих способів реваскуляризації до сьогодні не має чіткого патофізіологічного пояснення та обґрунтування. Складність ситуації полягає в тому, що максимальний ефект після непрямого реваскуляризуючого втручання виникає через 1–6 місяців [4, 8].
Немає однозначної відповіді, при яких стадіях ішемії потрібно використовувати ці втручання, хоча достеменно відомо, що до тяжких ішемічних розладів призводить комбінація порушень гемодинаміки в магістральних артеріях і на рівні мікроциркуляції.
Зрозуміти суть гемодинамічних порушень, що розвиваються при тяжких стадіях артеріальної ішемії, можливо тільки при одночасному дослідженні всіх ланок судинного русла — артеріального, венозного, внутрішньокісткового та мікроциркуляторного [10].
Мета дослідження: оцінити стан периферійного кровообігу, мікроциркуляторного русла, венозної гемодинаміки, внутрішньокісткового тиску в пацієнтів iз хронічною ішемією нижніх кінцівок внаслідок атеросклеротичного ураження артерій на фоні цукрового діабету та ізольованого атеросклеротичного ураження дистального артеріального русла, на основі чого розробити показання до використання непрямих способів реваскуляризації.
Матеріал та методи
Для досягнення поставленої мети обстежено 46 пацієнтів з атеросклеротичним ураженням дистального сегмента артерій нижніх кінцівок зі стадіями ішемії 2б, 3а та 3б, які перебували на стаціонарному лікуванні у відділенні хірургії судин ЗОКЛ ім. А. Новака. Хворі поділені на 2 групи:
— І група (n = 24) — пацієнти з ізольованим атеросклеротичним ураженням артерій нижніх кінцівок (стадія 2б — 5, 3а — 13 та 3б — 6 хворих);
— ІІ група (n = 22) — пацієнти з атеросклеротичним ураженням артерій нижніх кінцівок і цукровим діабетом (стадія 2б — 4 хворі, 3а — 11 і 3б — 7).
Для обстеження застосовували інструментальні методи дослідження: ультразвукову допплерографію, ультразвукове дуплексне сканування (Aloka-3500, Японія; SIM-5000, Радмір; ULTIMA PRO-30, z.one Ultra, ZONARE Medical Systems Inc., США); радіонуклідну ангіографію («Тамара», ГКС-301Т).
Проводилося визначення індексу кісточкового тиску (ІКТ), регіонарного систолічного тиску (РСТ) на підколінній артерії, реологічного індексу (РІ), об’ємного кровотоку (ОК), постоклюзійного венозного тиску (ПОВТ) та внутрішньокісткового тиску (ВКТ) великогомілкової кістки.
Для оцінки порушення периферійного кровообігу ми використовували радіонуклідну ангіографію з
99mТс-альбуміном (недифундуючий радiофармпрепарат (РФП)), що вводили внутрішньовенно, і оцінювали характер кривої надходження та накопичення радіонукліду в гомілках (окремо в проксимальному та дистальному відділах).
Дослідження мікроциркуляторних порушень проведено за допомогою радіонуклідного кліренс-методу, шляхом введення в литкові м’язи 99mТс-пертехнетату з реєстрацією періоду напіввиведення (Т1/2) в секундах.
Результати та обговорення
Встановлено, що час надходження радіонукліду в уражену кінцівку, відображаючи лінійну швидкість кровотоку, при прогресуванні артеріальної недостатності має тенденцію до поступового збільшення (табл. 1). При цьому різниця між надходженням РФП у проксимальні та дистальні відділи гомілки в пацієнтів І групи становила при стадії 2б 0,5 с, а при стадії 3а і 3б — 1,8–2 с; у ІІ групі — 1,8–2 і 7–7,7 с відповідно, що свідчить про більш виражене ураження дистального судинного русла нижніх кінцівок. У середньому в пацієнтів ІІ групи час надходження радіонукліду в дистальні відділи гомілки порівняно з І групою вищий залежно від стадії артеріальної недостатності. У проксимальному відділі гомілки відмічаються аналогічні зміни.
При оцінці кривої часу виходу радіонукліду на Т-плато встановлена наступна закономірність (табл. 2).
/6.jpg)
У дистальному відділі гомілки ураженої кінцівки (що представлена переважно сухожиллями) час насичення тканин РФП на стадії 2б пришвидшено щодо норми в обох групах пацієнтів, що може бути обумовлено незначним об’ємом м’язової тканини в цiй ділянці. У проксимальній частині гомілки об’єм м’язової тканини значно більший, що визначає більш тривале насичення. При артеріальній ішемії, більш вираженій у дистальних відділах ураженої кінцівки, незважаючи на невеликий об’єм м’язової тканини, час початку рівноваги між надходженням та евакуацією радіофармпрепарату значно зростає. Пояснити цей феномен можна з позицій артеріовенозного скиду крові, що призводить до «обкрадання» капілярного русла і, відповідно, до розвитку тяжких порушень мікроциркуляції [10]. Цьому передував етап пришвидшеного кровотоку за рахунок артеріовенозного і артеріоловенулярного скиду крові, ще без вираженого ураження капілярного русла. Подібна закономірність відмічена щодо величини об’ємного кровотоку (табл. 3).
/7.jpg)
В ураженій кінцівці відмічено збільшення ОК у дистальних відділах гомілки при стадії 2б в обох групах пацієнтів (8,8 та 5,8 мл/с відповідно). Привертає увагу також значне зниження ОК у дистальному відділі кінцівки при критичній ішемії (у І групі — 1,8 мл/с, у ІІ — 1,4 мл/с, що в 1,5–2 рази нижче від норми). Якщо це зниження кровотоку достатньо очевидне, то його збільшення при критичній ішемії в проксимальних відділах гомілки (14,3 та 14,7 мл/с відповідно) може носити компенсаторний характер та направлено на збільшення притоку крові в дистальні відділи. На противагу цьому на стадії 2б кровотік дещо пришвидшений у проксимальному відділі гомілки, що може бути обумовлено підвищеним опором току крові на рівні мікроциркуляції. У контралатеральній кінцівці слід відмітити значне збільшення ОК (до 8,2 ± 0,3 мл/с) у дистальному відділі гомілки при критичній ішемії, що, вірогідно, пов’язано з артеріовенозним шунтуванням.
В ураженій кінцівці у хворих зi стадією 2б час виведення радіонукліду із м’язової тканини сповільнено (у І групі — 17,3 ± 2,6 хв, у ІІ групі — 18,5 ± 1,8 хв при нормі 11,0 ± 1,0 хв), що описано в таблицi 4. Однак при більш тяжких стадіях ішемії відбувається парадоксальне пришвидшення виведення РФП (до 12,2 ± 1,9 хв та 15,3 ± 1,2 хв при стадії 3а), при стадії 3б у І групі 8,6 ± 0,8 хв та 9,4 ± 1,1 хв у ІІ групі. Цю закономірність можна пояснити двома патофізіологічними феноменами: артеріоловенулярним скидом крові, коли замість повільного кровотоку по капілярах все більшу роль починає відігравати значно швидший тік крові по мікрошунтах (юкстакапілярний кровотік), що має місце при стадії 3а. У стадії 3б додається підвищена судинна проникність iз наростаючим набряком гомілки (при цьому розширюється ділянка поширення радіонукліду в місці його введення із залученням у процес вимивання радіонукліда з більшої кількості мікросудин).
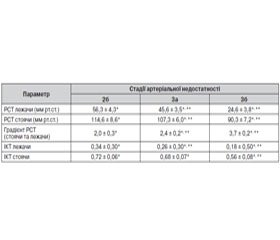
Результати, отримані при вимірюванні регіонарного систолічного тиску на підколінній артерії та індекса кісточкового тиску за допомогою ультразвукової допплерографії в ураженій кінцівці у пацієнтів І та ІІ груп, наведені у таблицях 5, 6.
Ці результати вказують на вірогідне зниження в горизонтальному положенні пацієнта в ураженій кінцівці величин РСТ на підколінній артерії при всіх стадіях ішемії як щодо норми, так і попередньої стадії. У контралатеральній кінцівці вірогідне зниження регіонарного систолічного тиску (93,6 ± 9,4 мм рт.ст.) відмічено тільки в пацієнтів із критичною ішемією (стадія 3б). В інших випадках (пацієнти зі стадіями ішемії 2б і 3а) вірогідно від норми відрізняється тільки ІКТ (0,81 ± 0,08 та 0,72 ± 0,06).
Порушення периферійної мікрогемодинаміки у хворих із тяжкими стадіями артеріальної недостатності характеризується прогресуючим зниженням величини РСТ, що особливо виражено у хворих із критичною ішемією та порушенням судинного тонусу, який при критичній ішемії практично повністю зникає (вазоплегія) [1].
Оцінюючи підвищення РСТ на підколінній артерії в ураженій кінцівці при ортостазі, перш за все варто відмітити поступове збільшення ступеня цього підвищення при горизонтальному положенні пацієнта в мiру прогресування ішемії відповідно в 1,9–2,2 і 2,9 раза в І групі та 2–2,4–3,7 у ІІ групі. Таке значне збільшення РСТ при критичній ішемії в ураженій кінцівці у вертикальному положенні пацієнта неможливо пояснити ні підвищенням судинного тонусу, ні гідростатичним тиском, що є в різко редукованому судинному руслі. Iмовiрно, розвиток такого феномена значною мірою обумовлений екстравазальною компресією судинного русла тканинами, що знаходяться в умовах ішемічного набряку, який, таким чином, відіграє певну компенсаторну роль, підтримуючи внутрішньосудинний тиск при ортостазі та в цілому.
У всіх спостереженнях відмічено підвищення постоклюзійного венозного тиску, що вірогідно відрізняється від норми. Одночасно з цим спостерігається тенденція до відносного зниження його величин при прогресуванні артеріальної недостатності (вірогідно порівняно з попередніми стадіями) (табл. 7).
Аналіз отриманих даних свідчить, що поряд із прогресуючим зниженням ПОВТ у горизонтальному положенні пацієнта відбувається його значне і прогресуюче підвищення в ортостазі. В ураженій кінцівці знижується також і лінійна швидкість спонтанного венозного кровотоку, що становить у середньому 43,6 % від норми при стадіях 2б–3а і 26 % від норми — при критичній ішемії.
Описані зміни параметрів, що характеризують венозний кровообіг, можна пояснити поступовим зниженням венозного тонусу, що є характерним при критичній ішемії.
Таким чином, при хронічній артеріальній недостатності нижніх кінцівок стадій 2б–3а параметри, що характеризують венозний відтік, вказують на наступне:
— підвищення ПОВТ у всіх групах пацієнтів;
— в ортостазі порівняно з горизонтальною позицією пацієнта відбувається значне підвищення ПОВТ — із прогресуванням артеріальної недостатності;
— прогресуюче зниження лінійної швидкості спонтанного венозного кровотоку;
— прогресуюче підвищення об’єму крові у венозному руслі ураженої кінцівки, що підтверджено радіонуклідним дослідженням з внутрішньовенним введенням 99mТс-альбуміну — радіофармпрепарату, який тривало зберігається в судинному руслі.
У контралатеральній кінцівці прогресуючого зниження ПОВТ не відбувається.
Таким чином, у хворих з облітеруючим атеросклерозом артерій нижніх кінцівок наявні виражені зміни венозного кровотоку, що посилюються з підвищенням стадії артеріальної недостатності ураженої кінцівки. На початку вони характеризуються венозним гіпертонусом, що поступово знижується і венозний тиск підтримується збільшенням об’єму крові у венозному руслі (гіперволемія) [2]. Це підтверджується за допомогою радіонуклідного методу з внутрішньовенним введенням 99mТс-альбуміну. Отримано збільшення об’єму крові в гомілці при ортостазі в середньому на 39 % щодо горизонтального положення в пацієнтів iз 2б та 3а стадiями і на 62 % — при критичній ішемії (при нормі 35,3 ± 1,8 %).
Критична ішемія (стадія 3б) характеризується різким зниженням венозного тонусу (вазоплегія), підвищенням венозного тиску як у горизонтальному положенні пацієнта, так і при переході в ортостаз, зростанням об’єму крові в дистальних відділах ураженої кінцівки (венозна гіперволемія). Підвищення венозного тиску має також і певний позитивний характер, бо сприяє збільшенню внутрішньосудинного тиску (венозного) і створює тим самим сприятливі умови для функціонування мікроциркуляції. Патофізіологічний зміст збільшення об’єму венозної крові — утримання венозної гіпертензії за рахунок не тільки венозного тонусу, але й гіперволемії. Певний патофізіологічний зміст має набряк стопи та гомілки при стадії 3б ішемії, який можна розцінювати як екстравазальну компресію, що дозволяє утримувати венозний тиск у ділянці ішемії [10, 11].
У контралатеральній кінцівці суттєвої різниці показників венозного тиску між стадіями 3а і 3б у горизонтальному та вертикальному положенні пацієнта немає.
Описані зміни венозної гемодинаміки пояснюють розвиток у деяких хворих при тяжких стадіях ішемії клапанної недостатності глибоких вен гомілки [9].
Судинні порушення кровопостачання кісток призводять до порушення венозного відтоку, що настає задовго до того, як реєструються клінічні прояви підвищення внутрішньокісткового тиску [6, 12].
Ми вимірювали внутрішньокістковий тиск великогомілкової кістки за допомогою спеціальної голки з клапаном, з’єднаної з манометром (табл. 8).
Наведені вище результати свідчать про те, що ВКТ великогомілкової кістки підвищений при стадіях 2б та 3а артеріальної ішемії щодо контралатеральної кінцівки та норми. Звертає увагу різке збільшення внутрішньокісткового тиску великогомілкової кістки при стадії 3а та його різке зниження при критичній ішемії в пацієнтів І групи.
При атеросклеротичному ураженні артерій нижніх кінцівок на фоні цукрового діабету (ІІ група) спостерігається підвищення ВКТ із прогресуванням артеріальної недостатності, та на відміну від І групи при стадії 3б ВКТ залишається високим. На контралатеральній кінцівці показники ВКТ є вищими порівняно з нормою та мають тенденцію до збільшення відповідно до прогресування артеріальної недостатності.
Отже, отримані дані обумовлюють обґрунтоване виділення наступних показань до застосування непрямих способів реваскуляризації при ішемії нижніх кінцівок:
— збільшення ОК більше нiж у 2 рази в дистальних відділах гомілки при стадії 2б за даними внутрішньовенної радіоізотопної ангіографії;
— сповільнення часу (Т1/2) виведення 99mТс в гомілці при стадії 2б ішемії;
— градієнт РСТ у горизонтальному та вертикальному положенні пацієнта в підколінній артерії більше за 2;
— збільшення постоклюзійного венозного тиску більше нiж у 2 рази;
— зниження спонтанного венозного кровотоку більше нiж на 40 %;
— підвищення внутрішньокісткового тиску понад 44 см вод.ст.
Незалежно від стадії ішемії нижніх кінцівок, за відсутності умов до виконання ендоваскулярних або прямих реконструкційно-відновних операційних втручань перераховані показники артеріального, венозного, мікроциркуляторного та внутрішньокісткового кровообігу є показаннями до застосування непрямих способів реваскуляризації.
Список литературы
1. Влияние реваскуляризации на результаты лечения хронической критической ишемии при нейропатической форме диабетической стопы / И.Н. Игнатович, Г.Г. Кондратенко, Г.А. Сергеев [и др.] // Ангиология и сосудистая хирургия. — 2011. — Т. 17, № 1. — С. 71-75.
2. Мішалов В.Г. Стратегія і тактика лікування критичної ішемії нижніх кінцівок / В.Г. Мішалов, В.А. Черняк // Науковий вісник Ужгородського університету, серія «Медицина». — 2012. — № 2(44). — С. 77-82.
3. Никоненко О.С. Ефективність PRP-терапії у хворих з оклюзією стегново-підколінно-гомілкового сегменту / О.С. Никоненко, О.М. Волошин // Науковий вісник Ужгородського університету, серія «Медицина». — 2012. — № 2(44). — С. 83-85.
4. Пиптюк О.В. Непряма реваскуляризація в комплексному лікуванні хворих з облітерацією дистального артеріального русла / О.В. Пиптюк, Р.В. Сабадош, В.О. Пиптюк // Практична медицина. — 2008. — Т. 14, № 5. — С. 194-197.
5. Пиптюк О.В. Досвід комплексного лікування хронічної критичної ішемії нижніх кінцівок / О.В. Пиптюк // Клінічна хірургія. — 2007. — № 2–3. — С. 117-118.
6. Пиптюк О.В. Стан кісткового мозку при хронічній критичній ішемії нижніх кінцівок / О.В. Пиптюк // Трансплантологія. — 2003. — № 4. — С. 273-275.
7. Русин В.І. Патогенетичне обґрунтування тактики хірургічного лікування критичної ішемії нижніх кінцівок при дистальних формах атеросклерозу / В.І. Русин, В.В. Корсак, В.В. Русин та ін. // Науковий вісник Ужгородського університету, серія «Медицина». — 2015. — № 1(51). — С. 163-167.
8. Русин В.И. Сочетание прямых и непрямых методов реваскуляризации при критической ишемии нижних конечностей / В.И. Русин, В.В. Корсак, В.В. Русин и др. // Хирургия. Восточная Европа. — 2015. — № 2(14). — С. 45-56.
9. Савельев В.С. Патогенез и консервативное лечение тяжелых стадий облитерирующего атеросклероза артерий нижних конечностей. Руководство для врачей / В.С. Савельев, В.М. Кошкин, А.В. Каралкин. — М.: МИА, 2010. — 216 с.
10. Хірургія дистальних відділів термінальної аорти: монографія / В.І. Русин, В.В. Корсак, С.М. Чобей [та ін.]. — Ужгород: Карпати, 2012. — 488 с.
11. Inter-Society Consensus for the Management of Peripheral Arterial Disease / L. Norgren, W.R. Hiatt, J.A. Dormandy [et al.] // Journal of Vascular Surgery. — January, 2007. — Р. 63.
12. Van Overhagen H. Below-the-knee interventions / H. van Overhagen, S. Spiliopoulos, D. Tsetis // Cardiovasc. Intervent. Radiol. — 2013. — Vol. 36(2). — P. 302-311.

/6.jpg)
/7.jpg)
/8.jpg)
/9.jpg)