Резюме
Вступ. У сучасних умовах радикальна простатектомія повинна забезпечувати не тільки хороші онкологічні результати, а саме — відсутність позитивного хірургічного краю у видаленому препараті та біохімічного рецидиву в післяопераційному періоді, але й повну функціональну реабілітацію пацієнта. При виконанні радикальної простатектомії з метою запобігання кровотечі перед перетинанням виконують прошивання венозно-дорсального комплексу або виділення його з подальшою перев’язкою, що дозволяє поліпшити візуалізацію на цьому етапі операції. У той же час ряд авторів стверджує, що будь-яке втручання в цій області так чи інакше призводить до травми зовнішнього сфінктера уретри. Метою нашого дослідження було вивчення можливості обробки (прошивання, перев’язки) венозно-дорсального комплексу без травматизації зовнішнього сфінктера уретри шляхом комплексного морфоанатомічного вивчення структур венозно-дорсального комплексу і його відношення до зовнішнього сфінктера уретри за даними патоморфологічного, гiстохiмiчного, морфометричного, імуногістохімічного дослідження і аналізу їх складу. Матеріал і методи. Особливості хірургічної анатомії венозно-дорсального комплексу і зовнішнього сфінктера уретри було вивчено на 30 препаратах, узятих від трупів чоловіків різного віку і типів статури, які померли від причин, не пов’язаних iз серцево-судинною патологією. Результати i обговорення. Проведений морфометричний аналіз показав, що середня відстань між венозно-дорсальним комплексом і зовнішнім сфінктером уретри становила 65,76 ± 8,26 мкм, що більше ніж у два рази (43,3 %) менше за діаметр голок. Висновки. Дані комплексного дослідження свідчать про те, що виконання прошивання або перев’язування венозно-дорсального комплексу неможливо без травматизації зовнішнього сфінктера уретри.
Введение. В современных условиях радикальная простатэктомия должна обеспечивать не только хорошие онкологические результаты, а именно — отсутствие позитивного хирургического края в удаленном препарате и биохимического рецидива в послеоперационном периоде, но и полную функциональную реабилитацию пациента. При выполнении радикальной простатэктомии с целью предотвращения кровотечения перед пересечением выполняют прошивание венозно-дорсального комплекса либо выделение его с последующей перевязкой, что позволяет улучшить визуализацию на данном этапе операции. В то же время ряд авторов утверждает, что любое вмешательство в данной области так или иначе приводит к травме наружного сфинктера уретры. Целью нашего исследования было изучение возможности обработки (прошивания, перевязки) венозно-дорсального комплекса без травматизации наружного сфинктера уретры путем комплексного морфоанатомического изучения структур венозно-дорсального комплекса и его отношения к наружному сфинктеру уретры по данным патоморфологического, гистохимического, морфометрического, иммуногистохимического исследования и анализа их состава. Материал и методы. Особенности хирургической анатомии венозно-дорсального комплекса и наружного сфинктера уретры были изучены на 30 препаратах, взятых от трупов мужчин разного возраста и типов телосложения, умерших по причинам, не связанным с сердечно-сосудистой патологией. Результаты и обсуждение. Проведенный морфометрический анализ показал, что среднее расстояние между венозно-дорсальным комплексом и наружным сфинктером уретры составило 65,76 ± 8,26 мкм, что более чем в два раза (43,3 %) меньше диаметра игл. Выводы. Данные комплексного исследования свидетельствуют о том, что выполнение прошивания либо перевязывания венозно-дорсального комплекса невозможно без травматизации наружного сфинктера уретры.
Introduction. In modern conditions, the radical prostatectomy should provide not only good oncological results, namely, the absence of a positive surgical margin in the removed preparation and biochemical recurrence in the postoperative period, but also the complete functional rehabilitation of the patient. When performing radical prostatectomy in order to prevent bleeding before dissection, suturing of the dorsal venous complex is preformed, or its separation followed by ligation, which improves the visualization at this stage of the surgery. At the same time, a number of authors argue that any intervention in this area anyhow leads to injury of external urethral sphincter. The aim of our study was to investigate the possibility of processing (suturing, ligation) the dorsal venous complex without traumatizing external urethral sphincter by comprehensive morphological and anatomical study of the structures of dorsal venous complex and its relationship to the external urethral sphincter according to pathological, histochemical, morphometric, immunohistochemical studies and analysis of their composition. Materials and methods. The characteristics of surgical anatomy of the dorsal venous complex and external urethral sphincter were studied on 30 specimens taken from the corpses of men of all ages and body types, who died of causes unrelated to cardiovascular diseases. Results and discussion. Morphometric analysis has shown that the average distance between the dorsal venous complex and the external urethral sphincter was 65.76 ± 8.26 μm that is more than half (43.3 %) less than the diameter of the needles. Conclusions. The data of comprehensive study indicate that suturing or ligation of the dorsal venous complex is not possible without the injury of external urethral sphincter.
Статья опубликована на с. 72-77
Введение
Заболеваемость раком предстательной железы (РПЖ) в Украине в 2013 году составила 40,5 случая на 100 000 мужского населения. Среди этих больных примерно у половины (43,7 %) патология была выявлена в стадии Т1–2 [1]. На сегодняшний день одним из наиболее эффективных методов лечения больных с локализованными формами рака простаты является радикальная простатэктомия (РПЭ). В современных условиях РПЭ должна обеспечивать не только хорошие онкологические результаты, а именно — отсутствие позитивного хирургического края в удаленном препарате и биохимического рецидива в послеоперационном периоде, но и полную функциональную реабилитацию пациента. Недержание мочи является состоянием, оказывающим первостепенное влияние на качество жизни больных после выполнения радикальной простатэктомии. Это осложнение РПЭ возникает в 6–52 % случаев [2]. Наиболее существенным фактором, способствующим предотвращению инконтиненции, является хорошая интраоперационная визуализация раны, при которой возможна аккуратная диссекция тканей в области верхушки простаты и сохранение наружного сфинктера уретры (НСУ) с последующим тщательным наложением уретрально-мочепузырного анастомоза. Как при выполнении лапароскопической радикальной простатэктомии, так и при открытой РПЭ наиболее сложным этапом в плане визуализации является пересечение венозно-дорсального комплекса (ВДК). Если не произведен адекватный контроль сосудов, кровотечение, возникающее после пересечения ВДК, может быть очень значительным и привести к ряду серьезных осложнений. Из-за ухудшения визуализации, связанной с кровотечением, возрастает риск травмы наружного сфинктера уретры, прямой кишки, возникновения позитивного края. При выполнении РПЭ с целью предотвращения кровотечения перед пересечением выполняют прошивание ВДК либо выделение его с последующей перевязкой, что позволяет улучшить визуализацию на данном этапе операции. В то же время ряд авторов утверждает, что любое вмешательство в этой области так или иначе приводит к травме наружного сфинктера уретры [3]. Таким образом, как меры, направленные на профилактику возникновения кровотечения, так и пересечение ВДК без предварительной обработки может привести к недержанию мочи. В связи с этим вышеизложенное показывает необходимость всестороннего морфоанатомического изучения структур ВДК и его отношения к наружному сфинктеру уретры.
Целью нашего исследования было изучение возможности обработки (прошивания, перевязки) ВДК без травматизации НСУ путем комплексного морфоанатомического изучения структур венозно-дорсального комплекса и его отношения к наружному сфинктеру уретры по данным патоморфологического, гистохимического, морфометрического, иммуногистохимического исследования (ИГХИ) и анализа их состава.
Материал и методы
Особенности хирургической анатомии ВДК и НСУ были изучены на 30 препаратах, взятых от трупов мужчин разного возраста и типов телосложения, умерших по причинам, не связанным с сердечно-сосудистой патологией. Анатомические исследования были выполнены на базе областного судебно-медицинского бюро г. Донецка. По типам телосложения умершие распределялись следующим образом: 10 — долихоморфные, 10 — мезоморфные и 10 — брахиморфные. В работе нами использовалась возрастная периодизация, предложенная В.В. Бунаком (1965), за исключением периодов детства и пожилого возраста, которая представлена в таблице 1 [4]. Исследованные нами трупы мужчин были в возрасте от 36 до 74 лет (табл. 1).
/73.jpg)
С целью изучения хирургической анатомии ВДК и НСУ было произведено антропометрическое изучение трупов с последующей корреляцией типов телосложения и морфометрических параметров. Изучение крайних типов телосложения проводили на основании индексов или относительных величин, характеризующих структурные особенности целого организма.
Основные признаки, позволяющие определить крайние типы телосложения, мы выделили согласно рекомендациям Д.Б. Бекова (1988) — по отношению длины нижней конечности к росту [5]. Брахиморфный тип телосложения имели лица, у которых индекс был > 55, мезоморфный — 50–55, а долихоморфный — < 50.
Доступ к предстательной железе осуществляли нижнесрединным разрезом длиной до 20 см. Выполняли выделение простаты из окружающих ее тканей по боковым поверхностям. После чего отсекали предстательную железу от мочевого пузыря, пересекали семенные протоки и выделяли семенные пузырьки. Далее освобождали предстательную железу по задней поверхности вплоть до уретры. После чего вырезали ВДК и уретру, стараясь высечь наиболее длинный участок уретры с покрывающим ее венозно-дорсальным комплексом. Затем отсекали интересующий участок от остальной части железы в области апекса, оставляя уретру и ВДК максимально длинными. Полученные препараты фиксировали 10% раствором забуференного нейтрального формалина. Исследуемый материал располагали таким образом, чтобы в срез попадали сосуды и часть уретры. После дегидратации материал заливали в высокоочищенный парафин с полимерными добавками (Richard-Allan Scientific, США) при температуре не выше 60 °С. Из парафиновых блоков на ротационном микротоме Microm HM325 с системой переноса срезов STS (Carl Zeiss, Германия) делали срезы толщиной 5 мкм. Дальнейшее микроскопическое исследование проводили с использованием методики серийных срезов. Срезы ткани помещали на предметные стекла, затем окрашивали гематоксилином и эозином, выполняли гистохимическое окрашивание по ван Гизону на коллагеновые и мышечные волокна. Для верификации морфологических структур в препаратах нами проведено иммуногистохимическое исследование серийных парафиновых срезов, которые помещали на покрытые адгезивом стекла Super Frost Plus (Menzel, Германия). Исследование осуществляли на депарафинированных и регидратированных срезах. Для демаскирования антигенности ткани использовали метод тепловой обработки срезов в буфер Target Retrieval Solution High pH (DAKO, Дания) путем кипячения в течение 15–20 минут в микроволновой печи Samsung CE 118KFR с учетом рекомендаций фирмы-производителя антител. После блокирования неспецифического связывания белков протеиновым блоком (DAKO), а эндогенной пероксидазной активности — пероксидазным блоком (DAKO) наносили немеченые первичные антитела. Использовали мышиные моноклональные антитела к CD34, S100, α-гладкомышечному актину — α-SMA (все фирмы DAKО). Визуализацию первичных антител проводили с помощью системы детекции DAKO Advance. В качестве субстрата для пероксидазы хрена использовали DAB+ (DAKO), систему визуализации Mouse/Rabbit PolyVue (HRP/DAB detection System). Для визуализации гистологической структуры исследуемой ткани обработанные иммуногистохимические препараты докрашивали гематоксилином Майера. Далее окрашенные срезы заключали в полусинтетическую среду Eukit (Kaltek, Италия).
Изучение препаратов в проходящем свете проводили на исследовательском микроскопе Olympus AX70 (Япония) с цифровой видеокамерой Olympus DP50, соединенной с персональным компьютером. Микрофотографирование и морфометрическое изучение препаратов выполнено с использованием программы AnalySIS Pro 3.2 (Soft Imaging, Германия).
Для объективизации морфотопографических особенностей структур в изучаемых препаратах применяли морфометрическое исследование. Морфометрический анализ дает возможность получить описание метрических свойств морфологических структур, установить характер их связей; количественные характеристики представлены в двух- и трехмерной системе. Для оценки процесса на плоскости использовали планиметрию — изучение морфологических изменений в объеме посредством стереометрии. Стереометрия позволяет использовать данные измерений на плоскости (двухмерная система) для перехода к характеристике трехмерной системы, т.е. для получения показателей количественно-пространственной организации морфологических структур и патологических изменений в них.
Морфометрическое исследование гистологических препаратов начиналось со стереометрического изучения с помощью микроскопа Primo Star (Carl Zeiss) при увеличении ×100. При этом морфометрический анализ гистологических препаратов осуществлялся методом точечного счета [6]. На компьютерное изображение микропрепарата накладывалась сетка из горизонтальных и вертикальных линий, пересечение которых образовывали 100 точек. Количество точек, которые «помещались» в изучаемой структуре, отвечало удельному объему этой структуры в исследуемой ткани [6].
Морфометрический анализ препаратов начинался с определения стромально-сосудистых соотношений при увеличении микроскопа ×100. В каждом наблюдении было исследовано 10 полей зрения микропрепарата, что составляло 1000 точек. Регистрировались все точки, которые «упали» на строму и сосуды.
Кроме изучения стромально-сосудистых соотношений, было проведено морфометрическое исследование структур предстательной железы в области апекса. Морфометрический анализ гистологических препаратов начинался со стереометрического изучения при увеличении микроскопа ×100. В каждом наблюдении исследовалось также 10 полей зрения микропрепарата. Вычислялся процент удельного объема коллагеновых и гладкомышечных волокон, структур уретры, венозно-дорсального комплекса, нервных клеток, периуретральных желез, а также сосудов.
Компьютерная морфометрия была проведена с помощью микроскопа Primo Star (Carl Zeiss, ФРГ), персонального компьютера, видеорегистратора и программы анализа изображений AxioVision (Rel.4.8.2). Данная программа позволила определить среднее расстояние венозно-дорсального комплекса от наружного сфинктера уретры (в микрометрах (мкм)). Статистическая обработка полученных данных проводилась на персональном компьютере с использованием пакета программ Statistica 6.0 (StatSoft Inc., USA).
Результаты и обсуждение
Выполнено комплексное морфотопографическое исследование участков ВДК, его отношения к НСУ на основании патоморфологического, гистохимического, морфометрического, иммуногистохимического исследования, а также анализа их состава. Морфометрический анализ препаратов с использованием техники точечного счета и стереометрическое исследование показали, что наибольший удельный объем структур (55,0 %) в изученных препаратах приходится на строму предстательной железы. Практически в равном количестве в препаратах обнаружены нервные клетки и сосуды — 21,2 и 22,13 % соответственно, и лишь 1,67 % пришлось на периуретральные железы, что показано на рисунке 1.
/74.jpg)
ВДК располагается в непосредственной близости к НСУ, тесно прилежит к железистым структурам предстательной железы, что представлено на рисунках 2 и 3. Большое количество сосудов разного анатомического строения, разного калибра, как венозного, так и артериального типа, расположены в изучаемых участках. В проекции ВДК венозные сосуды представлены широко — от мелкого до крупного калибра, часть из них неравномерно расширены, что создает предпосылки, с одной стороны, для послеоперационного тромбообразования, с другой — для кровотечения в течение оперативного вмешательства и/или после него (рис. 2, 3).
Верификация и определение особенностей расположения сосудов в изучаемых препаратах выполнены нами при помощи ИГХИ с маркером CD34, что представлено на рисунках 4, 5.
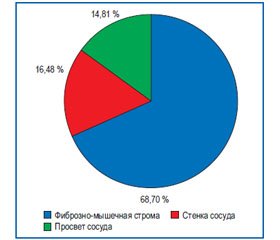
Обнаружено, что в изучаемых препаратах удельный объем фиброзно-мышечной стромы составил 68,7 %, сосудов — 31,3 %, причем из них 16,5 % составили стенки сосудов и 14,8 % — просвет сосудов, что представлено на рисунке 6.
Был проведен морфометрический подсчет и определено среднее расстояние ВДК от НСУ, которое составило 65,76 ± 8,26 мкм, где 1 мкм = 0,001 мм, 1 мм = 1000 мкм (рис. 7, 8).
Таким образом, по данным проведенного комплексного исследования наглядно показана тесная связь мышечных, сосудистых и нервных компонентов, расположенных в проекции ВДК и НСУ. Наличие сосудов разного калибра в составе ВДК создает предпосылки для «избирательного» прошивания сосудов только крупного калибра. В то же время анализ структур препаратов и соотношения сосудистого пространства свидетельствует о том, что сосуды расположены в непосредственной близости друг к другу и прошивание одного сосуда повлечет за собой травму другого, что приведет к еще большему кровотечению и травме НСУ. Диаметр игл, которые применяются при оперативных вмешательствах на предстательной железе, составляет 0,15–1,8 мм (150–1800 мкм).
Проведенный морфометрический анализ показал, что среднее расстояние между ВДК и НСУ составило 65,76 ± 8,26 мкм, что более чем в два раза (43,3 %) меньше диаметра игл. Таким образом, невозможно обойтись без травматизации НСУ при выполнении прошивания либо перевязывания ВДК.
Выводы
1. Данные проведенного комплексного морфологического анализа с применением гистохимического, иммуногистохимического и морфометрического исследования подтвердили тесную взаимосвязь анатомических структур в области ВДК.
2. Полученные данные достоверно подтверждают, что среднее расстояние между венозно-дорсальным комплексом и наружным сфинктером уретры равно 65,76 ± 8,26 мкм.
3. Данные комплексного исследования свидетельствуют о том, что выполнение прошивания либо перевязывания венозно-дорсального комплекса невозможно без травматизации наружного сфинктера уретры.
/73.jpg)
/76.jpg)

/74.jpg)
/75.jpg)