Статья опубликована на с. 35-43
Неуклонный рост числа людей, страдающих сахарным диабетом (СД) 2-го типа, в современном обществе диктует необходимость разработки и использования передовых стратегий для повышения эффективности лечения этого заболевания и его осложнений. Важнейшим требованием к новым противодиабетическим препаратам, наряду с высокой терапевтической эффективностью, является наличие доказанного профиля безопасности, а также способность оказывать нивелирующее влияние на сопутствующие факторы, содействующие дальнейшему прогрессированию основной патологии. В Консенсусах по медицинскому контролю гипергликемии при СД 2-го типа, принятых в разные годы Американской диабетологической ассоциацией (ADA) и Европейской ассоциацией по изучению диабета (EASD), красной нитью проходит утверждение о необходимости всестороннего управления заболеванием, включая воздействие не только на параметры гликемического контроля, но и на другие факторы риска (Nathan, 2009; Rodbard, 2009).
В настоящее время установлено, что традиционно используемые в повседневной клинической практике пероральные сахароснижающие препараты (ПССП), такие как метформин, производные сульфонилмочевины (ПСМ) и тиазолидиндионы, имеют ограниченные возможности в предотвращении прогрессирования СД 2-го типа. Более того, некоторые ПСМ способствуют увеличению массы тела, повышают риск гипогликемий и развития сердечно-сосудистых нарушений, ускоряют прогрессирование функциональной недостаточности β-клеток (например, глибенкламид). Применение метформина, в отличие от ПСМ, позволяет избежать повышения массы тела и гипогликемий, однако поддерживать только с его помощью необходимый уровень контроля гликемии в течение длительного времени не представляется возможным (Корпачев В.В., 2002, 2005; Анциферов М.Б., 2012; Kahn, 2006; Riedel, 2007).
Необходимость применения инсулинотерапии при СД 2-го типа в большинстве случаев возникает тогда, когда воздействие ПССП не позволяет добиться адекватного контроля гликемии. Инсулинотерапия является не только наиболее эффективным средством борьбы с гипергликемией, но и методом лечения, оказывающим протективное действие в отношении развития микроваскулярных осложнений. Однако его применение может привести к повышению массы тела, преимущественно в первые 9–12 месяцев терапии (в среднем на 2–6 кг), что особенно нежелательно у лиц с уже имеющимся избытком веса (Корпачев, 2001, 2016). Поэтому в этот период крайне желательно применение препаратов, предотвращающих данный негативный эффект (Pieber, 2015).
В последнее время внимание исследователей и клиницистов привлекает терапия на основе инкретинов, представляющая собой новое перспективное направление в фармакотерапии СД. Их изучение началось еще в начале прошлого века. Так, в 1902 г. Baylis и Starling описали фактор, который вырабатывается в тонком кишечнике и стимулирует секрецию поджелудочной железы, а уже в 1932 г. термин «инкретин» был окончательно внедрен в практику. В 1964 г. впервые описан «инкретиновый эффект» в эксперименте, результат которого продемонстрировал, что секреция инсулина β-клетками более выражена в случае введения глюкозы перорально, нежели внутривенно (Elrick, 1964). Согласно оценкам M. Nauck и соавторов, приблизительно 60 % инсулина, секретируемого в ответ на прием пищи, выделяется вследствие данного эффекта. Известно, что у пациентов с СД 2-го типа инкретиновый эффект снижен или даже отсутствует вследствие специфического сокращения выработки глюкагоноподобного пептида-1 (ГПП‑1) в ответ на прием пищи и снижения чувствительности β-клеток к физиологическому уровню ГПП‑1 (Nauck, 1986, 1993; Vilsboll, 2002, Schjoldager, 1989).
При разработке средств медикаментозного воздействия на инкретиновую регуляторную систему сформировалось два направления: 1) создание агонистов рецепторов ГПП‑1 (инкретиномиметиков), резистентных к ферментативному разрушению специфическим ферментом дипептидилпептидазой‑4 (ДПП‑4) (эксенатид, лираглутид, ликсисенатид, албиглутид); 2) производство ингибиторов ДПП‑4, которые пролонгируют эффект эндогенных инкретиновых гормонов за счет конкурентного ингибирования ДПП‑4, ответственного за их деградацию (ситаглиптин, вилдаглиптин, саксаглиптин, линаглиптин, алоглиптин) (Корпачев, 2011; Анциферов, 2012; Панькив, 2011). Проводятся также исследования веществ (агонистов рецепторов GPR119 и GPR40), стимулирующих секрецию эндогенного ГПП‑1 клетками кишечника (Nadkarni, 2014; Leech, 2011).
Первый аналог человеческого ГПП‑1 длительного действия, соответствующий природному ГПП‑1, лираглутид (Виктоза®) был создан в 1997 году. Лираглутид содержит пальмитиновую (С16) жирную кислоту, присоединенную к основной полипептидной цепочке через глутаминовую кислоту. Такая модификация способствует ассоциации его молекул в гептамеры, пролонгируя всасывание препарата из места введения и обеспечивая высокую ферментативную устойчивость к ДПП‑4 и эндопептидазам (Knudsen, 2000; Steensgaard, 2008). Период полураспада лираглутида составляет около 13 часов, что дает возможность поддерживать его стабильную концентрацию в циркуляторном русле в течение 24 часов, а также позволяет вводить один раз в сутки в любое время, независимо от приема пищи (Elbrond, 2002; Shyangdan, 2011).
Следует отметить, что ингибиторы ДПП‑4 и аналоги ГПП‑1 относятся к химически различным и структурно независимым соединениям, но имеют сходный механизм действия, состоящий в регулировании гомеостаза глюкозы путем воздействия на процессы глюкозозависимого синтеза инсулина и глюкагона, влияния на потребление пищи и ее эвакуацию из желудка, на пролиферацию и дифференциацию β-клеток поджелудочной железы (Lee, 2014).
Учитывая, что рецепторы ГПП‑1 обнаружены в различных тканях, в том числе в миокарде и эндотелии сосудов, предполагается плейотропная активность ГПП‑1. На сегодняшний день опубликованы результаты исследований, указывающие на положительный эффект ГПП‑1 и его метаболитов на состояние миокарда, эндотелия сосудов животных и человека, а также их потенциальное противовоспалительное и антиатерогенное действие (Vergès, 2011; Anagnostis, 2011). В экспериментах на животных продемонстрировано улучшение левожелудочковой и системной гемодинамики, уменьшение зоны индуцированной ишемии под влиянием ГПП‑1 (Bose, 2005). У больных СД 2-го типа отмечена нормализация функции эндотелиальной ткани при внутривенном введении ГПП‑1, а у пациентов с инфарктом миокарда зарегистрировано улучшение функции левого желудочка, сокращение периода госпитализации и показателя внутрибольничной смертности (Nikolaidis, 2004; Nystrom, 2004). Заслуживают внимания недавно опубликованные результаты многоцентрового международного исследования LEADER (NCT01179048), которые продемонстрировали, что применение лираглутида (Виктоза®) у больных СД 2-го типа имеет дополнительное преимущество — уменьшение кардиоваскулярного риска, что отразилось в снижении смертности от сердечно-сосудистых событий. Продолжительность наблюдения составила 3,5–5 лет. В исследовании принимали участие 9340 больных СД 2-го типа с высоким кардиоваскулярным риском, которые были рандомизированы на группы, получавшие либо подкожную инъекцию лираглутида 1,8 мг один раз в день (или максимально переносимая доза), либо плацебо наряду со стандартной терапией. Первичной конечной точкой являлось впервые возникшее одно из трех серьезных неблагоприятных событий: смерть вследствие сердечно-сосудистой патологии, нефатальный инфаркт миокарда (ИМ) или нефатальный инсульт. В группе пациентов, принимавших лираглутид, продемонстрировано снижение случаев смерти на 22 % (до 4,7 % в сравнении с 6,0 % в группе плацебо, Р = 0,007), а также было меньше эпизодов подтвержденной гипогликемии (снижение гликемии ˂ 3,1 ммоль/л). Также в этой группе отмечено достоверное снижение уровня HbA1c и массы тела. На основании выводов исследования LEADER эксперты говорят о новой эре в управлении СД 2-го типа, которая началась с появлением препаратов, позволяющих предотвратить опасные для сердечно-сосудистой системы гипогликемии, связанные с использованием инсулина и ПССП (Tucker, 2016, Nauck, 2013).
Уникальным преимуществом терапии на основе инкретинов также является возможность коррекции функционального дисбаланса α- и β-клеток поджелудочной железы, который тесно связан с состоянием глюкозорезистентности этих клеток (т.е. с нарушением чувствительности к изменениям концентрации глюкозы в крови), что ведет к изменению профиля постпрандиальной секреции инсулина и глюкагона (Корпачев, 2011). Инкретины стимулируют выделение инсулина и снижают секрецию глюкагона α-клетками поджелудочной железы, в результате происходит восстановление нарушенной при СД 2-го типа первой фазы секреции инсулина и снижение постпрандиальной гипергликемии (Holst, 2009). Кроме того, доказано, что ГПП‑1 оказывает положительное влияние на β-клетки, подавляя апоптоз, способствуя пролиферации, повышая дифференцировку и неогенез из эпителиальных клеток-предшественников, что приводит к увеличению массы β-клеток (Drucker, 1987, 2003). С учетом потенциальных положительных эффектов ГПП‑1 по отношению к β-клеткам поджелудочной железы и его возможности подавлять секрецию глюкагона проведен ряд исследований по применению ГПП‑1, в частности лираглутида, у пациентов с СД 1-го типа с неудовлетворительным контролем гликемии (Pieber, 2015; Dupre, 2004; Raman, 2010; Kielgast, 2011). Однако полученные результаты были неоднозначны. Так, в одном из клинических исследований с участием 14 больных СД 1-го типа добавление лираглутида к базальной терапии инсулином в течение одной недели привело к снижению концентрации глюкозы в крови натощак, уменьшению суточных колебаний гликемии и среднего уровня глюкозы за неделю. Это сопровождалось уменьшением средней потребности в базальном инсулине с 24,5 ± 6,0 единицы до 16,5 ± 6,0 единицы (р < 0,01) и болюсной дозы инсулина с 22,5 ± 4,0 единицы до 15,5 ± 4,0 единицы (р < 0,01). У пациентов, которые продолжали терапию лираглутидом в течение 24 недель, отмечено улучшение параметров гликемического контроля, снижение базальной и болюсной дозы инсулина, снижение уровня HbA1c (с 6,5 до 6,1 %, р = 0,02) и массы тела (на 4,5 ± 1,5 кг, р = 0,02). Авторы сделали вывод, что применение лираглутида может представлять собой дополнительную стратегию для улучшения гликемического контроля и снижения веса у больных СД 1-го типа (Varanasi, 2011; Lee S., 2016). Однако в 2016 г. опубликованы результаты рандомизированного двойного слепого, плацебо-контролируемого исследования, проведенного в Дании, свидетельствующие о том, что у пациентов с СД 1-го типа с избыточным весом и недостаточным гликемическим контролем степень снижения HbA1c практически не отличалась в группе больных, получавших лираглутид, и контрольной группе, получавшей плацебо (–0,5 % и –0,3 % соответственно). В это исследование было включено 100 больных СД 1-го типа старше 18 лет с HbA1c > 8 % и ИМТ > 25 кг/м2, находившихся на инсулинотерапии, к которой добавляли лираглутид или плацебо (контроль). Суточную дозу лираглутида еженедельно титровали от 0,6 до 1,2 мг и далее до 1,8 мг. Первичной конечной точкой было изменение HbA1c от исходного уровня к 24-й неделе. Вторичными конечными точками для анализа установлены: частота гипогликемии, колебания гликемии, доза инсулина, масса тела, постпрандиальные концентрации в плазме крови глюкагона и ГПП‑1, время опорожнения желудка, артериальное давление, частота сердечных сокращений, отмечаемые пациентами побочные эффекты, время, проведенное в состоянии гипогликемии, нормогликемии и гипергликемии, глюкоза плазмы крови натощак, средний уровень глюкозы и холестерина. Несмотря на отсутствие различий между двумя группами в снижении HbA1c, введение лираглутида ассоциировалось со снижением частоты гипогликемических событий, уменьшением болюсной и общей дозы инсулина, снижением массы тела, увеличением частоты сердечных сокращений (Dejgaard, 2016; Frandsen, 2010).Вопрос целесообразности применения лираглютида у пациентов с СД 1-го типа всесторонне освещен T.F. Dejgaard в недавно опубликованном аналитическом обзоре (на основе имеющихся научных работ в Cochrane library, MEDLINE и EMBASE по февраль 2016 г.). Анализ показал, что лираглутид в качестве дополнения к лечению инсулином снижал вес тела и суточную дозу инсулина по сравнению с монотерапией инсулином. При этом эффект лираглутида на показатель HbA1c, выявленный в неконтролируемых мелкомасштабных исследованиях, не соответствовал результатам, полученным в плацебо-контролируемых исследованиях, в которых не продемонстрировано никакого клинически значимого влияния на его уровень. Побочные эффекты встречались в основном в виде временных желудочно-кишечных нарушений, в первую очередь тошноты. Авторы заключают, что «…на основании имеющихся данных лираглутид не может быть рекомендован в качестве дополнительной терапии к инсулину у людей с диабетом 1-го типа с целью улучшения гликемического контроля». Продолжающиеся исследования эффективности лечения аналогами ГПП‑1 у лиц с недавно диагностированным СД 1-го типа и у больных, использующих инсулиновую помпу, возможно, помогут определить их будущую роль в терапии этих пациентов (Dejgaard‑2, 2016; Halland, 2016).
Иная ситуация с применением аналогов ГПП‑1 у пациентов с СД 2-го типа. Известно, что существенными причинами, ответственными за развитие гипергликемии при СД 2-го типа, являются не только снижение функции β-клеток и наличие резистентности к инсулину, но также и повышенный уровень глюкагона в крови. Как указывалось выше, ГПП‑1 оказывает глюкозозависимое подавляющее влияние на секрецию глюкагона не только за счет прямого воздействия на α-клетки поджелудочной железы, но и за счет увеличения синтеза соматостатина, тем самым нивелируя его контринсулярное влияние. Такой эффект инкретинов имеет большое значение в регуляции углеводного обмена у пациентов с СД 2-го типа, в частности для снижения гликемии — как постпрандиальной, так и гликемии натощак, обусловленной процессами глюконеогенеза в печени (Sun, 2015; Mikhail, 2008; Pinelli, 2011).
Пример успешного применения препарата ГПП‑1 у пациента с неэффективно контролируемой гликемией натощак рассматривается далее.
Пациент Ч., возраст 45 лет, поступил в отделение клинической фармакологии и возрастной эндокринологии. Болеет СД 2-го типа в течение 5 лет. Рост — 178 см, вес — 91 кг, ИМТ — 28,7 кг/м2, окружность талии (ОТ) — 96 см. С начала заболевания получал терапию метформином 1700 мг в сутки, затем комбинацию ситаглиптина и метформина 50/850 мг 2 раза в день. Показатель НbА1с за все время наблюдения за пациентом не превышал 8,0 %, однако уровень гликемии натощак практически ежедневно был самым высоким в течение суток и составлял 8,0–9,2 ммоль/л при последующем снижении в течение дня до 5,7–7,0 ммоль/л.
Учитывая необходимость поддержания нормогликемии натощак и нивелирования влияния контринсулярных гормонов, в частности глюкагона, принято решение заменить прием ингибитора ДПП‑4 (ситаглиптина) на лираглутид, при этом сохранив прежнюю суточную дозу метформина 1700 мг. Доза лираглутида титровалась до 1,8 мг в сутки в течение 3 недель. Спустя 2 недели применения дозы 1,8 мг/сутки уровень гликемии у пациента на протяжении дня значительно снизился (до 4,5 ммоль/л), что позволило снизить дозу лираглутида до 1,2 мг/сутки и метформина до 850 мг/сутки. Уровень гликемии натощак стабилизировался на значениях 6,2–6,6 ммоль/л. Показатель НbА1с через 3 мес. снизился до 7,2 %. Применение лираглутида позволило также уменьшить вес пациента на 7 кг, в результате чего стало возможным продолжить монотерапию лираглутидом в дозе 0,6 мг/сутки.
Зависимость инсулинотропных и ингибирующих секрецию глюкагона эффектов от изменений уровня гликемии с одновременным снижением веса представляется логичным обоснованием использования инкретиновой терапии в комбинации с экзогенной инсулинотерапией у пациентов с СД 2-го типа. Такой союз открывает перспективу получения синергического сахароснижающего эффекта без повышения риска развития гипогликемии по сравнению с монотерапией инсулином, а также позволяет нивелировать ассоциированное с инсулинотерапией увеличение веса. Так, результаты целого ряда клинических исследований оценивали эффективность и преимущества применения у больных СД 2-го типа тройной комбинации — инсулин, аналог ГПП‑1 и метформин (Vora, 2013; Garber, 2011; King, 2013, Jadinsky, 2009). В транснациональном открытом рандомизированном клиническом исследовании BEGIN: VICTOZA ADD-ON, в котором участвовали 119 медицинских учреждений из 12 стран (с сентября 2011 по июль 2012 г.), проведен сравнительный анализ двух стратегий лечения больных СД 2-го типа, изначально получавших базальную терапию инсулином деглюдек и метформином, которым в связи с неадекватным контролем гликемии (HbA1c ≥ 7,0 %) требовалась интенсификация сахароснижающей терапии. Первая стратегия состояла в добавлении лираглутида один раз в день (88 пациентов), вторая (традиционная) — в добавлении болюса инсулина аспарт один раз в день перед обедом (89 пациентов). Продолжительность наблюдения составляла 28 недель. Результаты показали более выраженное снижение уровня HbA1c в группе, получавшей лираглутид, чем в группе с дополнительным введением инсулина аспарт (0,74 и 0,39 % соответственно). В основной группе целевого уровня HbA1c < 7,0 % достигли 49,4 % участников против 7,2 % в группе сравнения, при этом у пациентов не зарегистрировано подтвержденных эпизодов гипогликемии и увеличения веса. Авторами сделан вывод о том, что лучших результатов в отношении долговременного контроля гликемии, снижения веса и уменьшения риска гипогликемии удалось достичь при помощи дополнительного введения аналогов ГПП‑1 по сравнению с добавлением инъекций инсулина аспарт (Mathieu, 2014).
В другом исследовании больные СД 2-го типа с неадекватным контролем гликемии при применении комбинации метформина с ПСС первые 12 недель (период «отмыва», run-in) принимали лираглутид в дозе 1,8 мг. Пациенты, достигшие за это время HbA1c < 7,0 %, продолжали лечение без изменений (наблюдательная группа, n = 498, или 61 %). Остальных пациентов рандомизировали на две группы для дальнейшей интенсификации лечения в течение последующих 52 недель. Больные группы «рандомизированное лечение» (РЛ, n = 162) получали тройную терапию — лираглутидом в комбинации с метформином и инсулином детемир, а пациенты группы «рандомизированный контроль» (РК, n = 161) продолжали получать лираглутид в комбинации с метформином без инсулина. Результаты показали, что достигнутое в начальный период снижение показателя HbА1с (с 8,3 до 7,6 %, Δ = –0,6 %) продолжилось и далее в группе РЛ (снижение до 7,1 %, Δ = –0,5 %), а в группе РК показатель HbА1с оставался почти на том же уровне (7,5 %, Δ = –0,01 %) в течение 52 недель. Доля пациентов, достигших целевого уровня HbА1с, в группе РЛ составила 52 %, в группе РК — 22 % (Р < 0,05). Первоначальное снижение массы тела (Δ = –3,5 кг) осталось почти неизменным в группе РЛ (Δ = –0,05 кг) и продолжилось в группе РК (Δ = –0,02 кг), Р < 0,05. В целом у больных СД 2-го типа длительная терапия метформином с добавлением лираглутида с инсулином или без него позволила либо поддерживать на удовлетворительном уровне, либо улучшить гликемический контроль при устойчивой потере массы и низкой частоте случаев гипогликемии в обеих группах (0,034–0,228 события/пациент/год) (Rosenstock, 2013; Zhang, 2016; Tzefos, 2012).
Как известно, для контроля гипергликемии у пациентов с CД 2-го типа с высокой степенью инсулинорезистентности (ИР) могут потребоваться высокие дозы инсулина, что приводит к ухудшению его абсорбции, дискомфорту и несоблюдению пациентами предписанного режима. В таких случаях предпочтительно использовать средства, сглаживающие неблагоприятные побочные эффекты инсулина (Buse, 2011; Vora, 2013; Lane, 2014; Kevin, 2013), такие как аналоги ГПП‑1. Подтверждением целесообразности использования указанной рекомендации являются результаты научной работы, проведенной в Швеции на базе 13 медицинских учреждений. В рандомизированное двойное слепое плацебо-контролируемое исследование были включены больные СД 2-го типа с неадекватным гликемическим контролем (HbA1c ≥ 7,5 %) и ожирением (ИМТ 27,5–45,0 кг/м2), которым в течение дня требовались многократные инъекции инсулина (суточная доза составляла более 100 ед.). 124 пациента были рандомизированы на 2 группы (1 : 1), получавшие подкожные инъекции лираглутида (титрация от 0,6 мг до 1,2 и 1,8 мг в день) или плацебо. Через 24 недели в группе, получавшей лираглутид, уровень HbA1c снизился на 1,5 %, в отличие от показателя в группе плацебо (–0,4 %); масса тела уменьшилась на 3,8 кг (без изменения в группе плацебо), суточная доза инсулина снизилась на 18,1 ед. (в группе плацебо — на 2,3 ед.), уменьшились колебания глюкозы в течение суток. Несмотря на краткосрочность наблюдения, получен очевидный положительный результат от дополнительного назначения лираглутида больным СД 2-го типа с выраженной инсулинорезистентностью, получающим высокие дозы экзогенного инсулина (Lind, 2012, 2015).
В унисон с выводами ряда зарубежных исследований о целесообразности применения ГПП‑1 у пациентов, получающих высокие дозы инсулина, к аналогичным заключениям пришли и отечественные врачи-эндокринологи. Особенности их лечебной тактики представлены в виде клинического случая далее.
Пациентка Ч., 66 лет, болеет СД 2-го типа с 47-летнего возраста. Длительное время получала ПССП, однако в течение последних 10 лет принимает терапию инсулином короткого и пролонгированного действия. На момент инициации инсулинотерапии показатель ИМТ составлял 38,1 кг/м2. Ввиду постоянного нарушения диеты и прогрессирующего ожирения доза инсулина в течение первого года применения составила 1,0 ЕД/кг без достижения компенсации углеводного обмена
Для предотвращения значительного увеличения дозы инсулина пациентке назначен прием метформина по 1000 мг 2 раза в сутки, но должный эффект не был получен. Через 3 месяца к метформину добавлен ситаглиптин в виде фиксированной комбинации 50/1000 мг, что улучшило компенсацию углеводного обмена (уровень НвА1с через 6 мес. снизился до 8,8 %), однако не привело к снижению веса (ИМТ — 43,8 кг/м2, окружность талии (ОТ) — 132 см). В дальнейшем пациентке был рекомендован прием третьего препарата — дапаглифлозина 10 мг в сутки. Ввиду развития в течение месяца инфекции мочевыводящих путей прием последнего был отменен, а доза инсулина увеличена до 130 ЕД/сутки (1,13 ЕД/кг).
Учитывая значительное увеличение веса и отсутствие адекватного контроля гликемии (HbA1c 8,6 %, колебания уровня глюкозы в плазме, по данным самоконтроля в течение суток, от 8,5 до 12,0 ммоль/л), пациентке назначен аналог ГПП‑1 — лираглутид в дозе 0,6 мг 1 раз в сутки подкожно в течение недели. В дальнейшем проведена титрация дозы до 1,2 мг и 1,8 мг с интервалом в 1 неделю, а прием фиксированной комбинации ситаглиптина с метформином 50/1000 мг заменен метформином в дозе 2500 мг в сутки. Применение лираглутида в течение 3 месяцев позволило уменьшить количество вводимого инсулина до 0,5 ЕД/кг, снизить вес на 13 кг (ИМТ составил 38,8 кг/м2). Последующий 3-месячный прием препарата привел к снижению ИМТ до 36,5 кг/м2 (Δ = –6 кг), доза инсулина уменьшилась до 0,4 ЕД/кг, уровень НвА1с снизился до 7,1 %.
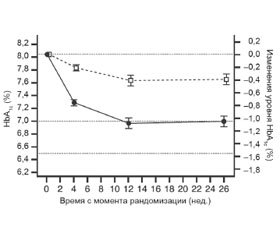
Следует отметить, что наличие выраженной ИР, ожирения, сопутствующей тяжелой кардиальной патологии является далеко не последним камнем преткновения на пути выбора надлежащей тактики лечения. Так, наличие диабетической нефропатии у пациентов с СД 2-го типа нередко заставляет отказаться от применения тех или иных сахароснижающих средств ввиду отсутствия данных об их безопасном использовании при патологии почек. В этом контексте стоит отметить, что в 2014 году Комитет по лекарственным средствам, предназначенным для применения у человека (Committee for Medicinal Products for Human Use, CHMP) Европейского агентства по лекарственным средствам (European Medicines Agency, EMA) вынес положительное решение относительно применения препарата лираглутид (Victoza®/liraglutide) для лечения взрослых с СД 2-го типа с умеренной почечной недостаточностью. Вердикт был основан на показателях эффективности и безопасности, полученных в 26-недельном двойном слепом рандомизированном контролируемом клиническом исследовании LIRA-RENAL IIIb фазы. В исследовании приняли участие пациенты с неадекватным контролем углеводного обмена и расчетной скоростью клубочковой фильтрации 30–59 мл/мин/1,73 м2, которые получали лираглутид в дозе 1,8 мг один раз в день (n = 140) или плацебо (n = 139) в комбинации со стандартной терапией (ПССП или инсулин). Анализ полученных данных показал, что применение лираглутида не влияло на функцию почек и демонстрировало лучший гликемический контроль без увеличения риска гипогликемии (рис. 1). Однако количество гастроинтестинальных побочных эффектов, в основном тошноты и рвоты, было выше среди лиц, принимавших лираглутид, а не плацебо (35,7 и 17,5 % соответственно) (Davies, 2012).
Положительный клинический опыт применения лираглутида у пациентов с хронической болезнью почек получен также и в рамках повседневной клинической практики отделения возрастной эндокринологии и клинической фармакологии, один из которых приводим ниже.
Пациентка С., 70 лет, болеет СД-го 2 типа с 1986 года. Наследственность по СД не отягощена. Страдает ожирением с 40-летнего возраста, артериальной гипертензией — с 45 лет. С начала заболевания СД получала ПСС. В анамнезе острое нарушение мозгового кровообращения в 2004 году. К 2005 году у пациентки диагностированы следующие осложнения СД: нефропатия, пролиферативная ретинопатия (на фоне витректомии OD и лазерной коагуляции OS), дистальная полинейропатия, синдром диабетической стопы, нейроишемическая форма. В 2007 году проведена ампутация І пальца левой стопы по поводу возникшей гангрены.
С 2003 года пациентка принимает комбинированную терапию инсулином гларгин и метформином. В 2009 году в связи с прогрессированием нефропатии и снижением CКФ до 44 мл/мин/1,73 м2 прием метформина был отменен и пациентка продолжила прием гларгина в суточной дозе 40 Ед/сутки в комбинации с глимепиридом 3 мг в сутки. После отмены метформина вес пациентки в течение года увеличился на 13 кг. По поводу артериальной гипертензии получала: рамиприл 20 мг в сутки, урапидил 60 мг в сутки, доксазозин 4 мг в сутки, индапамид 2,5 мг в сутки, лерканидипина гидрохлорид 20 мг в сутки, небиволола гидрохлорид 5 мг в сутки, торасемид 10 мг через день.
На момент госпитализации: рост — 164 см, вес — 118 кг, ИМТ — 43,9 кг/м2, окружность талии (ОТ) — 130 см, HbA1c — 8,8 %, уровень глюкозы в плазме (по данным самоконтроля) в течение суток варьирует от 6,5 до 13,0 ммоль/л, показатель креатинина — 165 мкмоль/л, CКФ (MDRD) — 31 мл/мин/1,73 м2, АД — 170/80 мм рт.ст. Принимая во внимание прогрессирование хронической почечной недостаточности (ХПН), проведено исследование показателя NT-proBNP (N-терминальный мозговой натрийуретический пропептид), который составил 398 пг/мл (при норме до 125 пг/мл), что указывает на развитие кардиоренального синдрома (КРС) и сердечной недостаточности. С учетом значительного увеличения веса и отсутствия адекватного контроля гликемии пациентке был назначен препарат лираглутид в дозе 0,6 мг 1 раз в сутки подкожно в течение недели с последующим увеличением дозы до 1,2 мг. Ввиду сниженного показателя СКФ дальнейшая титрация дозы лираглутида не проводилась. В течение первого месяца пациентка отметила уменьшение аппетита и количества потребляемой пищи, особенно во второй половине дня, уровень гликемии не превышал 7–8 ммоль/л в течение дня. Суточная доза гларгина в течение первого месяца снизилась на 6 ед. За 6-месячный период лечения проведена отмена глимепирида, доза инсулина снизилась до 24 Ед/сутки, уровень НвА1с составил 7,3 %, масса тела снизилась на 15 кг.
Следует особо отметить, что СКФ у пациентки за 6 месяцев при ежемесячном мониторировании уровня креатинина составила 34–39 мл/мин/1,73 м2, показатель NT-proBNP снизился до 180 пг/мл, а уровень АД поддерживался в пределах 140/80 — 150/90 мм рт.ст., что свидетельствует о стабилизации ХПН и уменьшении тяжести КРС.
Рассматривая вышеизложенный клинический случай, стоит упомянуть о том, что у пациентов с конечными стадиями почечной недостаточности кардиоваскулярные заболевания являются основной причиной смерти. Сочетание сердечной и почечной недостаточности относится к так называемому кардиоренальному синдрому. Повышение показателя NT-proBNP при почечной недостаточности происходит вследствие увеличивающегося количества внутрисосудистой жидкости и ухудшения функции сердца и является предиктором смертности у пациентов с сердечной недостаточностью, а также популяционным маркером развития хронической сердечной недостаточности, острого коронарного синдрома в целом и инфаркта миокарда в частности. Таким образом, выявленный дополнительный положительный эффект терапии лираглутидом, попадающий, на наш взгляд, в фокус научно-исследовательского интереса, а именно снижение NT-proBNP, свидетельствует о потенциальной возможности уменьшения риска смерти от кардиоваскулярных причин у пациентов с умеренной почечной недостаточностью.
В соответствии с рекомендациями совместного консенсуса Американской диабетической ассоциации и Европейского общества по изучению сахарного диабета (Inzucchi S.E., 2012, 2015) назначение сахароснижающей терапии пациентам с СД 2-го типа следует проводить поэтапно, что обусловлено степенью декомпенсации углеводного обмена. Как следует из алгоритма, в случае недостижения целевого уровня HbA1c ≤ 7 % при использовании монотерапии метформином аналоги ГПП‑1 могут применяться в качестве средств второй линии, а в комбинации с инсулином — третьей линии терапии. Однако стоит подчеркнуть, что на сегодняшний день все активнее закладываются основы персонифицированного подхода к лечению больных сахарным диабетом 2-го типа, в том числе в зависимости от их фенотипических особенностей. В соответствии с разработанной отделом возрастной эндокринологии и клинической фармакологии ГУ «Институт эндокринологии и обмена веществ им. В.П. Комиссаренко НАМН Украины» концепции метаболический фенотип у больных СД 2-го типа может быть представлен тремя вариантами, имеющими в основе различные механизмы формирования, а соответственно, и внешние проявления (Корпачев, 2016). Особенности фенотипа больного с СД 2-го типа тесно связаны с нарушением различных гормонально-метаболических процессов. Так, развитие алиментарно-кинетического фенотипа (АКФ) происходит при дисбалансе между расходованием и поступлением в организм энергетического материала. Психосоциальный фенотип формируется за счет инстинктов самосохранения и самореализации, гормонально-метаболическое обеспечение которых предопределяется действием глюкокортикостероидов (в частности, кортизола). Адипозо-висцеральный фенотип (АВФ) обусловлен перераспределением влияния половых стероидных гормонов, дегидроэпиандростерона и дегидроэпиандростеронсульфата, что связано с особенностями сексуальной активности в преклонном возрасте. Несмотря на неодинаковые причины формирования АКФ и АВФ, оба характеризуются наличием избыточной жировой ткани в организме (АКФ — преимущественно подкожное распределение жира, АВФ — висцеральное). При психосоциальном фенотипе ожирения не наблюдается, однако на первый план в его формировании выступают эффекты контринсулярных гормонов. На наш взгляд, логичным было бы применение лираглутида у пациентов с АКФ и АВФ с целью достижения компенсации углеводного обмена, снижения массы тела, нормализации показателей липидного обмена. Ввиду того что аналоги ГПП‑1 оказывают экстрапанкреатическое воздействие, направленное на коррекцию сердечно-сосудистых осложнений, их применение у лиц с психосоциальным фенотипом также представляется небезосновательным, однако требуется проведение дополнительных исследований в этом направлении. Концепция дифференцированного применения инкретинов у пациентов с СД 2-го типа с различными нарушениями гормонально-метаболического баланса, отражающимися на особенностях их фенотипов, выступает патогенетически обоснованным перспективным направлением в диабетологии, а потенциальная возможность коррекции ключевых возрастных изменений с помощью аналогов ГПП‑1 представляется весьма реальной.
В целом широкий спектр разнонаправленного влияния аналогов ГПП‑1, в частности лираглутида, открывает новые горизонты их применения не только у пациентов с СД 2-го типа, но и у лиц без дисгликемических состояний.
Список литературы
1. Анциферов М.Б. Глюкагоноподобный пептид‑1: от физиологии к эффективному управлению сахарным диабетом 2-го типа // Фарматека. — 2012. — № 3. — С. 9-15
2. Корпачев В.В. и др. Руководство по клиническому изучению сахароснижающих лекарственных средств у больных сахарным диабетом: Методические рекомендации. — К.: Авиценна, 2005. — 96 с.
3. Корпачев В.В. Инсулин и инсулинотерапия. — К.: Тріумф, 2001. — 454 с.
4. Корпачев В.В. Калиевые каналы и механизм действия производных сульфонилмочевины // Укр. мед. часопис. — 2002. — № 3 (29), V/VI. — С. 16-22.
5. Корпачев В.В. Механизмы действия, безопасность и переносимость глиптинов — нового класса противодиабетических препаратов с инкретиновым эффектом / В.В. Корпачев, Н.М. Гурина // Международный эндокринологический журнал. — 2011. — № 7 (39). — С. 17-22.
6. Корпачев В.В., Гурина Н.М. Онглиза™ (саксаглиптин) — ингибитор дипептидилпептидазы‑4: инкретиновый эффект и клиническое применение / В.В. Корпачев // Международный эндокринологический журнал. — 2011. — № 1 (33). — С. 24-36.
7. Корпачев В.В., Прибила О.В., Корпачева-Зиныч О.В., Кушнарева Н.Н., Гурина Н.М., Ковальчук А.В. Антропометрические, гормональные и биохимические маркеры метаболических фенотипов у больных сахарным диабетом 2-го типа // Universum: Медицина и фармакология: электрон. научн. журн. — 2016. — № 1–2 (24). URL: http://7universum.com/ru/med/archive/item/2945 (дата обращения: 24.10.2016).
8. Панькив В.И. Инкретины: новая веха в лечении сахарного диабета 2-го типа. Bозможности ситаглиптина в достижении компенсации сахарного диабета 2-го типа // Международный эндокринологический журнал. — 2011. — № 6 (38). — С. 6-12.
9. Anagnostis P., Athyros V.G., Adamidou F., Panagiotou A., Kita M., Karagiannis A., Mikhailidis D.P. Glucagon-like peptide‑1-based therapies and cardiovascular disease: looking beyond glycaemic control // Diabetes Obes. Metab. — 2011. — V. 13 (4). — P. 302-312.
10. Bose A.K., Mocanu M.M., Carr R.D. et al. Glucagon-like peptide 1 can directly protect the heart against ischemia/reperfusion injury // Diabetes. — 2005. — V. 54. — P. 146-151.
11. Buse J.B., Bergenstal R.M., Glass L.C. et al. Use of twice-daily exenatide in basal insulin-treated patients with type 2 diabetes: a randomized controlled trial // Ann. Intern. Med. — 2011. — V. 154. — P. 103-112.
12. Davies M.J., Bain S.C., Atkin S.L. et al. Efficacy and Safety of Liraglutide Versus Placebo as Add-on to Glucose-Lowering Therapy in Patients With Type 2 Diabetes and Moderate Renal Impairment (LIRA-RENAL): A Randomized Clinical Trial // Diabetes Care. — 2016. — V. 39 (2). — P. 222-230.
13. Davies M.J., Bain S.C., Atkin S.L. et al. Sequential Intensification of Metformin Treatment in Type 2 Diabetes with Liraglutide Followed by Randomized Addition of Basal Insulin Prompted by A1C Targets // Diabetes Care. — 2012. — V. 35. — P. 1446-1454.
14. Dejgaard‑2 T.F., Frandsen C., Holst J., Madsbad S. Liraglutide for treating type 1 diabetes // Expert Opin. Biol. Ther. — 2016. — V. 16, № 4. — P. 579-590.
15. Dejgaard T.F., Frandsen C.S., Hansen T.S., Almdal T. Efficacy and safety of liraglutide for overweight adult patients with type 1 diabetes and insufficient glycaemic control (Lira‑1): a randomised, double-blind, placebo-controlled trial // Lancet Diabetes Endocrinol. — 2016. — V. 4, № 3. — P. 221-232.
16. Drucker D. Glucagon-like peptides: regulators of cell proliferation, differentiation, and apoptosis // Mol. Endocrinol. — 2003. — 17. — P. 161-171.
17. Drucker D., Philippe J., Mojsov S. et al. Glucagon-like peptide‑1 stimulates insulin gene expression and increases cyclic FMP levels in a rat islet cell line // Proc. Natl. Acad. Sci. USA. — 1987. — V. 84. — P. 3434-3438.
18. Dupre J., Behme M.T., McDonald T.J. Exendin‑4 normalized postcibal glycemic excursions in type 1 diabetes // J. Clin. Endocr. Metab. — 2004. — V. 89. — P. 3469-3473.
19. Elbrond B., Jakobsen G., Larsen S. et al. Pharmacokinetics, pharmacodynamics, safety, and tolerability of a single-dose of NN2211, a long-acting glucagon-like peptide 1 derivative, in healthy male subjects // Diabetes Care. — 2002. — V. 25. — P. 1398-1404.
20. Elrick H., Stimmler L., Hlad C., Arai Y. Plasma insulin response to oral and intravenous glucose administration // J. Clin. Endocrinol. Metab. — 1964. — V. 24. — P. 1076-1082.
21. Frandsen C.S., Dejgaard T.F., Holst J., Andersen H., Thorsteinsson B., Madsbad S. Twelve-Week Treatment With Liraglutide as Add-on to Insulin in Normal-Weight Patients With Poorly Controlled Type 1 Diabetes: A Randomized, Placebo-Controlled, Double-Blind Parallel Study // Diabetes Care. — 2010. — V. 38 (12). — P. 2250-2157.
22. Garber A. Incretin effects on beta-cell function, replication and mass: the human perspective // Diabetes Care. — 2011. — V. 34 (2). — P. 258-263.
23. Inzucchi S.E., Bergensta R.M., Buse J.B. et al. Management of hyperglycemia in type 2 diabetes: a patient-centered approach. Position statement of the American Diabetes Association (ADA) and the European Association for the Study of Diabetes (EASD) // Diabetes Care. — 2012. — V. 35. — P. 1364-1379.
24. Inzucchi S.E., Bergensta R.M., Buse J.B. et al. Management of hyperglycemia in type 2 diabetes, 2015: a patient-centered approach: update to a position statement of the American Diabetes Association and the European Association for the Study of Diabetes // Diabetes Care. — 2015. — V. 38 (1). — P. 140-149.
25. Halland M., Bharucha A.E. Relationship Between Control of Glycemia and Gastric Emptying Disturbances in Diabetes Mellitus // Clin. Gastroenterol. Hepatol. — 2016. — V. 14 (7). — P. 929-936.
26. Jadinsky M., Pfutzner A., Paz-Pacheco E. Saxagliptin given in combination with metformin in patients with type 2 diabetes, compared with either monotherapy: a randomised controlled trial // Diabetes Obes. Metab. — 2009. — V. 10. — P. 110-115.
27. Kahn S.E., Haffner S.M., Heise M.A. et al. ADOPT Study Group. Glycemic durability of rosiglitazone, metformin, or glyburide monotherapy // N. Engl. J. Med. — 2006. — V. 355. — P. 2427-2443.
28. Kevin M. Pantaloneand Charles Faiman Liraglutide Effective in the Severely Insulin-Resistant Patient with Type 2 Diabetes Requiring U‑500 Insulin: A Case Report // Diab. Techn. Ther. — 2013. — V. 15 (4). — P. 342-343.
29. Kielgast U., Krarup T., Holst J.J., Madsbad S. Four weeks of treatment with liraglutide reduces insulin dose without loss of glycemic control in type 1 diabetic patients with and without residual beta-cell function // Diabetes Care. — 2011. — V. 34 (7). — P. 1463-1468.
30. King A.B., Montanya E., Pratley R.E., Blonde L., Svendsen C.B., Donsmark M., Sesti G. Liraglutide achieves A1C targets more often than sitagliptin or exenatide when added to metformin in patients with type 2 diabetes and a baseline A1C < 8.0 % // Endocr. Pract. — 2013. — V.19 (1). — P. 64-72.
31. Knudsen L.B. et al. Potent derivatives of glucagon-like peptide‑1 with pharmacokinetic properties suitable for once daily administration // J. Med. Chem. — 2000. — V. 43 (9). — P. 1664-1669.
32. Lane W., Weinrib S., Rappaport J., Hale C. The effect of addition of liraglutide to high-dose intensive insulin therapy: a randomized prospective trial // Diabetes Obes. Metab. — 2014. — 16 (9). — P. 827-32.
33. Lee S.J., Diener K., Kaufman S., Krieger J. et al. Limiting glucocorticoid secretion increases the anorexigenic property of Exendin‑4 // Mol. Metab. — 2016. — V. 5 (7). — P. 552-565.
34. Lee Y., Jun H.S. Anti-diabetic actions of glucagon-like peptide‑1 on pancreatic beta-cells // Metabolism. — 2014. — 63 (1). — P. 9-19.
35. Leech C.A., Dzhura I., Chepurny O.G., Kang G., Schwede F., Genieser H.G., Holz G.G. Molecular physiology of glucagon-like peptide‑1 insulin secretagogue action in pancreatic β cells // Prog. Biophys. Mol. Biol. — 2011. — V. 07 (2). — P. 236-247.
36. Lind M., Jendle J., Torffvit O., Lager I. Glucagon-like peptide (GLP‑1) analogue combined with insulin reduces HbA1c and weight with low risk of hypoglycemia and high treatment satisfaction // Prim. Care Diabetes. — 2012. — V. 6. — P. 41-46.
37. Lind M., Hirsch I.B., Tuomilehto J., Dahlqvist S. et al. Liraglutide in people treated for type 2 diabetes with multiple daily insulin injections: randomised clinical trial (MDI Liraglutide trial) // BMJ. — 2015. — V. 351:h5398.
38. Mathieu C., Rodbard H.W., Cariou B. et al. BEGIN: VICTOZA ADD-ON (NN1250-3948) study group. A comparison of adding liraglutide versus a single daily dose of insulin aspart to insulin degludec in subjects with type 2 diabetes (BEGIN: VICTOZA ADD-ON) // Diabetes Obes. Metab. — 2014. — V. 16, № 7. — P. 636-644.
39. Mikhail N. Incretin mimetics and dipeptidyl peptidase 4 inhibitors in clinical trials for the treatment of type 2 diabetes // Expert Opin Investig Drugs. — 2008. — V. 17 (6). — P. 845-853.
40. Nadkarni P., Chepurny O.G., Holz G.G. Regulation of glucose homeostasis by GLP‑1 // Prog Mol Biol Transl Sci. — 2014. — V. 121. — P. 23-65.
41. Nathan D.M., Buse J.B., Davidson M.B. et al. Medical management of hyperglycemia in type 2 diabetes: a consensus algorithm for the initiation and adjustment of therapy. A consensus statement of the American Diabetes Association and the European Association for the Study of Diabetes // Diabetologia. — 2009. — V. 52. — P. 17-30.
42. Nauck M., Heimesaat M., Orskov C. et al. Preserved incretin activity of glucagon-like peptide‑1 (7-36) amide but not not synthetic human gastric inhibitory polypeptide in patients with type‑2 diabetes mellitus // J. Clin. Invest. — 1993. — V. 91. — P. 301-307.
43. Nauck M., Homberger F., Siegel E. et al. Incretin effects of increasing glucose loаds in man calculated from venous insulin and C-peptide responses // J. Clin. Endocrinol. Metab. — 1986. — V. 63. — P. 492-498.
44. Nauck M., Frid A., Hermansen K., Thomsen A.B., During M., Shah N., Tankova T., Mitha I., Matthews D.R. Long-term efficacy and safety comparison of liraglutide, glimepiride and placebo, all in combination with metformin in type 2 diabetes: 2-year results from the LEAD‑2 study // Diabetes Obes. Metab. — 2013. — V. 15, № 3. — P. 204-212.
45. Nikolaidis L.A., Mankad S., Sokos G.G. et al. Effects of glucagon-like peptide‑1 in patients with acute myocardial infarction and left ventricular dysfunction after successful reperfusion // Circulation. — 2004. — 109. — 962-5.
46. Nystrom T., Gutniak M.K., Zhang Q. et al. Effects of glucagon-like peptide‑1 on endothelial function in type 2 diabetes patients with stable coronary artery disease // Am. J. Physiol. Endocrinol. Metab. — 2004. — V. 287. — P. 1209-1215.
47. Pieber T.R., Deller S., Korsatko S., Jensen L., Christiansen E., Madsen J., Heller S.R. Counter-regulatory hormone responses to hypoglycaemia in people with type 1 diabetes after 4 weeks of treatment with liraglutide adjunct to insulin: a randomized, placebo-controlled, double-blind, crossover trial // Diabetes Obes. Metab. — 2015. — V. 17 (8). — P. 742-750.
48. Pinelli N.R., Hurren K.M. Efficacy and safety of long-acting glucagon-like peptide‑1 receptor agonists compared with exenatide twice daily and sitagliptin in type 2 diabetes mellitus: a systematic review and meta-analysis // Ann. Pharmacother. — 2011. — V. 45 (7–8). — P. 850-860.
49. Raman V.S., Mason K.J., Rodriguez L.M., Hassan K., Yu X., Bomgaars L., Heptulla R.A. The role of adjunctive exenatide therapy in pediatric type 1 diabetes // Diabetes Care. — 2010. — V. 33 (6). — P. 1294-1296.
50. Riedel A.A. et al. Secondary failure of glycemic control for patients adding thiazolidinedione or sulfonylurea therapy to a metformin regimen // Am. J. Manag. Care. — 2007. — V. 13. — P. 457-463.
51. Rodbard H.W. et al. Statement by an American Association of Clinical Endocrinologists / American College of Endocrinology consensus panel on type 2 diabetes mellitus: an algorithm for glycemic control // Endocr. Pract. — 2009. — V. 15. — P. 540-559.
52. Rosenstock J., Rodbard H.W., Bain S.C. et al. (Liraglutide-Detemir Study Group). One-year sustained glycemic control and weight reduction in type 2 diabetes after addition of liraglutide to metformin followed by insulin detemir according to HbA1c target // J. Diab. Complic. — 2013. — V. 27. — P. 492-500.
53. Schjoldager B., Mortensen P., Christiansen J. et al. GLP‑1 (glucagon-like peptide‑1) and truncated GLP‑1, fragments of human proglucagon, inhibit gastric acid secretion in humans // Dig. Dis. Sci. — 1989. — V. 34. — P. 703-708.
54. Shyangdan D., Cummins E., Royle P., Waugh N. Liraglutide for the treatment of type 2 diabetes // Health Technol. Assess. — 2011. — V. 15 (1). — P. 77-86.
55. Steensgaard D.B. et al. The molecular basis for the delayed absorption of the once-daily human GLP‑1 analogue, liraglutide // Diabetes. — 2008. — V. 57 (1). — A164.
56. Sun F., Chai S., Li L., Yu K., Yang Z., Wu S., Zhang Y., Ji L., Zhan S. Effects of glucagon-like peptide‑1 receptor agonists on weight loss in patients with type 2 diabetes: a systematic review and network meta-analysis // J. Diabetes Res. — 2015. — V. 2015. — Article ID157201.
57. Tucker M.E. New Era’ of Type 2 Diabetes Treatment as LEADER Unveiled? // N. Engl. J. Med. — 2016. — Published online June 13, 2016.
58. Tzefos M., Olin J. Glucagon-like peptide‑1 analog and insulin combination therapy in the management of adults with type 2 diabetes mellitus // Ann. Pharmacother. — 2010. — V. 44. — P. 1294-1300.
59. Varanasi A., Bellini N., Rawal D., Vora M., Makdissi A., Dhindsa S., Chaudhuri A., Dandona Liraglutide as additional treatment for type 1 diabetes // Eur. J. Endocrinol. — 2011. — V. 165 (1). — P. 77-84.
60. Vergès B., Bonnard C., Renard E. Beyond glucose lowering: glucagon-like peptide‑1 receptor agonists, body weight and the cardiovascular system // Diabetes Metab. — 2011. — V. 37 (6). — P. 477-488.
61. Vilsboll T. et al. Defective amplification of the late phase insulin response to glucose by GIP in obese type II diabetic patients // Diabetologia. — 2002. — V. 45. — P. 1111-1119.
62. Vora J., Bain S.C., Dzida T. et al. Incretin-based therapy in combination with basal insulin: a promising tactic for the treatment of type 2 diabetes // Diabetes Metab. — 2013. — V. 39. — P. 6-15.
63. Zhang L., Zhang M., Zhang Y., Tong N. Efficacy and safety of dulaglutide in patients with type 2 diabetes: a meta-analysis and systematic review // Sci. Rep. — 2016. — 6, Article number: 18904.

/40.jpg)