Статтю опубліковано на с. 13-19
Вступ
Хвороба малих судин (ХМС) мозку є захворюванням, що притаманне капілярам і малим перфоруючим артеріолам [1]. Навіть за відсутності судинної патології, що фізично обмежує церебральний кровотік, капілярна дисфункція є джерелом інсультоподібної симптоматики та нейродегенерації [2, 3]. У подальшому морфоструктурні зміни мозку у пацієнтів з ХМС мозку призводять до погіршення фізичного стану хворих, зниження когнітивних функцій та якості життя. На думку деяких авторів, найбільш ефективним підходом у встановленні ймовірності церебральної атрофії (ЦА) при ХМС мозку є визначення зв’язку між нею та маркерами ХМС мозку [4–8]. Однак на цей час через розбіжності у дизайні та методах оцінки [4] погляди дослідників на зв’язок ХМС мозку з морфоструктурними змінами дуже різняться. Деякі автори розглядають ХМС мозку як чинник ризику церебральної атрофії, але при цьому не пов’язують атрофічні зміни з тяжкістю ХМС мозку [5], а деякі дослідники, навпаки, вважають, що тяжкість ХМС мозку є тісно пов’язаною з ЦА, і саме патерн ЦА відрізняє тяжкість цієї хвороби від старіння та може бути предиктором кількісної оцінки тяжкості загального бала за ХМС мозку [6, 7]. Також існує думка, що ЦА є не лише асоційованою з ХМС мозку, а може розглядатися поряд з асимптомними ураженнями мозку як ознака цієї хвороби [8]. Однією з причин розбіжностей у поглядах на зв’язок між ЦА і ХМС мозку та її тяжкістю може бути надання переваги лише або типу маркерів ХМС мозку, або їх кількості [4–8]. Чітке визначення ризику ЦА при ХМС мозку за маркерами останньої потребує комплексного підходу з урахуванням одночасно якісних і кількісних ознак хвороби, за допомогою якого було б можливим визначення предикативної цінності як окремих маркерів, так і різних їх комбінацій.
Матеріали та методи
Для визначення найбільш адекватного методу оцінки ймовірності ЦА при ХМС мозку за маркерами цієї хвороби було проведено ретроспективне когортне дослідження, у яке було включено 308 пацієнтів (у тому числі 148 жінок) із ХМС мозку віком від 50 до 85 років (середній вік — 64,54 ± 0,45 року), без інсульту в анамнезі, які проходили стаціонарне лікування у відділенні судинної патології головного мозку ДУ «ІНПН НАМН України» (2011–2014 рр.). Діагноз ХМС мозку встановлювався при виявленні під час проведення магнітно-резонансної томографії (у режимі дифузно-зваженої візуалізації та FLAIR-режимах (матриця = 256 × 256)) одного або більше МРТ-маркерів хвороби: розширення периваскулярних просторів (рПВП) [9]; гіпер-/гіпоінтенсивність білої речовини (ГБР) мозку [10], що є МРТ-проявом лейкоареозу (ЛА); «німі» інфаркти мозку (НІМ); церебральні мікрокрововиливи (цМКВ) [1, 3, 7]. Тяжкість ХМС мозку було визначено у діапазоні від 0 до 4 балів за допомогою шкали загального бала за ХМС мозку [4, 5, 11], згідно з якою в 1 бал окремо оцінювалася наявність на МРТ: будь-якої кількості цМКВ [7]; НІМ [7]; рПВП у 2–4 бали за Semi quantitative scale [9]; ГБР мозку у 2–3 бали за Fazekas scale [10]. Оцінку значущості характеристик ХМС мозку (тяжкість, окремі маркери хвороби та їх комбінації) було проведено одночасно за кількома дизайнами, які використовували інші автори [5–8].
Статистичну обробку даних проведено за допомогою t-критерію Стьюдента. Для оцінки зв’язку чинників судинного ризику з ХМС мозку було застосовано регресійний аналіз, результати якого наведено у вигляді очікування шансів у 95% з довірчим інтервалом (ОR, 95% СІ); також було розраховано значення відносного ризику з точністю 95 % випадків та з довірчим інтервалом (RR, 95% СІ).
Прогностичну модель для опису ймовірності ЦА при ХМС мозку (1) було розроблено за допомогою логістичної регресії за рівнянням (2):
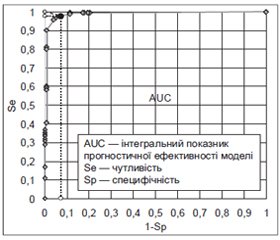
де Pi — ймовірність події для i-го пацієнта, Zi — результат стандартного рівняння регресії, β0 — вільний член (інтерцепт), хj — j-й предиктор, βj — j-й коефіцієнт предиктора, m — кількість предикторів. Встановлення найкращого співвідношення показників чутливості (Se) та специфічності (Sp) логіт-моделі було проведено за допомогою ROC-аналізу (Receiver Operator Characteristic) з подальшим обчисленням інтегрального показника прогностичної ефективності моделі (AUC) (Area Under Curve):
Якість прогностичної цінності моделі оцінювалася за міжнародною експертною шкалою M.H. Zweig, G. Campbell [12]. Середньозважену ймовірність морфоструктурних змін мозку було розраховано за формулою:
де wi — частка пацієнтів з і-комбінацією, а pi — ймовірність події у пацієнтів з і-комбінацією.
Результати
Під час МРТ-дослідження 308 пацієнтів з ХМС мозку ознаки церебральної атрофії було виявлено у 185 хворих (60 %). Пацієнти з ЦА були того ж самого віку, що і хворі без ознак атрофічних змін мозку: 64,32 ± 0,60 та 64,88 ± 0,68 року відповідно, але, навпаки, відрізнялися за переважанням чоловіків: серед хворих з ЦА було 114 чоловіків (61,62 ± 3,59 %), а серед пацієнтів без ЦА — 46 (37,40 ± 4,38 %) (р = 0,00001).
При визначені зв’язку ЦА окремо з кожним маркером ХМС мозку було використано дизайн 1, за яким не бралися до уваги кількість та типи комбінації цих маркерів. Пацієнти з ЦА вірогідно відрізнялися від хворих без ознак атрофії за поширеністю усіх маркерів ХМС мозку (рис. 1).
Практично в усіх пацієнтів з ЦА (95 %) було виявлено ЛА, який у цих хворих спостерігався у 7 разів частіше, ніж у хворих без ЦА (р < 0,0001). Кількість цМКВ у пацієнтів з ЦА у 10 разів перевищувала цей показник пацієнтів без атрофічних змін (р < 0,0001), а поширеність НІМ — у 20 разів (р < 0,0001). Розбіжність між хворими з ЦА та без неї за кількістю випадків рПВП становила 5 % (р = 0,02).
У пацієнтів дослідженої когорти оцінка зв’язку ЦА з кожним з 4 маркерів ХМС мозку (дизайн 1) без урахування кількості та комбінації маркерів виявила високі показники очікування шансів атрофічних змін мозку, але на тлі дуже великих довірчих інтервалів, при наявності: ЛА (сукупний облік від 1 до 3 балів за Fazekas scale) (ОR 121,93; 95% CI 52,48–283,33) (р < 0,00001), НІМ (ОR 97,68; 95% CI 37,17–256,67) (р < 0,00001), цМКВ (ОR 13,62; 95% CI 4,13–44,89) (р < 0,00001) (табл. 1). У підсумку тільки 3 з 4 маркерів збільшували відносний ризик ЦА: ЛА — у 11,65 раза (95% CI 6,21–21,85), НІМ — у 4,14 (95% CI 3,11–5,52) та цМКВ — у 1,76 (95% CI 1,54–2,01) (табл. 1).
/15.jpg)
Для з’ясування можливостей впливу на розвиток ЦА прогресування рПВП та ЛА було застосовано дизайн 2 — деталізовану версію дизайну 1. За умовами нового дизайну 2 облік рПВП та ЛА проводився відповідно до вимог оцінювання тяжкості ХМС мозку [5, 11], тобто окремо аналізували зв’язок ЦА з випадками рПВП (2–4) (2–4 бали за Semi quantitative scale) та ЛА (2–3) (2–3 бали за Fazekas scale), кожний з яких оцінювався у 1 бал за шкалою тяжкості ХМС мозку, а окремо з випадками рПВП (1) та ЛА (1), які не збільшували тяжкість хвороби. У результаті подібної зміни дизайну обліку виявилося, що наявність зв’язку ЦА з рПВП залежала від прогресування останнього: випадки рПВП у 1 бал за Semi quantitative scale не були пов’язаними з ЦА, але рПВП у 2–4 бали за Semi quantitative scale у 2,12 раза (95% CI 1,82–2,49) збільшували відносний ризик атрофічних змін. У той же час ЦА була асоційованою з ЛА незалежно від бала за Fazekas scale, хоча сила цього зв’язку була у рази меншою, ніж при сукупній оцінці ЛА (табл. 1), а відносний ризик атрофічних змін мозку становив лише 1,66 (95% CI 1,43–1,94) при наявності ЛА (1) та 2,43 (95% CI 2,02–2,91) у випадках ЛА (2–3). Таким чином, усі маркери ХМС мозку мають тісний зв’язок з ЦА, винятком є лише легкі форми рПВП. У підсумку, за даними аналізу, дизайн (1 або 2) якого передбачав оцінку значущості для ЦА лише якості окремого маркера ХМС мозку, було показано, що ЦА є опосередковано асоційованою з ХМС мозку, оскільки саме маркери останньої виявилися чинниками ризику атрофічних змін мозку.
Визначення внеску тяжкості ХМС мозку у розвиток ЦА за дизайном 3 з урахуванням виключно кількості маркерів хвороби продемонструвало, що пацієнти з різним балом за шкалою тяжкості ХМС мозку, тобто з різною кількістю маркерів [4, 5, 11], відрізнялися за поширеністю ЦА: при 0 балів цей показник становив 1,87 %; при 1 балі — 76 % (р < 0,0001); при 2 балах — 98,5 %; у хворих з 3–4 балами за ХМС мозку ЦА спостерігалася у 100 % випадків (р < 0,001). Очікування шансів для ЦА при тяжкості хвороби у 1 бал становило 2,57 (95% СІ 1,41–4,69); при 2 балах — 66,08 (95% СІ 9,02–483,93), а тяжкість у 3–4 бали була асоційована з ЦА. Відносний ризик наявності ЦА: при 1 балі цей ризик збільшувався в 1,38 (95% СІ 1,16–1,64); при 2 балах — в 1,99 (95% СІ 1,74–2,26); при 3 балах — в 1,87 (95% СІ 1,67–2,10); при 4 балах — в 1,75 (95% СІ 1,58–1,93). Таким чином, за результатами аналізу зв’язку ЦА з тяжкістю ХМС мозку за дизайном 3 чинником ризику ЦА є наявність одночасно двох та більше маркерів хвороби незалежно від їх якості та комбінації.
Кожний з трьох застосованих дизайнів оцінки ризику розвитку ЦА при ХМС мозку за маркерами цієї хвороби, маючи на меті висвітлення лише одного питання (зв’язок ЦА з певним типом маркера), завжди відокремлював комбінаційні, а також кількісні або якісні характеристики маркерів хвороби, викривлюючи таким чином дійсність. Найбільш адекватним методом визначення реального впливу на розвиток ЦА одночасно кількості, якості та комбінації 4 маркерів ХМС мозку може бути використання логіт-моделі. Результатом логістичної регресії даних когорти з 308 пацієнтів з ХМС мозку стала логіт-модель (А) для ЦА з наступним рівнянням:
/16.jpg)
де β0 = –4,90 — вільний член (інтерцепт), хn — бінарний показник наявності маркера ХМС (хn = 0 або хn = 1); х1 — рПВП; х2 — ЛА; х3 — НІМ; х4 — цМКВ. При точці відсічення 0,5 показник прогностичної цінності логіт-моделі (В) становив 99,33 %, чутливості — 90,09 %, специфічності — 97,17 % (рис. 2), а рівень значущості за тестом Хосмера — Лемешева 15,93 підтвердив високу відповідність розробленої моделі реальним даним.
Згідно з розробленою логіт-моделлю (А) при окремому розвитку ЛА має дуже низьку прогностичну силу відносно атрофічних змін мозку (57 %), НІМ є випадковим класифікатором, а наявність у пацієнта виключно рПВП або цМКВ не може бути предиктором ЦА при ХМС мозку (рис. 3). У той же час поєднання ЛА з будь-яким іншим маркером, як і комбінація НІМ з цМКВ, підвищують імовірність наявності ЦА від 93 до 99 % (рис. 3).
Випадки, коли облік рПВП та ЛА проводиться з оцінюванням їх прогресування, потребують розширеної логіт-моделі (В) для ЦА при ХМС мозку, рівняння якої, відповідно, має інший вигляд через збільшення кількості показників, значення інтерцепту та коефіцієнтів:
де β0 = –5,22 — вільний член (інтерцепт), хn — бінарний показник наявності маркера ХМС (хn = 0 або хn = 1); х1 — рПВП (1); х2 — рПВП (2–4); х3 — ЛА (1); х4 — ЛА (2–3); х5 — НІМ; х6 — цМКВ. При точці відсічення 0,5 показник прогностичної цінності даної логіт-моделі становив 99,20 %, чутливості — 97,84 %, специфічності — 92,68 % (рис. 4), високу відповідність реальним даним та вірогідність даної розширеної версії моделі підтвердив рівень значущості за тестом Хосмера — Лемешева (32,56).
Згідно з розширеною версією логіт-моделі (В), у пацієнтів з ХМС мозку при наявності одного маркера незначна ймовірність ЦА існує лише у випадку, якщо цим маркером є НІМ (Рі = 0,59) (рис. 4). Окремий розвиток трьох інших маркерів ХМС мозку не може бути предиктором ЦА при ХМС мозку (рис. 5). У той же час поєднання рПВП (2–4) з ЛА (1–3) або ЛА (1–3) з НІМ підвищують імовірність наявності ЦА від 79 до 99 % (рис. 5). Тобто при ХМС мозку визначення імовірність ЦА шляхом визначення зв’язку лише з окремими маркерами (дизайн 1, 2) або за їх кількістю (дизайн 3) не відбиває реальної картини, оскільки відмінну предикторну ефективність мають не окремі маркери ХМС мозку, а одночасна наявність як мінімум двох маркеров, одним з яких має бути рПВП (2–4) або поєднання НІМ та ЛА (1–3). Оцінка середньозваженої ймовірності морфоструктурних змін мозку у дослідженій когорті пацієнтів з ХМС мозку підтвердила асоційованість ЦА з 3- і 4-бальною тяжкістю хвороби.
Обговорення
Під час ретроспективного когортного дослідження 308 пацієнтів з ХМС мозку одночасне використання декількох запропонованих різними авторами дизайнів оцінки зв’язку ЦА з ХМС мозку за допомогою маркерів хвороби [5–8] виявило слабкі місця цих підходів. За даними аналізу зв’язку ЦА з якістю маркерів ХМС мозку (дизайн 1, 2), будь-який з маркерів у рази збільшує відносний ризик атрофічних змін мозку. Але оцінка впливу тяжкості хвороби на ЦА (дизайн 3) продемонструвала, що лише наявність одночасно двох маркерів ХМС мозку будь-якої якості збільшує ризик ЦА. Вирішенням проблеми розбіжностей результатів при різних дизайнах аналізу ймовірності атрофічних змін при ХМС мозку, на нашу думку, може бути розроблена нами логіт-модель (А), яка, враховуючи більшість параметрів маркерів хвороби, дозволяє отримати чіткі відповіді стосовно зв’язку ЦА з ХМС мозку. У певних випадках, коли існує потреба у визначенні впливу прогресування рПВП та ЛА на ймовірність ЦА, може бути використано розширену версію логіт-моделі (В). Кількість пацієнтів із ХМС мозку (60 %), у яких було виявлено МРТ-ознаки ЦА, не дає можливості підтвердити думку деякі дослідників [5], що ЦА є чинником ризику цієї хвороби. Більше того, характер поширеності ЦА при ХМС мозку та її зв’язок з маркерами цієї хвороби свідчать про те, що ЦА є опосередковано асоційованою з ХМС мозку і через те не може бути незалежним маркером цієї хвороби, як вважають деякі автори [8]. На відміну від одних дослідників [6, 7] та відповідно до даних інших [5] нами було показано, що ЦА не є пов’язаною з балом тяжкості ХМС мозку, оскільки через практично 100% ймовірність ЦА як при 3-бальній, так і 4-бальній тяжкості ХМС мозку атрофічні зміни мозку не можуть розглядатися як маркери певної тяжкості хвороби. Встановлена нами відсутність при ХМС мозку вікових розбіжностей між пацієнтами з ЦА та без неї дозволила виключити старіння зі списку чинників ризику ЦА у пацієнтів з ХМС мозку, що підтверджує думку інших дослідників про відмінність ЦА при цієї хворобі від вікових змін [6, 7]. У той же час було з’ясовано, що стать пацієнтів при ХМС мозку є ймовірним фактором ризику ЦА (р = 0,00001).
Висновки
Ретроспективне когортне дослідження поширеності церебральної атрофії, її зв’язків з окремими маркерами та тяжкістю хвороби малих судин мозку за даними обстеження 308 пацієнтів похилого віку з цією хворобою продемонструвало:
1. Поширеність церебральної атрофії серед пацієнтів з хворобою малих судин мозку становила 60 %, при цьому виявлені атрофічні зміни мозку не були пов’язаними зі старінням.
2. Чоловіча стать при хворобі малих судин мозку є ймовірним чинником ризику ЦА (р = 0,00001).
3. Церебральна атрофія є опосередковано асоційованою з хворобою малих судин мозку, через що вона не може розглядатися як чинник, предиктор або маркер цієї хвороби.
4. Церебральна атрофія мозку при хворобі малих судин мозку найтісніше пов’язана: за якістю маркерів — з лейкоареозом, «німі» інфаркти мозку посідають друге місце; за кількістю маркерів — з комбінацією будь-яких 3 або 4 маркерів.
5. При хворобі малих судин мозку найбільш адекватним методом оцінки ймовірності церебральної атрофії за маркерами хвороби є логіт-модель (А) з відповідним рівнянням:
Zi = –4,90 + 0,33(рПВП+ + 5,18(ЛА) + 4,60(НІМ) + 2,85(цМКВ).
6. При необхідності уточнення впливу рівня прогресування лейкоареозу та розширення перивентрикулярних просторів на ймовірність атрофічних змін у мозку може використовуватися розширена версія логіт-моделі (В):
Zi = –5,22 + (–0,26)(рПВП (1)) + 3,06(рПВП (2)) + 3,48(ЛА (1)) + 4,83(ЛА (2–3)) + 5,60(НІМ) + 2,60(цМКВ).
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Wardlaw J. Mechanisms of sporadic cerebral small vessel disease: insights from neuroimaging / J. Wardlaw, С. Smith, М. Dichgans // Lancet Neurol. — 2013. — V. 12. — P. 483-497.
2. Cerebral small vessel disease: Capillary pathways to stroke and cognitive decline / L. Østergaard, T.S. Engedal, F. Moreton et al. // J. Cereb. Blood Flow Metab. — 2016. — V. 36, № 2. — P. 302-325.
3. Capillary dysfunction: its detection and causative role in dementias and stroke / L. Østergaard, S.N. Jespersen, T.S. Engedal et al. // Curr. Neurol. Neurosci. Rep. — 2015. — V. 15, № 6. — P. 37.
4. Rationale, design and methodology of the image analysis protocol for studies of patients with cerebral small vessel disease and mild stroke / M. del C. Valdés Hernández, P.A. Armitage, M.J. Thrippleton et al. // Brain Behav. — 2015. — V. 5, № 12. — e00415.
5. Stroke subtype, vascular risk factors, and total MRI brain small-vessel disease burden / J. Staals, S.D. Makin, F.N. Doubal et al. // Neurology. — 2014. — V. 83, № 14. — P. 1228-1234.
6. Characterising the grey matter correlates of leukoaraiosis in cerebral small vessel disease / C. Lambert, J. Sam Narean, P. Benjamin et al. // Neuroimage Clin. — 2015. — V. 9. — P. 194-205.
7. Neuroimaging standards for research into small vessel disease and its contribution to ageing and neurodegeneration / J.M. Wardlaw, E.E. Smith, G.J. Biessels et al. // Lancet Neurol. — 2013. — V. 12. — Р. 822-838.
8. Structural network connectivity and cognition in cerebral small vessel disease / А.М. Tuladhar, Е. van Dijk, М.Р. Zwiers et al. // Hum. Brain Марр. — 2016. — V. 37, № 1. — P. 300-310.
9. Enlarged perivascular spaces on MRI are a feature of cerebral small vessel disease / F.N. Doubal, A.M. MacLullich, K.J. Ferguson et al. // Stroke. — 2010. — V. 41. — P. 450-454.
10. MR signal abnormalities at 1.5 T in Alzheimer’s dementia and normal aging / F. Fazekas, J.B. Chawluk, A. Alavi et al. // AJR Am. J. Roentgenol. — 1987. — V. 149. — P. 351-356.
11. Progression of MRI markers in cerebral small vessel disease: sample size considerations for clinical trials / Р. Benjamin, Е. Zeestraten, С. Lambert et al. // J. Cereb. Blood Flow Metab. — 2016. — V. 36, № 1. — P. 228-240.
12. Zweig M.H. Receiver-operating characteristic (ROC) plots: a fundamental evaluation tool in clinical medicine / M.H. Zweig, G. Campbell // Clinical Chemistry. — 1993. — V. 39, № 4. — P. 561-577.
/14.jpg)
/14_2.jpg)
/14_3.jpg)
/16.jpg)
/16_2.jpg)

/14_4.jpg)
/15.jpg)
/16_3.jpg)
/17.jpg)