Останніми десятиліттями патологія органів травлення домінує у структурі загальної захворюваності дітей та має неухильну тенденцію до зростання [1–6]. У широкому спектрі хронічних захворювань шлунково-–кишкового тракту в дітей перше місце –займають ушкодження його верхніх відділів [6].
На початку XXI століття відмічаються певні зміни в структурі захворювань травного каналу, серед яких спостерігається чітка тенденція до повсюдного зростання поширеності гастроезофагеальної рефлюксної хвороби (ГЕРХ) у всіх вікових групах [1–3, 6], зокрема і серед дитячого населення.
За результатами епідеміологічних досліджень, проведених у багатьох країнах світу, частота ГЕРХ у загальній популяції становить від 7 до 60 %, а в дітей коливається, за даними різних авторів, від 2–4 до 8,7–49 %, цей показник щороку зростає. Проте вірогідних даних про поширеність ГЕРХ у дітей в Україні немає [1, 6].
ГЕРХ є однією із важливих проблем сучасної гастроентерології, що пов’язано зі зростанням кількості хворих з цією патологією, наявністю як типових симптомів, що значно погіршують якість життя хворих, так і нетипових, що утруднює діагностику, призводить до помилкової гіпердіагностики деяких інших захворювань. Невчасна діагностика ГЕРХ погіршує перебіг захворювання, обумовлює можливість прогресування та розвиток серйозних ускладнень, що вимагає тривалого медикаментозного лікування [6]. Достатньо вагомою проблемою є недостатня інформованість лікарів про різноманітність клінічних проявів ГЕРХ.
Відомо, що у виникненні і прогресуванні ГЕРХ важливе значення надається недостатності нижнього стравохідного сфінктера (НСС). Установлено, що його розслаблення стимулюється блукаючим нервом через прегангліонарні холінергічні волокна й постгангліонарні нехолінергічні та неадренергічні нервові волокна. Тому дослідження стану вегетативної нервової системи при ГЕРХ у дітей сприяє уточненню патогенетичних механізмів виникнення і прогресування хвороби [1].
Надзвичайно важливим компонентом відновлення загального стану організму є нормалізація вегетативного балансу [1, 2]. Роль автономної нервової системи в забезпеченні регуляції процесів життєдіяльності є надзвичайно важливою, і стабілізація вегетативних показників має першочергове значення для повноцінного відновлення функціональної активності організму [12]. Водночас традиційна схема терапії при ГЕРХ передбачає лише непрямий, опосередкований вплив на стан автономної нервової системи через відновлення нормальної діяльності органів травлення та забезпечення їх повноцінного функціонування [13].
Дослідження показали, що в схеми лікування ГЕРХ слід включати препарати, що впливають на порушення вегетативного балансу [13]. Найбільший інтерес для корекції вегетативного дисбалансу при ГЕРХ представляє препарат Ноофен® (Olain Farma, Латвія), що є похідним ГАМК і фенілетіламіну.
ГАМК є природним метаболітом тканин мозку, гальмівним медіатором центральної нервової системи (цим пояснюється транквілізуюча та ноотропна вегетостабілізуюча, антигіпоксична та антиастенічна дія препарату), β-фенілетиламін – природний моноамін, який підвищує вміст дофаміну і норадреналіну в мозку і забезпечує психостимулюючу та антиастенічну дію.
Препарат Ноофен, маючи протитривожну, ноотропну, транквілізуючу та вегетостабілізуючу дію, покращує стан пацієнтів, тим самим підвищуючи якість життя [1, 13].
Як відомо, препарат Ноофен має багаторічну доведену ефективність за ноотропною дією. Окрім того, його застосування справляє вегетостабілізуючий, антидепресантний ефекти за наявності мінімуму можливих побічних ефектів, що має вагоме значення, особливо при застосуванні в дитячому віці [16].
Мета роботи: визначити клініко-ендоскопічні та морфологічні особливості езофагітів у дітей з ознаками вегетативних дисфункцій для удосконалення методів діагностики та оцінити ефективність транквілоноотропів у лікуванні цієї патології.
Матеріали та методи
Під нашим спостереженням знаходились 40 дітей віком 10–18 років, серед них 16 хлопців та 24 дівчини, які лікувалися на базі міської дитячої клінічної лікарні м. Львова, у яких можна було запідозрити езофагіт. Усім дітям була проведена ендоскопічна фіброезофагогастродуоденоскопія, під час якої брали біопсійний матеріал із трьох відділів стравоходу для подальшої верифікації діагнозу.
Для оцінки вегетативних змін нервової системи використовували опитувальник А.М. Вейна (1998) та вегетативний індекс Кердо.
Діти були розподілені на 2 групи. Контрольну групу становили 20 дітей (6 хлопців та 14 дівчат), середній вік — 15,1 ± 1,83 року, із діагнозом ГЕРХ, у яких були ознаки вегетативної дисфункції та які одержували лікування за стандартною схемою відповідно до наказу МОЗ України № 59 від 29.01.2013 року «Уніфіковані клінічні протоколи медичної допомоги дітям із захворюваннями органів травлення». Дітям надавалися загальні рекомендації щодо режиму: сон з підняттям головного кінця ліжка (на 15 см); виключення фізичних вправ із напруженням черевної порожнини; зниження маси тіла; відмова від носіння корсетів та тугих поясів, що збільшують внутрішньочеревний тиск; обмеження робіт, пов’язаних із нахилом тулуба та підняттям ваги понад 5 кг.
Особливу увагу звертали на дієту: рекомендували 4–5-разове регулярне харчування невеликими порціями без переїдання та поспіху, зберігання вертикального положення протягом не менше 1,5 години після їжі, останній прийом їжі не менше ніж за 3 години до сну та відмову від перекусів уночі. Окремо наголошували на необхідності обмеження продуктів, що знижують тонус НСС (кава, міцний чай, шоколад, м’ята, молоко, жирне м’ясо і риба), та продуктів, що підвищують внутрішньошлунковий тиск, стимулюють функцію шлунка (газовані напої, бобові, пиво). В дієту рекомендували включити більшу кількість білка, який має здатність підвищувати тонус НСС.
Патогенетична медикаментозна терапія проводилась з урахуванням стадії хвороби — призначались антациди, препарати альгінової кислоти, прокінетики, блокатори Н2-гістамінових рецепторів або інгібітори протонної помпи, цитопротектори.
Основну групу становили 20 дітей (10 хлопців та 10 дівчат), середній вік — 14,7 ± 1,81 року, із діагнозом ГЕРХ, у яких були ознаки вегетативної дисфункції та які отримували, крім зазначеного лікування, фенібут (Ноофен®, Olain Farma, Латвія) у дозі 250 мг 2 рази на добу протягом 21 дня.
Обстеження хворих для визначення динаміки основних проявів ГЕРХ проводилося двічі — на початку лікування та через 4 тижні шляхом анкетування за формою, аналогічною тій, що використовувалася під час первинного обстеження.
Результати дослідження та їх обговорення
За нашими даними, до початку лікування діти обох груп істотно не відрізнялися за своїми основними показниками. Основними скаргами при первинному обстеженні дітей були біль у надчеревній ділянці різної інтенсивності (100 % дітей обох груп), зниження апетиту (80 % дітей основної та 75 % — контрольної групи), печія (70 та 60 % дітей відповідно), періодична регургітація (50 та 45 % відповідно), нудота (35 та 30 % відповідно) та блювання (10 та 15 % відповідно).
При об’єктивному обстеженні в 100 % дітей обох груп спостерігався біль при пальпації у надчеревній ділянці.
Згідно з результатами опитування дітей за Вейном, середній бал в основній групі становив 24,55 ± 3,30, у контрольній — 23,90 ± 1,94. Нами було виявлено, що схильність до почервоніння обличчя (при хвилюванні) мала місце у 35 % дітей основної та 40 % дітей контрольної групи, до збліднення обличчя — у 5 % дітей основної групи, оніміння або похолодання пальців кистей, стоп — у 45 % дітей основної та 40 % дітей контрольної групи, кистей, стоп повністю — у 5 % дітей обох груп, зміна кольору (збліднення, синюшність, почервоніння) пальців кистей, стоп — у 30 та 35 % дітей відповідно, зміна кольору кистей повністю, стоп — у 5 % пацієнтів контрольної групи, відчуття серцебиття, завмирання, зупинки серця — у 50 % дітей основної та 45 % дітей контрольної групи, підвищена пітливість — у 60 та 65 % відповідно, відчуття утруднення при диханні (відчуття нестачі повітря, бажання глибоко вдихнути, покашлювання) — у 30 та 25 % відповідно, порушення функції травного тракту (схильність до запору, проносу, здуття живота, біль) — у 90 та 85 % відповідно, випадки непритомності — у 15 та 10 % відповідно, приступоподібний біль голови — у 25 та 20 % відповідно, зниження працездатності, швидка стомлюваність — у 60 % дітей обох груп, порушення сну (труднощі засинання; поверхневий сон з частими пробудженнями; відчуття невиспаності, втоми при пробудженні зранку) — у 25 % дітей основної та 20 % дітей контрольної групи (рис. 1).
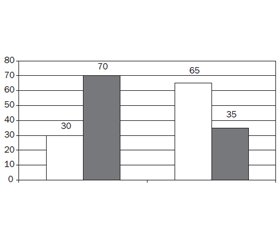
При ендоскопічному дослідженні макроскопічні зміни слизової оболонки стравоходу були зареєстровані у 100 % обстежених дітей та підлітків. В усіх дітей основної та контрольної груп були виявлені вогнищева або дифузна еритема та набряк слизової оболонки, у 60 % дітей контрольної групи — множинні білуваті налети діаметром 0,1–0,2 см за типом крипт-абсцесів, у 70 % дітей основної та у 35 % дітей контрольної групи — ерозивні зміни (рис. 2).
При морфологічному дослідженні біоптатів слизової оболонки стравоходу були виявлені такі зміни: дистрофія епітеліоцитів — у 75 % дітей основної та 65 % дітей контрольної групи, деструкція гранул кератогіаліну — у 40 та 50 % дітей відповідно, гіперемія судин мікроциркуляторного русла (СМР) — у 90 та 85 % відповідно, крововиливи діапедезного характеру — у 50 та 65 % відповідно, периваскулярна поліморфноклітинна інфільтрація — у 35 та 5 % відповідно, вогнищеві інтраепітеліальні крововиливи — у 25 та 5 % відповідно, набряк строми — у 10 % дітей основної групи (рис. 3).
/27-1.gif)
/27-2.gif)
Після проведеного лікування ми отримали однонаправлені зміни всіх показників в обох групах, проте в основній групі вони були більш виражені. Так, скарги на болі в епігастральній ділянці утримувалися у 20 % дітей основної групи та у 25 % — контрольної, зниження апетиту — у 40 та 45 % дітей відповідно, печію — у 30 % дітей обох груп, періодичну регургітацію — у 10 та 15 % дітей відповідно, нудоту — у 5 % дітей обох груп. Скарги на блювання та дисфагію були відсутні в обох групах. Об’єктивне дослідження показало, що у 25 % дітей обох груп утримувався біль при пальпації в епігастральній ділянці, проте меншої інтенсивності (табл. 1).
У дітей обох груп спостерігалася позитивна динаміка ознак вегетативного дисбалансу, проте в дітей основної групи вона була більш виражена (табл. 2, 3).
Позитивна динаміка спостерігалася і при визначенні вегетативного індексу Кердо (рис. 4). На початку дослідження він становив 14,7 ± 12,3 в основній групі, зменшився до 5,9 ± 7,4 (р < 0,01), а в контрольній групі знизився з 14,4 ± 11,2 до 11,0 ± 9,0 (табл. 3).
Висновки
Для дітей шкільного віку з ГЕРХ типовими є скарги на біль, печію, зниження апетиту, періодичну регургітацію. При ендоскопічному та морфологічному дослідженні виявляються ознаки катарального або ерозивного рефлюкс-езофагіту з наявністю дистрофії епітеліоцитів, деструкції гранул кератогіаліну, гіперемії судин мікроциркуляторного русла, діапедезних крововиливів.
Типовими для дітей шкільного віку з гастроезофагеальною рефлюксною хворобою є зміни вегетативного статусу, які проявляються порушеннями моторики травного каналу, підвищеною –пітливістю, зниженою працездатністю, швидкою втомлюваністю та іншими симптомами вегетативного дисбалансу.
Клінічна оцінка динаміки вегетативного статусу школярів із ГЕРХ дозволяє стверджувати, що включення у комплекс терапії цієї патології препарату Ноофен 250 мг 2 рази на добу протягом 21 дня позитивно впливає на результати лікування дітей, забезпечує добрий вегетостабілізуючий ефект, що обумовлює кращу динаміку зменшення проявів вегетативної дисфункції та відповідне зменшення клінічної симптоматики. За даними нашого дослідження, Ноофен добре переноситься дітьми й не викликає побічних реакцій.
Конфлікт інтересів. Не заявлений.
Список литературы
1. Белоусов Ю.В. Гастроэзофагеальная рефлюксная болезнь в детском возрасте / Ю.В. Белоусов // Здоров’я України. — 2005. — № 5. — С. 24-25.
2. Бєлоусов Ю.В. Гастроентерологія дитячого віку / Ю.В. Бєлоусов. — К.: СПД Коляда О.П., 2007. — 440 с.
3. Волосовець О.П. Сучасний погляд на проблему порушень моторної функції верхнього відділу травного каналу / О.П. Волосовець, С.П. Кривопустов, Ю.В. Карулина // Здоровье ребенка. — 2007. — № 5 (114). — С. 7-9.
4. Давыдова А.Н. Особенности течения гастроэзофагеальной рефлюксной болезни у детей школьного возраста при различных вегетативных нарушениях и пути их коррекции: Автореф. дис… канд. мед. наук: спец. 14.00.09 — «Педиатрия» / А.Н. Давыдова. — Волгоград, 2008. — 24 с.
5. Шадрин О.Г. Педиатрические аспекты гастроэзофагеальной рефлюксной болезни / О.Г. Шадрин // Здоров’я України. — 2009. — № 6/1. — С. 11.
6. Зубаренко О.В. Сучасний погляд на гастроезофагеальну рефлюксну хворобу у дітей / О.В. Зубаренко, Т.Ю. Кравченко // Перинатология и педиатрия. — 2013. — № 1. — С. 114-122.
7. Бельмер С.В. Гастроэзофагеальная рефлюксная болезнь / С.В. Бельмер // РМЖ. — 2008. — Т. 16, № 3. — С. 144-147.
8. Шептулин А.А. Гастроэзофагеальная рефлюксная болезнь: спорные и нерешенные вопросы / А.А. Шептулин // Клин. медицина. — 2008. — № 6. — С. 8-12.
9. Gold B.D. Outcomes of pediatric gastroesophageal reflux disease: in the first year of life, in childhood, and in adults… Oh, and should we really leave Helicobacter pylori alone? / B.D. Gold // J. Pediatr. Gastroenterol. Nutr. — 2003. — Vol. 37(Suppl.). — S33-S39.
10. Боярська Л.М. До питання про частоту та особливості проявів гастроезофагеальної рефлюксної хвороби у дітей / Л.М. Боярська, К.О. Іванова // Современная педиатрия. — 2010. — № 2. — С. 162-163.
11. Осьодло Г.В. Про стан вегетативної нервової системи у військовослужбовців із різними варіантами ГЕРХ / Г.В. Осьдло // Світ медицини та біології. — 2010. — № 2.
12. Абрагамович О.О. Особливості стану вегетативної нервової системи в осіб з Нр (+) виразковою хворобою за результатами дослідження варіабельності серцевого ритму та її зміни під впливом комплексного лікування з використанням флуренізиду AML ХІІ / О.О. Абрагамович, Я.Л. Лещук // Acta Medica Leopoliensia. — 2007. — № 1–2. — C. 59-63.
13. Ігнащук О.В. Вплив терапії Ноофеном на стан автономної нервової системи у хворих на гастроезофагеальну рефлюксну хворобу // О.В. Ігнащук, В.К. Сєркова // Медичні перспективи. — 2010. — № 4. — С. 52-56.
14. Кішко Н.Ю. Корекція порушень вегетативного гомео–стазу у дітей з гастроезофагеальним рефлюксом / Н.Ю. Кішко // Педіатрія, акушерство та гінекологія. — 2003. — № 4. — C. 17-20.
15. Николаева О.В. Функциональное состояние вегетативной нервной системы у детей с гастроэзофагеальной рефлюксной болезнью / О.В. Николаева, Осама С.А. Саламех // Врачебная практика. — 2002. — № 2. — C. 95-98.
16. Кузьминова Н.В. Вегетативные расстройства у пациентов с гипертонической болезнью: диагностика и медикаментозная коррекция / Н.В. Кузьминова, В.К. Сер–кова // Укр. терапевтичний журнал. — 2009. — № 2 (70). —
C. 37-39.

/27-1.gif)
/27-2.gif)
/28-1.gif)
/29-1.gif)
/29-2.gif)