Введение
Избыточная продукция активированных кислородсодержащих метаболитов (АКМ) и азотсодержащих метаболитов (ААК) может привести к деструкции клеток и поражению ткани респираторного тракта. АКМ и ААК инактивируются функционально активными компонентами антиоксидантной системы респираторного тракта, одними из которых являются пероксиредоксины [1].
Пероксиредоксины
Семейство пероксиредоксинов
Пероксиредоксины (Prx, КФ 1.11.1.15), образующие суперсемейство Se-независимых пероксидаз, были открыты около 10 лет назад. Первоначально пероксиредоксин получил название «протеиновый покровитель» или «специализированный тиольный антиоксидант». В настоящее время создана база данных PREX (http://www.csb.wfu.edu/prex/), которая содержит информацию о 3516 пероксиредоксиновых протеинах [6, 33]. Пероксиредоксины осуществляют ферментативную деградацию H2O2, органических гидропероксидов (ROOH), пероксинитрита (OONO–) [6]. Гены Prx характеризуются высоким уровнем экспрессии, на долю пероксиредоксиновых протеинов приходится более 1 % клеточного протеома. На основании данных сравнительного кинетического анализа установлено, что при физиологических условиях внутриклеточные Prx выполняют восстановление практически 90 % митохондриальной H2O2 и почти 100 % цитоплазматической H2O2, в связи с чем Prx определены как доминирующий компонент антиоксидантной системы в условиях низкого уровня концентрации перекиси водорода [37]. Пероксиредоксины не похожи ни на один антиоксидант, так как их молекула не содержит таких обычных окислительно-восстановительных активных центров, как ионы металлов, гем, флавин или селеноцистеин. Характерным признаком Prx является наличие цистеинового остатка Cys47 в N-терминальном регионе молекулы. В отличие от тиоредоксинов (Trx), имеющих активный двухцистеиновый каталитический центр и образующих при окислении внутримолекулярную дисульфидную связь, молекулы Prx не содержат таких участков, однако присутствующие в их структуре цистеиновые остатки способны образовывать межмолекулярные дисульфидные связи [3, 4, 35]. Пероксиредоксины являются гомодимерами, а в некоторых случаях они могут организовывать гомооктамеры, гомодекамеры, гомододекамеры и более крупные молекулярные образования. Исключение составляет Prx5, который является мономером [7, 11, 22].
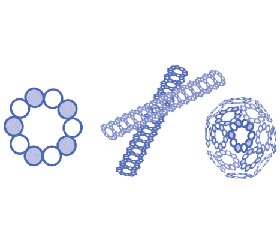
Шесть изоформ Prx человека в зависимости от количества и положения цистеиновых остатков подразделяют на три структурно-функциональные группы: 1) типичные двухцистеиновые (2-Cys) — Prx1, Prx2, Prx3, Prx4; 2) атипичные 2-Cys — Prx5; 3) одноцистеиновые (1-Cys) — Prx6 (рис. 1) [22]. В настоящее время данная классификация подвергается достаточно жесткой критике [37].
/127-1.gif)
Молекула Prx содержит два домена: N-терми-нальный — пероксидазный, тиольная группа цистеинового остатка которого получила обозначение SP; и С-терминальный — разрешающий домен, тиольная группа цистеинового остатка которого 2-Cys Prx получила обозначение SR. Протеин Prx отличается пространственно консервативной компактной, шаровидной структурой. Третичная структура Prx состоит из семи β-нитей (β1-β7) и пяти α-спиралей (α1-α5), центральный β-слой формируется из пяти β-нитей (β5-β4-β3-β6-β7) и с одной стороны покрыт β1, β2 и α1, α4, с другой — α2, α3 и α5. Примерно у половины из известных структур Prx α1 является 310-спиралью. В конформации FF (fully folded) SP консервативного цистеинового остатка находится на первом витке α2-спирали. У всех молекул Prx за изломом α2-спирали следует еще один или два дополнительных витка. Активный сайт SP находится на дне «кармана» в окружении трех консервативных остатков: Pro, Thr и Arg [39].
Типичные двухцистеиновые Prx (Prx1, Prx2, Prx3, Prx4) характеризуются наличием цистеиновых остатков, организующих два каталитических центра в N-терминальной (Cys47) и C-терминальной областях (Cys170). Молекула атипичного двухцистеинового Prx (Prx5) кроме N-терминального консервативного цистеинового остатка содержит еще два цистеиновых остатка в положении 73 и 152, однако окружающие их последовательности не соответствуют структуре типичных 2-Cys Prx. Пероксиредоксины различных типов локализуются в различных внутриклеточных компартментах. Так, протеины Prx1 и Prx2 локализуются в цитоплазме; Prx3 находится в митохондриях; Prx4 — в цитоплазме, лизосомах и может секретироваться во внеклеточное пространство; Prx5 локализуется в цитоплазме, митохондриях и микросомах, Prx6 — в цитоплазме и эндоплазматическом ретикулуме [23, 29, 31, 34, 37].
В бронхиальных эпителиальных клетках, как правило, наблюдается высокий или умеренный уровень экспрессии Prx1, Prx3, Prx5 и Prx6; в альвеолярном эпителии присутствуют в основном Prx5 и Prx6, а в альвеолярных макрофагах — Prx1 и Prx6. Самый высокий уровень экспрессии в респираторном тракте отмечается у Prx6, он выше, чем в любых других тканях человека. Считают, что вклад Prx6 в результат функционирования системы антиоксидантной защиты верхних дыхательных путей млекопитающих составляет около 75 %. Аппликация Prx6 при острых воспалительных процессах органов дыхания существенно сокращает время регенерации ткани [3, 19, 25].
Пероксиредоксинзависимые окислительно-восстановительные реакции
Несмотря на то что каталитическая активность Prx по отношению к Н2О2 ниже, чем у глутатионпероксидазы и каталазы, Prx играют физиологически значимую роль в инактивации Н2О2. Считают, что при высоких концентрациях Н2О2, при которых Prx очень быстро окисляются, основную роль в инактивации Н2О2 играет каталаза, а в условиях низких концентраций Н2О2 — Prx. В качестве донора электронов Prx1–Prx5 используют тиоредоксины, а Prx6 — глутатион. Взаимодействие двухцистеиновых Prx с Н2О2 приводит к образованию цистеинсульфеновой кислоты, которая в последующем участвует в формировании межпептидной дисульфидной связи. Образовавшийся дисульфид восстанавливается Trx (рис. 2) [20].
/128-1.gif)
Взаимодействие мономерного Prx6 с Н2О2 сопровождается окислением активного Cys47 в цистеинсульфеновую кислоту, которая в дальнейшем восстанавливается до дисульфида за счет S-глутатионилирования при условии гетеродимеризиции Prx6 с глутатионтрансферазой P1-1. В восстановлении дисульфида участвует GSH. Также Prx6 восстанавливает гидроперекиси фосфолипидов и обладает активностью фосфолипазы А2 [3, 14, 31]. Особенности каталитических реакций Prx различных групп представлены на рис. 3.
/128-2.gif)
В отличие от бактерий, у которых перекись водорода обычно быстро элиминируется, высшие многоклеточные организмы используют молекулы Н2О2 в условиях среднего уровня ее концентрации в качестве внутриклеточных сигнальных элементов. Zachary A. Wood и соавт. [39] было высказано предположение о том, что во внутриклеточной регуляции АКМ 2-Cys пероксиредоксины играют ключевую роль шлюзов, которые удерживают концентрацию АКМ на низком «досигнальном» уровне. Повышение содержания АКМ выше потенциальной инактивирующей возможности локального пула Prx превращает АКМ в «ощущаемый» внутриклеточный сигнал, который достигает кислородсенситивных целевых протеинов.
Другие физиологические эффекты системы пероксиредоксинов
Многообразная физиологическая роль Prx была продемонстрирована исследованиями на экспериментальных животных с нокаутом генов отдельных пероксиредоксинов. Так, у мышей с нокаутом гена PRDX1 наблюдается развитие гемолитической анемии; с нокаутом гена PRDX2 — анемии, которая сопровождалась укорочением продолжительности жизни; с нокаутом гена PRDX6 отмечается высокий уровень окисления протеинов, выраженное поражение легких, почек и печени [3].
Пероксиредоксины оказывают регулирующее действие на клеточную пролиферацию, препятствуют развитию апоптоза, регулируют процесс воспаления.
Пероксиредоксины Prx1, Prx2 оказывают антиапоптотическое действие. Prx1, взаимодействуя с Trx, непосредственно ингибирует H2O2-индуцирован-ную активацию двух апоптотических сигнальных регуляторов — ASK1 и p66Shc. В условиях физиологических концентраций H2O2 протеины Trx и Prx1 удерживают молекулы ASK1 и p66Shc в неактивном состоянии за счет организации с ними гетеродимеров. При повышении внутриклеточной концентрации H2O2 происходит окисление протеина Prx1, что обусловливает его отъединение от ASK1 и p66Shc. В дальнейшем киназа JNK фосфорилирует Ser36 протеина p66Shc, что приводит к его тетрамеризации и перемещению в митохондрии, обусловливая усиление генерации АКМ. Prx2 ингибирует активацию ASK1 [16].
Установлено, что Prx1, Prx6 модулируют LPS-индуцированный воспалительный процесс. Prx1 может активировать TLR4-ассоциированные молекулярные пути возбуждения и стимулировать MyD88-зависимым способом продукцию TNF-α и IL-6 макрофагами и дендритными клетками [27]. Ядерно расположенный Prx1 активирует трансактивность факторов NF-kB, AP-1 [15, 24]. Макрофаги, лишенные гена Prx1, на возбуждающий стимул LPS реагируют повышением продукции не провоспалительных цитокинов, а IL-10, что, по всей вероятности, связано с активацией фактора транскрипции STAT3 [30, 36]. Установлено, что TGF-β, ИЛ-1β и онкостатин M индуцируют секрецию Prx1. Протеин Prx1, попадая в экстрацеллюлярное пространство, может связываться с TLR4 и индуцировать продукцию провоспалительных цитокинов [16]. В то же время было продемонстрировано, что Prx1 ингибирует Th2-ассоциированное воспаление респираторного тракта и достоверно снижает уровень гиперреактивности бронхиального дерева. Также продемонстрирована способность Prx1 ингибировать аллерген-специфическую пролиферацию Т-клеток, по всей вероятности, снижая эффективность работы иммунологических синапсов [26].
У экспериментальных мышей с нокаутом гена Prx6 LPS-индуцированное воспаление сопровождается значительно выраженным поражением ткани легкого [36]. Полагают, что протеин Prx6 играет центральную роль в восстановлении пероксидов в альвеолоцитах II типа и других эпителиальных клетках респираторного тракта. Кроме того, Prx6 в органах дыхания эмулирует функционирование глутатионпероксидазы и ингибирует экспрессию ICAM-1/CD54 и VCAM-1, которые рекрутируют макрофаги в очаг поражения [12]. С другой стороны, Prx6 участвует в активации НАДФH-оксидазы-2 (NOX2) человеческих нейтрофилов, облегчая сборку NOX2-комплекса, который генерирует супероксид анион-радикал. По всей вероятности, данное действие Prx6 представляет собой один из механизмов защиты респираторного тракта от инфекционных агентов [28]. Человеческие бронхиальные эпителиальные клетки (BEAS2B) с нокаутом гена Prx6 также продуцируют провоспалительные цитокины (IL-1β) в достоверно сниженных объемах. Данные клетки высокорезистентны к апоптозу, индуцированному TNF-α, и высокочувствительны к апоптозу, индуцированному АКМ [10]. Prx6 играет важную роль в деградации легочного сурфактанта и синтезе дипальмитоилфосфатидилхолина [5].
Повышенная экспрессия Prx5 во время воспалительного процесса респираторного тракта, вызванного бактериальными инфекционными агентами, индуцирует активный хемотаксис лейкоцитов [21].
Антиоксидантный фактор с опосредованным действием APEX-нуклеаза-1/Ref-1
APEX-нуклеаза-1 (APEX1/Ref-1) млекопитающих — основная апуриновая/апиримидиновая эндонуклеаза-1, ортолог Х кишечной палочки — является многофункциональным протеином, который участвует в репарации ДНК, регуляции активности транскрипции генов, контроле над окислительно-восстановительным состоянием клетки. APEX1/Ref-1 инициализирует удаление апуриновых/апиримидиновых сайтов. В связи с высокой частотой возникновения апуриновых/апиримидиновых сайтов (примерно 10 000 сайтов в сутки) механизм их репарации носит глобальный характер [2].
Протеин APEX1/Ref-1 (молекулярная масса около 37 кДа) кодируется геном, который находится на 14-й хромосоме и состоит из четырех интронов и пяти экзонов. Молекула APEX1/Ref-1 состоит из глобулярного плотно упакованного нуклеазного домена и гибкого N-терминального региона. С-терминальный домен ответствен за взаимодействие с ДНК и обеспечивает эндонуклеазную активность. N-терминальный домен отвечает за окислительно-восстановительную функцию протеина APEX1/Ref-1, не зависящую от репаративных функций этого фермента. Основную роль в проявлении этой активности играет цистеиновый аминокислотный остаток 65 в восстановленной форме. В окисленной форме Cys65 предположительно образует дисульфидный мостик с Cys93. Молекула APEX1/Ref-1 представляет собой четырехслойную α,β-сэндвич-структуру, характерную для нуклеаз. APEX1/Ref-1 локализуется преимущественно в ядре или в цитоплазме клетки [2, 13, 17, 18].
APEX1/Ref-1 была идентифицирована как протеин, который в ядре клетки поддерживает окислительно-восстановительный баланс, индуцируя ДНК-связывающую активность убиквитарных (AP-1, NF-κB, Egr-1, HIF-1α, семейства ATF/CREB, p53) и тканеспецифичных (PEBP-2, Pax-5, Pax-8, TTF-1) транскрипционных факторов. Данный эффект обусловлен восстановлением цистеиновых остатков молекул факторов транскрипции (рис. 4) [17, 38].
/130-1.gif)
Как правило, в тиолопосредованных окислительно-восстановительных реакциях сульфгидрильная группа одного цистеинового остатка редокс-фактора выступает в качестве нуклеофильного агента, который взаимодействует с другим протеином — белком-мишенью — и образует смешанные дисульфиды, т.е. комплекс, в котором окислительно-восстановительный фактор соединен с белком-мишенью дисульфидной связью. Смешанные дисульфиды в последующем взаимодействуют с другим цистеиновым остатком окислительно-восстановительного фактора, что приводит к образованию дисульфидных связей в самой молекуле окислительно-восстановительного фактора. Данная реакция приводит к восстановлению белка-мишени и окислению редокс-фактора. В процессе редукции дисульфидных связей протеинов факторов транскрипции аминокислотный остаток Cys65 молекулы APEX1/Ref-1 выступает в роли нуклеофила, а аминокислотный остаток Cys93 — разрешающего цистеинового остатка [17].
Способность взаимодействовать и модулировать активность многочисленных факторов транскрипции объясняет полифункциональность APEX1/Ref-1 (рис. 5) [8, 38].
Однако длительное повышение экспрессии APEX1/Ref-1 ассоциировано с агрессивной пролиферацией, высокой активностью ангиогенеза, повышенной резистентностью к действию лекарственных средств, плохим прогнозом заболевания и низким уровнем пятилетней выживаемости у больных с онкологическими заболеваниями. Так, высокий уровень экспрессии APEX1/Ref-1 наблюдается у больных с раком молочной железы, яичников, саркомами (остеосаркомами, рабдомиосаркомами), множественными миеломами [17, 40].
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Абатуров А.Е. Антиоксидантная система респираторного тракта. Антиоксидантные эффекторы в надэпителиальном и экстрацеллюлярном пространстве (часть 1) / А.Е. Абатуров, А.П. Волосовец, А.Е. Худяков // Здоровье ребенка. — 2016. — № 3 (71). — С. 161-171.
2. Дырхеева Н.С. Полифункциональная апуриновая/апиримидиновая эндонуклеаза 1 человека: роль дополнительных функций / Н.С. Дырхеева, С.Н. Ходырева, О.И. Лаврик // Молекулярная биология. — 2007. — Т. 41, № 3. — С. 450-466.
3. Калинина Е.В. Участие тио-, перокси- и глутаредоксинов в клеточных редоксзависимых процессах / Е.В. Калинина, Н.Н. Чернов, А.Н. Саприн // Успехи биологической химии. — 2008. — Т. 48. — С. 319-331.
4. Пероксиредоксины — новое семейство антиоксидантных белков / T.M. Шуваева, В.И. Новоселов, E.E. Фесенко, В.M. Липкин // Биоорганическая химия. — 2009. — T. 35, № 5. — C. 581-596.
5. Altered lung phospholipid metabolism in mice with targeted deletion of lysosomal-type phospholipase A2 / A.B. Fisher, C. Dodia, S.I. Feinstein, Y.S. Ho // J. Lipid. Res. — 2005. — Vol. 46, № 6. — P. 1248-1256. DOI: 10.1194/jlr.M400499-JLR200.
6. Analysis of the peroxiredoxin family: using active-site structure and sequence information for global classification and residue analysis / K.J. Nelson, S.T. Knutson, L. Soito et al. // Proteins. — 2011. — Vol. 79, № 3. — P. 947-964. doi: 10.1002/prot.22936. Epub 2010 Dec 22.
7. Barranco-Medina S. The oligomeric conformation of peroxiredoxins links redox state to function / S. Barranco-Medina, J.J. Lázaro, KJ. Dietz // FEBS Lett. — 2009. — Vol. 583, № 12. — P. 1809-1816. doi: 10.1016/j.febslet.2009.05.029. Epub 2009 May 22.
8. Bhakat K.K. Transcriptional regulatory functions of mammalian AP-endonuclease (APE1/Ref-1), an essential multifunctional protein / K.K. Bhakat, A.K. Mantha, S. Mitra // Antioxid. Redox Signal. — 2009. — Vol. 11, № 3. doi: 10.1089/ARS.2008.2198.
9. Busso C.S. Posttranslational modification of mammalian AP endonuclease (APE1) / C.S. Busso, M.W. Lake, T. Izumi // Cell. Mol. Life Sci. — 2010. — Vol. 67, № 21. — P. 3609–3620. doi: 10.1007/s00018-010-0487-3. Epub 2010 Aug 14.
10. Characterization of the endoribonuclease active site of human apurinic/apyrimidinic endonuclease 1 / W.C. Kim, B.R. Berquist, M. Chohanm et al. // J. Mol. Biol. — 2011. — Vol. 411, № 5. — P. 960-971. doi: 10.1016/j.jmb.2011.06.050. Epub 2011 Jul 6.
11. Crystal structure of reduced and of oxidized peroxiredoxin IV enzyme reveals a stable oxidized decamer and a non-disulfide-bonded intermediate in the catalytic cycle / Z. Cao, T.J. Tavender, A.W. Roszak et al. // J. Biol. Chem. — 2011. — Vol. 286, № 49. — P. 42257-42266. doi: 10.1074/jbc.M111.298810. Epub 2011 Oct 12.
12. Environmentally persistent free radicals induce airway hyperresponsiveness in neonatal rat lungs / S. Balakrishna, J. Saravia, P. Thevenot et al. // Part. Fibre Toxicol. — 2011. — Vol. 8. — P. 11. doi: 10.1186/1743-8977-8-11.
13. Evolution of the redox function in mammalian apurinic/apyrimidinic endonuclease/ M.M. Georgiadis, M. Luo, R.K. Gaur et al. // Mutat. Res. — 2008. — Vol. 643, № 1–2. — P. 54-63. doi: 10.1016/j.mrfmmm.2008.04.008. Epub 2008 May 18.
14. Hall A. Typical 2-Cys peroxiredoxins--structures, mechanisms and functions / A. Hall, P.A. Karplus, L.B. Poole // FEBS J. — 2009. — Vol. 276, № 9. — P. 2469-2477. doi: 10.1111/j.1742-4658.2009.06985.x. Epub 2009 Mar 24.
15. Hansen J.M. Nuclear and cytoplasmic peroxiredoxin-1 differentially regulate NF-kappaB activities / J.M. Hansen, S. Moriarty-Craige, D.P. Jones // Free Radic. Biol. Med. — 2007. — Vol. 43, № 2. — P. 282-288. doi: 10.1016/j.freeradbiomed.2007.04.029.
16. Ishii T. Novel roles of peroxiredoxins in inflammation, cancer and innate immunity / T. Ishii, E. Warabi, T. Yanagawa // J. Clin. Biochem. Nutr. — 2012. — Vol. 50, № 2. — P. 91-105. doi: 10.3164/jcbn.11-109. Epub 2012 Feb 18.
17. Kelley M.R. APE1/Ref-1 role in redox signaling: translational applications of targeting the redox function of the DNA repair/redox protein APE1/Ref-1 / M.R. Kelley, M.M. Georgiadis, M.L. Fishel // Curr. Mol. Pharmacol. — 2012. — Vol. 5, № 1. — P. 36-53. PMCID: PMC3319314.
18. Kim S.Y. Phospholipase A(2) of peroxiredoxin 6 has a critical role in tumor necrosis factor-induced apoptosis / S.Y. Kim, E. Chun, K.Y. Lee // Cell. Death Differ. — 2011. — Vol. 18, № 10. — P. 1573-1583. doi: 10.1038/cdd.2011.21. Epub 2011 Mar 18.
19. Knoops B., Goemaere J., Van der Eecken V., Declercq J.P. Peroxiredoxin 5: structure, mechanism, and function of the mammalian atypical 2-Cys peroxiredoxin // Antioxid. Redox Signal. — 2011. — Vol. 15, № 3. — P. 817-829. doi: 10.1089/ars.2010.3584. Epub 2011 Apr 20.
20. Lowther W.T. Reduction of cysteine sulfinic acid in eukaryotic, typical 2-Cys peroxiredoxins by sulfiredoxin / W.T. Lowther, A.C. Haynes // Antioxid. Redox Signal. — 2011. — Vol. 15, № 1. — P. 99-109. doi: 10.1089/ars.2010.3564. Epub 2010 Dec 17.
21. Migrating leukocytes are the source of peroxiredoxin V during inflammation in the airways / R.I. Krutilina, A.V. Kropotov, C. Leutenegger, V.B. Serikov // J. Inflamm. (Lond). — 2006. — Vol. 3. — P. 13. DOI: 10.1186/1476-9255-3-13.
22. Neumann C.A. Peroxiredoxin 1 and its role in cell signa-ling / C.A. Neumann, J. Cao, Y. Manevich // Cell. Cycle. — 2009. — Vol. 8, № 24. — P. 4072-4078. DOI: 10.4161/cc.8.24.10242.
23. Peroxiredoxin, a novel family of peroxidases / S.G. Rhee, S.W. Kang, T.S. Chang et al. // IUBMB Life. — 2001. — Vol. 52, № 1—2. — P. 35-41. doi: 10.1080/15216540252774748.
24. Peroxiredoxin 1 interacts with androgen receptor and enhan-ces its transactivation / S.Y Park., X. Yu, C. Ip et al. // Cancer. Res. — 2007. — Vol. 67, № 19. — P. 9294-9303. doi: 10.1158/0008-5472.CAN-07-0651.
25. Peroxiredoxins in the lung with emphasis on peroxiredoxin VI / B. Schremmer, Y. Manevich, S.I. Feinstein, A.B. Fisher // Subcell. Biochem. — 2007. — Vol. 44. — P. 317-344. PMID: 18084901.
26. Peroxiredoxin I is a negative regulator of Th2-dominant allergic asthma / K. Inoue, H. Takano, E. Koike et al. // Int. Immunopharmacol. — 2009. — Vol. 9, № 11. — P. 1281-1288. doi: 10.1016/j.intimp.2009.07.010. Epub 2009 Aug 5.
27. Peroxiredoxin 1 stimulates secretion of proinflammatory cytokines by binding to TLR4 / J.R. Riddell, X.Y. Wang, H. Minderman, S.O. Gollnick // J. Immunol. — 2010. — Vol. 184, № 2. — P. 1022-1030. doi: 10.4049/jimmunol.0901945. Epub 2009 Dec 16.
28. Peroxiredoxin 6 phosphorylation and subsequent phospholipase A2 activity are required for agonist-mediated activation of NADPH oxidase in mouse pulmonary microvascular endothelium and alveolar macrophages / S. Chatterjee, S.I. Feinstein, C. Dodia et al. // J. Biol. Chem. — 2011. — Vol. 286, № 13. — P. 11696-11706. doi: 10.1074/jbc.M110.206623. Epub 2011 Jan 24.
29. Peroxiredoxin functions as a peroxidase and a regulator and sensor of local peroxides / S.G. Rhee, H.A. Woo, I.S. Kil, S.H. Bae // J. Biol. Chem. — 2012. — Vol. 287, № 7. — P. 4403-4410. doi: 10.1074/jbc.R111.283432. Epub 2011 Dec 6.
30. Peroxiredoxin-1, a possible target in modulating inflammatory cytokine production in macrophage like cell line RAW264.7 / Y. Tae Lim, D. Sup Song, T. Joon Won et al. // Microbiol. Immunol. — 2012. — Vol. 56, № 6. — P. 411-419. doi: 10.1111/j.1348-0421.2012.00453.x.
31. Poole L.B. The catalytic mechanism of peroxiredoxins / Flohé L., Harris J.R., editors // Peroxiredoxin Systems. — NY: Springer, 2007. — P. 61-81.
32. Poole L.B. Overview of peroxiredoxins in oxidant defense and redox regulation / L.B. Poole, A. Hall, K.J. Nelson // Curr. Protoc. Toxicol. — 2011. — Chapter 7. — Unit 7.9. doi: 10.1002/0471140856.tx0709s49.
33. PREX: PeroxiRedoxin classification indEX, a database of subfamily assignments across the diverse peroxiredoxin family / L. Soito, C. Williamson, S.T. Knutson et al. // Nucleic Acids Res. — 2011. — Vol. 39(Database issue). — P. D332- D337. doi: 10.1093/nar/gkq1060. Epub 2010 Oct 29.
34. Rhee S.G. Peroxiredoxins: a historical overview and speculative preview of novel mechanisms and emerging concepts in cell signaling / S.G. Rhee, H.Z. Chae, K. Kim // Free Radic. Biol. Med. — 2005. — Vol. 38, № 12. — P. 1543-1552. DOI: 10.1016/j.freeradbiomed.2005.02.026.
35. Rhee S.G., Woo H.A. Multiple functions of peroxiredoxins: peroxidases, sensors and regulators of the intracellular messenger H2O2, and protein chaperones / S.G. Rhee, H.A. Woo // Antioxid. Redox Signal. — 2011. — Vol. 15, № 3. — P. 781-794. doi: 10.1089/ars.2010.3393. Epub 2011 Mar 31.
36. Roles of peroxiredoxin 6 in the regulation of oxidative stress to lipopolysaccharide-induced acute lung injury / D. Yang, C.X. Bai, X. Wang et al. // Zhonghua Jie He He Hu Xi Za Zhi. — 2011. — Vol. 34, № 9. — P. 679-683. PMID: 22177494.
37. Structure-based insights into the catalytic power and conformational dexterity of peroxiredoxins / A. Hall, K. Nelson, L.B. Poole, P.A. Karplus // Antioxid. Redox Signal. — 2011. — Vol. 15, № 3. — P. 795-815. doi: 10.1089/ars.2010.3624. Epub 2011 Apr 20.
38. The many functions of APE1/Ref-1: not only a DNA repair enzyme / G. Tell, F. Quadrifoglio, C. Tiribelli, M.R. Kelley // Antioxid. Redox Signal. — 2009. — Vol. 11, № 3. — P. 601-620. doi: 10.1089/ars.2008.2194.
39. Wood L.G. Biomarkers of lipid peroxidation, airway inflammation and asthma / L.G. Wood, P.G. Gibson, M.L. Garg // Eur. Respir. J. — 2003. — Vol. 21. — P. 177-186. PMID: 12570126.
40. Zhang Y. Anticancer clinical utility of the apurinic/apyrimidinic endonuclease/redox factor-1 (APE/Ref-1) / Y. Zhang, J. Wang // Chin. J. Cancer. — 2010. — Vol. 29, № 3. — P. 333-339. PMID: 20193121.

/127-1.gif)
/128-1.gif)
/128-2.gif)
/130-1.gif)
/131-1.gif)