Введение
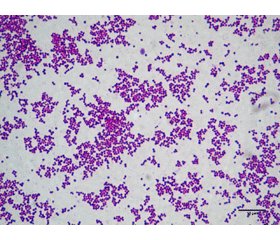
Золотистый стафилококк впервые был описан в 1882 году шотландским хирургом Alexander Ogston при микроскопическом изучении гноя из абсцессов человека [43]. Золотистые стафилококки являются грамположительными неспорообразующими, факультативными, β-гемолитическими, каталаза-позитивными кокками семейства Micrococcaceae [30].
Согласно данным метаанализа, проведенного Pui-Ying Iroh Tam и соавт. [29], удельный вес бактерий Staphylococcus aureus в современной этиологической структуре пневмоний у детей составляет всего 2,1 %, однако стафилококковые пневмонии отличаются высоким риском неблагоприятного течения [3, 40, 54]. По мнению Jan Kluytmans и соавт. [31], 26 % внебольничных пневмоний, протекающих с высоким риском неблагоприятного исхода, вызваны Staphylococcus aureus.
Бактерии Staphylococcus aureus являются комменсалами, которые колонизируют различные ниши организма (слизистые оболочки носовой полости, ротоглотки, влагалища, кожные покровы в области подмышечных впадин, поврежденную поверхность кожи). Большинство детей колонизируются стафилококком вскоре после рождения, однако с возрастом количество носителей уменьшается (с 63,8 %, наблюдаемых в период новорожденности, до 28,2 %, регистрируемых к 6-месячному возрасту). Носителями высокопатогенных метициллин-резистентных штаммов Staphylococcus aureus (methicillin resistant Staphylococcus aureus — MRSA) являются примерно 0,75–1 % здоровых представителей человечества [2, 44]. Именно MRSA-штамм, USA300, ассоциирован с большинством тяжело протекающих инфекций [13, 37]. Бактерии Staphylococcus aureus, кроме пневмонии, могут вызывать остеомиелит, эндокардит, гнойные поражения кожи.
Основными патоген-ассоциированными молекулярными структурами (pathogen associated molecular patterns — PAMP) бактерий Staphylococcus aureus, которые, взаимодействуя с образ-распознающими рецепторами (pattern recognition receptors — PRR) макроорганизма, вызывают развитие воспалительного процесса, являются стафилококковые факторы вирулентности: компоненты бактериальной стенки, токсины, адгезины, ферменты (табл. 1) [19, 60].
В развитии стафилококковой инфекции особую роль играют факторы вирулентности возбудителя (поверхностный протеин A, энтеротоксины, гемолизины, лейкоцидины), которые могут индуцировать воспалительный процесс без активации образ-распознающих рецепторов. Токсины Staphylococcus aureus способны взаимодействовать непосредственно с различными рецепторами, активность которых определяет течение бактериально-индуцированного воспалительного процесса (табл. 2).
Протеины Staphylococcus aureus оказывают мультифакторное влияние на иммунную систему, модулируя ее активность. Так, суперантигены (SEA/SEB и TSST) активируют Т-клетки; поверхностный протеин А вызывает поликлональную пролиферацию В-клеток и продукцию CXCL8, гемолизины индуцируют NLRP3-инфламмасому, токсины вызывают гибель различных эффекторных клеток [45, 48].
Суперантигены
В настоящее время под суперантигенами (SAg) понимают антигены, которые без предварительного процессинга и презентации антигенпрезентирующими клетками индуцируют неспецифическую активацию множества Т-лимфоцитов. Молекула SAg состоит из N-терминального региона, связывающегося с молекулами главного комплекса гистосовместимости, и C-терминального региона, взаимодействующего с Т-клеточным рецептором. В связи с этим SAg связываются, с одной стороны, с молекулами главного комплекса гистосовместимости (MHC) II класса, расположенными на мембране антигенпрезентирующей клетки, а с другой стороны — с вариабельной областью β-цепи (Vβ) Т-клеточного рецептора (TCR), локализованного на мембране Т-клетки, индуцируя неспецифическую активацию Т-лимфоцита (рис. 1) [38]. Каждый SAg взаимодействует с относительно уникальным набором Vβ-TCR. Эти взаимодействия вызывают активацию и пролиферацию Т-клеток. Типичный антиген стимулирует приблизительно 1 из 10 000 Т-клеток, в то время как SAg индуцирует до 50 % всех Т-клеток. Такая массовая активация Т-клеток приводит к гиперпродукции провоспалительных цитокинов [49].
/137-1.gif)
К SAg бактерий Staphylococcus aureus относятся стафилококковые энтеротоксины (SE), энтеротоксин-подобные вещества (SE-like — SE-l), которые вызывают проявления энтерита, и токсин 1 синдрома токсического шока (TSST-1), индуцирующий синдром токсического шока. Стафилококковые энтеротоксины, SE-l и TSST-1 представляют собой короткие секретируемые протеины, молекулярная масса которых составляет 22–30 кД [20, 58]. В настоящее время идентифицировано более чем 20 вариантов SE и примерно 10 SE-l протеинов [25, 27, 47].
Организм человека чрезвычайно чувствителен к действию SAg: внутривенное введение даже такой малой дозы, как 0,001 мкг/кг TSST-1, приводит к проявлениям токсического шока — лихорадки и выраженной гипотонии, а подкожное введение 0,05 мкг/кг TSST-1 кроликам приводит к гибели в 100 % случаев [35].
Считают, что бактерии Staphylococcus aureus используют SAg для облегчения процесса инвазии. Так, под влиянием SAg индуцируется продукция цитокинов и хемокинов, которые рекрутируют и активируют эффекторные иммунные клетки, нарушающие естественные барьеры макроорганизма [55].
Суперантигены Staphylococcus aureus оказывают влияние на многочисленные процессы макроорганизма, активируя и модулируя иммунный ответ, оксидативный и метаболический стресс, апоптоз клеток (табл. 3).
Необходимо отметить, что SAg бактерий Staphylococcus aureus ингибируют антительный ответ иммунной системы, и в настоящее время механизмы SAg-опосредованной иммуносупрессии в значительной степени неизвестны [35].
Стафилококковые энтеротоксины
Стафилококковые энтеротоксины впервые были описаны M.A. Barber в 1914 году как «трупный яд» — ptomaine (от греческого ptōma — труп). С действием данных веществ было связано возникновение рвоты и диареи у лиц, употребивших внутрь коровье молоко, инфицированное стафилококком [12]. Именно SE являются причиной развития клиники пищевого отравления при пероральном инфицировании золотистым стафилококком [27].
Неспецифическая активация стафилококковыми энтеротоксинами CD4+Т-лимфоцитов приводит к выраженному повышению продукции IL-2, IFN-γ, TNF-α.
Имитация антигензависимого взаимодействия антигенпрезентирующей клетки с Т-лимфоцитами, осуществляемая SE, индуцируется двумя сигналами. Сигнал 1 обусловлен взаимодействием суперантигена с TCR, которое обусловливает активацию протеинтирозинкиназы (protein tyrosine kinases — PTK), которая, в свою очередь, фосфорилирует тирозиновые активирующие мотивы интрадоменов TCR, что приводит к фосфорилированию фосфолипазы γ (phospholipase C gamma — PLC-γ) [33, 38]. Функционирование фосфолипазы γ активирует протеинкиназу С (protein kinase C — PKC), которая возбуждает фактор транскрипции NF-κB
и способствует увеличению внутриклеточной концентрации кальция, который активирует через кальциневрин фактор транскрипции NF-AT. Вторым сигналом активации Т-клеток являются поверхностные молекулы антигенпрезентирующей клетки и Т-лимфоцита. Показано, что в суперантиген-индуцированной активации Т-клеток происходит взаимодействие LFA-1 Т-лимфоцита с молекулой адгезии ICAM-1 антигенпрезентирующей клетки и CD28 Т-лимфоцита с костимулирующей молекулой CD80 антигенпрезентирующей клетки [36, 38]. Данное взаимодействие приводит к активации митоген-активируемой протеинкиназы (mitogen-activated protein kinase — МАРК), внеклеточной регулируемой киназы (extracellular signal regulated kinase — ERK) и с-Jun N-терминальной киназы (c-Jun N-terminal kinase — JNK), предопределяя активацию транскрипционных факторов
NF-κB, NF-AT и AP-1 [34, 50]. Транслокация факторов транскрипции в ядро клетки и их взаимодействие с энхансерами целевых генов усиливает экспрессию провоспалительных цитокинов (IL-1β,
IL-2, IL-6, TNF-α, IFN-γ) и хемокинов, в частности CCL2, вызывающего хемотаксис моноцитов и макрофагов. Продуцируемые цитокины могут выступать в качестве третьего сигнала активации Т-лимфоцитов. Цитокины IL-1β и TNF-α могут активировать фибробласты, эпителиальные и эндотелиальные клетки, обеспечивая воспалительную среду для активации Т-клеток. Влияние провоспалительных цитокинов на гепатоциты приводит к продукции острофазовых белков [33, 34].
Помимо активации CD4+Т-клеток, SE непосредственно взаимодействуют и с другими клетками организма: эпителиоцитами, макрофагами, эозинофилами, В-лимфоцитами и тучными клетками. Подобно макрофагам, эозинофилы и тучные клетки могут быть не только непосредственно активированы SE, но и функционировать в качестве вспомогательных клеток для активации Т-клеток. Взаимодействие SE с эпителиальными клетками слизистой оболочки способствует их активации и продукции хемокинов, рекрутирующих нейтрофилы и макрофаги [21]. Альвеолярные макрофаги под влиянием SE усиливают продукцию IL-8/СХСL8, рекрутирующего нейтрофилы; эотаксина, рекрутирующего эозинофилы; и IL-6 [14, 39].
Энтеротоксин SEB способствует развитию Th2-ассоциированного ответа и подавляет активность Treg-клеток, индуцируя состояние пролонгированного воспаления [57]. Взаимодействие эпителиальных клеток человека с SEB активирует продукцию IL-5, тимического стромального лимфопоэтина и GM-CSF [8]. Установлено, что уровень содержания антител IgE к энтеротоксину коррелирует с вероятностью развития бронхиальной астмы и концентрацией маркера аллергических процессов — катионного белка эозинофилов. Низкие дозы SEB индуцируют продукцию цитокинов в легких и приводят к увеличению представительства эозинофилов, в то время как высокие дозы SEB вызывают увеличение количества нейтрофилов и моноцитов в ткани легкого и способны индуцировать развитие интерстициальной пневмо-
нии [46].
Токсин 1 синдрома токсического шока
Фактор вирулентности TSST-1, взаимодействуя с CD40 или другим неопределенным рецептором эпителиальных клеток, индуцирует продукцию провоспалительных хемокинов: IL-8/СХСL8, CCL20, которые рекрутируют нейтрофилы и дендритные клетки соответственно. Важно также отметить, что эпителиальные клетки взаимодействуют с TSST-1 менее эффективно, чем Т- и антигенпрезентирующие клетки [4, 32, 53]. Содействие TSST-1 Staphylococcus aureus в процессе активации CD4+Т-лимфоцитов приводит к продукции широкого спектра цитокинов: IL-1β,
IL-2, IL-6, IFN-γ, TNF-α. Так, Norbert Stich и соавт. [56] показали, что TSST-1 способствует продукции IL-2 Т-клетками не только в очаге поражения, но и в селезенке. Совместное действие TSST-1 и LPS приводит к более выраженной гиперцитокинемии, преимущественно обусловленной гиперпродукцией IL-6, IFN-γ, TNF-α, чем влияние только TSST-1. Вероятно, данный синергизм обусловлен TSST-1-зависимым усилением экспрессии TLR4 на моноцитах. Показано, что после стимуляции TSST-1 провоспалительные цитокины IL-6, IFN-γ, TNF-α в основном продуцируются макрофагами и дендритными клетками, а не Т-лимфоцитами. Таким образом, авторы считают, что в ответ на действие TSST-1
Staphylococcus aureus первично активируются CD4+Т-клетки, которые в последующем способствуют усилению экспрессии IL-6, IFN-γ, TNF-α макрофагами и дендритными клетками. Гиперпродукция цитокинов может достигать такого уровня, при котором развивается клиника токсического шока.
Также TSST-1 может быть причинно-значимым фактором развития аутоиммунных процессов, в частности аутоиммунного артрита [50].
Поверхностный протеин А
Поверхностный протеин A (surface protein A — SpA) активно экспрессируется практически всеми штаммами Staphylococcus aureus. Молекула SpA в N-терминальной сигнальной последовательности содержит пять повторных доменов (E, D, A, B, C), обладающих аффинитетом к IgG, в С-терминальном регионе — LPXTG мотив, которым протеин SpA прикрепляется к поверхности бактериальной клетки
[22, 42].
Поверхностный протеин A взаимодействует с рецепторами тумор-некротизирующего фактора (tumor necrosis factor receptor superfamily, member 1 — TNFR1) и эпидермального фактора роста (epidermal growth factor receptor — EGFR) клеток макроорганизма [41].
Рецептор TNFR1 экспрессируется на различных типах клеток легочной ткани и при возбуждении протеином SpA, который непосредственно связывается с данным рецептором при помощи своих IgG-связывающих доменов, имитируя TNF-TNFR1 взаимодействие, активирует провоспалительные и антиапоптические сигнальные пути [23]. Установлено, что SpA-TNFR1 взаимодействие через TRAF2/TRADD/RIP1/MAPK и фактор транскрипции NF-κB индуцирует высвобождение эпителиальными клетками хемокина CXCL8, который рекрутирует нейтрофилы в очаг поражения [46].
Протеин SpA, взаимодействуя с EGFR, стимулирует металлопептидазу ADAM17 (ADAM metallopeptidase domain 17), которая расщеп-ляет TNFR1 [24]. Протеолитическими целями ADAM17 также являются амфирегулин, TGF-α, синдикан-1. ADAM17, расщепляя лиганды на поверхности клетки, способствует дальнейшей активации EGFR, ERK1/2 и продукции CXCL8 (рис. 2) [9]. Активация EGFR индуцирует репарацию эпителия и продукцию муцина [5].
Бактерии Staphylococcus aureus также индуцируют экспансию В-клеток через связывание белка SpA с Fab доменом VH3 IgM-рецепторов В-клеток [1].
Гемолизины
α-токсин
Основным секретируемым фактором вирулентности Staphylococcus aureus является α-токсин, или α-гемолизин, который представляет собой солютабный мономерный порообразующий протеин [7]. Гемолизин связывается и активирует дизинтегрин и металлопротеиназу 10 (ADAM metallopeptidase domain 10 — ADAM10) в эпителиальных, эндотелиальных и мононуклеарных клетках. Взаимодействуя с
мембраносвязанным протеином ADAM10 на эпителиальных клетках, Т- и В-лимфоцитах, α-токсин образует гептамер, формирующий малую пору, пропускающую ионы, что приводит к гибели клетки [48]. В мононуклеарных клетках α-гемолизин активирует протеин NLRP3 (nucleotide-binding domain and leucine-rich repeat containing gene family, pyrin domain containing 3), способствуя формированию инфламмасомы. Показано, что протеин ADAM10 имеет решающее значение для α-гемолизин-индуци-рованной активации NLRP3-инфламмасомы в человеческих моноцитах. Гемолизин-индуцированная гибель клеток опосредована активацией NLRP3-инфламмасомы. Токсический α-гемолизин активирует пироптоз, обусловливая выброс больших объе-мов провоспалительных цитокинов IL-1β и IL-18 [11, 17, 18, 52]. Глобальный дефицит NLRP3 за счет делеции гена сопровождается снижением смертности мышей, инфицированных Staphylococcus aureus. Однако дефицит протеина ADAM10 в клетках миелоидного происхождения сопровождается увеличением бактериальной нагрузки при стафилококковой инфекции [6]. Необходимо отметить, что активность инфламмасомы индуцируют и β-, σ-токсины, и PVL [45]. Также α-гемолизин связывается с металлопротеиназой ADAM10, что приводит к расщеплению Е-кадгерина и нарушению эпителиального барьера [28, 59].
Лейкоцидин LukAB
Лейкоцидин LukAB связывается с α-компонентом макрофагального интегрина 1 (CD11β) фагоцитов (нейтрофилов, моноцитов, макрофагов), индуцируя их гибель [15].
Лейкоцидин LukED и γ-токсин
Целевыми протеинами лейкоцидина LukAB и γ-токсина являются типичные хемокиновые рецепторы CCR5, CXCR1, CXCR2 и атипичный хемокиновый рецептор ACKR1 (atypical chemokine receptor 1), используя которые LukAB вызывает гибель клетки [48].
Лейкоцидин Пантона — Валентина
Лейкоцидин PVL представляет собой протеин, кодируемый двумя котранскрибируемыми генами lukF-PV и lukS-PV. Лейкоцидин PVL формирует октамерные поры в клеточных мембранах нейтрофилов и макрофагов [51]. Как пороформирующий токсин PVL индуцирует апоптоз клеток, индуцируя NLRP3-инфламмасомы [26]. Также PVL возбуждает TLR2, способствуя развитию воспаления легочной ткани [61].
В развитии стафилококковой пневмонии особое участие принимают патоген-ассоциированные молекулярные структуры Staphylococcus aureus: пептидогликаны, тейхоевые и липотейхоевые кислоты, ДНК бактерии, взаимодействующие с образ-распознающими рецепторами.
Конфликт интересов. Авторы заявляют об отсутствии какого-либо конфликта интересов при подготовке данной статьи.
Список литературы
1. Лапко А.В. Пептидные аналоги эпитопов взаимодействия протеина а с иммуноглобулинами класса g, их синтез и исследование целевых свойств / А.В. Лапко, Д.Н. Кислая, В.П. Голубович // Весці Нацыянальнай акадэміі навук Беларусі. — 2015. — № 4. — С. 56-61.
2. Лунева Е.Ю. Метициллинрезистентные штаммы Staphylococcus aureus — возбудители инфекционного процесса // Зыряновские чтения: материалы Всероссийской научно-практической конференции. — 2015. — С. 268-269.
3. Николаева И.В., Анохин В.А. Стафилококковые инфекции в педиатрии // Практическая медицина. — 2010. — № 1(40). — С. 24-27.
4. Aubert V. Induction of tumor necrosis factor alpha and interleukin-8 gene expression in bronchial epithelial cells by toxic shock syndrome toxin 1 / V. Aubert, D. Schneeberger, A. Sauty et al. // Infect. Immun. 2000 Jan; 68(1): 120-4. doi: 10.1128/IAI.68.1.120-124.2000.
5. Basbaum C. Mechanisms by which gram-positive bacteria and tobacco smoke stimulate mucin induction through the epidermal growth factor receptor (EGFR) / C. Basbaum, D. Li, E. Gensch et al. // Novartis Found Symp. 2002; 248: 171-6; discussion 176-80, 277-82. PMID: 12568494.
6. Becker R.E. Tissue-specific patterning of host innate immune responses by Staphylococcus aureus α-toxin / R.E. Becker, B.J. Berube, G.R. Sampedro et al. // J. Innate Immun. 2014; 6(5): 619-31. doi: 10.1159/000360006.
7. Berube B.J., Bubeck Wardenburg J. Staphylococcus aureus α-toxin: nearly a century of intrigue // Toxins (Basel). 2013 Jun; 5(6): 1140-66. doi: 10.3390/toxins5061140.
8. Bleier B.S. P-glycoprotein regulates Staphylococcus aureus enterotoxin B-stimulated interleukin-5 and thymic stromal lymphopoietin secretion in organotypic mucosal explants / B.S. Bleier, A. Singleton, A.L. Nocera et al. // Int. Forum Allergy Rhinol. 2016 Feb; 6(2): 169-77. doi: 10.1002/alr.21566.
9. Breshears L.M., Schlievert P.M., Peterson M.L. A disintegrin and metalloproteinase 17 (ADAM17) and epidermal growth factor receptor (EGFR) signaling drive the epithelial response to Staphylococcus aureus toxic shock syndrome toxin-1 (TSST-1) // J. Biol. Chem. 2012 Sep 21; 287(39): 32578-87. doi: 10.1074/jbc.M112.352534.
10. Clarke S.R., Foster S.J. Surface adhesins of Staphylococcus aureus // Adv. Microb. Physiol. 2006; 51: 187-224. PMID: 17010697.
11. Craven R.R Staphylococcus aureus alpha-hemolysin activates the NLRP3-inflammasome in human and mouse monocytic cells / R.R. Craven, X. Gao, I.C. Allen et al. // PLoS One. 2009 Oct 14; 4(10): e7446. doi: 10.1371/journal.pone.0007446.
12. Cretenet M., Even S., Le Loir Y. Unveiling Staphylococcus aureus enterotoxin production in dairy products: a review of recent advances to face new challenges // J. Dairy Sci. 2011; 91(2): 127-150.
13. DeLeo F.R. Community-associated meticillin-resistant Staphylococcus aureus / F.R. DeLeo, M. Otto, B.N. Kreiswirth, H.F. Chambers // Lancet. 2010 May 1; 375(9725): 1557-68. doi: 10.1016/S0140-6736(09)61999-1.
14. Desouza I.A. Role of sensory innervation in the rat pulmonary neutrophil recruitment induced by staphylococcal enterotoxins type A and B / I.A. Desouza, E.A. Camargo, N.S. Mariano et al. // Eur. J. Pharmacol. 2009 Jun 24; 613(1-3): 128-34. doi: 10.1016/j.ejphar.2009.04.010.
15. DuMont A.L. Staphylococcus aureus LukAB cytotoxin kills human neutrophils by targeting the CD11b subunit of the integrin Mac-1 / A.L. DuMont, P. Yoong, C.J. Day et al. // Proc. Natl. Acad. Sci USA. 2013 Jun 25; 110(26): 10794-9. doi: 10.1073/pnas. 1305121110.
16. Dunyach-Remy C. Staphylococcus aureus Toxins and Diabetic Foot Ulcers: Role in Pathogenesis and Interest in Diagnosis / C. Dunyach-Remy, C. Ngba Essebe, A. Sotto, J.P. Lavigne // Toxins (Basel). 2016 Jul 7; 8(7): E209. doi: 10.3390/toxins8070209.
17. Ezekwe E.A. Jr, Weng C., Duncan J.A. ADAM10 Cell Surface Expression but Not Activity Is Critical for Staphylococcus aureus α-Hemolysin-Mediated Activation of the NLRP3 Inflammasome in Human Monocytes // Toxins (Basel). 2016 Mar 30; 8(4): 95. doi: 10.3390/toxins8040095.
18. Fitzpatrick E.A. A Neonatal Murine Model of MRSA Pneumonia / E.A. Fitzpatrick, D. You, B. Shrestha et al. // PLoS One. 2017 Jan 6; 12(1): e0169273. doi: 10.1371/journal.pone.0169273.
19. Foster T.J. Adhesion, invasion and evasion: the many functions of the surface proteins of Staphylococcus aureus / T.J. Foster, J.A. Geoghegan, V.K. Ganesh, M. Höök // Nat. Rev. Microbiol. 2014 Jan; 12(1): 49-62. doi: 10.1038/nrmicro3161.
20. Fraser J.D., Proft T. The bacterial superantigen and super-antigen-like proteins // Immunol. Rev. 2008 Oct; 225: 226-43. doi: 10.1111/j.1600-065X.2008.00681.x.
21. Fujisawa N. Staphylococcal enterotoxin A-induced injury of human lung endothelial cells and IL-8 accumulation are mediated by TNF-alpha / N. Fujisawa, S. Hayashi, A. Kurdowska et al. // J. Immunol. 1998 Nov 15; 161(10): 5627-32. PMID: 9820542.
22. Ganesh V.K. Lessons from the Crystal Structure of the S. aureus Surface Protein Clumping Factor A in Complex With Tefibazumab, an Inhibiting Monoclonal Antibody / V.K. Ganesh, X. Liang, J.A. Geoghegan et al. // EBioMedicine. 2016 Nov; 13: 328-338. doi: 10.1016/j.ebiom.2016.09.027.
23. Gómez M.I. Staphylococcus aureus protein A activates TNFR1 signaling through conserved IgG binding domains / M.I. Gómez, M. O’Seaghdha, M. Magargee et al. // J. Biol. Chem. 2006 Jul 21; 281(29): 20190-6. doi: 10.1074/jbc.M601956200.
24. Gómez M.I. Staphylococcus aureus protein A induces airway epithelial inflammatory responses by activating TNFR1 / M.I. Gómez, A. Lee, B. Reddy et al. // Nat. Med. 2004 Aug; 10(8): 842-8. doi: 10.1038/nm1079.
25. Grumann D., Nübel U., Bröker B.M. Staphylococcus aureus toxins-their functions and genetics // Infect. Genet. Evol. 2014 Jan; 21: 583-92. doi: 10.1016/j.meegid.2013.03.013.
26. Holzinger D. Staphylococcus aureus Panton-Valentine leukocidin induces an inflammatory response in human phagocytes via the NLRP3 inflammasome / D. Holzinger, L. Gieldon, V. Mysore et al. // J. Leukoc. Biol. 2012 Nov; 92(5): 1069-81. doi: 10.1189/jlb.0112014.
27. Huvenne W., Hellings P.W., Bachert C. Role of staphylococcal superantigens in airway disease // Int. Arch. Allergy Immunol. 2013; 161(4): 304-14. doi: 10.1159/000350329.
28. Inoshima I. A Staphylococcus aureus pore-forming toxin subverts the activity of ADAM10 to cause lethal infection in mice / I. Inoshima, N. Inoshima, G.A. Wilke et al. // Nat. Med. 2011 Sep 18; 17(10): 1310-4. doi: 10.1038/nm.2451.
29. Iroh Tam P.Y. Blood Culture in Evaluation of Pediatric Community-Acquired Pneumonia: A Systematic Review and Meta-analysis / P.Y. Iroh Tam, E. Bernstein, X. Ma, P. Ferrieri // Hosp. Pediatr. 2015 Jun; 5(6): 324-36. doi: 10.1542/hpeds.2014-0138.
30. Kloos W.E., Smith P.B. Staphylococci / Lennette E.H., Balows A., Hausler W.J., Truant J.P. // Manual of Clinical Microbiology. Washington, DC: American Society for Microbiology; 1980. 83-87.
31. Kluytmans J., van Belkum A., Verbrugh H. Nasal carriage of Staphylococcus aureus: epidemiology, underlying mechanisms, and associated risks // Clin. Microbiol. Rev. 1997 Jul; 10(3): 505-20. PMID: 9227864.
32. Krakauer T. Stimulant-dependent modulation of cytokines and chemokines by airway epithelial cells: cross talk between pulmonary epithelial and peripheral blood mononuclear cells // Clin. Diagn. Lab. Immunol. 2002 Jan; 9(1): 126-31. doi: 10.1128/CDLI.9.1.126-131.2002.
33. Krakauer T., Pradhan K., Stiles B.G. Staphylococcal Super-antigens Spark Host-Mediated Danger Signals // Front. Immunol. 2016 Feb 2; 7: 23. doi: 10.3389/fimmu.2016.00023.
34. Krakauer T., Stiles B.G. The staphylococcal enterotoxin (SE) family: SEB and siblings // Virulence. 2013 Nov 15; 4(8): 759-73. doi: 10.4161/viru.23905.
35. Kulhankova K., King J., Salgado-Pabón W. Staphylococcal toxic shock syndrome: superantigen-mediated enhancement of endotoxin shock and adaptive immune suppression // Immunol. Res. 2014 Aug; 59(1-3): 182-7. doi: 10.1007/s12026-014-8538-8.
36. Levy R. Superantigens hyperinduce inflammatory cytokines by enhancing the B7-2/CD28 costimulatory receptor interaction / R. Levy, Z. Rotfogel, D. Hillman et al. // Proc. Natl. Acad. Sci USA. 2016 Oct 18; 113(42): E6437-E6446.
37. Liu Y. Characterization of community-associated Staphylococcus aureus from skin and soft-tissue infections: a multicenter study in China / Y. Liu, Z Xu., Z. Yang et al. // Emerg. Microbes. Infect. 2016 Dec 21; 5(12): e127. doi: 10.1038/emi.2016.128.
38. Louis-Dit-Sully C. Activation of the TCR complex by peptide-MHC and superantigens / C. Louis-Dit-Sully, B. Blumenthal, M. Duchniewicz et al. // EXS. 2014; 104: 9-23. doi: 10.1007/978-3-0348-0726-5_2.
39. Mariano N.S. Pre-exposure to Staphylococcal entero-toxin A exacerbates the pulmonary allergic eosinophil recruitment in rats / N.S. Mariano, G.C. de Mello, T. Ferreira et al. // Int. Immunopharmacol. 2010 Jan; 10(1): 43-9. doi: 10.1016/j.intimp. 2009.09.017.
40. McMullan B.J. Epidemiology and Mortality of Staphylococcus aureus Bacteremia in Australian and New Zealand Children / B.J. McMullan, A. Bowen, C.C. Blyth et al. // JAMA Pediatr. 2016 Oct 1; 170(10): 979-986. doi: 10.1001/jamapediatrics.2016. 1477.
41. Mendoza Bertelli A. Staphylococcus aureus protein A enhances osteoclastogenesis via TNFR1 and EGFR signaling / A. Mendoza Bertelli, M.V. Delpino, S. Lattar et al. // Biochim. Biophys. Acta. 2016 Oct; 1862(10): 1975-83. doi: 10.1016/j.bbadis.2016.07.016.
42. Nagarajan R., Hendrickx A.P., Ponnuraj K. The crystal structure of the ligand-binding region of serine-glutamate repeat containing protein A (SgrA) of Enterococcus faecium reveals a new protein fold: functional characterization and insights into its adhesion function // FEBS J. 2016 Aug; 283(16): 3039-55. doi: 10.1111/febs. 13792.
43. Ogston A. Micrococcus Poisoning // J. Anat. Physiol. 1882 Jul; 16(Pt 4): 526-67. PMID: 17231444.
44. Palavecino E.L. Clinical, epidemiologic, and laboratory aspects of methicillin-resistant Staphylococcus aureus infections // Methods Mol. Biol. 2014; 1085: 1-24. doi: 10.1007/978-1-62703-664-1_1.
45. Parker D. Innate Immune Signaling Activated by MDR Bacteria in the Airway / D. Parker, D. Ahn, T. Cohen, A. Prince // Physiol. Rev. 2016 Jan; 96(1): 19-53. doi: 10.1152/physrev.00009.2015.
46. Parker D., Prince A. Immunopathogenesis of Staphylococcus aureus pulmonary infection // Semin. Immunopathol. 2012 Mar; 34(2): 281-97. doi: 10.1007/s00281-011-0291-7.
47. Pinchuk I.V., Beswick E.J., Reyes V.E. Staphylococcal enterotoxins // Toxins (Basel). 2010 Aug; 2(8): 2177-97. doi: 10.3390/toxins2082177.
48. Reyes-Robles T., Torres V.J. Staphylococcus aureus Pore-Forming Toxins // Curr. Top. Microbiol. Immunol. 2016 Jul 13. doi: 10.1007/82_2016_16.
49. Sharma P., Wang N., Kranz D.M. Soluble T cell receptor Vβ domains engineered for high-affinity binding to staphylococcal or streptococcal superantigens // Toxins (Basel). 2014 Jan 28; 6(2): 556-74. doi: 10.3390/toxins6020556.
50. Shokrollahi M.R. Searching the Staphylococcal Superantigens: Enterotoxins A, B, C, and TSST1 in Synovial Fluid of Cases With Negative Culture Inflammatory Arthritis / M.R. Shokrollahi, S. Noorbakhsh, M. Aliakbari, A. Tabatabaei // Jundishapur J. Microbiol. 2014 Jul; 7(7): e11647. doi: 10.5812/jjm.11647.
51. Shrestha B. Review on Panton Valentine leukocidin toxin carriage among Staphylococcus aureus // J. Nepal. Health Res. Counc. 2013 Sep; 11(25): 305-12. PMID: 24908537.
52. Soong G. Staphylococcus aureus activation of caspase 1/calpain signaling mediates invasion through human keratinocytes / G. Soong, J. Chun, D. Parker, A. Prince // J. Infect. Dis. 2012 May 15; 205(10): 1571-9. doi: 10.1093/infdis/jis244.
53. Spaulding A.R. Staphylococcal and streptococcal superantigen exotoxins / A.R. Spaulding, W. Salgado-Pabón, P.L. Kohler et al. // Clin. Microbiol. Rev. 2013 Jul; 26(3): 422-47. doi: 10.1128/CMR.00104-12.
54. Spencer D.A., Thomas M.F. Necrotising pneumonia in children // Paediatr Respir Rev. 2014 Sep; 15(3): 240-5; quiz 245. doi: 10.1016/j.prrv.2013.10.001.
55. Stach C.S., Herrera A., Schlievert P.M. Staphylococcal superantigens interact with multiple host receptors to cause serious di-seases // Immunol. Res. 2014 Aug; 59(1-3): 177-81. doi: 10.1007/s12026-014-8539-7.
56. Stich N. Staphylococcal superantigen (TSST-1) mutant analysis reveals that t cell activation is required for biological effects in the rabbit including the cytokine storm / N. Stich, M. Waclavicek, N. Model, M.M. Eibl // Toxins (Basel). 2010 Sep; 2(9): 2272-88. doi: 10.3390/toxins2092272.
57. Tilahun A.Y. Systemic inflammatory response elicited by super-antigen destabilizes T regulatory cells, rendering them ineffective du-ring toxic shock syndrome / A.Y. Tilahun, V.R. Chowdhary, C.S. David, G. Rajagopalan // J. Immunol. 2014 Sep 15; 193(6): 2919-30. doi: 10.4049/jimmunol.1400980.
58. Uchiyama T. Staphylococcal superantigens and the diseases they cause / Alouf J.E., Popoff M.R. // The Comprehensive Sourcebook of Bacterial Protein Toxins, 3rd Edition. London, Academic Press, 2006: 830-43.
59. Wilke G.A., Bubeck Wardenburg J. Role of a disintegrin and metalloprotease 10 in Staphylococcus aureus alpha-hemolysin-mediated cellular injury // Proc. Natl. Acad. Sci USA. 2010 Jul 27; 107(30): 13473-8. doi: 10.1073/pnas.1001815107.
60. Zecconi A., Scali F. Staphylococcus aureus virulence factors in evasion from innate immune defenses in human and animal di-seases // Immunol. Lett. 2013 Feb; 150(1-2): 12-22. doi: 10.1016/j.imlet.2013.01.004.
61. Zivkovic A. TLR 2 and CD14 mediate innate immunity and lung inflammation to staphylococcal Panton-Valentine leukocidin in vivo / A. Zivkovic, O. Sharif, K. Stich et al. // J. Immunol. 2011 Feb 1; 186(3): 1608-17. doi: 10.4049/jimmunol.1001665.

/134-1.gif)
/135-1.gif)
/136-1.gif)
/137-2.gif)
/137-1.gif)
/138-1.gif)
/140-1.gif)