Резюме
Актуальність. Схильність до частих гострих респіраторних вірусних інфекцій (ГРВІ) і, зокрема, повторного перебігу бронхообструктивного синдрому (БОС) у дітей раннього віку залишається актуальним питанням педіатрії. Останнім часом серед факторів ризику повторних епізодів БОС особлива увага приділяється вивченню рівня забезпеченості вітаміном D (VD, 25-гідроксивітамін-D (25(ОН)D). Нещодавні дослідження демонструють зв’язок між низьким рівнем VD і підвищеною сприйнятливістю до вірусних інфекцій. Водночас питання щодо вивчення необхідності корекції статусу VD у дітей із повторним БОС є досі не вивченим. Мета. Вивчення рівня забезпеченості VD та ефективності корекції його порушень у дітей раннього віку з повторними епізодами БОС. Матеріали та методи. Обстежено 120 дітей віком від 6 місяців до 3 років із клінічним діагнозом «гострий обструктивний бронхіт». Пацієнти були розподілені на дві групи (1-ша група — 60 дітей з епізодичним БОС (менше 3 епізодів протягом року), 2-га група — 60 дітей із повторним БОС (3 і більше епізодів протягом року)). Групу контролю становили 30 клінічно здорових дітей віком від 6 місяців до 3 років. Усім хворим проводили оцінку анамнестичних даних і в тому числі тих, що впливають на рівень забезпеченості VD. Визначали концентрацію 25(OH)D у сироватці крові електрохемілюмінесцентним методом на аналізаторі Cobas e411 (серійний номер 1041-24, виробник — Roche Diagnostics GmbH, Німеччина). Методом простої рандомізації із групи з повторним БОС обрано 30 пацієнтів (2а група), яким призначали препарат вітаміну D3 у дозі 1000 МО щодня протягом року, за винятком літніх місяців. Тривалість катамнестичного спостереження — 12 місяців. Ефективність застосування вітаміну D3 оцінювали на підставі динаміки респіраторної захворюваності, частоти епізодів БОС, а також за динамікою показників сироваткового рівня 25(OH)D. При аналізі отриманих даних використовували непараметричні статистичні критерії. Різниця між показниками, що порівнювались, вважалась вірогідною при р < 0,05. Результати. Більшість пацієнтів із повторним перебігом захворювання (56,6 %) мали 4 епізоди БОС за останні 12 місяців. Середній вміст 25(OH)D у сироватці крові в дітей 1-ї групи становив 33,0 (28,19; 41,97) нг/мл, 2-ї групи — 13,68 (7,96; 19,51) нг/мл (p < 0,001). Аналіз анамнестичних показників, які впливають на рівень VD, виявив, що ймовірність недостатності або дефіциту VD у дітей раннього віку з БОС, які не отримують вітамін D, набагато вища, ніж у дітей, які приймають його щодня в дозі 500–1000 МО (OR = 0,047; 95% СІ 0,018–0,126; р < 0,001). Виявлено зворотну залежність між рівнем VD як із частотою БОС (r = –0,27, р = 0,002), так і з віком обстежених пацієнтів (r = –0,33, р = 0,009). У дітей 2-ї групи середня частота епізодів ГРВІ за останній рік була вище, ніж у пацієнтів 1-ї групи (4,5 (3,0;5,5) і 3 (2,0;5,0) відповідно, р < 0,001), при цьому виявлено, що середній рівень 25(OH)D у сироватці крові мав тенденцію до більш низьких показників за наявності 5 і більше епізодів ГРВІ на рік. Після прийому препарату вітаміну D3 у більшості пацієнтів відзначалось зменшення частоти БОС до 1–2 епізодів протягом року, а також зниження респіраторної захворюваності на 50 %. Ми виявили, що після застосування вітаміну D3 спостерігалось вірогідне зростання концентрації сироваткового рівня 25(OH)D порівняно з його рівнем, визначеним на початку дослідження (25,11 (12,14; 42,47) нг/мл і 13,93 (9,60; 20,5) нг/мл відповідно, p = 0,002 за Т-критерієм Вілкоксона). Висновки. Преважна більшість пацієнтів із повторним перебігом БОС мають дефіцит VD, що може розглядатись як предиктор повторних епізодів захворювання. На рівень забезпеченості VD найбільшою мірою впливає рівень його саплементації. Дітям раннього віку, які часто хворіють на ГРВІ, і в тому числі з повторним БОС, важливо оцінювати анамнестичні дані щодо застосування вітаміну D та при необхідності визначати рівень 25(OH)D у сироватці крові. Встановлено, що при зниженні сироваткової концентрації 25(OH)D кількість епізодів БОС і ГРВІ зростає. Також рівень VD має тенденцію до більш низьких показників при збільшенні віку пацієнтів. Щоденний прийом 1000 МО вітаміну D3 протягом 12 місяців сприяє зменшенню частоти ГРВІ і в тому числі епізодів БОС у дітей раннього віку.
Актуальность. Склонность к частым острым респираторным вирусным инфекциям (ОРВИ) и, в частности, повторного течения бронхообструктивного синдрома (БОС) у детей раннего возраста остается актуальным вопросом педиатрии. В последнее время среди факторов риска повторных эпизодов БОС особое внимание уделяется изучению уровня обеспеченности витамином D (VD, 25-гидроксивитамин-D (25(ОН)D)). В последних исследованиях была продемонстрирована связь между низким уровнем VD и повышенной восприимчивостью к вирусным инфекциям. В то же время вопрос об изучении необходимости коррекции статуса VD у детей с повторным БОС является неизученным. Цель. Изучение уровня обеспеченности VD и эффективности коррекции его нарушений у детей раннего возраста с повторными эпизодами БОС. Материалы и методы. Обследовано 120 детей в возрасте от 6 месяцев до 3 лет с клиническим диагнозом «острый обструктивный бронхит». Пациенты были распределены на две группы (1-я группа — 60 детей с эпизодическим БОС (менее 3 эпизодов в течение года), 2-я группа — 60 детей с повторным БОС (3 и более эпизода в течение года)). Группу контроля составили 30 клинически здоровых детей в возрасте от 6 месяцев до 3 лет. Всем больным проводили оценку анамнестических данных, в том числе тех, которые влияют на уровень обеспеченности VD. Определяли концентрацию 25(OH)D в сыворотке крови электрохемилюминесцентным методом на анализаторе Cobas e411 (серийный номер 1041-24, производитель — Roche Diagnostics GmbH, Германия). Методом простой рандомизации из группы с повторным БОС отобраны 30 пациентов (2а группа), которым назначали препарат витамина D3 в дозе 1000 МЕ ежедневно в течение года, за исключением летних месяцев. Продолжительность катамнестического наблюдения составила 12 месяцев. Эффективность применения витамина D3 оценивалась на основании динамики респираторной заболеваемости, частоты эпизодов БОС, а также по динамике показателей сывороточного уровня 25(OH)D. При анализе полученных данных использовали непараметрические статистические критерии. Разница между показателями, которые сравнивались, считалась достоверной при р < 0,05. Результаты. Большинство пациентов с повторным течением заболевания (56,6 %) имели 4 эпизода БОС за последние 12 месяцев. Среднее содержание 25(OH)D в сыворотке крови у детей 1-й группы составило 33,0 (28,19; 41,97) нг/мл, 2-й группы — 13,68 (7,96; 19,51) нг/мл (p < 0,001). При анализе анамнестических показателей, влияющих на уровень VD, обнаружено, что вероятность недостаточности или дефицита VD у детей раннего возраста с БОС, которые не получают витамин D, намного выше, чем у детей, принимающих его ежедневно в дозе 500–1000 МЕ (OR = 0,047; 95% CI 0,018–0,126; р < 0,001). Выявлена обратная зависимость между уровнем VD как с частотой БОС (r = –0,27, р = 0,002), так и с возрастом обследованных пациентов (r = –0,33, р = 0,009). У детей 2-й группы средняя частота эпизодов ОРВИ за последний год была выше, чем у пациентов 1-й группы (4,5 (3,0; 5,5) и 3 (2,0; 5,0) соответственно, р < 0,001), при этом выявлено, что средний уровень 25(OH)D в сыворотке крови имел тенденцию к более низким показателям при наличии 5 и более эпизодов ОРВИ в год. После приема препарата витамина D3 у большинства пациентов отмечалось уменьшение частоты БОС до 1–2 эпизодов в течение года, а также снижение респираторной заболеваемости на 50 %. Мы обнаружили, что после применения витамина D3 наблюдалось достоверное увеличение концентрации сывороточного уровня 25(OH)D по сравнению с его уровнем, определенным в начале исследования (25,11 (12,14; 42,47) нг/мл и 13,93 (9,60; 20,5) нг/мл соответственно; p = 0,002 по Т-критерию Вилкоксона). Выводы. Подавляющее большинство пациентов с повторным течением БОС имеют дефицит VD, что может рассматриваться в качестве предиктора повторных эпизодов заболевания. На уровень обеспеченности VD в наибольшей степени влияет уровень его саплементации. Детям раннего возраста, часто болеющим ОРВИ, в том числе с повторным БОС, важно оценивать анамнестические данные о применении витамина D и при необходимости определять уровень 25(OH)D в сыворотке крови. Установлено, что при снижении концентрации 25(OH)D в сыворотке крови количество эпизодов БОС и ОРВИ возрастает. Также уровень VD имеет тенденцию к более низким показателям при увеличении возраста пациентов. Ежедневный прием 1000 МЕ витамина D3 в течение 12 месяцев способствует уменьшению частоты ОРВИ, в том числе эпизодов БОС, у детей раннего возраста.
Background. Predisposition to frequent acute respiratory viral infections (ARVI), in particular recurrent course of broncho-obstructive syndrome (BOS), in young children remains an important issue in pediatrics. Special attention has been recently paid to studying the level of vitamin D (VD, 25(OH)D) among other risk factors of recurrent episodes of BOS. Recent studies demonstrate a correlation between low levels of VD and increased susceptibility to viral infections. At the same time, the issue of studying the need to correct VD status in children with recurrent BOS is still unexplored. Thus, the purpose of the research was to study VD level and effectiveness of correction of its disturbances in young children with recurrent episodes of BOS. Materials and methods. We examined 120 children aged 6 months to 3 years with a clinical diagnosis of acute obstructive bronchitis. Patients were divided into two groups (group I — 60 children with episodic BOS (less than 3 episodes per year), group II — 60 children with recurrent BOS (3 and more episodes per year)). The control group consisted of 30 clinically healthy children aged from 6 months to 3 years. All patients were evaluated for anamnestic data, including those that affect VD. The concentration of 25-hydroxyvitamin D (25(OH)D) in the blood serum was determined by an electrochemiluminescence method on the Cobas e411 analyzer (serial number 1041-24, manufactured by Roche Diagnostics GmbH, Germany). We chose 30 patients from a group with recurrent BOS by a simple randomization, they received 1,000 IU of vitamin D3 daily during the year, except summer. The duration of follow-up was 12 months. The effectiveness of vitamin D3 was evaluated based on the dynamics of respiratory morbidity, incidence of BOS episodes and dynamics of serum level of 25(OH)D. Nonparametric statistical criteria were used in the analysis of the obtained data. The difference between compared indicators was considered to be significant at a rate of p < 0.05. Results. Most patients with a recurrent course of the disease (56.6 %) had 4 episodes of BOS for the last 12 months. The mean 25(OH)D serum level in children of group I was 33.0 (28.19; 41.97) ng/ml and group II — 13.68 (7.96; 19.51) ng/ml (p < 0.001). The analysis of anamnestic parameters that affect VD level showed that the probability of VD insufficiency or deficiency in young children with BOS who are not receiving vitamin D is much higher than in children who is taking it daily at a dose of 500–1,000 IU (odds ratio = 0.047; 95% confidence interval 0.018–0.126; p < 0.001). The inverse relationship was revealed between VD level and both the incidence of BOS (r = –0.27, p = 0.002) and the age of examined patients (r = –0.33, p = 0.009). The average incidence of episodes of acute respiratory infections in children of group II for the last year was higher than that of patients in group I (4.5 (3.0; 5.5) and 3 (2.0; 5.0), respectively, p < 0.001). We found that the mean 25(OH)D level tended to be lower in the presence of 5 or more episodes of ARVI per year. In most patients after taking vitamin D3, the incidence of BOS was reduced to 1–2 episodes per year, and respiratory morbidity decreased by 50 %. We revealed that after vitamin D3 supplementation, 25(OH)D level was significantly increased as compared to that of determined at baseline (25.11 (12.14; 42.47) ng/ml and 13.93 (9.60; 20.5) ng/ml, respectively, p = 0.002 according to the Wilcoxon T test). Conclusions. The majority of patients with recurrent BOS has VD deficiency that might be considered as a predictor of recurrent episodes of the disease. VD content is mostly dependent on the level of its supplementation. It is important to assess anamnestic data about using vitamin D and if necessary to determine serum level of 25(OH)D in young children who are often suffer from ARVI, including recurrent BOS. It has been established that in case of decreased serum concentration of 25(OH)D, the number of BOS and ARVI episodes increases. Also, VD level tends to be lower with increasing age. A daily intake of 1,000 IU of vitamin D3 for 12 months contributes to a decrease in ARVI incidence, including episodes of BOS, in young children.
Вступ
На сьогодні проблема схильності дітей раннього віку до гострих респіраторних вірусних інфекцій (ГРВІ) і, зокрема, повторних епізодів бронхообструктивного синдрому (БОС) залишається досить актуальною для сучасної педіатрії. Чимало досліджень присвячено вивченню предикторів повторного перебігу БОС у дітей раннього віку. Одним із факторів, що підвищують схильність до частих респіраторних захворювань, вважається низький рівень забезпеченості вітаміном D (VD, 25-гідроксивітамін-D (25(ОН)D) [1–3]. Результати клінічних досліджень демонструють зв’язок між низькими рівнями VD і підвищеною сприйнятливістю до інфекцій вірусної, бактеріальної та грибкової етіології [4–6], що, в свою чергу, свідчить про важливу роль VD у забезпеченні протиінфекційного імунітету. Доведено, що численні ефекти VD реалізуються на різних етапах імунної відповіді, починаючи з неспецифічної внаслідок підтримання індукції антимікробних пептидів і закінчуючи синтезом специфічних антитіл [4, 7–9].
За даними Л.В. Квашніної (2017), понад 80 % дитячого населення України має недостатній рівень забезпеченості VD, при цьому даний показник у дітей віком від 1 місяця до 3 років становить 78,6 % [7]. Зважаючи на дані щодо впливу VD на перебіг і частоту гострої респіраторної патології, актуальним залишається питання профілактики та корекції дефіциту VD. Вважається, що оптимальною концентрацією 25(ОН)D у сироватці крові є 30–60 нг/мл, що відзначається при прийомі добової дози вітаміну 1000–2000 МО залежно від віку [7].
На сьогодні зв’язок між рівнем забезпеченості VD і частотою повторних епізодів БОС у дітей раннього віку вивчений недостатньо. Лише в одиничних дослідженнях вивчалось прогностичне значення недостатності VD у дітей раннього віку з повторним перебігом БОС, результати яких не–однозначні та обмежені. Слід також зазначити, що роботи з вивчення ефективності корекції статусу VD у дітей із повторним БОС досі відсутні.
Метою нашого дослідження стало вивчення рівня забезпеченості VD та ефективності корекції його порушень у дітей раннього віку з повторними епізодами БОС.
Матеріали та методи
Проведене клінічне дослідження включало обстеження 150 дітей віком від 6 місяців до 3 років. Основну групу становили 120 пацієнтів із клінічним діагнозом «гострий обструктивний бронхіт», серед них 1-шу групу становили 60 дітей з епізодичним БОС (менше трьох епізодів протягом попереднього року) та 2-гу групу — 60 дітей із повторним БОС (3 і більше епізоди протягом попереднього року). Набір пацієнтів проводився з січня 2016 по квітень 2017 року.
Дослідження проводилось за згодою Комісії з питань біомедичної етики ДЗ «Дніпропетровська медична академія МОЗ України» та за наявності письмової інформованої згоди батьків на участь у дослідженні.
Із дослідження виключались діти з уродженими захворюваннями бронхолегеневої системи, імунодефіцитами, затримкою фізичного розвитку, проявами рахіту, такі, що народилися недоношеними, а також пацієнти, які приймали системні глюкокортикостероїди або антиконвульсанти в анамнезі.
Середній вік хворих 1-ї групи становив 18,16 ± 7,6 місяця, 2-ї групи — 22,86 ± 7,75 місяця (р > 0,05). За гендерною ознакою в обох групах переважали хлопчики, їх було приблизно по 70 % від загальної кількості обстежених (р > 0,05).
Клініко-лабораторне обстеження хворих проводилось на другу або третю добу від початку захворювання. Було зібрано анамнестичні дані всіх пацієнтів, зокрема, ті, що впливають на рівень забезпеченості VD. Серед інших факторів оцінювався рівень інсоляції, тобто час перебування на сонці з 10-ї до 15-ї години дня мінімальною тривалістю 15 хвилин [10]. Рівень інсоляції вважали низьким, якщо цей показник становив менше 15 діб на місяць, помірним — від 15 до 30 діб на місяць, а показник 30 діб і більше оцінювався як високий рівень інсоляції [11].
Лабораторні дослідження проводились у лікувально-діагностичному центрі ТОВ «Аптека медичної академії» та включали визначення концентрації 25(OH)D у сироватці крові електрохемілюмінесцентним методом на аналізаторі Cobas e411 (серійний номер 1041-24, виробник — Roche Diagnostics GmbH, Німеччина). Слід зазначити, що у 90 % пацієнтів 1-ї групи та 96,6 % пацієнтів 2-ї групи рівень 25(OH)D у сироватці крові визначали у зимово-весняний період, за винятком травня. Рівень забезпеченості VD оцінювали згідно з рекомендаціями Endocrine Practice Guidelines Committee (Holick M.F., 2011). Достатнім рівнем VD вважали показник 25(OH)D у сироватці крові 30 нг/мл і більше, недостатність VD діагностували при рівні 20–29 нг/мл та дефіцит, якщо показник 25(OH)D у сироватці крові був нижче 20 нг/мл [12].
Методом простої рандомізації з групи із повторним БОС обрано 30 пацієнтів (2а група), яким призначали препарат вітаміну D3 у дозі 1000 МО щодня протягом року, за винятком літніх місяців. Доза препарату вітаміну D3 для корекції статусу VD була обрана з урахуванням рекомендацій V Конгресу педіатрів України (2008) і методичних рекомендацій з лікування та профілактики дефіциту вітаміну D для населення країн Центральної Європи (2013), в яких зазначено, що доза 1000 МО є найбільш оптимальною для профілактики дефіциту VD у дітей раннього віку [4, 13]. Тривалість катамнестичного спостереження дорівнювала 12 місяцям. Ефективність застосування вітаміну D3 оцінювалась на підставі динаміки респіраторної захворюваності, частоти епізодів БОС, а також за динамікою показників сироваткового рівня 25(OH)D через 12 місяців.
Як групу контролю обстежено 30 клінічно здорових дітей віком від 6 місяців до 3 років, середній вік яких становив 20,50 ± 11,24 місяця. За гендерними співвідношеннями, як і в основній групі, хлопчики становили 70 % від загальної кількості обстежених. Критеріями включення дітей у контрольну групу були: відсутність хронічних захворювань, гострої респіраторної патології у момент огляду та епізодів БОС в анамнезі, частота ГРВІ не більше 3 разів на рік.
Статистична обробка отриманих результатів проводилась за допомогою програмного забезпечення Statistica 6.1 (серійний номер AGAR909 E415822FA) та Excel 2010. При статистичному аналізі результатів дослідження використовували непараметричні показники: медіана (Ме), нижній і верхній квартилі (Q25 та Q75), оскільки переважна більшість кількісних показників характеризувались типом розподілу, що відрізняється від нормального. Вірогідність відмінностей відносних показників оцінювалась з використанням критерію χ2 Пірсона, для кількісних ознак використовувався U-критерій Манна — Уїтні. З метою порівняння результатів 12-місячних спостережень за дітьми з повторним БОС використовували Т-критерій Вілкоксона. Для визначення зв’язку між кількісними параметрами розраховували показники рангової кореляції Спірмена та відношення шансів між якісними показниками. Різниця між показниками, що порівнювалися, вважалась вірогідною при р < 0,05.
Результати
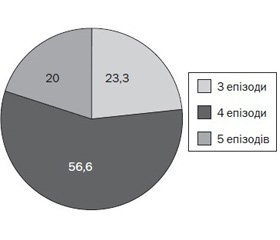
За нашими даними, частка пацієнтів із повторним перебігом захворювання, які мали 3 епізоди БОС за останні 12 місяців, становила 21,7 %, 4 епізоди — 56,6 %, 5 епізодів — 21,7 %.
Проведене дослідження рівня забезпеченості VD показало, що у дітей 2-ї групи середній вміст 25(OH)D
у сироватці крові був значно нижчим, ніж у пацієнтів 1-ї групи (13,68 (7,96; 19,51) нг/мл і 33,0 (28,19; 41,97) нг/мл відповідно, p < 0,001 за U-критерієм Манна — Уїтні). Під час подальшого вивчення особливостей статусу VD у дітей досліджуваних груп ми встановили, що оптимальний рівень 25(OH)D у сироватці крові набагато частіше реєструвався в дітей 1-ї групи, при цьому в 2-й групі переважали діти з дефіцитом VD. Недостатність VD реєструвалась з однаковою частотою в обох досліджуваних групах (р = 0,673 за критерієм χ2 Пірсона). Отримані результати наведені на рис. 1.
/57-1.jpg)
Вивчення деяких анамнестичних показників у дітей із БОС, які впливають на рівень забезпеченості VD, показало, що досліджувані групи відрізнялись між собою лише за рівнем саплементації VD на першому році життя і на момент огляду, а також за показником щодо прийому антибіотиків в анамнезі (табл. 2). Так, пацієнти 1-ї групи майже вдвічі частіше приймали 500 МО вітаміну D на першому році життя у порівнянні з 2-ю групою. Показник саплементації VD на момент дослідження у пацієнтів 2-ї групи був у межах 5 % на відміну від пацієнтів 1-ї групи, в яких даний показник становив 60 % (χ2 = 68,76, р < 0,001). Згідно з отриманими результатами, діти з повторним БОС вдвічі частіше приймали антибіотики в анамнезі, ніж пацієнти з епізодичним БОС. За іншими показниками, наведеними в табл. 1, досліджувані групи вірогідно не відрізнялись (р < 0,05).
/58-2.jpg)
Розрахунок показників відношення шансів (OR) показав, що ймовірність виявлення недостатності або дефіциту VD у дітей раннього віку з БОС, які не отримують вітамін D, набагато вища, ніж у дітей, які приймають його щодня в дозі 500–1000 МО (OR = 0,047; 95% СІ 0,018–0,126; р < 0,001). Крім того, при застосуванні антибіотиків в анамнезі також існує ймовірність виявлення низького рівня забезпеченості VD у дітей із БОС (OR = 2,851; 95% СІ 1,288–6,309; р = 0,009).
Проведений кореляційний аналіз показав, що рівень 25(OH)D у сироватці крові зворотно корелює з частотою епізодів БОС (r = –0,27, р = 0,002), що відображено на рис. 2, а також із віком обстежених пацієнтів (r = –0,33, р = 0,009).
Аналіз респіраторної захворюваності показав, що у дітей із повторним БОС середня частота епізодів ГРВІ за останній рік була вище, ніж у пацієнтів з епізодичним БОС (4,5 (3,0; 5,5) і 3 (2,0; 5,0) відповідно; р < 0,001 за U-критерієм Манна — Уїтні). Подальше дослідження особливостей статусу VD у дітей із БОС залежно від частоти епізодів ГРВІ ви–явило, що середній рівень 25(OH)D у сироватці крові мав тенденцію до більш низьких показників за наявності 5 і більше епізодів гострих респіраторних захворювань на рік. Отримані дані наведені в табл. 2.
Беручи до уваги вплив VD на частоту епізодів БОС і ГРВІ, ми проводили корекцію його недостатності та дефіциту у дітей із повторним БОС протягом року. Щоденне застосування препарату вітаміну D3 у дітей із повторним БОС супроводжувалось зменшенням респіраторної захворюваності протягом року на 50 %. Так, медіана кількості епізодів ГРВІ на рік у дітей 2а групи до призначення вітаміну D3 була вірогідно вищою, ніж через 12 місяців від початку його прийому (5,0 (4,0; 6,0) і 2,5 (2,0; 3,0) відповідно, р < 0,001 за Т-критерієм Вілкоксона).
При порівняльному аналізі частоти розвитку епізодів БОС виявлено значні відмінності у пацієнтів до і після прийому вітаміну D3. Так, на початку дослідження більшість пацієнтів (56,6 %) мали 4 епізоди БОС за останні 12 місяців, а після проведеної корекції статусу VD даний показник у переважної більшості хворих (63,4 %) знизився до 1–2 епізодів БОС протягом року. Отримані дані відображено на рис. 3.
Згідно з отриманими результатами, у дітей із повторним БОС спостерігалось вірогідне зростання концентрації сироваткового рівня 25(OH)D після застосування вітаміну D3 у порівнянні з його рівнем, визначеним на початку дослідження (25,11 (12,14; 42,47) нг/мл і 13,93 (9,60; 20,5) нг/мл відповідно; p = 0,002 за Т-критерієм Вілкоксона), хоча обидва показники виявились вірогідно нижчими, ніж у групі контролю, в якій медіана 25(OH)D становила 37,96 (26,47; 43,52) нг/мл (p = 0,02 і p < 0,001 відповідно за U-критерієм Манна — Уїтні).
Дані щодо статусу забезпеченості VD через 12 місяців після призначення вітаміну D3 наведені в табл. 3.
Відповідно до табл. 3, кількість пацієнтів із недостатнім рівнем VD залишалась майже незмінною після прийому вітаміну D3, однак частка пацієнтів із дефіцитом VD суттєво зменшилась, водночас відмічалось зростання частки пацієнтів, які мали оптимальний рівень VD.
Обговорення
Проведене дослідження продемонструвало, що діти з повторним перебігом гострого обструктивного бронхіту в середньому мали 4 епізоди БОС за останні 12 місяців. На сьогодні одним із факторів, що сприяють розвитку повторних епізодів БОС на фоні ГРВІ, вважається дефіцит VD, адже останніми роками встановлено, що рівень VD корелює з частотою і тяжкістю перебігу ГРВІ [3, 14–17]. Ризик гострих респіраторних захворювань із рекурентним перебігом підвищується за наявності недостатнього рівня забезпеченості VD (рівень 25(OH)D у сироватці крові нижче 30 нг/мл) [18, 19]. Згідно з нашими даними, 3/4 пацієнтів із повторним БОС мали дефіцит VD, тобто показник 25(OH)D у сироватці крові був 19,9 нг/мл і нижче, що збігається з результатами дослідження Santosh Prasad et al. (2016), в якому 73,8 % пацієнтів із повторним гострим обструктивним бронхітом мали дефіцит VD [20]. Проте у схожому дослідженні Durmaz et al. (2013) рівень дефіциту VD становив лише 12 %, тобто результати щодо статусу VD у дітей раннього віку з повторним БОС залишаються досі не однозначними [21].
У нашому дослідженні сироватковий рівень 25(OH)D зворотно корелював із частотою БОС. Встановлено, що у пацієнтів, які мали 4 і більше епізодів БОС за останній рік, середній показник 25(OH)D у сироватці крові відповідав критеріям дефіциту. Ми також виявили, що статус VD впливав не тільки на частоту епізодів БОС, але й на кількість гострих інфекцій верхніх дихальних шляхів, при цьому за наявності 5 і більше епізодів ГРВІ на рік рівень забезпеченості VD був нижчим, ніж у пацієнтів із меншою частотою ГРВІ.
Серед досліджуваних чинників, що впливають на статус VD, низький рівень його саплементації та прийом антибіотиків в анамнезі виявились найбільш значущими. Так, розрахунок показників відношення шансів виявив, що ймовірність недостатності або дефіциту VD суттєво підвищується при відсутності регулярного прийому вітаміну D. Крім того ми виявили, що середня сироваткова концентрація 25(OH)D має тенденцію до більш низьких показників зі збільшенням віку пацієнтів, що можна пояснити недостатнім рівнем саплементації даного вітаміну після 12 місяців життя. Багато лікарів і батьків впевнені у відсутності потреби VD після року, прийом якого помилково пов’язують тільки з профілактикою рахіту. Зв’язок між низьким рівнем VD та прийомом антибіотиків, ймовірніше, обумовлений тим, що за наявності недостатнього рівня VD діти виявились більш схильними до ГРВІ, що, в свою чергу, супроводжувалось більш частим призначенням антибактеріальних засобів. Водночас тривалість грудного вигодовування, щоденних прогулянок на свіжому повітрі, прийому VD під час вагітності, рівень інсоляції, обтяжений індивідуальний алергоанамнез, пасивне куріння, перебіг вагітності не мають суттєвого впливу на рівень забезпеченості VD у дітей раннього віку з повторними БОС. Проте, згідно з результатами деяких зарубіжних учених, тривале грудне вигодовування та пізнє введення прикорму є предикторами дефіциту VD [19]. Крім того, результати дослідження L.N. Anderson et al. (2015) вказують на те, що зниження частоти БОС на 35–40 % пов’язано з підвищеним споживанням VD під час вагітності [22].
Одним із завдань дослідження було вивчення ефективності застосування вітаміну D3 у дітей із повторними епізодами БОС. За нашими даними, застосування препарату вітаміну D3 у дозі 1000 МО щодня протягом 12 місяців супроводжувалось вираженими змінами в статусі VD у дітей із повторним БОС, а саме зменшення частки пацієнтів зі встановленим дефіцитом вдвічі. Водночас оптимальний рівень VD вірогідно частіше реєструвався серед обстежених після проведеного втручання. Дослідження сироваткового вмісту 25(OH)D у динаміці виявило зростання його середньої концентрації вдвічі у порівнянні з показниками, отриманими до початку прийому вітаміну D3. Якщо до застосування вітаміну D3 середній показник 25(OH)D у сироватці крові в дітей із повторним БОС знаходиться в межах дефіциту, то після призначення вітаміну D3 відповідає критеріям недостатності (рівень 25(OH)D
у сироватці крові — 20–29 нг/мл), але все ж таки залишається нижчим, ніж у групі контролю. Так чи інакше, можна стверджувати, що регулярний прийом 1000 МО вітаміну D3 у дітей раннього віку з повторним БОС призводить до підвищення рівня забезпеченості VD.
Катамнестичне спостереження показало, що на фоні прийому вітаміну D3 у більшої частини пацієнтів спостерігалось зменшення кількості епізодів БОС до 1–2 на рік, при цьому 1/4 пацієнтів не мали жодного епізоду БОС протягом року спостереження. В цей же період відзначена позитивна динаміка у показниках частоти гострих респіраторних захворювань у вигляді зменшення кількості епізодів ГРВІ вдвічі через 12 місяців після прийому вітаміну D3. Так, канадські вчені дійшли висновку, що зниження рівня 25(OH)D у сироватці крові нижче 30 нг/мл підвищує ризик гострої респіраторної інфекції на 50 % у дітей та підлітків [14], що повністю узгоджується з отриманими даними під час нашого дослідження. Крім того, нещодавнє дослідження Adrian R. Martineau et al. (2017) показало, що застосування вітаміну D знижує ризик інфекцій верхніх дихальних шляхів серед усіх учасників віком від 0 до 95 років, зокрема в дітей раннього віку [23].
Отже, дефіцит VD можна розглядати як предиктор і повторних епізодів БОС, і схильності до частих ГРВІ у дітей раннього віку. Серед факторів, що найбільшою мірою впливають на розвиток недостатності або дефіциту VD, важливу роль відіграє низький рівень його саплементації та, можливо, прийом антибіотиків в анамнезі. Водночас застосування вітаміну D3 в дозі 1000 МО щодня підвищує рівень забезпеченості VD, тим самим сприяючи зниженню частоти повторних епізодів БОС у дітей раннього віку.
З огляду на отримані результати, існує необхідність проведення подальших наукових досліджень для встановлення необхідного рівня саплементації VD з метою профілактики та лікування повторних епізодів БОС у дітей раннього віку.
Висновки
1. У переважної більшості дітей раннього віку з повторним БОС статус VD відповідає критеріям дефіциту та недостатності (нижче 30 нг/мл у сироватці крові), що може розглядатись як предиктор повторних епізодів БОС.
2. Рівень сироваткового VD зворотно корелює не тільки з частотою БОС, але й з рівнем захворюваності на ГРВІ, тобто при зниженні сироваткової концентрації 25(OH)D кількість епізодів БОС і ГРВІ зростає.
3. Низький рівень саплементації VD слід розглядати як головний фактор ризику недостатнього рівня забезпеченості VD. Рівень забезпеченості VD має тенденцію до більш низьких показників при збільшенні віку пацієнтів.
4. У дітей раннього віку, які часто хворіють на ГРВІ, зокрема повторний БОС, важливо оцінювати анамнестичні дані щодо застосування вітаміну D та при необхідності визначати рівень 25(OH)D у сироватці крові.
5. Щоденний прийом 1000 МО вітаміну D3 протягом 12 місяців сприяє вірогідному зменшенню частоти гострих інфекцій верхній дихальних шляхів, зокрема епізодів БОС у дітей раннього віку.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
Список литературы
1. Vitamin D in the Healthy European Paediatric Population / Christian Braegger, Cristina Campoy, Virginie Colomb [et al.] // JPGN. — 2013. — Vol. 56, № 6. — Р. 692-701. doi: 10.1097/MPG.0b013e31828f3c05.
2. The role of vitamin D in chronic obstructive pulmonary di–sease, asthma and other respiratory diseases / J. Garsia de Tena, A. EI Hachem Debek, C. Hernandez Gutierrez [et al.] // J. Arch. Bronconeumol. — 2014. — Vol. 50, № 5. — Р. 179-184. doi: 10.1016/j.arbr.2014.03.015.
3. Vitamin D and respiratory tract infections: A systematic review and meta-analysis of randomized controlled trials / P. Bergman, Åsa U. Lindh, L. Björkhem-Bergman [et al.] // Plos One. — 2014. — Vol. 8, № 6. — Р. 1-9. doi: 10.1371/journal.pone.0065835.
4. Дефіцит та недостатність вітаміну D: епідемологія, діагностика, профілактика та лікування / За ред. проф. В.В. Поворознюка, проф. П. Плудовські. — Донецьк: Видавець Заславський О.Ю., 2014. — 262 с.
5. Vitamin D effects on musculoskeletal health, immunity, autoimmunity, cardiovascular disease, cancer, fertility, pregnancy, dementia and mortality — a review of recent evidence / Р. Pludowski, M.F. Holick, S. Pilz [et al.] // Autoimmun. Rev. — 2013. — Vol. 12, № 10. — Р. 976-989. doi: 10.1016/j.autrev.2013.02.004.
6. Lee J. A review on vitamin D deficiency treatment in pediatric patients / Ji Yeon Lee, Tsz-Yin So, Jennifer Thackray // J. Pediatr. Pharmacol. Ther. — 2013. — Vol. 18, № 4. — Р. 277-291. doi: 10.5863/1551-6776-18.4.277.
7. Квашніна Л.В. Вітамін D у різні періоди дитинства: що знаємо, що треба пам’ятати і що забули / Л.В. Квашніна // Здоров’я України. — грудень 2017. — С. 29-31.
8. Antimicrobial implications of vitamin D / D.A. Youssef, Christopher W.T. Miller, Adel M. El-Abbassi [et al.] // Dermatoendocrinol. — 2011. — Vol. 3, № 4. — Р. 220-229. doi: 10.4161/derm.3.4.15027.
9. Абатуров А.Е. Витамин-D-зависимая продукция антимикробных пептидов / А.Е. Абатуров, Н.Ю. Завгородняя // Здоровье ребенка. — 2012. — Т. 36, № 1. — С. 105-111.
10. Holick Michael F. Vitamin D: A D-Lightful Vitamin for Health / Michael F. Holick // Endocrinol. Metab. — 2012. — Vol. 27, № 4. — Р. 255-267. doi: 10.1177/0148607111430189.
11. Association of vitamin D with respiratory outcomes in Canadian children / S.J. Niruban, K. Alagiakrishnan, J. Beach [et al.] // European Journal of Clinical Nutrition. — 2014. — Vol. 68, № 12. — Р. 1-7. doi: 10.1038/ejcn.2014.121.
12. Evolution, treatment and prevention of vitamin D deficiency: an Endocrine Society Clinical Practice Guideline / M.F. Holick, N.C. Binkley, Bischoff-Ferrari [et al.] // J. Clin. Endocrinol. Metab. — 2011. — Vol. 96, № 7. — P. 1911-1930. doi: 10.1210/jc.2011-0385.
13. Майданник В.Г. Современные подходы к профилактике и лечению витамин D-дефицитного рахита с позиции доказательной медицины / В.Г. Майданник, С.М. Демчук. — Международный журнал педиатрии, акушерства и гинекологии. — 2015. — Т. 8, № 1. — С. 133-143.
14. Low serum 25-hydroxyvitamin D level and risk of upper respiratory tract infection in children and adolescents / Michelle Science, Jonathon L. Maguire, Margaret L. Russell [et al.] // Clinical Infectious Di–seases. — 2013. — Vol. 57, № 3. — Р. 392-397. doi: 10.1093/cid/cit289.
15. Починок Т.В. Корекція дефіциту вітаміну D і його вплив на імунологічні та метаболічні порушення у дітей раннього віку, які страждають від частих респіраторних захворювань / Т.В. Починок // Здоров’я дитини. — 2016. — Т. 70, № 2. — С. 41-46.
16. Esposito S. Vitamin D and respiratory tract infections in childhood / Susanna Esposito, Mara Lelii // BMC Infectious Diseases. — 2015. — Vol. 15. — P. 487. doi: 10.1186/s12879-015-1196-1.
17. Larkin A. Vitamin D Deficiency and Acute Lower Respiratory Infections in Children Younger Than 5 Years: Identification and Treatment / Allison Larkin, Jane Lassetter // Journal of Pediatric Health Care. — 2014. — Vol. 28, № 6. — Р. 572-582. doi: 10.1016/j.pedhc.2014.08.013.
18. Del Fiol F.S. Vitamin D and respiratory infections / Fernando de Sa Del Fiol, Silvio Barberato-Filho, Luciane Cruz Lopes // J. Infect. Dev. Ctries. — 2015. — Vol. 9, № 4. — Р. 355-361. doi: 10.3855/jidc.5711.
19. Vitamin D for prevention of respiratory tract infections: A systematic review and meta-analysis / J. Charan, J.P. Goyal, D. Saxena [et al.] // J. Pharmacol Pharmacother. — 2012. — Vol. 3, № 4. — Р. 300-303. doi: 10.4103/0976-500X.103685.
20. Prasad S. A Hospital Based Study to Establish the Correlation between Recurrent Wheeze and Vitamin D Deficiency Among Children of Age Group Less than 3 Years in Indian Scenario / S. Prasad, R. Rana, R. Sheth // J. Clin. Diagn. Res. — 2016. — Vol. 10, № 2. — Р. 18-21. doi: 10.7860/JCDR/2016/17318.7287.
21. Durmaz C. Serum Vitamin D Levels Among Recurrently Wheezy Infants / C. Durmaz, S. Asilsoy, B. Güç Usta // Turkiye Klinikleri J. Med. Sci. — 2013. — Vol. 33, № 6. — Р. 1337-1343. doi: 10.5336/medsci.2012-30610.
22. Vitamin D exposure during pregnancy, but not early childhood, is associated with risk of childhood wheezing / L.N. Anderson, Y. Chen, J.A. Omand [et al.] // Journal of Developmental Origins of Health and Disease. — 2015. — Vol. 6, № 4. — Р. 308-316. doi: 10.1017/S2040174415001063.
23. Vitamin D supplementation to prevent acute respiratory tract infections: systematic review and meta-analysis of individual participant data / Adrian R. Martineau, David A. Jolliffe, Richard L. Hooper [et al.] // BMJ. — 2017. — Р. 356-369. doi:10.1136/bmj.i6583.

/57-1.jpg)
/58-2.jpg)
/58-1.jpg)
/59-1.jpg)