Введение
Острые респираторные вирусные инфекции (ОРВИ) на протяжении не одного десятка лет занимают первое место в структуре инфекционных заболеваний у детей [10, 11, 14]. В последнее время, несмотря на достижения медицины, отмечается неуклонный рост ОРВИ, которые характеризуются затяжным течением и высоким риском развития ослож–нений [16, 25].
В основе затяжного течения ОРВИ лежат нарушения механизмов иммунной системы, которые обеспечивают элиминацию инфекционных агентов и участвуют в развитии воспалительного ответа [1, 41]. В связи с этим применение иммунотропных препаратов при лечении детей c риском пролонгированного течения ОРВИ является целесообразным терапевтическим приемом. Одним из таких препаратов, обладающим сочетанным противовирусным и иммуномодулирующим действием, является инозин пранобекс [18].
Нарушения иммунной системы, обусловливающие неэффективность элиминации инфекционных вирусных агентов
Основным механизмом элиминации инфекционных агентов из организма является фагоцитоз, которому способствуют иммуноциты, лизирующие инфицированные клетки.
Фагоцитоз инфицированных клеток и экстрацеллюлярно расположенных вирусных агентов, –высвобожденных при помощи лизиса вирус-инфицированных клеток, преимущественно осуществляют макрофаги. Лизирование инфицированных клеток выполняют макрофаги, натуральные киллеры (NK-клетки) и цитотоксические T-клетки (cytotoxic T lymphocytes, CTL) [42].
Установлено, что альвеолярные макрофаги принимают активное участие в патогенезе вирусной инфекции, обеспечивая раннюю продукцию цитокинов, которые организуют противовирусный ответ [21].
Активированные NK-клетки, обладающие цитотоксическим действием, неспецифическим образом лизируют вирус-инфицированные клетки. Каждая NK-клетка может нанести несколько цитотоксических ударов по разным клеткам. Лизируя инфицированные клетки, NK-клетки способствуют эффективности элиминации вновь образованных вирионов [22, 29]. Истощение пула легочных NK-клеток сопровождается снижением уровня клиренса вирусных агентов, а замедление скорости элиминации вирусов приводит к пролонгированию инфекционно-воспалительного процесса и может являться причиной неблагоприятного течения заболевания [26, 35].
Однако необходимо отметить, что истощение NK-клеток in vivo сопровождается снижением летальности при экспериментальной гриппозной инфекции, протекающей с гиперреакцией иммунной системы [45].
Установлено, что лицензированные (функциональные) NK-клетки выступают в качестве ранних врожденных эффекторов, которые продуцируют интерферон гамма (IFN-γ) в регионах воспаления и опосредуют прямые противовирусные реакции [44]. Нелицензированные NK-клетки, у которых отсутствуют рецепторы системы MHC-I, локализуются в региональных лимфатических узлах и способствуют активации и пролиферации дендритных клеток, что, в конечном счете, приводит к устойчивому антигенспецифическому CD8+Т-клеточному ответу. Повышение функциональной активности CTL обусловливает специфическое лизирование клеток. Клетка CTL наносит единственный цитотоксический удар и осуществляет его по клетке, инфицированной исключительно определенным вирусом [37]. Дефицит продукции IFN-γ или недостаточная активность CTL приводят к нарушению элиминации вирусов, вызвавших заболевание, и ухудшению прогноза течения инфекции.
Инозин пранобекс
Одним из иммуномодулирующих препаратов является инозин пранобекс, который в отличие от многих других лекарственных средств данной группы также обладает и противовирусным действием [5].
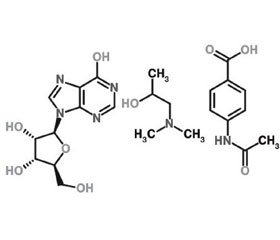
Инозин пранобекс (inosine pranobex, inosiplex, methisoprinol, инозин и 4-ацетамидобензойная соль N,N-диметиламино-2-пропанола) (рис. 1) представляет собой комбинацию инозина, производного пуринового нуклеозида аденозина, с пранобексом, который повышает доступность инозина для лимфоцитов. Инозин и пранобекс в препарате инозин пранобекс содержатся в соотношении 3 : 1 [4, 23].
Иммуномодулирующее действие инозина пранобекса
Инозин пранобекс оказывает потенцирующее влияние на основные клетки неспецифических механизмов защиты: нейтрофилы, моноциты, макрофаги, NK-клетки [23].
Инозин пранобекс увеличивает или восстанавливает подавленную активность хемотаксиса и фагоцитоза нейтрофилов [23]. Установлено, что инозин пранобекс активирует моноциты и макрофаги, индуцируя хемотаксис, продукцию цитокинов [27, 39]. После приема первой дозы инозина пранобекса у 75 % пациентов наблюдается быстрое увеличение представительства мононуклеарных клеток, и этот индуцированный ответ мононуклеарных клеток сопряжен с более быстрым процессом выздоровления и благоприятным течением острых респираторных инфекций [20].
Ежедневное применение инозина пранобекса в дозе 100 мг/кг массы тела на протяжении семи суток индуцирует значительное увеличение пролиферативной активности лимфоцитов и цитотоксичности NK-клеток у экспериментальных животных [38].
Инозин пранобекс является лекарственным средством, которое оказывает достоверное влияние на активность продукции цитокинов. Установлено, что инозин пранобекс in vivo увеличивает активность продукции интерлейкинов (IL)-1, IL-2, IL-12, IFN-γ, фактора некроза опухоли альфа и подавляет продукцию IL-3, IL-4, IL-10 [30, 33, 34, 36]. Witold Lasek и соавторы [30] считают, что инозин пранобекс способствует усилению Th1-опосредованного иммунного ответа. По всей вероятности, активация Th1-ответа и предопределяет усиление элиминации инфекционных агентов при ОРВИ. С другой стороны, инозин пранобекс ингибирует активность Th2-ответа и продукцию IL-10. Авторы считают, что назначение инозина пранобекса в качестве адъювантной терапии является целесообразным выбором у больных с рецидивирующими, длительно протекающими вирусными инфекциями.
Инозин пранобекс индуцирует цитотоксичность CD8+Т-лимфоцитов [20], дифференцировку В-клеток в плазматические клетки и способствует продукции иммуноглобулинов, в том числе и специфических антител, направленных против антигенов возбудителей инфекционных заболеваний. Повышение активности синтеза специфических антител предопределяет усиление клиренса патогенных вирусов и бактерий [27]. Таким образом, инозин пранобекс способствует эффективности элиминации инфекционных агентов и является препаратом выбора при лечении больных с пролонгированным течением ОРВИ.
Противовирусное действие
Способность инозина пранобекса оказывать противовирусное действие была продемонстрирована на примере разнообразных респираторно-тропных вирусных агентов: вирусов гриппа A и B, парагриппа, риновируса, аденовирусов, респираторно-синцитиального вируса, герпесвирусов и др. [2, 9, 31, 32, 43].
Инозин пранобекс оказывает противовирусное действие, ингибируя процесс репликации ДНК и РНК вирусов [23].
Показания для назначения инозина пранобекса
Учитывая, что основными точками приложения действия инозина пранобекса являются эффекторные механизмы, участвующие в элиминации инфекционных агентов и развитии Th1-опосредованной воспалительной реакции, а также непосредственно вирусные агенты, основными показаниями для назначения инозина пранобекса можно считать ОРВИ, особенно в тех случаях, когда существует риск затяжного, неблагоприятного или персистирующего течения. Л.В. Осидак, Е.В. Образцова [13] рекомендуют использовать инозин пранобекс для лечения острых и персистирующих вирусных инфекций, в том числе и у иммунокомпрометированных лиц.
Применение инозина пранобекса разрешено у детей в зависимости от фирмы-производителя с годовалого или после трехлетнего возраста [4].
Дозирование и длительность курса терапии
Инозин пранобекс рекомендуется больным с ОРВИ назначать внутрь после еды в суточной дозе 50 мг/кг, которую равномерно делят на 3–4 приема. Считают, что при тяжелом течении инфекционного процесса как у детей, так и у взрослых суточная доза препарата может быть увеличена до 100 мг/кг. Длительность терапии составляет от 5 до 14 суток [8].
Клиническая эффективность
Учитывая, что ОРВИ у детей с высоким уровнем чувствительности к респираторным инфекционным агентам, как правило, характеризуется торпидным течением заболевания, демонстративным исследованием влияния препарата инозина пранобекса является работа, выполненная Т.К. Чудаковой с соавторами [19]. Авторы провели оценку эффективности терапии препаратом инозина пранобекс 70 часто болеющих детей в возрасте от 3 до 6 лет, больных ОРВИ, и показали, что назначение инозина пранобекса достоверно сокращает продолжительность проявлений как симптомов интоксикации (лихорадки, вялости, гипертермии, снижения аппетита), так и катарального синдрома (гиперемии слизистой оболочки глотки, кашля). Лечение инозином пранобексом сопровождается более быстрым исчезновением признаков ОРВИ и сокращением продолжительности стационарного лечения больных на двое суток. Подобные результаты исследования клинической эффективности применения инозина пранобекса в суточной дозе 50 мг/кг у детей в возрасте от 1 до 18 лет с ОРВИ продемонстрировали и Л.В. Осидак с соавторами [12]. Авторы показали, что продолжительность заболевания на фоне приема инозина пранобекса у 64–70 % детей не превышала 6–8 суток, в то время как среди контрольной группы доля детей с такой продолжительностью ОРВИ составляла всего 4–25 %.
Также доказана высокая клиническая эффективность применения инозина пранобекса у больных, инфекции которых вызваны определенными вирусными респираторно-тропными агентами. Показано, что при гриппе и гриппоподобных заболеваниях применение инозина пранобекса сопровождалось укорочением продолжительности заболевания практически на двое суток — с 11 суток, наблюдаемых в контрольной группе, до 9 дней у больных, получавших данный препарат [20]. Инозин пранобекс, согласно результатам исследования, проведенного Е.Н. Сергиенко и соавторами [15], проявляет противовирусную активность в отношении штаммов вирусов гриппа А/Минск/108/09 (Н3N2), A/Минск/124/08 (H1N1) и штамма пандемического вируса гриппа А/Минск/94/09 (H1N1)-р.
Согласно результатам контролируемого двойного слепого исследования клинической эффективности терапии инозином пранобексом волонтеров, инфицированных 21-м серотипом риновируса, целесообразно рекомендовать назначение данного препарата при риновирусной инфекции. Было отмечено, что применение инозина пранобекса приводит к сокращению продолжительности репликации риновирусов и стимуляции активности митогенного ответа лимфоцитов. Авторы считают, что инозин пранобекс проявляет высокую эффективность при лечении риновирусной инфекции [40].
Применение инозина пранобекса не только уменьшает манифестацию симптомов ОРВИ, но и предотвращает развитие бактериальных осложнений и позволяет снизить потребность в назначении других лекарственных средств [3, 7].
Метаанализ эффективности применения инозина пранобекса у детей с ОРВИ, проведенный М.Ю. Елисеевой и коллегами [6], показал, что назначение инозина пранобекса способствует снижению последующей частоты и продолжительности эпизодов ОРВИ.
Безопасность, побочные эффекты
На основании результатов 4-й фазы рандомизированного плацебо-контролируемого двойного слепого многоцентрового исследования J. Beran и соавторы [20] считают, что применение инозина пранобекса при лечении острых респираторных инфекций характеризуется высоким профилем эффективности и безопасности. Т.К. Чудакова и соавторы [17] продемонстрировали высокую степень клинической эффективности применения инозина пранобекса при лечении ОРВИ у детей.
Побочные эффекты применения инозина пранобекса регистрируются крайне редко и проявляются в виде головной боли, чувства тяжести в эпигастральной области живота, чувства прилива жара [4]. В первые дни назначения инозина пранобекса возможно снижение аппетита, диспептический синдром (тошнота, диарея), незначительное повышение концентрации мочевой кислоты в крови и моче, аллергические реакции [8].
Гропивирин
На протяжении последних нескольких лет на фармацевтическом рынке Украины присутствует препарат инозина пранобекса — Гропивирин –отечественного производства ПАО «Фармак». Препарат Гропивирин выпускается в форме таблеток. Каждая таблетка содержит 500 мг активного действующего вещества инозина пранобекса. Препарат Гропивирин вызывает все присущие инозину пранобексу иммуномодулирующие и противовирусные эффекты. Препарат Гропивирин рекомендован к применению у детей c первого года жизни и взрослых.
Выводы
Острые респираторные вирусные инфекции занимают первое место в структуре заболеваемости детей, в некоторых случаях могут оказать существенное патогенное влияние на состояние здоровья ребенка. Девиации в активности функционирования механизмов элиминации вирусных агентов, которые проявляются удлинением продолжительности заболевания и риском осложненного течения, требуют медикаментозной коррекции. Препаратом выбора в данной ситуации считают инозин пранобекс, который индуцирует макрофаги, NK-клетки, CTL, определяющие элиминацию вирусов; Th1-лимфоциты, участвующие в развитии воспаления; и оказывает непосредственное противовирусное действие. Назначение инозина пранобекса при ОРВИ, особенно при риске затяжного течения, способствует более быстрому выздоровлению и снижению вероятности возникновения бактериальных осложнений. Применение инозина пранобекса оказывает и профилактическое действие, предупреждая развитие последующих респираторных инфекций. Одним из препаратов инозина пранобекса, которые можно рекомендовать для назначения детям, является Гропивирин.
Конфликт интересов. Не заявлен.
Список литературы
1. Абатуров А.Е., Волосовец А.П., Юлиш Е.И. Роль Toll-подобных рецепторов в рекогниции патоген-ассоциированных молекулярных структур инфекционных патогенных агентов в развитии воспаления. Часть 1. Семейство TLR // Здоровье ребенка. — 2012. — Т. 5, № 40. — С. 116-121.
2. Булгакова В.А. Клинико-иммунологическая эффективность применения инозина пранобекс при острых респираторных инфекциях у детей с атопической бронхиальной астмой // Педиатрическая фармакология. — 2010. — Т. 7, № 3. — С. 58-65.
3. Булгакова В.А. Острые респираторные инфекции: расширение возможностей противовирусной терапии // Вопросы современной педиатрии. — 2013. — Т. 12, № 5. — С. 74-79.
4. Булгакова В.А. Оригинальный препарат инозина пранобекс для этиопатогенетической терапии ОРВИ // Участковый педиатр. — 2014. — № 5. — С. 22-23.
5. Дронов И.А. Инозин пранобекс: возможности этиотропной терапии при острой респираторной инфекции у детей / И.А. Дронов, Н.А. Геппе, А.Б. Малахов, Н.Г. Колосова // Вопросы практической педиатрии. — 2016. — Т. 11, № 4. — С. 39-43.
6. Елисеева М.Ю. Эффективность вспомогательной иммунотерапии у пациентов с иммунодефицитом и часто болеющих детей: систематический обзор и метаанализ применения инозина пранобекса / М.Ю. Елисеева, В.Н. Царев, К.Н. Масихи и др. // РМЖ. — 2010. — Т. 18, № 5. — С. 313-320.
7. Ерофеева С.Б. Изопринозин: решение проблемы полипрагмазии в лечении гриппа и острых респираторных вирусных инфекций // Фарматека. — 2015. — № 20(313). — С. 87-90.
8. Исаков В.А., Исаков Д.В., Алексеева Е.А. Современные возможности терапии респираторных инфекций // Клини–ческая фармакология и терапия. — 2017. — Т. 26, № 5. — С. 51-56.
9. Крамарев С.А. Инозин пранобекс в практике врача-педиатра. Препараты, зарегистрированные в Украине // Педиатрия. Восточная Европа. — 2014. — № 1(5). — С. 70-76.
10. Крамарев С.А. Лечение гриппа и других острых респираторных вирусных инфекций / С.А. Крамарев, В.В. Евтушенко, О.А. Голубовская, В.А. Дорошенко // Клиническая инфектология и паразитология. — 2014. — № 4(11). — С. 147-155.
11. Львова И.И. Острые респираторные вирусные инфекции у детей. Диагностика, лечение, профилактика: Учебное пособие / И.И. Львова, Л.Ю. Гришкина, А.В. Дерюшева и др. — Пермь: ПГМА, 2014. — 162 с.
12. Осидак Л.В. Изопринозин в терапии ОРВИ у часто болеющих детей / Л.В. Осидак, В.В. Зарубаев, Е.В. Образцова и др. // Детские инфекции. — 2008. — Т. 7, № 4. — С. 35-40.
13. Осидак Л.В., Образцова Е.В. Эффективность молекулы инозина пранобекс в терапевтической и педиатрической практике // Эпидемиология и инфекционные болезни. Актуальные вопросы. — 2012. — № 4. — С. 26-32.
14. Семенова А.Р., Царенко О.Е. Заболеваемость детского населения города Ижевска острой респираторной вирусной инфекцией за 2014–2015 годы // Теоретические и прикладные исследования в области естественных, гуманитарных и технических наук. Сборник научных трудов. — 2015. — С. 13-17.
15. Сергиенко Е.Н. Грипп у детей: клинико-эпидемиологические особенности и новые возможности терапии / Е.Н. Сергиенко, Н.П. Шмелева, И.Г. Германенко, Н.В. Грибкова // Новости медицины и фармации. — 2010. — Т. 3, № 308. — С. 15-7.
16. Сміян О.І. Сучасні етіопатогенетичні та клініко-діагностичні особливості перебігу гострих респіраторних вірусних інфекцій у дітей / О.І. Сміян, Т.П. Бинда, Є.В. Дмітрова, В.А. Сухарєва // Журнал клінічних та експериментальних медичних досліджень. — 2013. — Т. 1, № 3. — С. 328-336.
17. Чудакова Т.К. Выбор этиотропной терапии острых респираторных вирусных инфекций у детей / Т.К. Чудакова, А.В. Романовская, Е.В. Михайлова и др. // Вопросы практической педиатрии. — 2015. — Т. 10, № 5. — С. 77-82.
18. Чудакова Т.К. Инозина пранобекс в этиотропной терапии острых респираторных вирусных инфекций у часто болеющих детей / Т.К. Чудакова, Е.В. Михайлова, Д.Ю. Левин и др. // Вопросы практической педиатрии. — 2016. — Т. 11, № 5. — С. 62-65.
19. Чудакова Т.К., Михайлова Е.В., Шведова Н.М. Эффективность противовирусной терапии острых респираторных вирусных инфекций у часто болеющих детей // Вопросы практической педиатрии. — 2015. — Т. 10, № 1. — С. 58-63.
20. Beran J. Inosine pranobex is safe and effective for the treatment of subjects with confirmed acute respiratory viral infections: analysis and subgroup analysis from a Phase 4, randomised, placebo-controlled, double-blind study / J. Beran, E. Šalapová, M. Špajdel et al. // BMC Infect. Dis. — 2016 Nov 7. — № 16(1). — 648. — doi: 10.1186/s12879-016-1965-5.
21. Bohmwald K. Functional Impairment of Mononuclear Phagocyte System by the Human Respiratory Syncytial Virus / K. Bohmwald, J.A. Espinoza, R.A. Pulgar et al. // Front. Immunol. — 2017 Nov 27. — № 8. — 1643. — doi: 10.3389/fimmu.2017.01643.
22. Brandstadter J.D., Yang Y. Natural killer cell responses to viral infection // J. Innate Immun. — 2011. — № 3(3). — Р. 274-9. — doi: 10.1159/000324176.
23. Campoli-Richards D.M., Sorkin E.M., Heel R.C. Inosine pranobex. A preliminary review of its pharmacodynamic and pharmacokinetic properties, and therapeutic efficacy / D.M. Campoli-Ri–chards, E.M. Sorkin, R.C. Heel // Drugs. — 1986 Nov. — № 32(5). — Р. 383-424. — doi: 10.2165/00003495-198632050-00001.
24. ChemSpider [Электронный ресурс]. Режим доступа: http://www.chemspider.com/Chemical-Structure.16736312.html (29.07.2018).
25. Choi E. Clinical and laboratory profiles of hospitalized children with acute respiratory virus infection / E. Choi, K.S. Ha, D.J. Song et al. // Korean J. Pediatr. — 2018 Jun. — № 61(6). — Р. 180-186. — doi: 10.3345/kjp.2018.61.6.180.
26. Fox A. Severe pandemic H1N1 2009 infection is associated with transient NK and T deficiency and aberrant CD8 responses / A. Fox, N.M. Le, P. Horby et al. // PLoS One. — 2012. — № 7(2). — Р. e31535. — doi: 10.1371/journal.pone.0031535.
27. Golebiowska-Wawrzyniak M. Immunological and clinical study on therapeutic efficacy of inosine pranobex / M. Golebiowska-Wawrzyniak, K. Markiewicz, A. Kozar et al. // Pol. Merkur. Lekarski. — 2005 Sep. — № 19(111). — Р. 379-82.
28. Hersey P. Effect of isoprinosine on interleukin 1 and 2 production and on suppressor cell activity in pokeweed mitogen stimulated cultures of B and T cells / P. Hersey, C. Bindon, M. Bradley, E. Hasic // Int. J. Immunopharmacol. — 1984. — № 6(4). — Р. 321-8. — PMID: 6207122.
29. Jost S., Altfeld M. Control of human viral infections by natural killer cells // Annu Rev. Immunol. — 2013. — № 31. — Р. 163-94. — doi: 10.1146/annurev-immunol-032712-100001.
30. Lasek W. Immunomodulatory effects of inosine pranobex on cytokine production by human lymphocytes / W. Lasek, M. Janyst, R. Wolny et al. // Acta Pharm. — 2015 Jun. — № 65(2). — Р. 171-80. — doi: 10.1515/acph-2015-0015.
31. Majewska A. Inhibition of adenovirus multiplication by inosine pranobex and interferon α in vitro / A. Majewska, W. Lasek, M. Janyst, G. Mlynarczyk // Cent. Eur. J. Immunol. — 2015. — № 40(4). — Р. 395-9. — doi: 10.5114/ceji.2015.56960.
32. Majewska A., Lasek W., Mlynarczyk G. Pranobeks inozyny — działanie cytotoksyczne oraz wpływ na replikację ludzkich wirusów paragrypy (HPIV-2, HPIV-4), enterowirusów (CA16, EV71) i adenowirusów (HAdV-2, HAdV-5) w badaniu in vitrо // Med. Dośw. Mikrobiol. — 2015. — № 67. — Р. 107-113.
33. Milano S. Effect of isoprinosine on IL-2, IFN-gamma and IL-4 production in vivo and in vitro / S. Milano, M. Dieli, S. Millott et al. // Int. J. Immunopharmacol. — 1991. — № 13(7). — Р. 1013-8. — PMID: 1722191.
34. Moniuszko T., Rogalewska A., Chyrek-Borowska S. The effect of therapy with selected immunomodulators on interleukin-2 production by peripheral blood lymphocytes // Pneumonol. Alergol. Pol. — 1992. — № 60(Suppl. 2). — Р. 120-1. — PMID: 1284817.
35. Newton A.H., Cardani A., Braciale T.J. The host immune response in respiratory virus infection: balancing virus clearance and immunopathology // Semin. Immunopathol. — 2016 Jul. — № 38(4). — Р. 471-82. — doi: 10.1007/s00281-016-0558-0.
36. Petrova M. Isoprinosine affects serum cytokine levels in healthy adults / M. Petrova, D. Jelev, A. Ivanova, Z. Krastev // J. Interferon Cytokine Res. — 2010 Apr. — № 30(4). — Р. 223-8. — doi: 10.1089/jir.2009.0057.
37. Schmidt S. Natural killer cells as a therapeutic tool for infectious diseases — current status and future perspectives / S. Schmidt, L. Tramsen, B. Rais et al. // Oncotarget. — 2018 Apr 17. — № 9(29). — Р. 20891-20907. — doi: 10.18632/oncotarget.25058.
38. Singh H., Herndon D.N. Effect of isoprinosine on lymphocyte proliferation and natural killer cell activity following thermal injury // Immunopharmacol. Immunotoxicol. — 1989. — № 11(4). — Р. 631-44. — DOI: 10.3109/08923978909005391.
39. Tsang K.Y., Fudenberg H.H., Gnagy M.J. Restoration of immune responses of aging hamsters by treatment with Isoprinosine // J. Clin. Invest. — 1983 Jun. — № 71(6). — Р. 1750-5. — PMID: 6190840.
40. Waldman R.H., Ganguly R. Therapeutic efficacy of inosiplex (Isoprinosine) in rhinovirus infection // Ann. N.Y. Acad. Sci. — 1977 Mar 4. — № 284. — Р. 153-60. — PMID: 81636.
41. Wong S.S. Severe Influenza Is Characterized by Prolonged Immune Activation: Results From the SHIVERS Cohort Study / S.S. Wong, C.M. Oshansky, X.J. Guo et al. // J. Infect. Dis. — 2018 Jan 4. — № 217(2). — Р. 245-256. — doi: 10.1093/infdis/jix571.
42. Yoo J.K. Viral infection of the lung: host response and se–quelae / J.K. Yoo, T.S. Kim, M.M. Hufford, T.J. Braciale // J. Allergy Clin. Immunol. — 2013 Dec. — № 132(6). — Р. 1263-76. — doi: 10.1016/j.jaci.2013.06.006.
43. You Y. Multicenter randomized study of inosine pranobex versus acyclovir in the treatment of recurrent herpes labialis and recurrent herpes genitalis in Chinese patients / Y. You, L. Wang, Y. Li et al. // J. Dermatol. — 2015 Jun. — № 42(6). — Р. 596-601. — doi: 10.1111/1346-8138.12845.
44. Zamora A.E. Licensing delineates helper and effector NK cell subsets during viral infection / A.E. Zamora, E.G. Aguilar, C.M. Sungur et al. // JCI Insight. — 2017 May 18. — № 2(10). — Р. 87032. — doi: 10.1172/jci.insight.87032.
45. Zhou G., Juang S.W., Kane K.P. NK cells exacerbate the pathology of influenza virus infection in mice // Eur. J. Immunol. — 2013 Apr. — № 43(4). — Р. 929-38. — doi: 10.1002/eji.201242620.

/120-1.jpg)