Комбинированные оральные контрацептивы (КОК) — препараты, которые относятся к группе гормональных контрацептивов и содержат два основных гормона (эстроген и прогестин). Основной областью применения КОК является предупреждение нежелательной беременности. Второй большой областью применения данных препаратов является лечение репродуктивных нарушений, в первую очередь при синдроме поликистозных яичников.
В основу предложенных алгоритмов обследования положены рекомендации из руководств мировых сообществ:
— Европейского сообщества по контрацепции «Medical eligibility criteria for contraceptive use» (5-е издание, 2015 г.);
— Американского общества эндокринологов «Diagnosis and Treatment of Polycystic Ovary Syndrome: An Endocrine Society Clinical Practice Guideline», 2013 г.;
— Европейского общества эндокринологов «The polycystic ovary syndrome: a position statement from the European Society of Endocrinology», 2014 г.
Рекомендация использовать КОК как метод контрацепции должна начинаться с оценки наличия факторов риска, которая поможет выделить группу женщин с высоким риском развития осложнений в результате приема данных препаратов.
Согласно руководству ВОЗ «Медицинские критерии приемлемости использования контрацептивов» (5-е издание, 2015 г.), выделяется четыре категории приемлемости для здоровья при использовании контрацептивов. Это позволяет определить, для каких женщин данный метод контрацепции абсолютно приемлем (1-я категория), а для кого неприемлем и необходимо рекомендовать другие методы контрацепции (4-я категория).
Категории критериев приемлемости для здоровья использования контрацептивов
Категория 1. Условие, для которого нет ограничений на использование метода контрацепции.
Категория 2. Условие, при котором преимущества использования метода в целом перевешивают теоретические или доказанные риски.
Категория 3. Условие, при котором теоретические или проверенные риски обычно перевешивают преимущества использования метода.
Категория 4. Условие, которое представляет собой неприемлемый риск для здоровья, если используется метод контрацепции.
Основные риски, которые необходимо оценивать у каждой женщины перед назначением КОК как метода контрацепции, это:
1. Риски тромбоза: венозного и артериального. Обязателен сбор анамнеза, включая оценку наличия в анамнезе тромботических событий как у женщины, так и у родственников первой линии родства, наличие данных о генетически детерминированных формах тромбофилии. Лабораторное тестирование в случаях наличия семейного анамнеза высокого риска тромбоза для выявления генетических форм тромбофилий не рекомендовано с учетом того, что невозможно протестировать все возможные формы. Важно учитывать, что отсутствие пяти наиболее распространенных наследственных тромбофилий на фоне семейного анамнеза тромбоза может привести к ошибочной оценке индивидуальных тромботических рисков у конкретной женщины как низких.
2. Наличие целого ряда заболеваний и других факторов риска: гипертензии, мигрени с аурой, ожирения, сахарного диабета с сосудистыми осложнениями, тяжелых заболеваний печени, крови, системной красной волчанки.
3. Возрастной фактор риска развития осложнений, курение (включая количество сигарет в день).
4. Риски при онкологической патологии.
5. Медикаментозный анамнез на момент консультирования по поводу назначения КОК, включая прием фитопрепаратов.
6. Риски в послеродовом периоде в зависимости от длительности послеродового периода и факта кормления грудью.
Более подробно можно оценить категории приемлемости назначения КОК в документе по ссылке: http://apps.who.int/iris/bitstream/handle/10665/181468/9789241549158_eng.pdf?sequence=1
С другой стороны, КОК могут применяться с лечебной целью. При синдроме поликистозных яичников (СПКЯ) они рекомендованы как препараты первой линии и их эффективность доказана в ходе многочисленных исследований. Однако, несмотря на это, оценка рисков развития осложнений при приеме данных препаратов должна проводиться аналогично вышеуказанному алгоритму.
Известно, что СПКЯ — это диагноз исключения. В каждом руководстве по диагностике и лечению данного синдрома указывается на необходимость исключения целого ряда заболеваний, которые имеют клинику, подобную СПКЯ. Независимо от того, какое руководство взять, перечень всегда включает патологию щитовидной железы, гиперпролактинемию, врожденную дисфункцию коры надпочечников (ВДКН) (неклассическая форма дефицита 21-гидро–ксилазы) и синдром Кушинга (гипер–кортизолемия).
Одним из четко определяющих данный перечень с градацией «всем» и «всем, у кого есть клиника СПКЯ и характерные для другого заболевания клинические данные» является руководство Американского общества эндокринологов «Diagnosis and Treatment of Polycystic Ovary Syndrome: An Endocrine Society Clinical Practice Guideline», 2013 г. Авторы руководства высказались в поддержку Роттердамских критериев постановки диагноза СПКЯ 2003 г., отметив некоторые особенности в разные периоды жизни женщины.
1. Диагностика у женщин репродуктивного возраста
Постановка диагноза СПКЯ проводится при наличии двух из трех следующих критериев: избыток андрогенов (клиническая и/или биохимическая гиперандрогения), дисфункция овуляции и поликистозные яичники, при условии, что исключены заболевания, которые могут приводить к клинической картине, подобной СПКЯ.
Согласно рекомендациям данного руководства, у всех женщин с подозрением на СПКЯ необходимо исключить:
— патологию щитовидной железы;
— гиперпролактинемию;
— ВДКН, неклассический вариант, обусловленный в первую очередь дефицитом фермента 21-гидроксилаза.
Данное обследование рекомендовано провести всем женщинам.
В клинических ситуациях, когда клиника СПКЯ (клиника гиперандрогении, овуляторные нарушения, данные УЗИ о поликистозных яичниках) сочетается с клиническими особенностями других заболеваний, необходимо провести исключение этих патологий для проведения коррекции объемов и методов лечения. Рекомендовано исключить следующие состояния и заболевания:
— беременность;
— гипоталамические формы аменореи, включая функциональную аменорею;
— первичную яичниковую недостаточность;
— андрогенпродуцирующие опухоли;
— синдром Кушинга;
— акромегалию;
— редкие формы — другие формы ВДКН (дефицит 11β-гидроксилазы, дефицит 3β-гидроксистероид–дегидрогеназы), синдром тяжелой инсулинорези–стентности, прием препаратов, нарушения полового развития и др.
2. Диагностика синдрома поликистозных яичников в подростковом периоде
В руководстве указано, что диагноз СПКЯ у девочки-подростка может быть поставлен на основании наличия клинических и/или биохимических признаков гиперандрогении (после исключения вышеперечисленных патологий) в присутствии постоянной олигоменореи. Ановуляторные симптомы и морфологические признаки поликистозных яичников в подростковом периоде не могут быть достаточными для постановки диагноза с учетом того, что это может быть отражением физиологического этапа репродуктивного созревания.
3. Диагностика синдрома поликистозных яичников в перименопаузе и менопаузе
Хотя в настоящее время нет разработанных диагностических критериев СПКЯ в перименопаузе и менопаузе у женщин, авторы указывают, что предполагаемый диагноз СПКЯ может быть основан на задокументированной истории олигоменореи и гиперандрогении в течение репродуктивного периода. Обнаружение по данным УЗИ поликистозных яичников с большой вероятностью свидетельствует о наличии СПКЯ, хотя этот признак маловероятен у менопаузальных женщин.
В документе Европейского общества эндокринологов «The polycystic ovary syndrome: a position statement from the European Society of Endocrinology» (2014) перечень заболеваний практически аналогичный. В 2018 году опубликовано новое мировое руководство «Recommendations from the international evidence-based guideline for the assessment and management of polycystic ovary syndrome», Australian National Health and Medical Research Council of Australia (NHMRC) в партнерстве с ESHRE и АSRM, в котором в очередной раз подтверждена необходимость исключения вышеперечисленных эндокринопатий, с особым акцентом на ВДКН с дефицитом по 21 гидроксилазе.
Далее в статье мы остановимся на основных алгоритмах скринингового обследования для исключения данных патологий.
Исключение патологии щитовидной железы
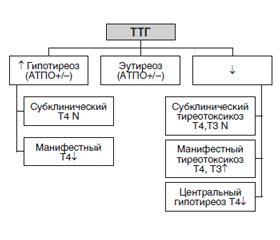
На первом этапе обследования женщины для исключения патологии щитовидной железы достаточно определения уровня тиреотропного гормона (ТТГ), который позволит выделить три категории (рис. 1):
— с эутиреоидным статусом (уровень ТТГ в пределах референтных значений лаборатории);
— с повышенным уровнем ТТГ, что будет свидетельствовать о гипотиреозе. Для решения вопроса, манифестный гипотиреоз или субклинический, необходимо будет дообследование: определение свободных фракций Т4, Т3 (при необходимости), наличия антител к тиреопероксидазе (АТПО), тирео–глобулину (при необходимости). Объем исследований будет определять эндокринолог;
— со снижением уровня ТТГ, что может свидетельствовать не только о тиреотоксикозе, но и о вторичном гипотиреозе. Для решения вопроса, манифестный тиреотоксикоз или субклинический, и проведения дифференциальной диагностики со вторичным гипотиреозом необходимо будет дообследование: определение свободных фракций Т4, Т3 (при необходимости), наличия антител к рецептору ТТГ (АТ рТТГ). Объем исследований будет определять эндокринолог.
При направлении на определение уровня ТТГ необходимо учитывать:
— суточную вариабельность ТТГ. Максимальные уровни наблюдаются в ночной период 2:00 — 4:00, минимальные уровни — в 14:00 — 16:00. Данные исследований суточной вариабельности констатируют, что в период с 8:00 до 9:30 уровень ТТГ может быть снижен на 50 % (по сравнению с ночным пиком). Все эти данные о вариабельности данного гормона определяют необходимость сдавать ТТГ в утреннее время, натощак, с учетом времени сдачи анализа. При повторном обследовании оптимально оценивать ТТГ в аналогичное время;
— вариабельность при определении на приборах и реагентах разных производителей. Оценку ТТГ необходимо проводить в одной лаборатории (на аппарате и реагентах одного производителя), т.к. минимальные отличия в определяемом уровне ТТГ присутствуют;
— вариабельность при стрессе. Важно соблюдать физический и эмоциональный покой перед сдачей анализа, в том числе нормальный режим сна. Это особенно важно для тех, кто работает в ночное время, летает со сменой часовых поясов — все это может отразиться на уровне ТТГ.
При интерпретации уровня ТТГ необходимо учитывать:
— референтные пределы — это уровни ТТГ только у 95 % всех здоровых людей, 5 % здоровых имеют уровни ТТГ несколько выше или ниже пределов. Это определяет необходимость дополнительного обследования и учета клинической картины в случаях, когда уровень ТТГ незначительно выходит за референтные пределы;
— диагностические пороги — это принятые уровни того или иного гормона, которые позволяют диагностировать то или иное заболевание или требуют дополнительного обследования. Данные уровни могут входить в референтные пределы. Например, известно, что во время беременности интерпретация ТТГ зависит от триместра (триместр-специфичные уровни): 2,5 мМЕ/л для первого и 3,0 для второго и третьего триместров по руководству ЕТА 2014 года, однако по АТА 2017 года предложен уровень 4,0 мМЕ/л. Поэтому при интерпретации необходимо учитывать диагностические цели лабораторного обследования;
— суточную вариабельность ТТГ, о которой сказано выше.
Исключение гиперпролактинемии
На первом этапе обследования женщины для исключения гиперпролактинемии достаточно опре–деления пролактина (ПРЛ), который позволит выявить гиперпролактинемию.
Согласно руководству «Diagnosis and Treatment of Hyperprolactinemia: An Endocrine Society Clinical Practice Guideline» (2011), для постановки диагноза гиперпролактинемии рекомендовано однократное определение уровня ПРЛ при условии исключения влияния факторов, которые могут повышать уровни гормона.
1. Физиологические причины повышения уровня ПРЛ: коитус, интенсивные физические нагрузки, сон, стресс (включая стресс при венепункции), лактация, беременность.
2. Прием медикаментов: эстрогенов, оральных –контрацептивов, препаратов заместительной гормональной терапии, блокаторов рецепторов допамина (фенотиазины), антагонистов допамина (метоклопрамид), антигипертензивных препаратов, антигистаминных препаратов (Н2), холинергических агонистов, анестетиков, противосудорожных, антидепрессантов, антипсихотических препаратов, нейролептиков, нейропептидов, опиатов и антагонистов опиатов.
Согласно руководству, данные препараты должны быть отменены (при клинической возможности) на 3 дня или заменены на препараты, которые не стимулируют синтез ПРЛ. В случае получения повышенных уровней ПРЛ на фоне приема данных препаратов необходимо повторное тестирование (в условиях отмены) или учет возможности препарат–индуцированной гиперпролактинемии. С другой стороны, необходимо учитывать прием препаратов, снижающих уровень ПРЛ, — допаминергических (бромкриптин, каберголин, тергурид, ропинерол), которые приведут к несвое–временной диагностике наличия патологии.
Уровни пролактина, которые позволяют установить диагноз гиперпролактинемии, согласно руководству, следующие:
— гиперпролактинемия — повышение более 25 нг/мл;
— повышение более 200 нг/мл наиболее вероятно обусловлено пролактиномой;
— повышение более 200 нг/мл может быть при приеме препаратов;
— уровень более 500 нг/мл характерен для макроаденомы.
После установления гиперпролактинемии необходимо дообследование для исключения целого ряда состояний и заболеваний (рис. 2):
1. Патологии щитовидной железы (гипоти–реоза) — определение ТТГ и свободного тироксина (Т4 свободный). Выявление гипотиреоза требует заместительной терапии, на фоне которой возможна нормализация уровня пролактина без назначения специфического лечения гиперпролактинемии.
2. Опухолей гипоталамо-гипофизарной области: соматотропиномы, краниофарингиомы, герминомы, менингиомы, гранулемы, травм, включая операционные, воспалительных поражений, воздействия облучения — проведение инструментальных методов визуализации, определение других гормонов гипофиза.
3. Почечной недостаточности — оценка уровня креатинина или более раннего и специфичного цистатина.
4. Гиперпролактинемии за счет увеличения макропролактина — определение макропролактина. Уровень макропролактина более 60 % (Roche, Cobas) будет свидетельствовать о макропролактинемии (увеличение ПРЛ за счет гормонально неактивной фракции). Это необходимо учитывать при определении тактики лечения гиперпролактинемии.
5. Целого ряда других причин: травмы грудной клетки, эпилептических эпизодов, синдрома поликистозных яичников.
При направлении на определение уровня ПРЛ необходимо учитывать:
— суточную вариабельность ПРЛ. Максимальные уровни наблюдаются в ночной период 2:00 — 4:00. Все это определяет необходимость сдавать ПРЛ в утреннее время, натощак, с учетом времени подъема после сна. При повторном обследовании оптимально оценивать ПРЛ в аналогичное время;
— вариабельность при определении на приборах и реагентах разных производителей. Оценку ПРЛ необходимо проводить в одной лаборатории (на аппарате и реагентах одного производителя), т.к. минимальные различия в определяемом уровне ПРЛ присутствуют;
— вариабельность при стрессе. Важно соблюдать физический, эмоциональный и сексуальный покой перед сдачей анализа, в том числе нормальный режим сна. Это особенно важно для тех, кто работает в ночное время, летает со сменой часовых поясов — все это может отразиться на уровне ПРЛ.
При интерпретации уровня ПРЛ необходимо учитывать:
— референтные пределы — это уровни ПРЛ только у 95 % всех здоровых людей, 5 % здоровых имеют уровни ПРЛ несколько выше или ниже пределов. Это определяет необходимость дополнительного обследования и учета клинической картины в случаях, когда уровень ПРЛ незначительно выходит за референтные пределы, в первую очередь факторы стресса;
— диагностические пороги — в руководстве по диагностике гиперпролактинемии за диагностический порог ПРЛ принят уровень 25 нг/мл;
— возможность hook-effect (лабораторный эффект, который может наблюдаться при крайне высоких уровнях гормона). Это ведет к невозможности определить истинные уровни гормона — чаще всего уровень находится в пределах референтных значений или несколько повышен. Для реагентов Roche на аппаратах Cobas данный эффект может быть при уровнях ПРЛ, превышающих 12 690 нг/мл. Данные уровни ПРЛ могут наблюдаться при макроаденомах, которые сопровождаются не только клиникой гиперпролактинемии, но и эффектами сдавления окружающих тканей опухолью (выраженными головными болями, нарушением полей зрения). Согласно вышеуказанному руководству, в ситуациях наличия клиники, данных МРТ о макроаденоме и уровнях ПРЛ в пределах референтных значений необходимо повторное тестирование уровня ПРЛ в пробах с разведением 1 : 100 для возможности получения истинного уровня гормона, определения объема терапии и контроля эффективности лечения (оценка динамики и степени снижения уровня ПРЛ);
— вариабельность ПРЛ — суточную, о которой указано выше, а также вследствие стресса, физической и сексуальной активности.
Конфликт интересов. Автор заявляет об отсутствии какого-либо конфликта интересов при подготовке данной статьи.

/599-1.jpg)
/600-1.jpg)