Украинский журнал хирургии 2 (37) 2018
Вернуться к номеру
Діагностика пошкоджень стравоходу з розвитком гострого гнійного медіастиніту
Авторы: Сніжко С.С.
Івано-Франківський національний медичний університет, м. Івано-Франківськ, Україна
Рубрики: Хирургия
Разделы: Клинические исследования
Версия для печати
Мета дослідження: підвищити якість діагностики перфорацій стравоходу (ПС) та гострого гнійного медіастиніту (ГГМ) із застосуванням інструментальних методів діагностики. Матеріали та методи. У 2000–2018 рр. на лікуванні у відділенні торакальної хірургії Івано-Франківської обласної лікарні перебували 92 хворі із ПС, із них ГГМ діагностований у 33 (35,8 %). Результати. Для вирішення поставлених завдань були проаналізовані результати діагностики із застосуванням рентгенографії органів грудної клітки, спіральної комп’ютерної томографії, рентгенконтрастного обстеження стравоходу, езофагогастродуоденоскопії, фібробронхоскопії, ультразвукової діагностики клітковини шиї, верхнього середостіння, плевральних синусів, серця та перикарду. Висновки. Використання комплексу інструментальних досліджень є вирішальним фактором у вірній діагностиці гострого гнійного медіастиніту. Найбільш інформативним методом для діагностики гострого гнійного медіастиніту є спіральна комп’ютерна томографія, діагностична цінність якої становить 100 %. Застосування додаткових методів дослідження, а саме ренгенконтрастного обстеження стравоходу, ультразвукового дослідження, фібробронхоскопії, дозволяє підтвердити діагноз гострого гнійного медіастиніту та визначити характер ускладнень, що є визначальним у виборі подальшої хірургічної тактики лікування.
Цель исследования: повысить качество диагностики перфораций пищевода (ПП) и острого гнойного медиастинита (ОГМ) с применением инструментальных методов диагностики. Материалы и методы. В 2000–2018 гг. на лечении в отделении торакальной хирургии Ивано-Франковской областной больницы находились 92 больных с ПП, из них ОГМ диагностирован у 33 (35,8 %). Результаты. Для решения поставленных задач были проанализированы результаты диагностики с применением рентгенографии органов грудной клетки, спиральной компьютерной томографии, рентгенконтрастного обследования пищевода, эзофагогастродуоденоскопии, фибробронхоскопии, ультразвуковой диагностики клетчатки шеи, верхнего средостения, плевральных синусов, сердца и перикарда. Выводы. Использование комплекса инструментальных исследований является решающим фактором в верной диагностике острого гнойного медиастинита. Наиболее информативным методом для диагностики острого гнойного медиастинита является спиральная компьютерная томография, диагностическая ценность которой составляет 100 %. Применение дополнительных методов исследования, а именно ренгенконтрастного обследования пищевода, ультразвукового исследования, фибробронхоскопии, позволяет подтвердить диагноз острого гнойного медиастинита и определить характер осложнений, является определяющим в выборе дальнейшей хирургической тактики лечения.
The purpose of the study: to improve the quality of diagnosis of esophageal perforations and acute purulent mediastinitis using instrumental diagnostic methods. Materials and methods. In 2000–2018, 92 patients with esophageal perforations were treated at the department of thoracic surgery of Ivano-Frankivsk Regional Hospital, 33 (35.8 %) of them were diagnosed with acute purulent mediastinitis. Results. To solve the taska, the results of the diagnosis were analyzed using chest X-ray, spiral computed tomography, esophagogram, esophagogastroduodenoscopy, fiber-optic bronchoscopy, ultrasound of the neck, upper mediastinum, pleural sinuses, heart and pericardium. Conclusions. The use of a set of instrumental researches is a decisive factor in the correct diagnosis of acute purulent mediastinitis. The most informative method for the diagnosis of acute purulent mediastinitis is spiral computed tomography with a diagnostic value of 100 %. The use of additional research methods, namely esophagogram, ultrasound, fiber-optic bronchoscopy, can confirm the diagnosis of acute purulent mediastinitis and determine the nature of complications, which is decisive in choosing further surgical treatment.
перфорація стравоходу; медіастиніт; діагностика перфорацій стравоходу
перфорация пищевода; медиастинит; диагностика перфорации пищевода
esophageal perforation; mediastinitis; diagnosis of esophageal perforations
Вступ
Проблема діагностики і лікування перфорацій стравоходу (ПС) залишається актуальною, що обумовлено високою летальністю (від 36 до 78 %), тривалою непрацездатністю і значною інвалідизацією цих хворих [1, 2].
Частота ПС має тенденцію до зростання, що обумовлено широким використанням ендоскопічної техніки, збільшенням частоти дорожньо-траспортних пригод, виробничого і побутового травматизму. Особливі труднощі в діагностиці і лікуванні ПС виникають при розвитку гострого гнійного медіастиніту (ГГМ) [3, 4]. У сучасній літературі гострий гнійний медіастиніт вважають однією із найбільш тяжких форм загальної хірургічної інфекції, що характеризується агресивним клінічним перебігом, швидким розвитком синдрому системної запальної відповіді з явищами вираженої ендогенної інтоксикації, сепсису та поліорганної недостатності [5–7].
Рання діагностика ПС здебільшого вирішує прогноз і результати лікування [7–9]. Найбільш поширеними методами діагностики є рентгенографія органів грудної клітки (ОГК), що дозволяє діагностувати гнійно-запальний процес, спіральна комп’ютерна томографія (СКТ), рентгенконтрастне обстеження стравоходу, езофагогастродуоденоскопія (ЕГДС), ультразвукове дослідження (УЗД). Саме така повна картина дозволяє вибрати найбільш раціональний хірургічний метод лікування із врахуванням всіх змін організму [10, 11]. Вирішення цих проблем і є метою нашого дослідження. Для вирішення поставлених завдань у хворих із ГГМ були проаналізовані результати діагностики гострого гнійного медіастиніту із застосуванням рентгенографії органів грудної клітки, СКТ, рентгенконтрастного обстеження стравоходу, ЕГДС, фібробронхоскопії (ФБС), УЗД клітковини шиї, верхнього середостіння, плевральних синусів, серця та перикарду.
Мета дослідження: підвищити якість діагностики перфорацій стравоходу, ускладненого гострим гнійним медіастинітом, із застосуванням інструментальних методів дослідження.
Матеріали та методи
За 2000–2018 рр. на лікуванні у відділенні торакальної хірургії Івано-Франківської обласної лікарні перебували 92 хворі із ПС, із них ГГМ діагностований у 33 (35,8 %) хворих. Серед 33 хворих із ПС, ускладненими ГГМ, — 21 (63,6 %) чоловік, 12 (36,4 %) жінок віком від 23 до 72 років, у середньому — 48,4 року. Причинами ПС були сторонні тіла стравоходу у 13 (39,44 %), спонтанний розрив стравоходу (синдром Бурхаве) — у 8 (24,24 %), ятрогенні пошкодження — у 8 (24,24 %), неспроможність швів після резекції стравоходу — у 2 (6,13 %), неспроможність швів після резекції дивертикулу стравоходу — у 1 хворого, стентування стравоходу при пухлинному процесі — у 1 хворого.
Серед цих хворих задній ГГМ діагностовано у 16 (48,45 %), тотальний ГГМ — у 13 (39,42 %), верхній ГГМ — у 4 (12,13 %) хворих.
Результати та обговорення
Інструментальним методам належить вирішальна роль у діагностиці ПС та ГГМ. До основних методів відносимо: оглядову рентгенографію органів грудної клітки, СКТ, контрастну рентгенографію стравоходу, ЕГДС, УЗД клітковини шиї, верхнього середостіння, плевральних синусів, серця та перикарду.
Оглядова рентгенографія ОГК проводилася всім хворим із підозрою на ПС та ГГМ. Незважаючи на появу більш сучасних методів обстеження, роль рентгенографії ОГК є вкрай важливою. Даний метод доступний для використання на всіх етапах діагностики, тому вірна оцінка даних рентгенографії ОГК може бути відправною точкою у діагностиці ГГМ.
Основним рентгенологічним симптомом ГГМ, як ознаку ПС, ми вважаємо розширення тіні середостіння, яке виявлено нами у 18 (64,2 %) хворих. Розширення тіні середостіння залежало від локалізації ПС і поширеності гнійного процесу. Найбільш специфічним даний симптом був у хворих із верхнім ГГМ. Враховуючи, що в нормі тінь середостіння у верхніх відділах не виходить за межі тіні хребетного стовпа і становить 4–5 см, розширення її виявлено у 4 (100 %) хворих із ПС та верхнім ГГМ. Величина розширення тіні середостіння становила від 6 до 14 см (в середньому — 8,9 ± 1,2 см). Розширення тіні середостіння мало випуклий або випрямлений зовнішній контур, зовнішня межа якого не чітка, розмита. При ПС та тотальних ГГМ розширення тіні середостіння виявлено у 9 (69,2 %) хворих, при задніх ГГМ — у 3 (18,7 %). Низька діагностика частоти розширення тіні середостіння, згідно з рентгенографією ОГК, при задніх ГГМ обумовлена переважною локалізацією гнійного процесу у нижніх відділах середостіння, які перекриваються тінню серця, що утруднює виявлення даного симптому. Тому виявлення розширення тіні середостіння слід вважати одним із вірогідних симптомів ГГМ при відповідній клінічній симптоматиці, і навпаки, відсутність симптому рентгенологічного розширення тіні середостіння не означає відсутність гнійного процесу у середостінні.
Рентгенконтрастне обстеження стравоходу проводили в усіх хворих із ГГМ при підозрі на його перфорацію. Метою даного дослідження було встановити сам факт витоку контрастної речовини за межі просвіту стравоходу, що вказує на його перфорацію, локалізацію пошкодження стравоходу, величину пошкодження, зв’язок із середостіння та плевральною порожниною. Дискусійним є питання вибору контрастної речовини для дослідження. При підозрі на пошкодження стравоходу ми використовували розчин сульфату барію у 19 (67,8 %) хворих, йодовмісні водорозчинні контрастні речовини використано у 9 (32,2 %) хворих. При застосуванні сульфату барію пошкодження стравоходу було виявлено у 15 (78,9 %) із 19 хворих, у яких в подальшому було діагностовано ПС. При використанні йодовмісних водорозчинних контрастних речовин пошкодження стравоходу виявлено у 6 (66,6 %) із 9 хворих, у яких в подальшому було діагностовано ПС. Перевагами використання розчину сульфату барію є його більша діагностична цінність, що дозволяє виявляти навіть незначні пошкодження стравоходу за рахунок більш тугого наповнення просвіту стравоходу. Недоліками є обмеження використання ендоскопічних методів обстеження стравоходу після застосування сульфату барію. Дискусійним також є вплив барієвої суміші на навколишні тканини, проте ускладнень чи інших неблагополучних впливів при потраплянні у клітковину середостіння чи плевральну порожнину нами не було виявлено [4, 5]. При використанні водорозчинних йодовмісних контрастних речовин ми не відмітили суттєвих переваг, проте вони більш широко застосовувалися при потребі у подальшому проводити ЕГДС та для контролю за перебігом загоєння пошкодження стравоходу у післяопераційному періоді.
Основним симптомом ПС при проведенні рентгенконтрастного обстеження стравоходу є витік контрасту за межі просвіту стравоходу. Величина пошкодження стравоходу залежала від причини. При пошкодженнях стравоходу, які виникли внаслідок спонтанного розриву стравоходу, у 100 % випадків встановлено витік контрасту за межі стравоходу. При цьому у 3 (37,5 %) хворих контраст був у клітковині середостіння, у 5 (62,5 %) відмічено витік контрасту у плевральну порожнину, що вказує на пошкодження стравоходу та розрив медіастинальної плеври. Розміри перфорації при спонтанному розриві стравоходу були найбільш значними і коливалися від 1,5 до 9 см. Локалізація ПС у 100 % випадків — нижня третина стравоходу, розрив лівої стінки діагностовано у 5 (62,5 %), правої — у 3 (37,5 %) хворих.
При ПС, які виникли внаслідок ятрогенних пошкоджень, дані рентгенконтрастного обстеження стравоходу були більш варіабельними. Так, витік контрастної речовини за межі просвіту стравоходу діагностовано у 5 (62,5 %) із 8 хворих. Пошкодження стравоходу, що виникали при проведенні бужування стравоходу внаслідок хімічних опіків, переважно діагностували у місцях фізіологічних звужень, де був найбільш виражений стеноз стравоходу. Розміри перфорації значно коливалися — від мікроперфорацій (0,3 см) до великих розривів (5–7 см).
При ПС, які виникали при пошкодженні сторонніми тілами, виявлення пошкодження стравоходу становило найбільші труднощі, оскільки ряд ПС виникав внаслідок пошкодження тонкими предметами, а саме риб’ячою кісткою, голками і т.д. Тому витік контрасту у таких хворих діагностовано лише у 6 (46,1 %) хворих. Встановити факт перфорації в таких хворих дозволяють інші методи інструментального дослідження, а саме СКТ та ендоскопічні методи, які можуть виявити вторинні ознаки ПС.
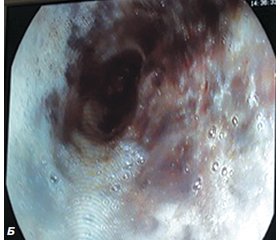
ЕГДС є одним із найбільш інформативних методів діагностики ПС [7, 11]. ЕГДС показана всім хворим із підозрою на ПС. Недоліками даного методу вважають можливість збільшення перфоративного отвору стравоходу і наростання медіастинальної емфіземи за рахунок нагнітання повітря при проведенні обстеження [5, 9]. Проте ми не відмічали суттєвого збільшення розмірів перфорації чи медіастинальної емфіземи. ЕГДС нами проведена у 24 (85,7 %) хворих із підозрінням на ПС. ЕГДС не проводили хворим, у яких факт ПС був чітко діагностований при проведенні рентгенконтрастного методу обстеження. Особливо доцільно використання ЕГДС у сумнівних випадках, у яких при проведенні рентгенконтрастного обстеження стравоходу не виявлено місця перфорації. При огляді виявляли стан слизової, наявність дефектів та їх характеристики — розміри, локалізація, краї дефекту, глибина; наявність сторонніх тіл стравоходу або ознак попереднього їх перебування — пролежні, зміни слизової. При проведенні ЕГДС виявити ПС вдалося лише у 15 (62,5 %) хворих (рис. 1).
На рис. 1А при проведенні ЕГДС виявлено спонтанний розрив правої стінки нижньої третини стравоходу розміром 5 ´ 2 см (синдром Бурхаве) із гнійним ураженням клітковини середостіння. На рис. 1Б у цього ж хворого виявлено «чорний» стравохід внаслідок тривалого блювання, що призвело до некротичних змін слизової стравоходу.
Проте у сумнівних випадках використання ЕГДС дозволяє прогнозувати ПС за вторинними ознаками. Так, серед 7 хворих, у яких не діагностовано ПС за допомогою рентгенконтрастного методу, при виконанні ЕГДС наскрізне пошкодження стінки стравоходу виявлено у 4 (57,1 %) хворих, зміни слизової в ділянці перфорації — у 6 (85,7 %), кровоточивість ділянки перфорації — у 3 (42,8 %), дефекти слизової — у 7 (100 %), некротичні зміни — у 4 (57,1 %) хворих. Дані вторинні ознаки ПС при ЕГДС дають основу для продовження активного діагностичного пошуку, а саме проведення СКТ.
СКТ є одним із вирішальних методів діагностики ПС та ГГМ. Починаючи з 2004 року СКТ проводилося всім хворим із підозрою на ПС та ГГМ. Діагностична цінність методу, за нашими даними, становить 100 %.
Патологічний процес у середостінні переважно був поширеним, і зміни, які були виявлені при СКТ, ми поділили на 2 групи: ознаки, що характеризують зміни клітковини середостіння, і ознаки, що відображають зміни органів середостіння, легень, плевральних порожнин, які виникають як результат гнійно-запального процесу у середостінні. Основними симптомами ГГМ, за результатами СКТ, були: інфільтрація клітковини середостіння, розширення меж середостіння, неоднорідність структури клітковини середостіння за рахунок появи ділянок м’якотканинної щільності, поява рідинних скупчень і бульбашок газу у клітковині середостіння, набряк і потовщення фасцій середостіння. До другої групи, а саме додаткових непрямих ознак ГГМ, відносили появу рідини у плевральній порожнині та порожнині перикарда, інфільтративні зміни легеневої тканини, зміщення або стиснення трахеї, стравоходу, судин середостіння.
Інфільтрація клітковини середостіння є одним із найбільш характерних СКТ симптомів ПС, ускладнених ГГМ, і виявлена нами у 31 (93,93 %) хворого (рис. 2).
Дифузна інфільтрація клітковини середостіння при ПС та ГГМ діагностована у 19 (57,57 %) хворих, у яких переважно спостерігали тотальний та поширений задній ГГМ. При цьому дифузна інфільтрація характеризувалася неоднорідністю структури клітковини за рахунок вогнищевих і лінійних ділянок м’якотканинної щільності на фоні дифузного підвищення щільності клітковини середостіння до рідинних значень. У таких хворих відмічали нечіткість контурів судин верхньої апертури грудної клітки. За шкалою щільності Хаунсфілда інфільтрація тканин середостіння при ГГМ становила від 12 до 29 HU, в середньому — 25,4 ± 3,1.
Обмежена інфільтрація була виявлена у 14 (42,43 %) хворих (рис. 3).
СКТ-ознаки обмеженого інфільтрату характеризувалися неоднорідністю клітковини середостіння за рахунок зони м’якотканинної щільності неправильної форми з нечітким зовнішнім контуром. Проте обмежена інфільтрація була проміжною стадією ГГМ і досить швидко переходила в абсцес середостіння у 100 % випадків. СКТ-ознаками абсцесу середостіння були: одностороннє розширення середостіння — у 12 (85,71 %), неоднорідність структури клітковини середостіння за рахунок наявності рідинної зони — у 13 (92,85 %), округла форма рідинного компонента з нечіткими контурами — у 9 (50 %), неоднорідність структури за рахунок м’якотканинної щільності по периферії зони — в 11 (78,57 %).
Розширення меж середостіння виникало за рахунок гнійно-інфільтративних змін клітковини, що є одним із найбільш частих симптомів ГГМ і діагностовано у 27 (81,82 %) хворих. Проте у 6 (18,18 %) хворих із ГГМ даний симптом був відсутній або мало виражений. Це спостерігали при гнійно-некротичних ГГМ, що перебігали за типом некротизуючого фасціїту, при яких інфільтрація клітковини середостіння була мало вираженою. Проте при використанні сучасної СКТ можлива ідентифікація гнійних і потовщених фасцій середостіння, що саме дозволяє встановити наявність некротизуючого фасціїту при наявних додаткових критеріях ГГМ (рис. 4).
Поява рідинних скупчень та бульбашок повітря ми вважаємо вірогідною ознакою ПС та ГГМ. Виявлення рідини (гною) у клітковині середостіння у всіх (100 %) випадках в подальшому підтверджувало діагноз ГГМ при проведенні оперативного втручання. Рідинні скупчення нами було діагностовано у 31 (93,94 %) хворого. Рідинні скупчення за шкалою Хаунсфілда мали щільність від 20 HU (переважно гнійний ексудат) до 49 HU (гній) і становили у середньому 37,0 ± 2,7. Появу бульбашок повітря у клітковині середостіння, при проведенні СКТ, теж вважаємо 100% діагностичним критерієм ПС та ГГМ при відповідній клінічній картині (рис. 5).
Переважно повітря у середостінні з’являлося при газоутворюючій мікрофлорі та внаслідок перфорації стравоходу або трахеї. Даний симптом при ПС виявлено у 30 (90,91 %) хворих.
До непрямих СКТ-ознак ПС та ГГМ відносять ознаки ураження інших органів грудної клітки. Так, однобічний плеврит або емпієму плеври при СКТ-обстеженні виявлено у 21 (63,64 %) хворого, двобічний — у 8 (24,24 %), пневмонії — у 12 (36,36 %), абсцес легень — в 1 (3,03 %), наявність рідини у порожнині перикарда — у 10 (30,3 %) (рис. 6).
Фібробронхоскопія як самостійний метод в діагностиці при ПС та ГГМ має досить обмежені показання. Основними показаннями для проведення бронхоскопії були підозри на пошкодження трахеї, яке виявлено нами в 1 (3,03 %) хворого. При використанні ФБС можна відмітити деякі із непрямих ознак ГГМ: пролабування мембранозної частини трахеї в просвіт — у 2 (6,06 %), стиснення однієї із стінок трахеї — у 2 (6,06 %) та зміщення трахеї — у 3 (9,09 %). При розвитку гнійного процесу у середостінні запальний процес швидко поширюється на трахею і стінки бронхів із розвитком гнійного бронхіту у 77 % хворих. Лежачий стан хворих із тривалою штучною вентиляцією легень сприяє розвитку гнійного бронхіту з накопиченням гнійного харкотиння у просвіті бронхів, що часто призводить до ателектазів легень, пневмоній і розвитку абсцесів легень. Тому використання санаційних ФБС є вкрай важливим в післяопераційному веденні таких хворих.
Ультразвукове дослідження у хворих із ГГМ використовується широко, проте його діагностична цінність саме в діагностиці ПС та ГГМ обмежена, оскільки не вдається візуалізувати клітковину середостіння через акустичні тіні ребер та грудини. Проте ми використовували УЗД при ПС у шийному відділі та передньо-верхніх ГГМ, де чітко могли спостерігати рідинні скупчення у міжфасціальних проміжках шиї та у клітковині передньо-верхнього середостіння, їх характер, розміри, локалізацію, збільшення лімфатичних вузлів, кровотік по яремних та підключичних венах. УЗД має вкрай важливе значення при діагностиці ускладнень ГГМ, які і є вторинними ознаками, а саме появи рідини у плевральних порожнинах і перикарді. Саме при УЗД запідозрити і в подальшому підтвердити наявність ексудативного плевриту та емпієми плеври нам вдалося у 30 (90,9 %) хворих, ексудативного перикардиту — у 10 (30,3 %).
Висновки
1. Використання комплексу інструментальних досліджень є вирішальним фактором у діагностиці перфорацій стравоходу, ускладнених гострим гнійним медіастинітом.
2. Найбільш інформативним методом для діагностики гострого гнійного медіастиніту є спіральна комп’ютерна томографія, діагностична цінність якої становить 100 %.
3. Застосування додаткових методів дослідження, а саме ренгенконтрастного обстеження стравоходу, езофагогастроскопії, ультразвукового дослідження, бронхоскопії, дозволяє підтвердити діагноз перфорації стравоходу, ускладненої гострим гнійним медіастинітом, та визначити характер ускладнень, що є визначальним у виборі подальшої хірургічної тактики лікування.
Конфлікт інтересів. Автор заявляє про відсутність конфлікту інтересів при підготовці даної статті.
1. Canbay G., Bertrand X. Mediastinitis on oesphagal perforation // Rev. Med. Liege. — 2017 Mar. — 72(3). — Р. 121-125.
2. Karagyozov P., Minchev T., Tishkov I., Plachkov I. Hybrid therapy of late diagnosed esophageal perforation, complicated by mediastinitis and bilateral empyema // Endoscopy. — 2017 Feb. — 49(S 01). — E127-E128. doi: 10.1055/s-0043-103947. Epub 2017 Mar 22.
3. Park I.H., Lim H.K., Song S.W., Lee K.H. Perforation of esophagus and subsequent mediastinitis following mussel shell ingestion // J. Thorac. Dis. — 2016 Aug. — 8(8). — E693-7. doi: 10.21037/jtd.2016.07.88.
4. Дробязгин E.A., Чикинев Ю.В., Аникина М.С. Диагностика и лечение пациентов с инструментальной перфорацией пищевода // Вестник хирургии. — 2016. — № 4. — С. 64-67.
5. Toru Nakano, Ko Onodera, Hirofumi Ichikawa, Takashi Kamei. Thoracoscopic primary repair with mediastinal drainage is a viable option for patients with Boerhaave’s syndrome // J. Thorac. Dis. — 2018 Feb. — 10(2). — Р. 784-789.
6. Шевчук І.М., Сніжко С.С. Аналіз ускладнень гострого гнійного медіастиніту // Клін. хірургія. — 2017. — № 1. — С. 36-38.
7. Soppimath S.S., Chiniwalar S., Hartimath B., Padasali P. Endoscopic mediastinal debridement for mediastinitis resulting from upper esophageal perforation // Endoscopy. — 2016. — 48(Suppl. 1). — E168-9. doi: 10.1055/s-0042-105562. Epub 2016 Apr 29.
8. Krüger M., Decker S., Schneider J.P., Haverich A., Schega O. Surgical treatment of acute mediastinitis // Chirurg. — 2016 Jun. — 87(6). — Р. 478-85.
9. Nirula R. Esophageal perforation // Surg. Clin. North Am. — 2014 Feb. — 94(1). — Р. 35-41. doi: 10.1016/j.suc.2013.10.003. Epub 2013 Nov 5.
10. Markar S.R., Mackenzie H., Wiggins T., Askari A., Faiz O., Zaninotto G., Hanna G.B. Management and Outcomes of Esophageal Perforation: A National Study of 2,564 Patients in England // Am. J. Gastroenterol. — 2015 Nov. — 110(11). — Р. 1559-66. doi: 10.1038/ajg.2015.304. Epub 2015 Oct 6.
11. Kim J.E., Ryoo S.M., Kim Y.J., Lee J.S., Ahn S., Seo D.W., Sohn C.H., Ryu J.M., Kim W.Y. Incidence and Clinical Features of Esophageal Perforation Caused by Ingested Foreign Body // Korean J. Gastroenterol. — 2015 Nov. — 66(5). — Р. 255-60. doi: 10.4166/kjg.2015.66.5.255.

/43-1.jpg)
/45-1.jpg)
/46-1.jpg)