Журнал «Здоровье ребенка» Том 13, №8, 2018
Вернуться к номеру
Гострий обструктивний бронхіт у дітей: ефективність і переносимість крапель і сиропу Проспан
Авторы: Лапшин В.Ф., Уманець Т.Р., Пустовалова О.І.
ДУ «Інститут педіатрії, акушерства і гінекології НАМН України», м. Київ, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Метою нашого відкритого рандомізованого проспективного порівняльного дослідження було вивчення ефективності й безпеки застосування крапель і сиропу Проспан у дітей із гострим обструктивним бронхітом. Під спостереженням перебували 54 дитини віком від 6 до 12 років із гострим обструктивним бронхітом. Критеріями ефективності проведеного лікування були регрес основних клінічних проявів хвороби, динаміка показників спірометрії, зміни клітинного складу індукованого мокротиння. Застосування двох форм препарату Проспан у дітей із гострим обструктивним бронхітом легкого перебігу сприяло більш швидкому регресу основних симптомів захворювання, покращенню функції зовнішнього дихання й показників клітинного складу індукованого мокротиння.
Целью нашего открытого рандомизированного проспективного сравнительного исследования было изучение эффективности и безопасности применения капель и сиропа Проспан у детей с острым обструктивным бронхитом. Под наблюдением находились 54 ребенка в возрасте от 6 до 12 лет с острым обструктивным бронхитом. Критериями эффективности проводимого лечения были регресс основных клинических симптомов болезни, динамика показателей спирометрии, изменение клеточного состава индуцированной мокроты. Применение двух форм препарата Проспан у детей с острым обструктивным бронхитом легкого течения способствовало более быстрому регрессу основных симптомов заболевания, улучшению функции внешнего дыхания и показателей клеточного состава индуцированной мокроты.
The objective of our open-label, randomized, prospective, comparative study was to evaluate the efficacy and safety of Prospan drops and syrup in children with acute obstructive bronchitis. We have examined 54 children aged 6 to 12 years with acute obstructive bronchitis. The criteria of treatment effectiveness were the regression of the main clinical manifestations of the disease, the dynamics of spirometry parameters, changes in the cellular composition of induced sputum. The use of two formulations of Prospan in children with mild acute obstructive bronchitis contributed to a more rapid regression of the main symptoms of the disease, improvement of the function of external respiration and indicators of cellular composition of induced sputum.
гострий обструктивний бронхіт; діти; екстракт плюща
острый обструктивный бронхит; дети; экстракт плюща
acute obstructive bronchitis; children; ivy extract
Вступ
До цього часу захворювання органів дихання посідають перше місце в структурі загальної захворюваності дітей від 0 до 17 років, серед яких гострим бронхітам належить провідна роль [1, 2]. За даними різних дослідників, у нозологічній структурі гострого бронхіту в дітей на гострий обструктивний бронхіт (ГОБ) припадає близько 20–25 % [1, 4, 8].
Протягом багатьох років ГОБ у дітей привертає пильну увагу практичних лікарів і вчених, що пов’язано з поширеністю й гетерогенністю даної патології, а отже, із труднощами диференціальної діагностики.
Анатомо-фізіологічні особливості органів дихання, а саме: відносна вузькість дихальних шляхів (ДШ), слабкий розвиток гладкої мускулатури бронхів, недостатня еластичність легеневої тканини, виражена васкуляризація слизової ДШ, велика кількість келихоподібних клітин на тлі активності парасимпатичного відділу вегетативної нервової системи обумовлюють перевагу вазосекреторного компонента запалення ДШ і схильність до розвитку ГОБ у дітей. Крім того, у дітей перших трьох років життя мають місце неспроможність інтерфероногенезу й Th2-спрямованість імунної відповіді, що також сприяють формуванню бронхіальної обструкції при гострих респіраторних інфекціях [5, 6, 9, 16].
Хоча етіологічні чинники ГОБ у дітей рідко ідентифікуються в рутинній клінічній практиці, до 90,0 % випадків спричинено респіраторними вірусами. При цьому найбільш частими збудниками є респіраторно-синцитіальний вірус, аденовірус, коронавірус, віруси грипа А і В, метапневмовірус, віруси парагрипу 1–3-го типів і риновірус. У дітей старшого віку збільшується значення бактеріальної інфекції — Chlamydia pneumoniaе, Mycoplasma pneumoniaе, Bordetella pertussis (у невакцинованих дітей) [3–9, 11, 15, 16]. Респіраторні збудники пошкоджують бронхіальний епітелій, що призводить до продукування прозапальних медіаторів із розвитком запального процесу в ДШ, компонентами якого є набряк слизової, гіперсекреція в’язкого бронхіального секрету й бронхоспазм [16].
При запаленні ДШ при ГОБ значно підвищується секреторна функція бронхіальних залоз і келихоподібних клітин, збільшується вміст у бронхіальному секреті продуктів розпаду клітин, життєдіяльності й розпаду мікроорганізмів, ексудату. Це супроводжується зміною у співвідношенні фукомуцинів і сіаломуцинів, що призводить до підвищення в’язкості слизу й порушення функціональних можливостей мукоциліарного апарату [10].
З позиції доказової медицини в табл. 1 подано ключові рекомендації з лікування гострого бронхіту в дітей [13, 15].
Питання про призначення мукоактивних препаратів у дітей із гострими бронхітами є дискусійним. Так, експекторанти не рекомендовані для рутинного призначення в лікуванні бронхітів, оскільки мають низьку ефективність, більшість із цих препаратів збільшують об’єм бронхіального секрету й можуть погіршувати стан дитини. З іншого боку, застосування деяких мукоактивних засобів патогенетично обґрунтоване, а їх ефективність доведена в низці рандомізованих клінічних досліджень.
У лікуванні обструктивних станів у дітей і дорослих привертає увагу рослинний препарат з оригінального сухого екстракту листя плюща (ЕА575) Проспан, який має комбіновану дію: бронхолітичну, відхаркувальну й протизапальну. Доведено, що один з сапонінів екстракту листя плюща (a-гедерин) перешкоджає зануренню й руйнуванню b2-адренорецепторів (інтерналізації рецепторів). У результаті збільшується площа активних рецепторів на поверхні клітини й чутливість її до адреналіну. Це призводить до зменшення концентрації внутрішньоклітинного Ca2+ у м’язах бронхів і до розслаблення бронхів. Одночасно з цим процесом у результаті стимулювання b2-активності епітеліальні альвеолярні клітини легень II типу продукують більшу кількість сурфактанту, що призводить до зменшення в’язкості слизу й полегшення відходження мокротиння при кашлі [12].
Доведений на 65 383 пацієнтах високий профіль безпеки й ефективності, бронхолітичний, відхаркувальний і протизапальний ефекти препарату дозволили рекомендувати Проспан хворим із різними гострими й хронічними запальними захворюваннями дихальних шляхів, а у віковому аспекті — починаючи з моменту народження [14].
З огляду на порушення слизоутворення й мукоциліарного транспорту бронхіального секрету, бронхоспазм у патогенезі ГОБ і здатність препарату Проспан впливати на ці процеси застосування даного препарату є патогенетично обґрунтованим і раціональним щодо вибору терапії в даної категорії дітей.
Метою нашого дослідження було вивчення ефективності й безпеки застосування двох форм (краплі, сироп) Проспану у дітей із ГОБ.
Матеріали та методи
Під нашим спостереженням перебували 54 дитини віком 6–12 років, які знаходилися на лікуванні в ДУ «Інститут педіатрії, акушерства і гінекології НАМН України» з приводу ГОБ. Верифікація діагнозу проводилась відповідно до Наказу МОЗ України № 18 від 13.01.2005 «Про затвердження Протоколів надання медичної допомоги дітям за спеціальністю «Дитяча пульмонологія». Критеріями включення пацієнтів у дослідження були: відповідний вік дітей, встановлений діагноз ГОБ, отримана в дітей і їх батьків інформована згода на участь; відсутність ознак дихальної недостатності; здатність виконувати спірометричні дослідження. Критеріями виключення були: тяжкі супутні захворювання серцево-судинної системи, печінки, центральної нервової системи; застосування інших муколітичних, відхаркувальних, бронхолітичних засобів; індивідуальна непереносимість фруктози й компонентів препарату.
Для оцінки ефективності й переносимості крапель і сиропу Проспан діти основної групи були розподілені методом пар-копій на дві підгрупи (1а, n = 14; 1b, n = 14). Діти основної групи як монотерапію отримували Проспан у вигляді крапель (1а підгрупа) і сиропу (1b підгрупа). Проспан сироп призначався по 5 мл, краплі — по 16 крапель (дітям 6–9 років) і 24 краплі (дітям 10–12 років) 3 рази на добу. Діти групи порівняння (2-га група, n = 26) отримували амброксол. Контрольну групу станови 20 практично здорових дітей відповідного віку.
Усі діти, взяті під спостереження були ідентичні за віком, статтю й тяжкістю перебігу ГОБ.
Дизайн дослідження відповідав моделі відкритого рандомізованого проспективного порівняльного дослідження і включав візити: скринінгу, лікувального періоду (на 3–4-й і 7–10-й день лікування) та етапу спостереження протягом 2 тижнів. Дослідження було проведене за період із лютого по жовтень 2016 року.
Критеріями ефективності проведеного лікування були: регрес основних клінічних проявів хвороби (частота й характер кашлю, кількість мокротиння, аускультативні дані в легенях, потреба в b2-агоністах короткої дії), динаміка показників спірометрії з використанням бронхолітичної проби з сальбутамолом (200–400 мкг), зміни клітинного складу індукованого мокротиння.
З метою оцінки переносимості препарату Проспан в обстежених дітей із ГОБ проведено загальноклінічні аналізи крові, сечі, біохімічні дослідження, реєструвались дані 12-канальної електрокардіограми.
Клінічні прояви захворювання були ранжовані залежно від їх інтенсивності за бальною шкалою: 0 балів — відсутність ознаки, 1 бал — незначна інтенсивність ознаки або симптому, 2 бали — помірна, 3 бали — виражена.
Дослідження функції зовнішнього дихання проводилось на спірографі BTL Type № 2003110660 на основі Mіcro Quark. За допомогою спірографії вивчались загальноприйняті статистичні (легеневі об’єми) і функціональні показники легеневої вентиляції. Реєстрація показників здійснювалась у відсотках від належних значень згідно з нормативом Європейського респіраторного товариства (1993), що обчислювалось автоматично комп’ютерною програмою спірографа. Нормальними вважались показники, які становили 80–120 % від належних.
З метою оцінки запальних змін дихальних шляхів проводили цитологічне дослідження індукованого мокротиння (ІМ) за спрощеною методикою, яка була нами розроблена й запатентована («Спосіб діагностики запальних змін дихальних шляхів у дітей із захворюваннями органів дихання» [7]).
Статистична обробка отриманих результатів дослідження здійснювалася на персональному комп’ютері з використанням програм Microsoft Office Excel 2010.
Результати та обговорення
Серед обстежених дітей переважали хлопчики (57,4 %), за віком — діти 6–8 років (68,5 %).
Частоту основних клінічних проявів ГОБ у дітей, які були включені в дослідження, подано в табл. 2. Особливостями перебігу ГОБ в обстежених дітей були: катаральні явища, малопродуктивний кашель, диспное, субфебрилітет, аускультативні зміни в легенях (на фоні жорстокого дихання з подовженим видихом вислуховувались сухі свистячі й вологі хрипи).
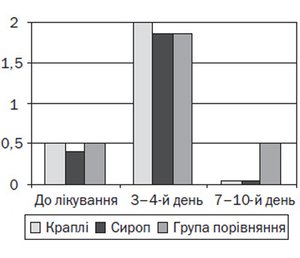
Згідно з результатами проведених досліджень, у дітей основної групи, які отримували краплі або сироп Проспан, спостерігалась краща динаміка основних клінічних проявів захворювання порівняно з групою порівняння (рис. 1). Так, у дітей основної групи відмічались вірогідне зменшення частоти кашлю й зміна його характеру на продуктивний на 3-тю — 4-ту добу від початку лікування та його відсутність на 7-му добу в підгрупі 1а і на 9–10-ту добу — в підгрупі 1b, а при аускультації легень вислуховувалось жорстке дихання. У 18 (69,2 %) дітей групи порівняння на 3–4-й день і у 12 (46,2 %) дітей — на 7–10-й день спостерігався малопродуктивний кашель, при аускультації вислуховувались сухі свистячі й вологі хрипи. Ці діти потребували додаткового призначення інгаляцій сальбутамолу 100 мкг, 1–2 інгаляції на добу.
Проведеними спірометричними дослідженнями встановлено, що в 6 (42,8 %) дітей підгрупи 1а, 5 (35,7 %) пацієнтів підгрупи 1b і 9 (34,6 %) хворих 2-ї групи спостереження на початку лікування реєструвались легкі обструктивні порушення. Бронходилатаційна проба із сальбутамолом показала відсутність відповіді у 2/3 обстежених дітей, що свідчило про порушення бронхіальної прохідності за рахунок таких компонентів, як набряк бронхіальної стінки та/або секреція мокротиння. Лише в 5 (35,7 %) дітей підгрупи 1а і 5 (35,7 %) дітей підгрупи 1b, 8 (30,8 %) хворих групи порівняння реєструвався латентний бронхоспазм.
Про адекватність проведеного лікування в обстежених дітей свідчила позитивна динаміка показників функції зовнішнього дихання. Лише в одного (7,2 %) хворого підгрупи 1а й одного (7,2 %) пацієнта підгрупи 1b основної групи після лікування виявлене зниження максимальної об’ємної швидкості видиху на рівні 25 і 50 % форсованої життєвої ємності легень (MEF25, MEF50), що відображає прохідність великих і середніх відділів бронхіального дерева. Ці діти при проведенні бронходилатаційної проби демонстрували позитивну відповідь на сальбутамол. У частини дітей групи порівняння (2-га група) зберігались легкі обструктивні порушення (у 8 (30,8 %) хворих) і латентний бронхоспазм (у 6 (23,1 %) пацієнтів). Отримані результати спірометричних досліджень у дітей основної групи, а також відсутність у них необхідності в призначенні b-агоністів короткої дії свідчить про бронхолітичний ефект препарату Проспан.
З метою оцінки динаміки запальних змін дихальних шляхів в обстежених дітей нами вивчався цитологічний склад індукованого мокротиння. У табл. 3, 4 подано динаміку клітинного складу ІМ обстежених дітей на тлі лікування.
Згідно з отриманими результатами дослідження, у дітей із ГОБ серед клітинних популяцій ІМ спостерігалась перевага нейтрофілів, лімфоцитів, макрофагів, що свідчило про нейтрофільний тип запалення в більшості дітей (43 (79,6 %) хворих). Лише 11 (20,4 %) дітей із ГОБ мали гіпогранулоцитарний тип запалення.
На тлі лікування в дітей підгрупи 1а спостерігалось вірогідне зменшення відносної кількості бронхіального епітелію, а в дітей підгрупи 1b і групи порівняння — лише тенденція. Однак при аналізі типів клітин бронхіального епітелію в більшості дітей групи порівняння після лікування виявлено ознаки неповної морфологічної ремісії. Так, у 20 (76,9 %) дітей групи порівняння визначено відносне збільшення келихоподібних і дистрофічно змінених війчастих клітин до 69,34 ± 3,16 % (у контролі — відсутність келихоподібних клітин і 23,45 ± 1,21 % війчастих, р < 0,05). Це вказує на структурно-функціональну перебудову війчастих клітин слизової оболонки респіраторного тракту, збільшену продукцію муцинів і, відповідно, порушення мукоциліарного транспорту за рахунок запалення, що зберігалось на 7–10-й день спостереження в дітей групи порівняння порівняно з відсутністю цих змін у дітей основної групи (р < 0,05).
Цитоморфологічна картина нейтрофілів і лімфоцитів у ІМ обстежених дітей характеризувалась на початку лікування збільшенням їх відносної кількості й вірогідним зменшенням на тлі лікування лише в дітей основної групи (р < 0,05).
Індуковане мокротиння дітей із ГОБ також характеризувалось зменшенням кількості макрофагів на початку лікування. На тлі лікування із застосуванням як сиропу, так і крапель Проспан відзначались підвищення макрофагальної реакції, нормалізація відносної кількості вищезазначених ефекторних клітин у дітей основної групи і лише тенденція до таких змін — у дітей групи порівняння. Це може бути пояснено протизапальним ефектом препарату Проспан, який був більше виражений у дітей основної підгрупи 1а, можливо, за рахунок більшої біодоступності крапель препарату.
Клінічна ефективність проведеного лікування в дітей основної групи оцінена як одужання у 25 (89,3 %) хворих, покращання — у 2 (7,14 %), без покращання — в 1 (3,6 %). Моніторинг клініко-біохімічних і електрокардіографічних показників на тлі лікування із застосуванням двох форм препарату Проспан у досліджуваних дітей не виявив побічних реакцій, що свідчило про його добру переносимість. Усі діти відмітили добрі смакові якості як сиропу, так і крапель.
Висновки
1. Діти з ГОБ характеризуються наявністю нейтрофільного типу запалення в слизовій оболонці бронхів (у 79,6 % хворих), легких обструктивних порушень легеневої функції й латентного бронхоспазму (у третини дітей).
2. Застосування двох форм препарату Проспан (краплі, сироп) у лікуванні дітей із ГОБ легкого перебігу сприяє регресу основних клінічних симптомів бронхообструкції, що супроводжується: зменшенням інтенсивності й зміною характеру кашлю на продуктивний на 3–4-й день лікування, нормалізацією фізикальних даних на 7–10-й день лікування, покращенням показників легеневої функції й зменшенням запальних змін дихальних шляхів.
3. Терапевтичний ефект препарату Проспан пов’язаний із бронхолітичним, відхаркувальним і протизапальним ефектами препарату.
4. Висока ефективність і добра переносимість двох форм препарату (краплі, сироп) в обстежених дітей дозволяє рекомендувати Проспан для широкого застосування в клінічній практиці при лікуванні дітей з бронхообструктивними захворюваннями.
Конфлікт інтересів. Не заявлений.
1. Абатуров О.Є. Лікування гострих респіраторних захворювань, які супроводжуються розвитком обструктивного синдрому, у дітей раннього віку / О.Є. Абатуров, І.Л. Височина, Н.М. Токарева // Здоров’я України. — 2009. — № 8/1. — С. 4-5.
2. Антипкін Ю.Г. Динаміка захворюваності та поширеності бронхолегеневої патології у дітей / Ю.Г. Антипкін [та ін.] // Современная педиатрия. — 2016. — № 2(74). — С. 73-77.
3. Бабушкина А.В. Острые респираторные вирусные заболевания и бронхообструктивный синдром / А.В. Бабушкина // Український медичний часопис. — 2011. — № 1(81). — С. 69-74.
4. Лапшин В.Ф. Бронхіти у дітей. Погляд педіатра / В.Ф. Лапшин // Здоров’я України (Medical Nature). — 2009. — № 1. — С. 8-11.
5. Майданник В.Г. Клинические рекомендации по диагностике и лечению острых бронхитов у детей с позиции доказательной медицины / В.Г. Майданник, Е.А. Емчинская. — К., 2014. — 56 с.
6. Охотникова Е.Н. Синдром обструкции дыхательных путей у детей: трудные вопросы — верные решения / Е.Н. Охотникова // Здоровье ребенка. — 2016. — № 1(69). — С. 88-96.
7. Патент № 67055. МПК (2011.01) А61В10/00 Спосіб діагностики запальних змін дихальних шляхів у дітей із захворюваннями органів дихання / Антипкін Ю.Г. [та ін.]. — № 201109545 від 29.07.2011, заявл. 29.07.11; опубл. 25.01.12, Бюл. № 2.
8. Сміян О.І. Особливості клінічного перебігу гострого обструктивного бронхіту в дітей раннього віку / О.І. Сміян, В.А. Плахута // Проблеми безперервної медичної освіти та науки. — 2014. — № 2. — С. 38-41.
9. Юлиш Е.И. О факторах риска развития бронхообструктивного синдрома у детей раннего возраста / Е.И. Юлиш, Ю.А. Сорока, О.Е. Чернышева // Здоровье ребенка. — 2012. — № 6. — С. 85-88.
10. Bruce K. Rubin Secretion properties, clearance, and therapy in airway disease / K.R. Bruce // Translational Respiratory Medicine. — 2014. — 2. — 6 [Електронний ресурс]. — Режим доступу: http://www.transrespmed.com/content/2/1/6
11. Gern J.E. The ABCs of Rhinoviruses, Wheezing, and Asthma / J.E. Gern // J. Virol. — 2010. — Vol. 84, № 15. — Р. 7418-7426.
12. a-Hederin inhibits G protein-coupled receptor kinase 2-mediated phosphorylation of b2-adrenergic receptors / J. Schulte-Michels [et al.] // Phytomedicine. — 2016. — Vol. 23. — P. 52-57.
13. Kinkade S. Acute Bronchitis / S. Kinkade, N.A. Long // Am. Fam. Physician. — 2016. — Vol. 1, № 94(7). — P. 560-565.
14. Lang C.A. Valuable Option for the Treatment of Respiratory Diseases: Review on the Clinical Evidence of the Ivy Leaves Dry Extract EA 575® / C. Lang, P. Röttger-Lüer, C. Staiger // Planta Med. — 2015. — Vol. 81. — P. 968-974.
15. Ross H. Diagnosis and Treatment of Acute bronchitis / H. Ross // Am. Fam. Physician. — 2010. — Vol. 82(11). — P. 1345-1350.
16. Tregoning J.S. Respiratory Viral Infections in Infants: Causes, Clinical Symptoms, Virology, and Immunology / J.S. Tregoning, J. Schwarze // Clin. Microbiol. Rev. — 2010. — Vol. 23, № 1. — P. 74-98.

/34-1.jpg)
/35-1.jpg)
/36-1.jpg)
/37-1.jpg)