Журнал «Здоровье ребенка» Том 14, №7, 2019
Вернуться к номеру
Досвід застосування препарату Фенокіт у лікуванні атопічного дерматиту в дітей раннього віку
Авторы: Беш Л.В., Мацюра О.І., Слюзар З.Л.
Львівський національний медичний університет імені Данила Галицького, м. Львів, Україна
Рубрики: Педиатрия/Неонатология
Разделы: Клинические исследования
Версия для печати
Актуальність. Щорічно близько 35 % населення Землі звертаються по медичну допомогу з клінічними симптомами алергії. Першим її проявом, як правило, є харчова алергія, яка діагностується вже в ранньому дитячому віці й переважно проявляється атопічним дерматитом. На сторінках спеціальної літератури активно обговорюються дискусійні питання щодо термінології, клінічних особливостей і лікування атопічного дерматиту. Зокрема, неоднозначно трактується застосування антигістамінних препаратів у лікуванні даної патології в дітей раннього віку. Мета роботи — представити власний досвід застосування препарату Фенокіт. Матеріали та методи. Досліджувану групу склали 50 дітей з атопічним дерматитом (перебіг легкої або середньої тяжкості) віком від 1 до 18 міс. Критеріями виключення були супутні соматичні та неврологічні захворювання, тяжка форма атопічного дерматиту. Моніторинг перебігу захворювання здійснювали на підставі оцінки ступеня тяжкості захворювання за індексом SCORAD, вираженості свербежу, реєстрації лікарем частоти небажаних явищ та побічних ефектів, якості життя пацієнтів. Результати. Спостереження дітей впродовж місяця дозволило виявити позитивну динаміку клінічних симптомів (зниження індексу SCORAD з 29,2 до 3,5; регрес свербежу з 6,4 до 0,3) і суттєве покращання якості життя пацієнтів (з 19,1 до 4,2). У процесі дослідження вибули четверо дітей, оскільки виникла потреба приєднання до схеми лікування додаткових препаратів (топічних кортикостероїдів). У трьох пацієнтів були зафіксовані побічні ефекти (епізодична нудота, дратівливість), які не потребували відміни препарату. Висновки. Антигістамінний препарат Фенокіт дозволяє ефективно контролювати прояви атопічного дерматиту в дітей раннього віку.
Актуальность. Ежегодно около 35 % населения Земли обращаются за медицинской помощью с клиническими симптомами аллергии. Первым ее проявлением, как правило, является пищевая аллергия, которая диагностируется уже в раннем детском возрасте и преимущественно проявляется атопическим дерматитом. На страницах специальной литературы активно обсуждаются дискуссионные вопросы терминологии, клинических особенностей и лечения атопического дерматита. В частности, неоднозначно трактуется применение антигистаминных препаратов в лечении данной патологии у детей раннего возраста. Цель работы — представить собственный опыт применения препарата Фенокит. Материалы и методы. Исследуемую группу составили 50 детей с атопическим дерматитом (легкой или средней тяжести) в возрасте от 1 до 18 мес. Критериями исключения были определены сопутствующие соматические и неврологические заболевания, тяжелая форма атопического дерматита. Мониторинг течения заболевания осуществляли на основании оценки степени тяжести заболевания по индексу SCORAD, интенсивности зуда, регистрации врачом частоты нежелательных явлений и побочных эффектов, качества жизни пациентов. Результаты. Наблюдение детей в течение месяца позволило выявить положительную динамику клинических симптомов (снижение индекса SCORAD с 29,2 до 3,5; регресс зуда с 6,4 до 0,3) и существенное улучшение качества жизни пациентов (с 19,1 до 4,2). В процессе нашего исследования выбыли четверо детей, поскольку возникла необходимость добавления в схему их лечения дополнительных препаратов (топических кортикостероидов). У трех пациентов были зафиксированы побочные эффекты (эпизодическая тошнота, раздражительность), не требующие отмены препарата. Выводы. Антигистаминный препарат Фенокит позволяет эффективно контролировать проявления атопического дерматита у детей раннего возраста.
Background. About 35 % of world population request for medical support for clinical allergy symptoms annually. Its first sign as usual is food allergy, which is diagnosed in early childhood and mainly manifests by atopic dermatitis. On the pages of special literature, the issues of terminology, clinical features and treatment of atopic dermatitis are debated a lot. In particular, the use of antihistamines for the treatment of this pathology in infants is interpreted ambiguously. The purpose is to presents our experience of using drug Fenokit. Materials and methods. The study group enrolled 50 children with atopic dermatitis (mild to moderate course) aged from 1 and 18 months old. Exclusion criteria were as follows: somatic and neurological diseases, a severe form of atopic dermatitis. The disease was monitored based on an assessment of the disease severity by the SCORAD index; severity of itching; the frequency of adverse events and side effects registered by the doctor; quality of life of patients. Results. The follow-up of children within a month revealed positive dynamics of clinical symptoms (decrease of SCORAD index from 29.2 to 3.5; itching regression from 6.4 to 0.3) and significant improvement of quality of life of patients (from 19.1 to 4.2). Four children dropped out of the study because they need additional drugs for treatment (topical corticosteroids). Three patients developed side effects (episodic nausea, irritability), but they did not require discontinuation of the drug. Conclusions. Antihistamine Fenokit makes it possible to control the manifestations of atopic dermatitis in infants effectively.
діти раннього віку; атопічний дерматит; лікування; Фенокіт
дети раннего возраста; атопический дерматит; лечение; Фенокит
infants; atopic dermatitis; treatment; Fenokit
Вступ
Щорічно близько 35 % населення Землі звертаються по медичну допомогу з клінічними симптомами алергії. Першим дзвіночком алергічної патології в дітей, як правило, є харчова алергія, яка переважно проявляється атопічним дерматитом. Поширеність атопічного дерматиту в різних країнах світу, згідно з даними International Study of Asthma and Allergies in Childhood (ІSАAC), становить: в Австрії — 9,7–19,9 %, Латвії — 5,4–6,5 %, Польщі — 13,2–15,5 %, Фінляндії — 15–19 %, Швеції — 46,9–48,8 %, у Росії — 5,9–40 % [1]. Водночас, згідно з даними офіційної статистики, частота даної патології в Україні коливається в межах 3–10 на 1000 дітей [2, 3]. Таку ситуацію можна пояснити наявністю термінологічних відмінностей у трактуванні атопічного дерматиту в дітей, різними методичними підходами до проведення статистичних досліджень, клінічним і віковим поліморфізмом захворювання [4]. Значна поширеність даної патології, неухильне зростання її частоти в усьому світі, горезвісний «алергічний марш», який, стартуючи в ранньому дитинстві, нерідко супроводжує хворого протягом усього життя, зумовлюють надзвичайну актуальність даної проблеми.
Протягом останніх років активно обговорюються дискусійні питання щодо термінології, клінічних особливостей і лікування атопічного дерматиту. Зокрема, неоднозначно трактується застосування різних груп антигістамінних препаратів у терапії захворювання. Існують дослідження, які доводять, що сьогодні немає переконливих доказів високого рівня, які підтверджують або спростовують ефективність і безпеку пероральних антигістамінних препаратів (антагоністів Н1-рецепторів) у лікуванні атопічного дерматиту [5]. Водночас в інших публікаціях відзначається, що ці препарати традиційно застосовують як монотерапію для лікування свербежу при атопічному дерматиті, що має великий вплив на якість життя хворого. Крім антигістамінного та протизапального ефекту, антигістамінні препарати виявляють заспокійливу дію, що для лікування атопічного дерматиту є надзвичайно актуальним [6, 7]. У цьому контексті на особливу увагу заслуговують антигістамінні препарати першої генерації, які, маючи седативний і антихолінергічний ефекти, здатні усунути свербіж шкіри, а отже, і порушення сну, які супроводжують ураження шкіри у хворих на атопічний дерматит. Тривалий і безпечний клінічний досвід застосування препаратів цієї групи робить їх привабливими для застосування в дітей раннього віку.
Викладена вище ситуація диктує потребу кропіткої роботи щодо підбору антигістамінних препаратів для лікування дітей, хворих на атопічний дерматит. У цьому контексті нас зацікавив препарат Фенокіт (СУІП ТОВ «Сперко Україна») (диметиндену малеат). Чому саме цей препарат? Фенокіт (диметиндену малеат) — антигістамінний препарат І покоління, конкурентний інгібітор Н1-гістамінових рецепторів, який завдяки високій селективності й афінності щодо рецепторів має виражений антигістамінний ефект [7, 8]. Водночас препарат проявляє потужний стабілізаційний вплив на мембрани тканинних базофілів, що сприяє опосередкованому протизапальному ефекту [7]. Виражені холінолітичні ефекти (тахікардія, нудота, збудження) при застосуванні препарату в терапевтичних дозах практично не розвиваються [8].
Диметиндену малеат, окрім гістамінових рецепторів, блокує ефекти інших медіаторів алергічного запалення (кінінів, серотоніну), що також дозволяє зменшити прояви алергічного запалення й свербежу. Будучи блокатором H1-гістамінових рецепторів I покоління, диметиндену малеат є високоліпофільним препаратом, що дозволяє йому легко проникати через гематоенцефалічний бар’єр, зв’язуватися з H1-гістаміновими рецепторами головного мозку і виявляти седативний ефект [8].
Вибір диметиндену малеату ґрунтується на його основних фармакологічних характеристиках. Тривалий досвід його перебування на фармацевтичному ринку (понад 70 років) робить цей препарат особливо привабливим для дослідження [8, 9].
Мета: оцінити ефективність перорального антигістамінного препарату першого покоління Фенокіт у лікуванні атопічного дерматиту в дітей раннього віку.
Матеріали та методи
Ми провели відкрите обсерваційне постреєстраційне клінічне дослідження з оцінки ефективності та переносимості препарату Фенокіт при лікуванні атопічного дерматиту в дітей раннього віку.
Критеріями включення в дослідження були: вік дитини 1–18 міс.; уперше діагностований атопічний дерматит (перебіг легкої або середньої тяжкості); грудне або змішане вигодовування; згода батьків на участь дитини в дослідженні.
Критерії виключення: супутні соматичні та неврологічні захворювання, тяжка форма атопічного дерматиту.
Методи обстеження:
— загальноклінічний аналіз крові та сечі;
— УЗД органів черевної порожнини;
— консультація дитячого невролога;
— оцінка ступеня тяжкості атопічного дерматиту за індексом SCORAD;
— опитувальник для матерів із метою оцінки вираженості свербежу;
— опитування батьків щодо якості життя дитини з атопічним дерматитом (Infant’s Dermatitis Quality of Life Questionnaire);
— реєстрація лікарем частоти небажаних явищ та побічних ефектів.
Досліджувану групу склали 50 пацієнтів, які як антигістамінну терапію отримували препарат Фенокіт у добовій дозі 2 краплі/кг, розділеній на три прийоми. Тривалість застосування препарату становила від 14 до 20 днів. Для догляду за шкірою використовували емолієнти.
Спостереження за дітьми проводили в умовах Львівського міського дитячого алергологічного центру Комунального некомерційного підприємства «Міська дитяча клінічна лікарня м. Львова». Передбачалося п’ять візитів у клініку — на старті лікування та щотижня в динаміці впродовж місяця.
Моніторинг перебігу атопічного дерматиту здійснювали на підставі оцінки ступеня тяжкості захворювання за індексом SCORAD (Scoring of Atopic Dermatitis), вираженості свербежу, реєстрації лікарем частоти небажаних явищ та побічних ефектів, якості життя пацієнтів.
При проведенні оцінки ступеня тяжкості атопічного дерматиту за шкалою SCORAD заповнювали спеціальний бланк. Оцінку клінічних симптомів проводили за допомогою шкали SCORAD на підставі поширеності висипу (%) (А) та інтенсивності симптомів (бали) (В).
Оцінку поширеності уражень на поверхні шкіри визначали в досліджуваних групах за правилом «дев’ятки» (табл. 1).
Визначення та інтенсивність морфологічних елементів оцінювали за чотирибальною шкалою (від 0 до 3):
— еритема (гіперемія);
— набряк/папула;
— мокнуття/кірки;
— екскоріації;
— ліхеніфікації;
— сухість.
SCORAD = A/5 + 7 х B/2,
де А — площа ураження шкіри у відсотках; B — сума балів оцінки інтенсивності морфологічних елементів дерматиту.
Найтяжчим симптомом, який має великий вплив на якість життя дітей, хворих на атопічний дерматит, є свербіж шкіри [2, 3]. Боротьба зі свербежем, який може негативно вплинути на сон дитини, — важлива складова терапії захворювання. Якщо дитина переживає тяжку безсонну ніч, то виснажуються і батьки, й інші члени сім’ї. Ми оцінювали свербіж за 10-бальною шкалою зі слів батьків (0 — відсутній, 10 — максимально виражений).
Опитування батьків щодо якості життя дитини з атопічним дерматитом (Infant’s Dermatitis Quality of Life Questionnaire) проводили за допомогою стандартизованої анкети, призначеної для дітей від 0 до 4 років. Анкета включала 10 запитань, кожне з яких оцінювали за чотирибальною шкалою — від 0 до 3. Запитання містили інформацію про сон, настрій, активність дитини, а також переживання, пов’язані зі споживанням їжі та отриманим лікуванням. Мінімальна кількість балів становила 0, а максимальна — 30. Таким чином, чим нижча сумарна бальна оцінка, тим краща якість життя дитини.
Результати та обговорення
У процесі дослідження із загальної групи 50 дітей вибуло четверо, оскільки виникла потреба приєднання до схеми лікування додаткових препаратів (топічних кортикостероїдів).
На рис. 1 показана динаміка зниження індексу SCORAD у пацієнтів упродовж лікування.
Інтенсивність свербежу становила 6,4 бала на початку лікування й суттєво зменшилася протягом спостереження (до 0,3). Динаміка інтенсивності свербежу відображена на рис. 2.
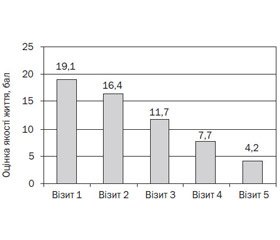
Сьогодні, оцінюючи ефективність будь-яких способів лікування, піддають аналізу не лише об’єктивні показники, але й суб’єктивну оцінку впливу хвороби на життя дитини. Суб’єктивний показник задоволення власних потреб у житті прийнято визначати як якість життя. Якість життя із загального поняття перетворилася на предмет наукових досліджень; її почали враховувати практичні лікарі, оскільки вона визначає ступінь комфортності пацієнта. Середній загальний бал опитування батьків щодо якості життя дитини з атопічним дерматитом оцінювався батьками на старті дослідження та протягом лікування дитини. Динаміка оцінки якості життя наведена на рис. 3.
Як бачимо, на початку лікування середній загальний бал оцінки якості життя становив 19,1. Повторна оцінка проведена через 4 тижні й показала суттєве покращання показників якості життя (до 4,2 бала). Безпечність і переносимість препаратів ми оцінювали за наявністю чи відсутністю побічних ефектів.
Під час застосування препарату у трьох пацієнтів були зафіксовані побічні ефекти, серед яких у 2 дітей спостерігалася епізодична нудота, в 1 — підвищена дратівливість. Зареєстровані випадки побічної дії не потребували відміни препарату.
Вагомим недоліком багатьох представників блокаторів H1-гістамінових рецепторів I покоління є феномен тахіфілаксії, який полягає в суттєвому зниженні лікувального ефекту при повторному застосуванні препарату, що зумовлює потребу нетривалого їх застосування (впродовж 7–10 днів) із наступною заміною на інший препарат [10].
Препарат Фенокіт показав високу клінічну ефективність при застосуванні протягом 14–20 днів, що робить можливим його тривале застосування.
Висновки
У процесі проведеного дослідження отримані переконливі результати ефективності застосування препарату Фенокіт у лікуванні дітей, хворих на атопічний дерматит. На підставі аналізу запропонованих у дослідженні об’єктивних і суб’єктивних критеріїв можна стверджувати, що даний препарат виявився ефективним у 87 % пацієнтів і не викликав значних побічних ефектів.
Конфлікт інтересів. Не заявлений.
1. [Електронний ресурс]: http://isaac.auckland.ac.nz/index.html (дата оновлення 05.04.2017).
2. Беш Л.В., Беш О.М. Атопічний дерматит у дітей: практичний погляд на проблему. Современная педиатрия. 2007. № 3.
С. 62-66.
3. Ласиця О.Л., Ласиця Т.С., Недельська С.М. Алергологія дитячого віку. К.: Книга плюс, 2004. 367 с.
4. Diagnostics and treatment of atopic dermatitis in children and adults Consensus EAACI/AAAAI/PRACTALL. J. Allergy Clin. Immunology. 2006. № 61. P. 969-987.
5. Khamaganova I., Potekaev N., Vorontsova I. Antihistamines in Atopic Dermatitis Therapy. J. Allergy. Disord. Ther. 2015. 2. 003. doi: 10.24966/ADT-749X/100003.
6. Yamanaka K., Motomura E., Noro Y., Umeda K., Morikawa T. et al. Olopatadine, a non-sedating H1 antihistamine, decreases the nocturnal scratching without affecting sleep quality in atopic dermatitis. Exp. Dermatol. 2015. 24. 227-229. doi: 10.1111/exd.12630.
7. Chrostowska-Plak D., Salomon J., Reich A., Szepietowski J.C. Clinical aspects of itch in adult atopic dermatitis patients. Acta Derm. Venereol. 2009. 89. 379-383. doi: 10.2340/00015555-2563.
8. Добмейер Т. Актуальность и опыт более чем 40-летнего применения диметиндена малеата. Врач. 2012. № 4. С. 51-54.
9. Абатуров О.Є., Кривуша О.Л., Агафонова О.А., Токарєва Н.М., Бабич В.Л. Эффективность антигистаминных препаратов I поколения при лечении аллергических заболеваний у детей. Здоровье ребенка. 2018. Т. 13. № 4. С. 394-400. doi: 10.22141/2224-0551.13.4.2018.137026.
10. Полосьянц О.Б. Обзор антигистаминных средств первого и второго поколений, рациональный подход к использованию в клинической практике. Лечащий врач. 2011. 09-02. 14. 12.

/30-3.jpg)
/30-1.jpg)
/30-2.jpg)