Журнал «Травма» Том 20, №5, 2019
Вернуться к номеру
Діагностичні методи і класифікації асептичного некрозу головки стегнової кістки
Авторы: Зазірний І.М. (1, 2), Климовицький В.Г. (2), Семенів І.П. (1), Михальченко О.М. (1), Рижков Б.С. (1)
1 - Клінічна лікарня «Феофанія» Державного управління справами, м. Київ, Україна
2 - Науково-дослідний інститут травматології і ортопедії при Донецькому національному медичному університеті, м. Лиман, Україна
Рубрики: Травматология и ортопедия
Разделы: Справочник специалиста
Версия для печати
Асептичний некроз головки стегнової кітки (АНГСК) — часте захворювання кульшового суглоба. АНГСК є не специфічним процесом, а, швидше, фіналом низки розладів, які призводять до зменшення кровотоку в головці стегнової кістки, що спричинює некроз клітин. У більшості випадків проводиться діагностика на пізніх стадіях розладу, коли хірургічне лікування, що може зберегти головку стегнової кістки й запобігти деструкції кульшового суглоба, уже не показане. Це, як правило, впливає на пацієнтів середнього віку, які більш активні. Тому багато хірургів намагаються відкласти їм виконання тотального ендопротезування кульшового суглоба. Без загальновизнаних системи класифікації та методу збору даних аналіз та порівняння пацієнтів є проблематичними та призводять до труднощів з оцінкою прогресування та визначенням стадії захворювання. Описані та використовуються декілька систем класифікації АНГСК. Нині до найбільш часто використовуваних класифікацій належать системи Ficat, Steinberg, класифікації Асоціації дослідження кровоциркуляції кістки (ARCO) та Японського дослідницького комітету (JIC). Кілька інших систем класифікації, такі як Kerboul et al., використовуються рідше. Кожна класифікація оцінює дещо інший критерій АНГСК. У той час як система Ficat використовує звичайні рентгенограми для визначення стадії та прогресування захворювання, Steinberg комбінував рентгенограми та магнітно-резонансну томографію (МРТ) для оцінки розмірів ураження. Система ARCO покращила класифікацію Ficat, включивши рентгенограми, комп’ютерну томографію, МРТ та сцинтиграфію для визначення розміру та розташування некротичної ділянки. Класифікація JIC, прийнята міністерством охорони здоров’я, праці та добробуту Японії, використовує Т1-зважений режим МРТ для класифікації остеонекрозу на основі локалізації некротичного ураження. Системи класифікації надають ортопеду можливість диференціювати це клінічно складне захворювання відповідно до тяжкості, прогнозу та показань для різних варіантів лікування. Успішність лікування АНГСК безпосередньо пов’язана зі стадією ураження. Чим раніше буде встановлений діагноз, тим більший шанс вплинути на механізми розвитку даної патології. Клінічні симптоми зазвичай передують рентгенологічним змінам, тому підозра щодо розвитку АНГСК і призначення відповідних діагностичних методик є важливим моментом у своєчасному встановленні правильного діагнозу. У цьому огляді ми хотіли показати найбільш часто використовувані системи класифікації АНГСК та важливі фактори, що слід врахувати в кожній.
Асептический некроз головки бедренной кости (АНГБК) — частое заболевание тазобедренного сустава. АНГБК является не специфическим процессом, а, скорее, финалом ряда расстройств, которые приводят к уменьшению кровотока в головке бедренной кости, что приводит к некрозу клеток. В большинстве случаев проводится диагностика на поздних стадиях расстройства, когда хирургическое лечение, которое может сохранить головку бедренной кости и предупредить деструкцию тазобедренного сустава, уже не показано. Это, как правило, влияет на пациентов среднего возраста, которые более активны. Поэтому много хирургов пробуют отложить им выполнение тотального эндопротезирования тазобедренного сустава. Без общепринятых системы классификации и метода сбора данных анализ и сравнение пациентов проблематичны и приводят к трудностям с оценкой прогрессирования и определением стадии заболевания. Описаны и используются несколько систем классификации АНГБК. В данный момент к наиболее часто используемым классификациям относятся системы Ficat, Steinberg, классификации Ассоциации исследования кровоциркуляции кости (ARCO) и Японского исследовательского комитета (JIC). Несколько других систем классификации, такие как Kerboul et al., используются реже. Каждая классификация оценивает несколько иной критерий АНГБК. В то время как система Ficat использует обычные рентгенограммы для определения стадии и прогрессирования заболевания, Steinberg комбинировал рентгенограммы и магнитно-резонансную томографию (МРТ) для оценки размеров поражения. Система ARCO улучшила классификацию Ficat, включив рентгенограммы, компьютерную томографию, МРТ и сцинтиграфию для определения размера и положення некротического участка. Классификация JIC, принятая министерством здравоохранения, труда и благосостояния Японии, использует Т1-взвешенный режим МРТ для классификации остеонекроза на основе локализации некротического поражения. Системы классификации предоставляют ортопеду возможность дифференцировать это клинически сложное заболевание в соответствии с тяжестью, прогнозом и показаниями для разных вариантов лечения. Успешность лечения АНГБК непосредственно связана со стадией поражения. Чем раньше будет установлен диагноз, тем більше шансов повлиять на механизмы развития данной патологии. Клинические симптомы обычно предшествуют рентгенологическим изменениям, поэтому подозрение относительно развития АНГБК и назначение соответствующих диагностических методик является важным моментом в своевременной постановке правильного диагноза. В этом обзоре мы хотели показать наиболее часто используемые системы классификации АНГБК и важные факторы, которые необходимо учитывать в каждой.
Aseptic femoral head necrosis (AFHN) is a common hip joint disease. AFHN is not a specific process, but rather the end of a series of disorders that lead to a decrease in blood flow in the femoral head, which leads to cell necrosis. In most cases, diagnosis is made in the later stages of the disorder, when surgical treatment that can preserve the femoral head and prevent destruction of the hip joint is no longer shown. This usually affects middle-aged patients who are more active. Therefore, many surgeons are trying to delay their performance of total hip replacement. Patient analysis and comparison are problematic and have difficulty assessing progression and determining the stage of the disease without a commonly recognized classification system and data collection method. Several ANFH classification systems are described and used. Currently, the most commonly used classifications include Ficat, Steinberg, Association Research Circulation Osseous (ARCO), and the Japan Investigation Committee (JIC). Several other classification systems, such as Kerboul et al., Are less commonly used. Each classification evaluates a slightly different criterion in the assessment of the ANSP. While Ficat uses conventional radiographs to determine the stage and progression of the disease, Steinberg combined radiographs and magnetic resonance imaging (MRI) to estimate the extent of the lesion. The ARCO system improved the Ficat classification by including radiographs, computed tomography, MRI and scintigraphy to determine the size and location of the necrotic area [16]. The JIC classification, adopted by the Ministry of Health, Labor and Welfare of Japan, uses the T1 weighted MRI regimen to classify osteonecrosis based on the localization of necrotic lesions. Classification systems provide the orthopedist with the opportunity to differentiate this clinically complex disease according to severity, prognosis, and indications for different treatment options. The success of the ANFH treatment is directly related to the stage of the lesion. As soon the diagnosis is made, the greater the chance to influence the mechanisms of development of this pathology. Clinical symptoms usually precede radiological changes, so suspicion of the development of ANFH and the appointment of appropriate diagnostic techniques is an important point in the timely diagnosis. We wanted to show the most commonly used ANFH classification systems and the important factors to consider in each in this review.
асептичний некроз; головка стегнової кістки; діагностика; класифікації; огляд
асептический некроз; головка бедренной кости; диагностика; классификации; обзор
aseptic necrosis; femoral head; diagnosis; classifications; review
Вступ
Асептичний некроз головки стегнової кітки (АНГСК) — часте захворювання кульшового суглоба [23]. АНГСК не є специфічним процесом, а, швидше, фіналом низки розладів, які призводять до зменшення кровотоку в головці стегнової кістки, що спричинює некроз клітин. АНГСК — це поступово зростаюче ураження, що зазвичай призводить до руйнування кульшового суглоба в пацієнтів віком від 20 до 50 років (середній вік — 38 років) [6]. У більшості випадків проводиться діагностика на пізніх стадіях розладу, коли хірургічне лікування, що може зберегти головку стегнової кістки й запобігти деструкції кульшового суглоба, уже не показане [1]. Це, як правило, впливає на пацієнтів середнього віку, які більш активні. Тому багато хірургів намагаються відкласти їм виконання тотального ендопротезування кульшового суглоба [28–31].
У хірургічному арсеналі є кілька варіантів оперативних втручань, що зберігають головку, але різні показання та рівень успішності призвели до дискусій щодо того, коли використовувати ті чи інші процедури [32–35]. Частково це пояснюється відсутністю узагальненої системи оцінки АНГСК, а також відсутністю стандартизованого методу збору даних для диференціації хворих [35–39].
Без загальновизнаних системи класифікації та методу збору даних аналіз та порівняння пацієнтів є проблематичними та призводять до труднощів з оцінкою прогресування та визначенням стадії захворювання.
Описані та використовуються декілька систем класифікації АНГСК [37]. Нині до найбільш часто використовуваних класифікацій належать системи Ficat [26], Steinberg [39], класифікації Асоціації дослідження кровоциркуляції кістки (ARCO) [16] та Японського дослідницького комітету (JIC) [40].
Кілька інших систем класифікації, такі як Kerboul et al. [7], використовуються рідше. Кожна класифікація оцінює дещо інший критерій АНГСК. У той час як система Ficat використовує звичайні рентгенограми для визначення стадії та прогресування захворювання [26], Steinberg комбінував рентгенограми та магнітно-резонансну томографію (МРТ) для оцінки розмірів ураження [39]. Система ARCO покращила класифікацію Ficat, включивши рентгенограми, комп’ютерну томографію (КТ), МРТ та сцинтиграфію для визначення розміру та розташування некротичної ділянки [6]. Класифікація JIC, прийнята міністерством охорони здоров’я, праці та добробуту Японії (JMHLW), використовує Т1-зважений режим МРТ для класифікації остеонекрозу на основі локалізації некротичного ураження [40].
Системи класифікації надають ортопеду можливість диференціювати це клінічно складне захворювання відповідно до тяжкості, прогнозу та показань для різних варіантів лікування [41].
АНГСК характеризується порушенням структури кісткової тканини, що пов’язане з порушенням кровопостачання хворої ділянки кістки [16]. Структурні властивості кістки змінюються в результаті репарації та розсмоктування [22], тому здатність головки стегнової кістки нести навантаження знижується порівняно із здоровим стегном [18, 25]. Перелом може виникнути в некротичній частині кістки, зрештою кістка руйнується [25]. Механічні властивості зазнають змін при остеонекрозі головки стегнової кістки [18]. Ці механічні зміни були предметом численних теоретичних досліджень: до них відносяться двовимірні лінійні, тривимірні лінійні та нелінійні методи скінченних елементів [17, 18, 20, 24, 25].
Результати аналізу методів скінченних елементів показують, що картина напруження в головці стегнової кістки при остеонекрозі істотно відрізняється від такої у здорової головки, з особливою чутливістю до розміру та форми ураження та до його розташування на несучій площі [21, 25], і що зниження міцності некротичного кісткового сегмента може сприяти переломам некротичної кістки [17, 19, 20, 25].
Успішність лікування АНГСК безпосередньо пов’язана зі стадією ураження. Чим раніше буде встановлений діагноз, тим більший шанс вплинути на механізми розвитку даної патології. Клінічні симптоми зазвичай передують рентгенологічним змінам, тому підозра щодо розвитку АНГСК і призначення відповідних діагностичних методик є важливим моментом у своєчасному встановленні правильного діагнозу.
У цьому огляді ми хотіли показати найбільш часто використовувані системи класифікації АНГСК та важливі фактори, які слід врахувати в кожній.
Клінічні прояви
Клінічно асептичний некроз головки стегнової кістки може проявлятися як самостійне захворювання або поєднуватися з іншими патологіями. Головною скаргою пацієнтів із даним захворюванням є біль, що зазвичай локалізується в ділянці паху або іноді іпсилатерально в ділянці сідниці та коліна. Біль характеризується як глибокий, періодичний, пульсуючий, що може виникати в будь-який момент. Під час клінічного огляду біль виникає при активних і пасивних рухах, особливо при пасивній внутрішній ротації стегна.
При першому рентгенографічному дослідженні знімки можуть бути без патологічних змін. Тому лікарі завжди повинні підозрювати АНГСК у пацієнтів, які страждають від болю у ділянці кульшового суглоба та мають будь-які фактори ризику, характерні для даного захворювання. Також завжди потрібно проводити обстеження обох кульшових суглобів, навіть у випадках, коли пацієнти скаржаться на біль в одному суглобі, тому що випадки двостороннього ураження становлять від 40 до 80 % [1, 6].
Рентгенографія
Прості рентгенографічні знімки повинні бути наступним кроком після збору анамнезу та клінічного обстеження. Потрібно завжди виконувати дослідження у фронтальній та аксіальній проєкціях. На підставі клінічних досліджень та інструментальних методів діагностики були запропоновані різні системи класифікації даного захворювання.
Перша — система оцінки стадійності АНГСК, запропонована Arlet і Ficat (рис. 1) [2], що базується на рентгенологічних змінах головки стегнової кістки. Arlet і Ficat описали чотири стадії прогресування захворювання. У I стадії (передрентгенологічна) наявні тільки клінічні симптоми. У ІІ стадії вже наявні рентгенологічні зміни, виникає реконструкція кісткової тканини без зміни форми головки стегнової кістки, також наявні субхондральний склероз та кісти. У ІІ стадії з’являється так званий «півмісяць», що є рентгенологічною ознакою переходу з ІІ до ІІІ стадії, також наявні секвестри та колапс остеонекротичного сегмента. Під час IV стадії виникає звуження суглобової щілини, з’являються остеофіти та виникає деформація головки стегнової кістки (рис. 1).
Інші класифікації є варіаціями рентгенологічної класифікації Arlet і Ficat. Класифікація Marcus і Enne–king [3] базується на клінічних симптомах і рентгенологічних змінах (табл. 1).
Класифікація Steinberg et al. [1, 4] (табл. 2, рис. 2) є більш високоспеціалізованою і не лише поєднує в собі дані рентгенографії та клінічних досліджень, а й також включає дані МТР і остеосцинтиграфії.
The Japanese Investigation Committee запропонував класифікацію, що ґрунтується на розмірі та розташуванні некрозу в головці стегнової кістки відносно купола вертлюгової западини [5] (рис. 3). Для оцінки використовуються рентгенограми у прямій проєкції.
Тип 1 характеризується наявністю некротичної ділянки, що знаходиться у зоні, яка має контакт із найбільш навантаженою частиною вертлюгової западини (тип 1А менший, ніж середня третина навантаженої частини; тип 1В більше однієї третини від навантаженої частини; тип 1С більше за дві третіх). Тип 2 характеризується сплющенням найбільш навантаженої частини без рентгенологічних ознак дегенерації. Тип 3 характеризується наявністю кістозного ураження: в типі 3А ураження не пов’язане з підкірковою зоною, тип 3В характеризується наявністю змін у найбільш навантажуваній зоні.
The Association Internationale de Recherche sur la Circulation Osseuse запропонувала нову класифікацію [6] (табл. 3), що поєднує в собі рентгенологічні характеристики, МРТ, остеосцинтиграфію і гістологічні дослідження та є найбільш повною та досконалою. Вона поєднує в собі рентгенологічну класифікацію Arlet і Ficat, систему кількісної оцінки Steinberg et al. [1, 4] та класифікацію розмірів і розташування некрозу The Japanese Investigation Committee [5].
Kerboul et al. [7] у свой роботі описують спосіб визначання ступеня пошкодження за допомогою рентгенографії. Для обчислення складного кута вони використовують рентгенограму як у прямій, так і в боковій проєкції, яку потім використовують для подальшого прогнозу лікування. Наприклад, кут більше 200 градусів є прогностично несприятливим.
Магнітно-резонансна томографія
На сьогодні магнітно-резонансна томографія є найбільш точною методикою візуалізації, що використовується для діагностики остеонекрозу головки стегнової кістки. Вважається, що її чутливість становить від 88 до 100 %, що вище, ніж у звичайної рентгенографії, комп’ютерної томографії або сканування кісток при виявленні ранніх захворювань (на 10–20 % вище, ніж у сцинтиграфії) [8–10]. Специфічність МРТ при диференціальній діагностиці остеонекрозу з іншими захворюваннями головки кульшового суглоба також дуже висока.
Коли остеоцити кісткового мозку, кровотворні клітини та жирові клітини кісткового мозку піддаються ішемії, смерть клітин виникає з різним інтервалом [10]. Кровотворні клітини вмирають протягом 6–12 годин, остеоцити — протягом 12–48 годин, а жирові клітини кісткового мозку — через 5 днів.
Нормальну високу інтенсивність сигналу видно на Т1-зважених зображеннях, та інтенсивність проміжного сигналу, виявленого на Т2-зважених МРТ-знімках головки стегнової кістки при остеонекрозі, відображає смерть і заміну жирових клітин кісткового мозку. Хоча смерть остеоцитів (зображених у вигляді порожніх лакун) не є загальноприйнятою, периферична смуга низької інтенсивності сигналу, що присутня як на T1-, так і на T2-зважених зображеннях, зазвичай є демаркаційною ділянкою остеонекрозу з оточуючих нормальних тканин кісткового мозку [10, 11]. На T2-зважених зображеннях ця лінія, що називається знаком подвійної лінії, присутня в 80 % випадків. Ця ознака являє собою концентричні низько- і високопотужні інтенсивні сигнали, що оточують ділянку некрозу.
Результати МРТ-досліджень моделей остеонекрозу на тваринах показали, що смерть клітин кісткового мозку визначається змінами інтенсивності сигналу, що спостерігається на зображеннях з Т1- і Т2-зважених знімків. Проте це може статися лише через 5 днів після того, як не буде відбуватися живлення [12]. Отже, до цього моменту змін на МРТ-зображенні не буде. Щоб збільшити ранню чутливість MРТ-зображень, деякі дослідники запропонували використання гадолінію, однак немає робіт, які наводять переконливі докази, що підтверджують ефективність цієї методики.
Sakamoto та ін. [11] повідомили, що зв’язок розташування ділянки остеонекрозу та більш навантаженої частини головки стегнової кістки і ступеня некрозу може бути предиктором колапсу (рис. 4). У їх системі площа ваги-підшипника ділиться на третину. Ураження, що поширюються менше ніж на третину медіальної зони, відносять до класу А; ті, що поширюються більше ніж на третину, але менше двох третин, — до класу В; ті, що поширюються на дві третини або більше, — до класу С; ті, що виходять за межі вертикального ребра, — до класу D.
Shimizu та ін. [13] додали до цієї класифікації третій критерій визначення прогнозу — інтенсивність зображення некротичної ділянки.
З метою виявлення предиктора майбутнього колапсу Koo та Kim [14] використовували МРТ-зображення, щоб кількісно визначити ступінь остеонекрозу головки стегнової кістки в 37 хворих з ранньою стадією остеонекрозу. Розміри некротичної ділянки на навантажуваній частині головки стегнової кістки вимірювалися у фронтальній та сагітальній площинах. Потім автори розрахували індекс некрозу за формулою:
(A/180) x (B/180) x 100,
де A являє собою дугу (в градусах) некротичної частини на фронтальному зображенні, а B — дугу на сагітальному зображенні. Отримані значення використовувались для визначення ступеня некрозу як малого (< 33) (клас А), середнього (34–66) (клас В) або високого (67–100) (клас C). У досліджуваній групі частота колапсу для класу А становила 13 %, для класу В — 95 %, а для класу С — 100 %.
Sugano та ін. [15] описали іншу систему встановлення діагнозу на підставі фронтальних T1-зважених МРТ-зображень (табл. 4). Ця система може бути корисною для визначення ризику розпаду головки стегна, коли ураження не видно на звичайних рентгенограмах.
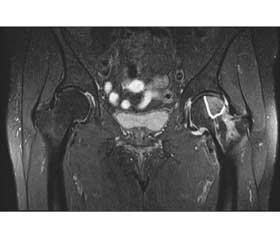
Проведені рентгенографія та МРТ лівого кульшового суглоба в 60-річної хворої, у якої за 3 місяці до звернення з’явився біль у лівому кульшовому суглобі (рис. 5, 6). Незважаючи на те, що пацієнтка мала клінічні симптоми, які свідчать про остеонекроз головки лівої стегнової кістки, рентгенограми не показали патологічних змін. МРТ-зображення яскраво демонструє остеонекроз головок стегнових кісток (Sugano stage IC).
Сканування кісток
Через низьку вартість деякі хірурги рекомендують сканування кістки з використанням метилендифосфонату технецію-99m як альтернативу МРТ. Поширеним показанням до використання даної методики є відсутність факторів ризику та наявність симптомів з нормальними рентгенограмами. Також хірургам, які лікують пацієнтів з однобічним остеонекрозом, у яких наявні симптоми даної патології, було запропоновано виконувати сканування кісток, а якщо дане дослідження буде негативним, жодне лікування, крім спостереження, не є необхідним.
У хворих на асептичний некроз головки стегнової кістки зона підвищеної активності, що представлена збільшенням перебудови кісткової тканини, буде візуалізуватися між зоною некрозу та зоною реактивної перебудови кістки. Оскільки ізотоп накопичується на цьому місці, ділянка відображається як «гаряча» зона, або зона високої щільності, оточена більш «холодною» зоною, або зоною меншої щільності. Одразу після виникнення некрозу сканування кісткок може не виявляти накопичення ізотопів, оскільки як тільки почалася реконструкція, «холодне» місце стає «гарячим». Інтервал між цими двома подіями становить від 10 до 14 днів, протягом даного періоду (період перехресту) сканування кісток може бути хибнонегативним [10].
Інші діагностичні методи
Альтернативні методи діагностики були впроваджені для ранньої діагностики асептичного остеонекрозу, що не виявляється при використанні візуалізаційних методів діагностики. Гістологічні дослідження, що виявляють порожні лакуни в кісткових трабекулах, можуть свідчити про некроз кістки. Також дана процедура використовується після декомпресії кістки. Біопсія також може використовуватися як метод передопераційної діагнос-
тики [6].
Вимірювання інтрамедулярного тиску і венографія є специфічними тестами для оцінки кісткової функції, але більше не використовуються для діагностики остеонекрозу. КТ може використовуватися для діагностики на ранніх стадіях захворювання (ІІ або ІІІ), однак, оскільки даний метод не входить до протоколу, він використовується нечасто.
Висновки
Хоча знання щодо етіології, патогенезу, діагностики та лікування остеонекрозу продовжують накопичуватися, важливі питання залишаються незрозумілими. Відмінності в результатах дослідження, складність збору даних та низький рівень захворювання перешкоджають дослідникам досягти консенсусу з багатьох питань. Багатоцентрове дослідження необхідне для забезпечення більшої кількості пацієнтів, що дозволить чітко зрозуміти цей стан. Оцінюють відповідне фармакологічне і хірургічне втручання лікування на ранніх стадіях остеонекрозу. Переваги декомпресії ядра при лікуванні остеонекрозу головки стегна продовжують викликати суперечки в ортопедичній спільноті, хоча, на думку деяких авторів, ця процедура дає прийнятне рішення для лікування раннього остеонекрозу.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
1. Steinberg M.E., Hayken G.D., Steinberg D.R. A quantitative system for staging avascular necrosis. J. Bone Joint Surg. Br. 1995. 77. 34-41.
2. Ficat R.P., Arlet J. Ischemia and Necrosis of Bone. Baltimore: Williams & Wilkins, 1980. 29-52.
3. Marcus N.D., Enneking W.F., Massam R.A. The silent hip in idopathic aseptic necrosis: Treatment by bone-grafting. J. Bone Joint Surg. Am. 1973. 55. 1351-1366.
4. Garino J.P., Steinberg M.E. Total hip arthroplasty in patients with avascular necrosis of the femoral head: A 2- to 10-year follow-up. Clin. Orthop. 1997. 334. 108-115.
5. Ohzono K., Saito M., Sugano N., Takaoka K., Ono K. The fate of nontraumatic avascular necrosis of the femoral head: A radiologic classification. Clin. Orthop. Relat. Res. 1992 Apr. 277. 73-8.
6. Mont M.A., Hungerford D.S. Non-traumatic avascular necrosis of the femoral head. J. Bone Joint Surg. Am. 1995. 77. 459-474.
7. Kerboul M., Thomine J., Postel M., Merle d’Aubigne R. The conservative surgical treatment of idiopathic aseptic necrosis of the femoral head. J. Bone Joint Surg. Br. 1974. 56. 291-296.
8. Nakamura T., Matsumoto T., Nishino M., Tomita K., Kadoya M. Early magnetic resonance imaging and histologic findings in a model of femoral head necrosis. Clin. Orthop. 1997. 334. 68-72.
9. Kokubo T., Takatori Y., Ninomiya S., Nakamura T., Kamogawa M. Magnetic resonance imaging and scintigraphy of avascular necrosis of the femoral head. Prediction of subsequent segmental collapse. Clin. Orthop. 1992. 277. 54-60.
10. Conway W.F., Totty W.G., McEnery K.W. CT and MR imaging of the hip. Radiology. 1996. 198. 297-307.
11. Sakamoto M., Shimizu K., Iida S., Akita T., Moriya H., Nawata T. Osteonecrosis of the femoral head: A prospective study with MRI. J. Bone Joint Surg. Br. 1997. 79. 213-219.
12. Brody A.S., Strong M., Babikian G., Sweet D.E., Sei-del F.G., Kuhn J.P. Avascular necrosis: Early MR imaging and histologic findings in a canine model. AJR Am. J. Roentgenol. 1991. 157. 341-345.
13. Shimizu K., Moriya H., Akita T., Sakamoto M., Suguro T. Prediction of collapse with magnetic resonance imaging of avascular necrosis of the femoral head. J. Bone Joint Surg. Am. 1994. 76. 215-223.
14. Koo K.H., Kim R. Quantifying the extent of osteonecrosis of the femoral head: A new method using MRI. J. Bone Joint Surg. Br. 1995. 77. 875-880.
15. Sugano N., Takaoka K., Ohzono K., Matsui M., Masuhara K., Ono K. Prognostication of nontraumatic avascular necrosis of the femoral head: Significance of location and size of the necrotic lesion. Clin. Orthop. Relat. Res. 1994 Jun. 303. 155-64.
16. Abu-Shakra M., Buskila D., Shoenfeld Y. Osteonecrosis in patients with SLE. Clin. Rev. Allergy Immunol. 2003. 25. 13-24.
17. Brown T.D., Baker K.J., Brand R.A. Structural consequences of subchondral bone involvement in segmental osteonecrosis of the femoral head. J. Orthop. Res. 1992. 10. 79-87.
18. Brown T.D., Baker K.J., Pedersen D.R. Biomechanics of femoral head aseptic necrosis. Biomed. Eng-App Bas. C. 1993. 5. 9-12.
19. Brown T.D., Hild G.L. Pre-collapse stress redistributions in femoral head osteonecrosis. a three-dimensional finite element analysis. J. Biomech. Eng. 1983. 105. 171-176.
20. Brown T.D., Mutschler T.A., Fergusson A.B. A non-linear finite element analysis of some early collapse processes in femoral head osteonecrosis. J. Biomech. 1982. 15. 707-715.
21. Brown T.D., Way M.E., Fergusson A.B. Stress transmission anomalies in femoral heads altered by aseptic necrosis. J. Biomech. 1980. 13. 687-699.
22. Brown T.D., Way M.E., Fergusson A.B. Mechanical characteristics of bone in femoral capital aseptic necrosis. Clin. Orthop. Relat. Res. 1981. 156. 240-247.
23. Hungerford D.M. Osteonecrosis: avoiding total hip arthroplasty. J. Arthroplasty. 2002. 17(4 suppl. 1). 121-124.
24. Ueo T., Tsutsumi S., Yamamuro T., Okumura H., Shimizu A., Nakamura T. Biomechanical aspects of the deve-lopment of aseptic necrosis of the femoral head. Arch. Orthop. Trauma Surg. 1985. 104. 145-149.
25. Yang J.W., Koo K.H., Lee M.C., Yang P., Noh M.D., Kim S.Y., Kim K.I., Ha Y.C., Joun M.S. Mechanics of femoral head osteonecrosis using three-dimensional finite element me-thod. Arch. Orthop. Trauma Surg. 2002. 122. 88-92.
26. Ficat R.P. Idiopathic bone necrosis of the femoral head. Early diagnosis and treatment. J. Bone Joint Surg. (Br.). 1985. 67. 3-9.
27. Seamon J., Keller T., Saleh J., Cui Q. The pathogenesis of nontraumatic osteonecrosis. Arthritis. 2012. 601763.
28. Mont M.A., Seyler T.M., Plate J.F. et al. Uncemented total hip arthroplasty in young adults with osteonecrosis of the femoral head: a comparative study. J. Bone Joint Surg. Am. 2006. 88(Suppl. 3). 104-109.
29. Mont M.A., Seyler T.M., Marker D.R. et al. Use of metal-on-metal total hip resurfacing for the treatment of osteonecrosis of the femoral head. J. Bone Joint Surg. Am. 2006. 88(Suppl. 3). 90-97.
30. Marker D.R., Seyler T.M., McGrath M.S. et al. Treatment of early stage osteonecrosis of the femoral head. J. Bone Joint Surg. Am. 2008. 90(Suppl. 4). 175-187.
31. Jacobs B. Epidemiology of traumatic and nontraumatic osteonecrosis. Clin. Orthop. Relat. Res. 1978. 130. 51-67.
32. Chughtai M., Piuzzi N.S., Khlopas A. et al. An evidence-based guide to the treatment of osteonecrosis of the femoral head. Bone Joint J. 2017. 99-B. 1267-1279.
33. Mont M.A., Ragland P.S., Etienne G. Core decompression of the femoral head for osteonecrosis using percutaneous multiple small-diameter drilling. Clin. Orthop. Relat. Res. 2004. 429. 131-8.
34. Kim S.-Y., Kim Y.-G., Kim P.-T. et al. Vascularized compared with nonvascularized fibular grafts for large Osteonecrotic lesions of the femoral head. J. Bone Joint Surg. 2005. 87. 2012-2018.
35. Dean M.T., Cabanela M.E. Transtrochanteric anterior rotational osteotomy for avascular necrosis of the femoral head. Long-term results. J. Bone Joint Surg. (Br.) 1993. 75. 597-601.
36. Lee G.-C., Steinberg M.E. Are we evaluating osteonecrosis adequately? Int. Orthop. 2012. 36. 2433-2439.
37. Mont M.A., Marulanda G.A., Jones L.C. et al. Systematic analysis of classification systems for osteonecrosis of the femoral head. J. Bone Joint Surg. Am. 2006. 88(Suppl. 3). 16-26.
38. Zibis A.H., Karantanas A.H., Roidis N.T. et al. The role of MR imaging in staging femoral head osteonecrosis. Eur. J. Radiol. 2007. 63. 3-9.
39. Steinberg M.E., Steinberg D.R. Classification systems for osteonecrosis: an overview. Orthop. Clin. N. Am. 2004. 35. 273-283.
40. Sugano N., Atsumi T., Ohzono K. et al. The 2001 revised criteria for diagnosis, classification, and staging of idiopathic osteonecrosis of the femoral head. J. Orthop. Sci. 2002. 7. 601-605.
41. Plakseychuk A.Y., Shah M., Varitimidis S.E. et al. Classification of osteonecrosis of the femoral head. Reliability, reproducibility, and prognostic value. Clin. Orthop. Relat. Res. 2001. 386. 34-41.

/90-1.jpg)
/90-2.jpg)
/91-1.jpg)
/91-2.jpg)
/92-1.jpg)
/92-2.jpg)
/93-1.jpg)
/93-2.jpg)
/94-1.jpg)