Резюме
Безпечна інфузійна терапія у дітей вимагає глибокого розуміння основних принципів, що ґрунтуються на особливостях водно-електролітного обміну та кислотно-основного стану у дитячому віці. Вміст води й електролітів в організмі дитини підтримується в дуже вузьких межах, тому необхідно розуміти потенційні фізіологічні ефекти порушень балансу води та розчинених в ній речовин, тому що ці зміни завжди супроводжують періопераційний період. Періопераційна інфузійна терапія має прямий вплив на клінічний результат лікування, у зв’язку з чим її призначення повинно відповідати потребам хворого. Ціллю інфузійної терапії у хворих дітей у періопераційному періоді є підтримка ефективного циркулюючого об’єму та недопущення, де тільки можливо, інтерстиціального перевантаження рідиною. Крім знань фізіології і патофізіології водно-електролітного обміну в дитячому віці, для адекватної інфузійної терапії необхідно розуміння фармакології інфузійних препаратів, їх дозування, техніки застосування, порушення яких може негативно позначитися на прогнозі захворювання. Саме тому метою нашого дослідження стало вивчення змін гемодинамічних показників, водно-електролітного, кислотно-лужного обмінів при застосуванні різних інфузійних розчинів в періопераційному періоді. Робота виконана на основі аналізу лікування 55 пацієнтів молодшого віку з ургентною абдомінальною патологією, яких залежно від виду проведення періопераційної інфузійної терапії було розподілено на 3 групи: 1-ша група — діти, у яких як інфузійну терапію в періопераційному періоді використовували гіпотонічні глюкозо-сольові розчини; 2-га група — діти, у яких використовували розчин Рінгера лактат; 3-тя група — діти, у яких використовували збалансований електролітний розчин Рінгера малат. Дослідження показало, що у дітей з ургентною абдомінальною патологією відмічається зневоднення організму та абсолютна гіповолемія, яка погіршується розвитком гіпоосмолярного стану, а для швидкої нормалізації гемодинамічних показників, водно-електролітного обміну, кислотно-основного стану та водних секторів організму оптимальною інфузійною рідиною має бути збалансований сольовий розчин з додаванням аспартату та малату.
Безопасная инфузионная терапия у детей требует глубокого понимания основных принципов, основанных на особенностях водно-электролитного обмена и кислотно-основного состояния в детском возрасте. Содержание воды и электролитов в организме ребенка поддерживается в очень узких пределах, поэтому необходимо понимать потенциальные физиологические эффекты нарушений баланса воды и растворенных в ней веществ, так как эти изменения всегда сопровождают периоперационный период. Периоперационная инфузионная терапия имеет прямое влияние на клинический результат лечения, в связи с чем ее назначение должно соответствовать потребностям больного. Целью инфузионной терапии у больных детей в периоперационном периоде является поддержка эффективного циркулирующего объема и недопущение, где только возможно, интерстициальной перегрузки жидкостью. Кроме знаний физиологии и патофизиологии водно-электролитного обмена в детском возрасте, для адекватной инфузионной терапии необходимо понимание фармакологии инфузионных препаратов, их дозировки, техники применения, нарушение которых может негативно сказаться на прогнозе заболевания. Именно поэтому целью нашего исследования стало изучение изменений гемодинамических показателей, водно-электролитного, кислотно-щелочного обменов при применении различных инфузионных растворов в периоперационном периоде. Работа выполнена на основе анализа лечения 55 пациентов младшего возраста с ургентной абдоминальной патологией, которые в зависимости от вида проведения периоперационной инфузионной терапии были разделены на 3 группы: 1-я группа — дети, у которых в качестве инфузионной терапии в периоперационном периоде использовали гипотонические глюкозо-солевые растворы; 2-я группа — дети, у которых использовали раствор Рингера лактат; 3-я группа — дети, у которых использовали сбалансированный электролитный раствор Рингера малат. Исследование показало, что у детей с острой ургентной абдоминальной патологией отмечается обезвоживание организма и абсолютная гиповолемия, которая ухудшается развитием гипоосмолярного состояния, а для быстрой нормализации гемодинамических показателей, водно-электролитного обмена, кислотно-щелочного состояния и водных секторов организма оптимальной инфузионной средой должен быть сбалансированный солевой раствор с добавлением аспартата и малата.
Safe fluid therapy in children requires deep knowledge of main principles, which are based on water-electrolyte metabolism and acid-base balance in childhood. Water and electrolyte content in children’s body is supported within very narrow limits, that is why it is very important to understand the potential physical effects of imbalances in water and substances dissolved in it because these changes always occur in the perioperative period. Perioperative fluid therapy directly impacts the clinical outcome of treatment, and therefore its appointment should meet the needs of a patient. The goal of fluid therapy in sick children in the perioperative period is to maintain effective circulating volume and to prevent, where possible, interstitial fluid overload. Besides the knowledge of the physiology and pathophysiology of water-electrolyte metabolism in childhood, an adequate fluid therapy requires an understanding of the pharmacology of infusion drugs, their dosage, techniques of use, violations of which may adversely affect the prognosis of the disease. That is why the purpose of our research is to study changes of hemodynamic indicators, water-electrolyte and acid-base metabolism while using various infusion solutions in the perioperative period. This work was done based on the analysis of the treatment of 55 pediatric patients with urgent abdominal pathology, which, depending on the type of perioperative infusion therapy conducted were divided into 3 groups. The 1st group covered the children who received as perioperative infusion therapy with hypotonic glucose-salt solutions, the 2nd group involved the children who had been treated with Ringer’s lactate solution, the 3rd group consisted of the children treated with a balanced electrolyte Ringer’s malate solution. This research showed that children with urgent abdominal pathology had dehydration and absolute hypovolemia, which worsened due to the development of hypoosmotic conditions. The quick normalization of hemodynamic parameters, water-electrolyte metabolism, acid-base balance and water sectors of a body needs an optimal infusion medium — a balanced saline solution with aspartate and malate added.
Вступ
Внутрішньовенне введення інфузійних розчинів залишається найпоширенішим терапевтичним втручанням у дітей із різною патологією [1]. Періопераційна інфузійна терапія має прямий вплив на клінічний результат лікування, у зв’язку з чим її призначення повинно відповідати потребам хворого. Ціллю інфузійної терапії у хворих дітей у періопераційному періоді є підтримка ефективного циркулюючого об’єму та недопущення, де тільки можливо, інтерстиціального перевантаження рідиною [2, 3]. Серед різноманіття завдань інфузійної терапії основними є адекватна гідратація тканин, запобігання електролітному дисбалансу і підтримка нормоглікемії [4]. Для цього застосовуються інфузійні розчини з фізіологічним вмістом електролітів, призначені для заміщення втрати внутрішньосудинної рідини і запобігання гіповолемії, стабілізації гемодинаміки і життєво важливих функцій організму. Безпечна інфузійна терапія у дітей вимагає глибокого розуміння основних принципів, що ґрунтуються на особливостях водно-електролітного обміну та кислотно-основного стану у дитячому віці, щоб уникнути несприятливих наслідків [3, 12]. Вміст води та електролітів в організмі підтримується в дуже вузьких межах, тому необхідно розуміти потенційні фізіологічні ефекти порушень балансу води та розчинених в ній речовин, тому що ці зміни завжди супроводжують періопераційний період у дітей [5].
При застосуванні в інфузійній терапії переважають різні сольові розчини. На сьогодні більшість анестезіологів воліють використовувати 0,9% розчин натрію хлориду для поповнення дефіциту рідини [6]. Останніми роками підхід до періопераційної інфузійної терапії у дітей зазнав змін. Протягом багатьох років у дітей для періопераційної інфузійної терапії використовувався гіпотонічний електролітний розчин з додаванням 5% глюкози, але нерідко його використання призводило до тяжкої гіпонатріємії і гіперглікемії [7, 8].
У своїй статті Holliday та Segar [10] запропонували норму та склад інфузійних рідин для госпіталізованих дітей. Описані принципи досі вважаються фундаментальними у дитячій практиці. Клініцисти покладаються на зазначені формули та концепції, однак використання традиційних гіпотонічних рідин, які запропонували автори, може спричиняти такі ускладнення, як гіперглікемія та гіпонатріємія. Існують серйозні суперечки дослідників щодо вибору гіпотонічної чи ізотонічної рідин у періопераційному періоді у дітей [10, 11].
При виборі інфузії потрібно враховувати час періопераційного голодування та проводити підтримку та/або корекцію водно-електролітного балансу. У European consensus statement for intraoperative fluid therapy in children 2011 було зазначено, що інфузійна рідина, що використовується як базова інфузія у дітей, повинна наближуватися за своєю осмолярністю та концентрацією натрію до фізіологічних значень у плазмі крові та мати у составі аніони, що метаболізуються (ацетат, малат або лактат) [13].
Таким чином, досі не вирішено питання базового інфузійного розчину для використання в періопераційному періоді у дітей. На сьогодні лікарі багатьох спеціальностей, які стикаються з необхідністю проведення інфузійної терапії, при виборі інфузійного препарату опираються на власні суб’єктивні переконання. На жаль, єдиного консенсусу поміж різних академічних шкіл поки що не має.
Мета дослідження: вивчення змін гемодинамічних показників, водно-електролітного, кислотно-лужного обмінів при застосуванні різних інфузійних розчинів в періопераційному періоді у дітей з ургентною абдомінальною патологією.
Матеріали та методи
Робота виконана на основі аналізу лікування 55 пацієнтів молодшого віку (6–12 років), які надійшли на лікування до відділення інтенсивної терапії КЗ «Дніпропетровська обласна дитяча клінічна лікарня» ДОР» з діагнозом «гострий апендицит, поширений перитоніт». Серед обстежених було 32 дитини чоловічої та 23 жіночої статі. У всіх пацієнтів в обсязі діагностики проводилися: визначення скарг, збір анамнезу захворювання, результати перкусії та аускультації живота, оцінювання даних огляду та обсягу дошпитальної допомоги.
Залежно від виду проведення періопераційної інфузійної терапії усіх хворих було розподілено на 3 групи: 1-ша група (21 дитина) — це діти, у яких як інфузійну терапію в періопераційному періоді використовували гіпотонічні глюкозо-сольові розчини; 2-га група (16 дітей) — це діти, у яких як періопераційну інфузійну терапію використовували розчин Рінгера лактат; 3-тя група (18 дітей) — це діти, у яких як періопераційну інфузійну терапію використовували збалансований електролітний розчин Рінгера малат.
Усім дітям досліджуваних груп проводили однакову інтенсивну терапію, за винятком вибору інфузійного середовища, що являє собою предмет дослідження.
Використовувалась стандартна схема лікування ускладненого апендициту, яка рекомендована наказом МОЗ України. Об’єм інфузійної терапії відповідає сучасним європейським рекомендаціям (Perioperative intravenous fluid therapy in children 2016). У передопераційному періоді протягом перших двох годин вводили інфузійні розчини зі швидкістю 10–20 мл/кг/год, упродовж хірургічного втручання швидкість інфузії становила 10 мл/кг/год. Середня тривалість передопераційного періоду становила 3,80 ± 0,32 години, тривалість операційного періоду — 1,20 ± 0,14 години. У дослідженні використовувалися три види інфузійних розчинів: глюкозо-сольовий, Рінгера лактат і Рінгера малат.
Глюкозо-сольовий розчин вміщує від 50 до 100 мг/мл глюкози, що відповідає молярній концентрації 33,3–66,6 ммоль/л із додаванням іонів Na+, К+. Вміст іонів формується згідно з рекомендаціями Holliday та Segar (1957) залежно від віку хворого.
Рінгера лактат — сольовий розчин із збалансованим вмістом електролітів. Іонний склад на 1 л препарату: Na+ — 131 ммоль, К+ — 5,0 ммоль, Са2+ — 2,0 ммоль, Cl– — 112 ммоль, лактат — 28 ммоль. Теоретична осмолярність розчину становить 276 мОсм/л, що нижче осмолярності плазми. Лактат, який входить до складу препарату, внаслідок метаболічних процесів перетворюється на аніони бікарбонату, що слабко змінює реакцію крові у лужний бік.
Рінгера малат — ізотонічний розчин електролітів, у якому концентрації електролітів відповідають їх плазмовим концентраціям. Він застосовується для корекції втрат позаклітинної рідини (тобто втрати води та електролітів у пропорційній кількості). Аніонний склад препарату являє собою збалансовану комбінацію ацетатів і малатів, що запобігає виникненню метаболічного ацидозу. Концентрація електролітів у розчині: натрій — 145 ммоль/л; калій — 4 ммоль/л; магній — 1 ммоль/л; кальцій — 2,5 ммоль/л; хлориди — 127 ммоль/л; ацетати — 24 ммоль/л; малати — 5 ммоль/л. Теоретична осмолярність — 309 мОсм/л.
З метою визначення особливостей первинного стану пацієнтів з ургентною абдомінальною патологією велику увагу ми приділили вивченню серцево-судинної системи, водно-електролітного та кислотно-лужного стану. Серед лабораторних методів дослідження ми використовували загальний аналіз крові, біохімічні дослідження на вміст електролітів крові, глюкози, лактату. Крім того, враховувався рівень сечовини для виключення транслокаційної (компенсаторної) гіпонатріємії. Вивчення складу водних секторів у всіх обстежених пацієнтів проводилось з допомогою багатофункціонального біоімпедансного аналізатора АР-01 «Діамант» в режимі аналізу імпедансного складу тіла.
Дослідження проводилося в два етапи. Перший етап починався відразу після надходження пацієнтів до палати інтенсивної терапії і був спрямований на визначення особливостей соматичного статусу дітей та наявності супутньої патології. Другий етап обстеження було виконано після проведення хірургічного лікування. Його завданням було визначення впливу інфузійної терапії на показники центрального гомеостазу та водно-електролітного стану дітей.
При створенні первинної бази даних використовувався редактор електронних таблиць MS Excel 2010. Статистична обробка окремих результатів виконана з використанням пакетів прикладних програм Statistica v.10.
Результати та обговорення
При аналізі функціонального стану дітей молодшого шкільного віку з ургентною абдомінальною патологією відмічалась наявність гемоконцентрації, що супроводжувалася підвищенням від норми рівнів гематокриту на 16,6 % (p < 0,001), еритроцитів — на 10,9 % (p < 0,003), гемоглобіну — на 5,3 % (p = 0,003). Зневоднення організму відповідало другому ступеню за рівнем дефіциту загальної рідини організму та зневодненню третього ступеня за показниками позаклітинного і внутрішньосудинного об’ємів рідини. Зниження об’єму циркулюючої крові (ОЦК) призводило до порушень гемодинаміки у вигляді тахікардії та централізації кровообігу (частота серцевих скорочень підвищувалася на 30,6 % понад норму (p < 0,001); загальний периферичний опір судин (ЗПОС) перевищував норму на 69,35 % (p < 0,001)). Проте артеріальна гіпотензія не розвивалася, компенсація досягалась підвищеною роботою серця та спазмом периферичних судин (довірчий інтервал — 3,72 ± 2,21 л/хв/м2; хвилинний об’єм крові (ХОК) — 3,60 ± 0,98 л/хв; ЗПОС — 2887,19 ± 489,03 дин × с × см2). Паралельно спостерігався метаболічний ацидоз із респіраторною компенсацією (зниження pH венозної крові на 1,5 % (p = 0,032); зниження рівня PCO2 на 9,05 % (p < 0,001)). Катаболічний синдром підтверджується наявністю значної кетонурії, розлад транспорту кисню до клітин призводив до перевищення рівня лактату на 47,5 % (p < 0,001). Мав місце гіпоосмолярний стан (рівень натрію був знижений на 7,4 % (p < 0,001); осмолярність крові менша за норму на 3,8 % (p = 0,03)). Олігурія (темп діурезу був знижений до 1,01 ± 0,47 мл/кг/год) носила екстраренальний характер. Вірогідної різниці на цьому етапі між групами не виявлено.
Дослідження електролітного обміну показало, що вихідний рівень натрію у групах був зниженим, проте всередині груп вірогідно вищий рівень спостерігався у I групі (р < 0,05). Корегування рівня натрію в післяопераційному періоді відбулося у дітей, які отримували збалансований сольовий розчин, а у дітей, які отримували розчин на основі глюкози, гіпонатріємія збільшилась на 3,2 % від початкового рівня (р < 0,05). Після оперативного втручання в групах ІІ та ІІІ відмічена вірогідна гіперхлоремія (р < 0,05), а ось у І групі відмінностей від норми не спостерігалося (табл. 1).
Досліджуючи осмолярність плазми, ми відзначили, що в усіх групах спостереження зберігався великий позитивний зв’язок її із рівнем натрію. Динамічні зміни цього показника доже схожі з коливаннями рівня натрію. Швидке корегування рівня натрію приводило до нормалізації показника осмолярності у ІІІ групі. Щодо дітей І групи, то у них спостерігалося прогресування гіпоосмолярного стану (р < 0,05) в післяопераційному періоді.
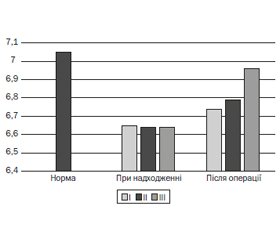
При дослідженні кислотно-лужного та газового складу крові (рис. 1) ми виявили, що кислотно-лужний стан стабілізувався в післяопераційному періоді у ІІІ групі та вірогідно відрізнявся від інших досліджуваних груп (р < 0,05). Такі зміни насамперед зумовлені наявністю у розчинах аніонів, що метаболізуються (лактату, малату, ацетату).
Аналіз вуглеводного обміну (табл. 2) показав відсутність порушень рівня глюкози крові при надходженні до стаціонару в усіх групах, проте спостерігалась гіперглікемія у післяопераційному періоді в І групі (p < 0,001; p = 0,002). Кетонурія, що спостерігалась при надходженні, зберігалась й після операції. Рівень лактату при надходженні перевищував норму на 46 % (p < 0,001) у всіх групах та залишався підвищеним після операції, проте у ІІІ групі відбулося вірогідне його зниження порівняно з вихідним рівнем.
/22_2.jpg)
При аналізі розподілу рідини по водних секторах організму (рис. 2–4) було встановлено, що при надходженні загальний уміст води в організмі в усіх групах був вірогідно знижений у середньому на 6,1–7,1 % (р < 0,05). У ранньому післяопераційному періоді відмінностей від норми та поміж групами не зафіксовано. При аналізі динаміки показників позаклітинної рідини в післяопераційному періоді показники всіх груп не відрізнялись від норми, проте у групі І об’єм був вірогідно вищим на 5,8 % від ІІ групи (p = 0,072). Щодо внутрішньосудинного об’єму, то при надходженні дітей його дефіцит становив 6,2–7,18 %, що вказувало на вихідну гіповолемію. У ІІІ групі вона була компенсована — у післяопераційному періоді. До того ж показники внутрішньосудинного об’єму І та ІІ групи на другому етапі дослідження були вірогідно нижчі, ніж у ІІІ групі (р < 0,05). Таким чином, при використанні «класичної» схеми інфузійної терапії загальний об’єм рідини достатньо швидко збільшувався, але за рахунок перерозподілу у позаклітинний та внутрішньоклітинний простір із зберіганням відносного зниження ОЦК.
/23.jpg)
Висновки
У хворих дітей з ургентною абдомінальною патологією відмічається зневоднення організму та абсолютна гіповолемія, яка погіршується розвитком гіпоосмолярного стану. Напруження компенсаторних функцій організму досягається підвищеною роботою серця та спазмом периферичних судин.
Використання гіпотонічного глюкозо-сольового розчину в періопераційному періоді призводить до збільшення гіпонатріємії та прогресування гіпоосмолярного стану в післяопераційному періоді. Загальний об’єм рідини збільшується, але за рахунок перерозподілу у позаклітинний та внутрішньоклітинний простір із зберіганням відносної гіповолемії.
Оптимальною інфузійною рідиною у дітей молодшого віку з ургентною абдомінальною патологією в періопераційному періоді виявляється збалансований сольовий розчин з додаванням аспартату та малату, використання якого призводить до швидкої нормалізації гемодинамічних показників, водно-електролітного обміну, кислотно-основного стану та водних секторів організму.
Конфлікт інтересів. Автори заявляють про відсутність конфлікту інтересів та власної фінансової зацікавленості при підготовці даної статті.
Список литературы
1. Fuchs J., Adams S.T., Byerley J. Current Issues in Intravenous Fluid Use in Hospitalized Children. Rev. Recent. Clin. Trials. 2017. Vol. 12(4). P. 284-289. doi: 10.2174/1574887112666170816145122.
2. Taniguchi Y. Parenteral fluid therapy in the pediatric surgical patient. Masui. 2013. Vol. 62(9). P. 1069-79.
3. Khan M.F., Siddiqui K.M., Asghar M.A. Fluid choice during perioperative care in children: A survey of present-day proposing practice by anesthesiologists in a tertiary care hospital. Saudi J. Anaesth. 2018. Vol. 12(1). P. 42-45.doi: 10.4103/sja.SJA_258_17.
4. Steurer M.A., Berger T.M. Infusion therapy for neonates, infants and children. Anaesthesist. 2011. Vol. 60(1). P. 10-22. doi: 10.1007/s00101-010-1824-5.
5. Fuchs J., Adams S.T., Byerley J. Current Issues in Intravenous Fluid Use in Hospitalized Children. Rev. Recent. Clin. Trials. 2017. Vol. 12(4). P. 284-289. doi: 10.2174 / 1574887112666170816145122.
6. Alves J.T., Troster E.J., Oliveira C.A. Isotonic saline solution as maintenance intravenous fluid therapy to prevent acquired hyponatremia in hospitalized children. J. Pediatr. (Rio J.). 2011. Vol. 87(6). P. 478-86. doi: 10.2223/JPED.2133.
7. Fernández A.R., Ariza M.A., Casielles J.L. et al. Postoperative hyponatremia in pediatric patients. Rev. Esp. Anestesiol. Reanim. 2009. Vol. 56(8). P. 507-10.
8. Easley D., Tillman E. Hospital-acquired hyponatremia in pediatric patients: a review of the literature. J. Pediatr. Pharmacol. Ther. 2013. Vol. 18(2). P. 105-11. doi: 10.5863/1551-6776-18.2.105.
9. Rius Peris J.M., Rivas-Juesas C., Maraña Pérez A.I. et al. Use of hypotonic fluids in the prescription of maintenance intravenous fluid therapy. An. Pediatr. (Barc.). 2019. Vol. 91(3). P. 158-165. doi: 10.1016/j.anpedi.2018.10.016.
10. Holliday M.A., Segar W.E. The maintenance need for water in parenteral fluid therapy. Pediatrics. 1957. Vol. 19(5). P. 823-32.
11. Way C., Dhamrait R., Wade A., Walker I. et al. Perioperative fluid therapy in children: a survey of current prescribing practice. Br. J. Anaesth. 2006. Vol. 97(3). P. 371-9.
12. Bailey A.G., McNaull P.P., Jooste E. et al. Perioperative crystalloid and colloid fluid management in children: where are we and how did we get here? Anesth. Analg. 2010. Vol. 110(2). P. 375-90. doi: 10.1213/ANE.0b013e3181b6b3b5.
13. Sümpelmann R., Becke K., Crean P., Jöhr M. et al. European consensus statement for intraoperative fluid therapy in children. Eur. J. Anaesthesiol. 2011. Vol. 28(9). P. 637-9. doi: 10.1097/EJA.0b013e3283446bb8.

/21.jpg)
/22.jpg)
/22_2.jpg)
/23.jpg)